একক 10 হেল'এলকেন আৰু হেল'এৰিন
হেল’জেনযুক্ত যৌগসমূহ মাটিৰ বেক্টেৰিয়াৰ দ্বাৰা ভাঙি যোৱাৰ প্ৰতিৰোধী হোৱাৰ বাবে পৰিৱেশত টিকে।
এটা এলিফেটিক বা এৰ’মেটিক হাইড্ৰকাৰ্বনত হাইড্ৰ’জেন পৰমাণু(সমূহ)ক হেল’জেন পৰমাণু(সমূহ)ৰ দ্বাৰা প্ৰতিস্থাপন কৰিলে ক্ৰমে এলকাইল হেলাইড (হেল’এলকেন) আৰু এৰাইল হেলাইড (হেল’এৰিন) গঠন হয়। হেল’এলকেনত হেল’জেন পৰমাণু(সমূহ) এলকাইল গোটৰ sp³ সংকৰিত কাৰ্বন পৰমাণুৰ লগত সংলগ্ন হৈ থাকে আনহাতে হেল’এৰিনত হেল’জেন পৰমাণু(সমূহ) এৰাইল গোটৰ sp² সংকৰিত কাৰ্বন পৰমাণু(সমূহ)ৰ লগত সংলগ্ন হৈ থাকে। বহুতো হেল’জেনযুক্ত জৈৱিক যৌগ প্ৰকৃতিত পোৱা যায় আৰু ইয়াৰে কিছুমান ক্লিনিকেলভাৱে উপযোগী। এই শ্ৰেণীৰ যৌগসমূহে উদ্যোগত আৰু দৈনন্দিন জীৱনত বহুল প্ৰয়োগ পায়। ইহঁত অপেক্ষাকৃত অপোলাৰ যৌগৰ দ্ৰাবক হিচাপে আৰু বিস্তৃত পৰিসৰৰ জৈৱিক যৌগৰ সংশ্লেষণৰ আৰম্ভণিৰ সামগ্ৰী হিচাপে ব্যৱহাৰ কৰা হয়। অণুজীৱৰ দ্বাৰা উৎপাদিত ক্ল’ৰিনযুক্ত প্ৰতিজৈৱিক, ক্ল’ৰাম্ফেনিকল, টাইফয়েড জ্বৰৰ চিকিৎসাৰ বাবে অতি প্ৰভাৱশালী। আমাৰ শৰীৰে আয়’ডিনযুক্ত হৰম’ন, থাইৰক্সিন উৎপাদন কৰে, যাৰ অভাৱত গয়টাৰ নামৰ ৰোগ হয়। কৃত্ৰিম হেল’জেন যৌগ, যেনে ক্ল’ৰ’কুইন মেলেৰিয়াৰ চিকিৎসাৰ বাবে ব্যৱহাৰ কৰা হয়; হেল’থেন শল্য চিকিৎসাৰ সময়ত এনাস্থেটিক হিচাপে ব্যৱহাৰ কৰা হয়। কিছুমান সম্পূৰ্ণৰূপে ফ্ল’ৰিনযুক্ত যৌগ শল্য চিকিৎসাত সম্ভাৱ্য ৰক্ত প্ৰতিস্থাপক হিচাপে বিবেচনা কৰা হৈছে।
এই এককত, আপুনি অৰ্গেন’হেল’জেন যৌগৰ প্ৰস্তুতিৰ গুৰুত্বপূৰ্ণ পদ্ধতি, ভৌতিক আৰু ৰাসায়নিক ধৰ্ম আৰু ব্যৱহাৰসমূহ অধ্যয়ন কৰিব।
10.1 শ্ৰেণীবিভাজন
হেল’এলকেন আৰু হেল’এৰিন নিম্নলিখিত ধৰণে শ্ৰেণীবিভাজন কৰিব পাৰি:
10.1.1 হেল’জেন পৰমাণুৰ সংখ্যাৰ ভিত্তিত
ইহঁতক মন’, ডাই, বা পলিহেল’জেন (ট্ৰাই-, টেট্ৰা-, আদি) যৌগ হিচাপে শ্ৰেণীবিভাজন কৰিব পাৰি যাৰ ভিত্তি হৈছে ইহঁতৰ গঠনত এটা, দুটা বা ততোধিক হেল’জেন পৰমাণু থাকে নে নাই। উদাহৰণস্বৰূপে,

মন’হেল’কম্পাউণ্ডসমূহক হেল’জেনটো সংলগ্ন হৈ থকা কাৰ্বন পৰমাণুৰ সংকৰণৰ ভিত্তিত অধিক শ্ৰেণীবিভাজন কৰিব পাৰি, তলত আলোচনা কৰা হৈছে।
10.1.2 $\mathbf{s p}^{\mathbf{3}} \mathbf{~C}-\mathbf{X}$ বন্ধন (X= F, Cl, Br, I) থকা যৌগ
এই শ্ৰেণীটোত অন্তৰ্ভুক্ত হৈছে
(ক) এলকাইল হেলাইড বা হেল’এলকেন ( $\mathbf{R}-\mathbf{X}$ )
এলকাইল হেলাইডত, হেল’জেন পৰমাণু এটা এলকাইল গোট $(\mathrm{R})$ৰ লগত বন্ধনযুক্ত হৈ থাকে। ইহঁতে $\mathrm{C} _{\mathrm{n}} \mathrm{H} _{2 \mathrm{n}+1} \mathrm{X}$ৰ দ্বাৰা প্ৰতিনিধিত্ব কৰা এক সমসংস্থ শৃংখলা গঠন কৰে। হেল’জেনটো সংলগ্ন হৈ থকা কাৰ্বনৰ প্ৰকৃতি অনুসৰি ইহঁতক প্ৰাথমিক, দ্বিতীয়ক বা তৃতীয়ক হিচাপে শ্ৰেণীবিভাজন কৰা হয়। যদি এলকাইল হেলাইডত হেল’জেন এটা প্ৰাথমিক কাৰ্বন পৰমাণুৰ লগত সংলগ্ন হৈ থাকে, তেন্তে এলকাইল হেলাইডটোক প্ৰাথমিক এলকাইল হেলাইড বা ($1^{\circ}$) এলকাইল হেলাইড বুলি কোৱা হয়। একেদৰে, যদি হেল’জেন দ্বিতীয়ক বা তৃতীয়ক কাৰ্বন পৰমাণুৰ লগত সংলগ্ন হৈ থাকে, তেন্তে এলকাইল হেলাইডটোক ক্ৰমে দ্বিতীয়ক এলকাইল হেলাইড ($2^{\circ}$) আৰু তৃতীয়ক ($3^{\circ}$) এলকাইল হেলাইড বুলি কোৱা হয়।

(খ) এলাইলিক হেলাইড
এইবোৰ হৈছে সেই যৌগ য’ত হেল’জেন পৰমাণু এটা $s p^{3}$-সংকৰিত কাৰ্বন পৰমাণুৰ লগত সংলগ্ন হৈ থাকে যিটো কাৰ্বন-কাৰ্বন দ্বি-বন্ধন $(\mathrm{C}=\mathrm{C})$ৰ সংলগ্ন, অৰ্থাৎ এটা এলাইলিক কাৰ্বনৰ লগত।

(গ) বেনজাইলিক হেলাইড
এইবোৰ হৈছে সেই যৌগ য’ত হেল’জেন পৰমাণু এটা $s p^{3}$-সংকৰিত কাৰ্বন পৰমাণুৰ লগত সংলগ্ন হৈ থাকে যিটো এৰ’মেটিক ৰিংৰ লগত সংযুক্ত।

10.1.3 $\boldsymbol{s p}^{2} \mathrm{C}-\mathrm{X}$ বন্ধন থকা যৌগ
এই শ্ৰেণীটোত অন্তৰ্ভুক্ত হৈছে:
(ক) ভিনাইলিক হেলাইড
এইবোৰ হৈছে সেই যৌগ য’ত হেল’জেন পৰমাণু এটা $s p^{2}$-সংকৰিত কাৰ্বন পৰমাণুৰ লগত সংলগ্ন হৈ থাকে যিটো কাৰ্বন-কাৰ্বন দ্বি-বন্ধন $(\mathrm{C}=\mathrm{C})$ৰ অংশ।

(খ) এৰাইল হেলাইড
এইবোৰ হৈছে সেই যৌগ য’ত হেল’জেন পৰমাণু পোনপটীয়াকৈ এৰ’মেটিক ৰিংৰ $s p^{2}$-সংকৰিত কাৰ্বন পৰমাণুৰ লগত বন্ধনযুক্ত হৈ থাকে।

10.2 নামকৰণ
হেল’জেনযুক্ত যৌগৰ শ্ৰেণীবিভাজন শিকাৰ পিছত, এতিয়া আহক ইহঁতক কেনেকৈ নামকৰণ কৰা হয় শিকো। এলকাইল হেলাইডৰ সাধাৰণ নামবোৰ এলকাইল গোটৰ নামকৰণ কৰি তাৰ পিছত হেলাইডৰ নাম দি উৎপন্ন কৰা হয়। IUPAC নামকৰণ পদ্ধতিত, এলকাইল হেলাইডবোৰক হেল’প্ৰতিস্থাপিত হাইড্ৰকাৰ্বন হিচাপে নামকৰণ কৰা হয়। বেনজিনৰ মন’ হেল’জেন প্ৰতিস্থাপিত ডেৰিভেটিভৰ বাবে, সাধাৰণ আৰু IUPAC নাম একে। ডাইহেল’জেন ডেৰিভেটিভৰ বাবে, সাধাৰণ পদ্ধতিত $o^{-,}, m_{-}, p$ - উপসৰ্গবোৰ ব্যৱহাৰ কৰা হয় কিন্তু IUPAC পদ্ধতিত, আপুনি শ্ৰেণী XI-ত শিকাৰ দৰে, 1,$2 ; 1,3$ আৰু 1,4 সংখ্যাবোৰ ব্যৱহাৰ কৰা হয়।

একেধৰণৰ হেল’জেন পৰমাণু থকা ডাইহেল’এলকেনবোৰক এলকাইলিডিন বা এলকাইলিন ডাইহেলাইড হিচাপে নামকৰণ কৰা হয়। দুয়োটা হেল’জেন পৰমাণু থকা ডাইহেল’কম্পাউণ্ডবোৰক জেমিনেল হেলাইড বা জেম-ডাইহেলাইড হিচাপে শ্ৰেণীবিভাজন কৰা হয় যেতিয়া দুয়োটা হেল’জেন পৰমাণু শৃংখলাৰ একেটা কাৰ্বন পৰমাণুত উপস্থিত থাকে আৰু ভিচিনেল হেলাইড বা ভিচ-ডাইহেলাইড হিচাপে শ্ৰেণীবিভাজন কৰা হয় যেতিয়া হেল’জেন পৰমাণুবোৰ সংলগ্ন কাৰ্বন পৰমাণুত উপস্থিত থাকে। সাধাৰণ নাম পদ্ধতিত, জেম-ডাইহেলাইডবোৰক এলকাইলিডিন হেলাইড হিচাপে নামকৰণ কৰা হয় আৰু ভিচ-ডাইহেলাইডবোৰক এলকাইলিন ডাইহেলাইড হিচাপে নামকৰণ কৰা হয়। IUPAC পদ্ধতিত, ইহঁতক ডাইহেল’এলকেন হিচাপে নামকৰণ কৰা হয়।
হেল’কম্পাউণ্ডৰ কিছুমান সাধাৰণ উদাহৰণ তালিকা 10.1-ত উল্লেখ কৰা হৈছে।

উদাহৰণ 10.1
$\mathrm{C_5} \mathrm{H_11} \mathrm{Br}$ আণৱিক সূত্ৰ থকা আটাইকেইটা আঠটা গাঠনিক সমাবয়বৰ গঠন অংকন কৰক। প্ৰতিটো সমাবয়বক IUPAC পদ্ধতি অনুসৰি নামকৰণ কৰক আৰু ইহঁতক প্ৰাথমিক, দ্বিতীয়ক বা তৃতীয়ক ব্ৰ’মাইড হিচাপে শ্ৰেণীবিভাজন কৰক।
সমাধান
| $\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{CH}_2 \mathrm{CH}_2 \mathrm{CH}_2 \mathrm{Br}$ | 1-ব্ৰ’ম’পেন্টেন (1 $\left.{ }^{\circ}\right)$ |
|---|---|
| $\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{CH}_2 \mathrm{CH}(\mathrm{Br}) \mathrm{CH}_3$ | 2-ব্ৰ’ম’পেন্টেন $\left(2^{\circ}\right)$ |
| $\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{CH}(\mathrm{Br}) \mathrm{CH}_2 \mathrm{CH}_3$ | 3-ব্ৰ’ম’পেন্টেন (2 $\left.{ }^{\circ}\right)$ |
| $\left(\mathrm{CH}_3\right)_2 \mathrm{CHCH}_2 \mathrm{CH}_2 \mathrm{Br}$ | 1-ব্ৰ’ম’-3-মিথাইলবিউটেন (1 $\left.{ }^{\circ}\right)$ |
| $\left(\mathrm{CH}_3\right)_2 \mathrm{CHCHBrCH}_3$ | 2-ব্ৰ’ম’-3-মিথাইলবিউটেন(2 $\left.{ }^{\circ}\right)$ |
| $\left(\mathrm{CH}_3\right)_2 \mathrm{CBrCH}_2 \mathrm{CH}_3$ | 2-ব্ৰ’ম’-2-মিথাইলবিউটেন $\left(3^{\circ}\right)$ |
| $\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{CH}\left(\mathrm{CH}_3\right) \mathrm{CH}_2 \mathrm{Br}$ | 1-ব্ৰ’ম’-2-মিথাইলবিউটেন(1 $\left.{ }^{\circ}\right)$ |
| $\left(\mathrm{CH}_3\right)_3 \mathrm{CCH}_2 \mathrm{Br}$ | 1-ব্ৰ’ম’-2,2-ডাইমিথাইলপ্ৰ’পেন (1 $\left.{ }^{\circ}\right)$ |
উদাহৰণ 10.2 তলত দিয়াবোৰৰ IUPAC নাম লিখা:

সমাধান
(i) 4-ব্ৰ’ম’পেন্ট-2-ইন
(ii) 3-ব্ৰ’ম’-2-মিথাইলবিউট-1-ইন
(iii) 4-ব্ৰ’ম’-3-মিথাইলপেন্ট-2-ইন
(iv) 1-ব্ৰ’ম’-2-মিথাইলবিউট-2-ইন
(v) 1-ব্ৰ’ম’বিউট-2-ইন
(vi) 3-ব্ৰ’ম’-2-মিথাইলপ্ৰ’পিন
10.3 C-X বন্ধনৰ প্ৰকৃতি
হেল’জেন পৰমাণুবোৰ কাৰ্বনতকৈ অধিক ইলেক্ট্ৰ’নেগেটিভ, সেয়েহে এলকাইল হেলাইডৰ কাৰ্বন-হেল’জেন বন্ধন পোলাৰাইজড হয়; কাৰ্বন পৰমাণুৱে আংশিক ধনাত্মক আধান বহন কৰে আনহাতে হেল’জেন পৰমাণুৱে আংশিক ঋণাত্মক আধান বহন কৰে।
আমি পৰ্যাবৃত্ত তালিকাৰ গোটটোত তললৈ গ’লে, হেল’জেন পৰমাণুৰ আকাৰ বৃদ্ধি পায়। ফ্ল’ৰিন পৰমাণু আটাইতকৈ সৰু আৰু আয়’ডিন পৰমাণু আটাইতকৈ ডাঙৰ। ফলস্বৰূপে কাৰ্বন-হেল’জেন বন্ধন দৈৰ্ঘ্যও $\mathrm{C}-\mathrm{F}$ ৰ পৰা $\mathrm{C}-\mathrm{I}$ লৈ বৃদ্ধি পায়। কিছুমান সাধাৰণ বন্ধন দৈৰ্ঘ্য, বন্ধন এন্থালপি আৰু ডাইপ’ল মমেন্ট তালিকা 10.2-ত দিয়া হৈছে।
এলকাইল হেলাইডবোৰ এলক’হলৰ পৰা সৰ্বোত্তমভাৱে প্ৰস্তুত কৰা হয়, যিবোৰ সহজে প্ৰাপ্য।
তালিকা 10.2: কাৰ্বন-হেল’জেন (C—X) বন্ধন দৈৰ্ঘ্য, বন্ধন এন্থালপি আৰু ডাইপ’ল মমেন্ট
| বন্ধন | বন্ধন দৈৰ্ঘ্য/pm | C-X বন্ধন এন্থালপি/ kJmol ${ }^{-1}$ | ডাইপ’ল মমেন্ট/ডেবাই |
|---|---|---|---|
| $\mathrm{CH}_3-\mathrm{F}$ | 139 | 452 | 1.847 |
| $\mathrm{CH}_3-\mathrm{Cl}$ | 178 | 351 | 1.860 |
| $\mathrm{CH}_3-\mathrm{Br}$ | 193 | 293 | 1.830 |
| $\mathrm{CH}_3-\mathrm{I}$ | 214 | 234 | 1.636 |
10.4 হেল’এলকেন প্ৰস্তুতিৰ পদ্ধতি
10.4.1 এলক’হলৰ পৰা
এলক’হলৰ হাইড্ৰক্সিল গোটক কেন্দ্ৰীভূত হেল’জেন এছিড, ফছফৰাছ হেলাইড বা থায়’নাইল ক্ল’ৰাইডৰ সৈতে বিক্ৰিয়া কৰিলে হেল’জেনৰ দ্বাৰা প্ৰতিস্থাপিত হয়। থায়’নাইল ক্ল’ৰাইড পছন্দ কৰা হয় কাৰণ এই বিক্ৰিয়াত এলকাইল হেলাইড গেছীয় উৎপাদ $\mathrm{SO_2}$ আৰু $\mathrm{HCl}$ৰ সৈতে গঠন হয়। দুয়োটা গেছীয় উৎপাদ পলায়নশীল, গতিকে বিক্ৰিয়াটোৱে বিশুদ্ধ এলকাইল হেলাইড দিয়ে। প্ৰাথমিক আৰু দ্বিতীয়ক এলক’হলৰ $\mathrm{HCl}$ৰ সৈতে বিক্ৰিয়াই এটা অনুঘটক, $\mathrm{ZnCl_2}$ৰ উপস্থিতিৰ প্ৰয়োজন। তৃতীয়ক এলক’হলৰ সৈতে, বিক্ৰিয়াটো কেৱল এলক’হলটোক কেন্দ্ৰীভূত $\mathrm{HCl}$ৰ সৈতে কোঠাৰ উষ্ণতাত জোকাৰি পৰিচালনা কৰা হয়। $\mathrm{HBr}(48 %)$ৰ সৈতে স্থিৰ উতলন এলকাইল ব্ৰ’মাইড প্ৰস্তুত কৰিবলৈ ব্যৱহাৰ কৰা হয়। R-I-ৰ ভাল উৎপাদন এলক’হলবোৰক 95% অৰ্থ’ফছফৰিক এছিডত ছ’ডিয়াম বা পটেছিয়াম আয়’ডাইডৰ সৈতে গৰম কৰি পাব পাৰি। দিয়া হেল’এছিডৰ সৈতে এলক’হলৰ সক্ৰিয়তাৰ ক্ৰম হৈছে $3^{\circ}>2^{\circ}>1^{\circ}$। ফছফৰাছ ট্ৰাইব্ৰ’মাইড আৰু ট্ৰাইআয়’ডাইড সাধাৰণতে ৰেড ফছফৰাছৰ ব্ৰ’মিন আৰু আয়’ডিনৰ সৈতে ক্ৰমে বিক্ৰিয়া কৰি ইন ছিটুতে (বিক্ৰিয়া মিশ্ৰণত উৎপাদিত) উৎপন্ন কৰা হয়।
$$ \begin{aligned} & \mathrm{R}-\mathrm{OH}+\mathrm{HCl} \xrightarrow{\mathrm{ZnCl_2}} \mathrm{R}-\mathrm{Cl}+\mathrm{H_2} \mathrm{O} \\ & \mathrm{R}-\mathrm{OH}+\mathrm{NaBr}+\mathrm{H_2} \mathrm{SO_4} \longrightarrow \mathrm{R}-\mathrm{Br}+\mathrm{NaHSO_4}+\mathrm{H_2} \mathrm{O} \\ & 3 \mathrm{R}-\mathrm{OH}+\mathrm{PX_3} \longrightarrow 3 \mathrm{R}-\mathrm{X}+\mathrm{H_3} \mathrm{PO_3} \quad(\mathrm{X}=\mathrm{Cl}, \mathrm{Br}) \\ & \mathrm{R}-\mathrm{OH}+\mathrm{PCl_5} \longrightarrow \mathrm{R}-\mathrm{Cl}+\mathrm{POCl_3}+\mathrm{HCl} \\ & \mathrm{R}-\mathrm{OH}+\frac{\mathrm{red} \mathrm{P} / \mathrm{X_2}}{\mathrm{X_2}=\mathrm{Br_2}, \mathrm{I_2}} \mathrm{R}-\mathrm{X} \\ & \mathrm{R}-\mathrm{OH}+\mathrm{SOCl_2} \longrightarrow \mathrm{R}-\mathrm{Cl}+\mathrm{SO_2}+\mathrm{HCl} \end{aligned} $$
এলকাইল ক্ল’ৰাইডৰ প্ৰস্তুতিকৰণ হয় শুকান হাইড্ৰ’জেন ক্ল’ৰাইড গেছ এলক’হলৰ দ্ৰৱণৰ মাজেৰে পাৰ কৰি বা এলক’হল আৰু কেন্দ্ৰীভূত জলীয় হেল’জেন এছিডৰ মিশ্ৰণ গৰম কৰি কৰা হয়।
ওপৰৰ পদ্ধতিবোৰ এৰাইল হেলাইড প্ৰস্তুত কৰিবলৈ প্ৰযোজ্য নহয় কাৰণ ফিনলত কাৰ্বন-অক্সিজেন বন্ধনৰ আংশিক দ্বি-বন্ধন চৰিত্ৰ থাকে আৰু একক বন্ধনতকৈ শক্তিশালী হোৱাৰ বাবে ভাঙিবলৈ টান।
10.4.2 হাইড্ৰকাৰ্বনৰ পৰা
(I) মুক্ত মূলক হেল’জেনেশ্যনৰ দ্বাৰা এলকেনৰ পৰা
এলকেনৰ মুক্ত মূলক ক্ল’ৰিনেশ্যন বা ব্ৰ’মিনেশ্যনে আইছ’মাৰিক মন’- আৰু পলিহেল’এলকেনৰ জটিল মিশ্ৰণ দিয়ে, যিটো বিশুদ্ধ যৌগ হিচাপে পৃথক কৰিবলৈ টান। ফলস্বৰূপে, যিকোনো একক যৌগৰ উৎপাদন কম।
$\mathrm{CH_3}\mathrm{CH_2}\mathrm{CH_2}\mathrm{CH_3} \xrightarrow[ \text {or heat}]{\mathrm{Cl_2} \text {/UV} \quad \text {light}} \mathrm{CH_3}\mathrm{CH_2}\mathrm{CH_2}\mathrm{CH_2}\mathrm{Cl_2} + \mathrm{CH_3}\mathrm{CH_2}\mathrm{CHCl}\mathrm{CH_3} $
(II) এলকিনৰ পৰা
(i) হাইড্ৰ’জেন হেলাইডৰ সংযোজন: এলকিন এটাক হাইড্ৰ’জেন ক্ল’ৰাইড, হাইড্ৰ’জেন ব্ৰ’মাইড বা হাইড্ৰ’জেন আয়’ডাইডৰ সৈতে বিক্ৰিয়া কৰি সংশ্লিষ্ট এলকাইল হেলাইলৈ ৰূপান্তৰিত কৰা হয়।
প্ৰ’পিনে দুটা উৎপাদন দিয়ে, কিন্তু মাৰ্ক’ভনিক’ভৰ নিয়ম অনুসৰি কেৱল এটাই প্ৰাধান্য পায়। (একক 13, শ্ৰেণী XI)
$$ \mathrm{CH_3} \mathrm{CH}=\mathrm{CH_2}+\mathrm{H}-\mathrm{I} \longrightarrow \underset {\text{minor}}{\mathrm{CH_3} \mathrm{CH_2} \mathrm{CH_2} \mathrm{I}} + \underset{ \text{major }}{\mathrm{CH_3} \mathrm{CHICH_3}} $$
(ii) হেল’জেনৰ সংযোজন: পৰীক্ষাগাৰত, $\mathrm{CCl}_{4}$ত থকা ব্ৰ’মিনৰ সংযোজনৰ ফলত এলকিন এটালৈ ৰঙচুৱা-মটিয়া ব্ৰ’মিনৰ ৰঙৰ নিষ্কাশন হোৱাটোৱে অণু এটাত দ্বি-বন্ধন সনাক্তকৰণৰ এক গুৰুত্বপূৰ্ণ পদ্ধতি গঠন কৰে। সংযোজনৰ ফলত ভিচ-ডাইব্ৰ’মাইডৰ সংশ্লেষণ হয়, যিবোৰ বৰণহীন (একক 9, শ্ৰেণী XI)।

উদাহৰণ 10.3
$\left(\mathrm{CH_3}\right)_{2} \mathrm{CHCH_2} \mathrm{CH_3}$ৰ মুক্ত মূলক মন’ক্ল’ৰিনেশ্যনত গঠন হোৱাৰ আশা কৰা সকলো সম্ভাৱ্য মন’ক্ল’ৰ’ গাঠনিক সমাবয়ব চিনাক্ত কৰক।
সমাধান
দিয়া অণুটোত, চাৰিটা ভিন্ন ধৰণৰ হাইড্ৰ’জেন পৰমাণু আছে। এই হাইড্ৰ’জেন পৰমাণুবোৰ প্ৰতিস্থাপন কৰিলে নিম্নলিখিতবোৰ দিব
| $\left(\mathrm{CH_3}\right)_{2} \mathrm{CHCH_2} \mathrm{CH_2} \mathrm{Cl}$ | $\left(\mathrm{CH_3}\right)_{2} \mathrm{CHCH}(\mathrm{Cl}) \mathrm{CH_3}$ |
|---|---|
| $\left(\mathrm{CH_3}\right)_{2} \mathrm{C}(\mathrm{Cl}) \mathrm{CH_2} \mathrm{CH_3}$ | $\mathrm{CH_3} \mathrm{CH}\left(\mathrm{CH_2} \mathrm{Cl_2} \mathrm{CH_2} \mathrm{CH_3}\right).$ |
10.4.3 হেল’জেন বিনিময়
এলকাইল আয়’ডাইডবোৰ প্ৰায়ে শুকান এচিটনত NaIৰ সৈতে এলকাইল ক্ল’ৰাইড/ব্ৰ’মাইডৰ বিক্ৰিয়াৰ দ্বাৰা প্ৰস্তুত কৰা হয়। এই বিক্ৰিয়াটো ফিনকেলষ্টেইন বিক্ৰিয়া বুলি জনা যায়।
$$ \begin{aligned} & \mathrm{R}-\mathrm{X}+\mathrm{NaI} \longrightarrow \mathrm{R}-\mathrm{I}+\mathrm{NaX} \\ & \mathrm{X}=\mathrm{Cl}, \mathrm{Br} \end{aligned} $$
এইদৰে গঠন হোৱা NaCl বা NaBr শুকান এচিটনত অধঃক্ষেপিত হয়। ই লে চেটেলিয়াৰৰ নীতি অনুসৰি আগবাঢ়ি যোৱা বিক্ৰিয়াটো সহজ কৰে। এলকাইল ফ্ল’ৰাইডৰ সংশ্লেষণ এলকাইল ক্ল’ৰাইড/ব্ৰ’মাইডক ধাতৱ ফ্ল’ৰাইড যেনে $\mathrm{AgF}, \mathrm{Hg}_2 \mathrm{~F}_2, \mathrm{CoF}_2$ বা $\mathrm{SbF}_3$ৰ উপস্থিতিত গৰম কৰি সৰ্বোত্তমভাৱে সম্পন্ন কৰা হয়। বিক্ৰিয়াটোক $\mathrm{Swarts}$ বিক্ৰিয়া বুলি কোৱা হয়।
$$ \mathrm{H}_3 \mathrm{C}-\mathrm{Br}+\mathrm{AgF} \longrightarrow \mathrm{H}_3 \mathrm{C}-\mathrm{F}+\mathrm{AgBr} $$
উদাহৰণ 6.3 $\left(\mathrm{CH}_3\right)_2 \mathrm{CHCH}_2 \mathrm{CH}_3$ৰ মুক্ত মূলক মন’ক্ল’ৰিনেশ্যনত গঠন হোৱাৰ আশা কৰা সকলো সম্ভাৱ্য মন’ক্ল’ৰ’ গাঠনিক সমাবয়ব চিনাক্ত কৰক।
সমাধান
দিয়া অণুটোত, চাৰিটা ভিন্ন ধৰণৰ হাইড্ৰ’জেন পৰমাণু আছে। এই হাইড্ৰ’জেন পৰমাণুবোৰ প্ৰতিস্থাপন কৰিলে নিম্নলিখিতবোৰ দিব
$\left(\mathrm{CH} _{3}\right) _{2} \mathrm{CHCH} _{2} \mathrm{CH} _{2} \mathrm{Cl}$,
$\left(\mathrm{CH} _{3}\right) _{2} \mathrm{CHCH}(\mathrm{Cl}) \mathrm{CH} _{3}$,
$\left(\mathrm{CH} _{3}\right) _{2} \mathrm{C}(\mathrm{Cl}) \mathrm{CH} _{2} \mathrm{CH} _{3}$,
$\mathrm{CH} _{3} \mathrm{CH}\left(\mathrm{CH} _{2} \mathrm{Cl}\right) \mathrm{CH} _{2} \mathrm{CH} _{3}$
10.5 হেল’এৰিন প্ৰস্তুতি
(i) ইলেক্ট্ৰ’ফিলিক প্ৰতিস্থাপনৰ দ্বাৰা হাইড্ৰকাৰ্বনৰ পৰা এৰাইল ক্ল’ৰাইড আৰু ব্ৰ’মাইডবোৰ ক্ৰমে ক্ল’ৰিন আৰু ব্ৰ’মিনৰ সৈতে এৰিনৰ ইলেক্ট্ৰ’ফিলিক প্ৰতিস্থাপনৰ দ্বাৰা লোহা বা আয়ৰন(III) ক্ল’ৰাইডৰ দৰে লুইছ এছিড অনুঘটকৰ উপস্থিতিত সহজে প্ৰস্তুত কৰিব পাৰি।

অৰ্থ’ আৰু পাৰা সমাবয়ববোৰৰ গলনাংকৰ পাৰ্থক্য বেছি হোৱাৰ বাবে সহজে পৃথক কৰিব পাৰি। আয়’ডিনৰ সৈতে বিক্ৰিয়াবোৰ প্ৰকৃতিত বিপৰীতমুখী আৰু আয়’ডিনেশ্যনৰ সময়ত গঠন হোৱা $\mathrm{HI}$ক জাৰিত কৰিবলৈ জাৰক এজেণ্ট $\left(\mathrm{HNO_3}\right).$, $\mathrm{HIO_4}$ )ৰ উপস্থিতিৰ প্ৰয়োজন। ফ্ল’ৰিনৰ উচ্চ সক্ৰিয়তাৰ বাবে ফ্ল’ৰ’ যৌগবোৰ এই পদ্ধতিৰে প্ৰস্তুত কৰা নহয়।
(ii) ছেণ্ডমায়াৰৰ বিক্ৰিয়াৰ দ্বাৰা এমিনৰ পৰা
যেতিয়া প্ৰাথমিক এৰ’মেটিক এমিন, শীতল জলীয় খনিজ এছিডত দ্ৰৱীভূত বা নিলম্বিত কৰি ছ’ডিয়াম নাইট্ৰাইটৰ সৈতে চিকিত্সা কৰা হয়, ডায়াজ’নিয়াম লৱণ গঠন হয়। নতুনকৈ প্ৰস্তুত কৰা ডায়াজ’নিয়াম লৱণৰ দ্ৰৱণ কুপ্ৰাছ ক্ল’ৰাইড বা কুপ্ৰাছ ব্ৰ’মাইডৰ সৈতে মিহলি কৰিলে ডায়াজ’নিয়াম গোট $-\mathrm{Cl}$ বা $-\mathrm{Br}$ৰ দ্বাৰা প্ৰতিস্থাপিত হয়।

ডায়াজ’নিয়াম গোটক আয়’ডিনৰ দ্বাৰা প্ৰতিস্থাপন কৰিবলৈ কুপ্ৰাছ হেলাইডৰ উপস্থিতিৰ প্ৰয়োজন নহয় আৰু ডায়াজ’নিয়াম লৱণটোক পটেছিয়াম আয়’ডাইডৰ সৈতে কেৱল জোকাৰি কৰা হয়।

উদাহৰণ 10.4 তলৰ বিক্ৰিয়াবোৰৰ উৎপাদ লিখা:

সমাধান

10.6 ভৌতিক ধৰ্ম
এলকাইল হেলাইডবোৰ বিশুদ্ধ হ’লে বৰণহীন। কিন্তু ব্ৰ’মাইড আৰু আয়’ডাইডবোৰে পোহৰৰ সংস্পৰ্শলৈ আহিলে ৰং বিকশিত কৰে। বহুতো উদ্বায়ী হেল’জেন যৌগৰ মিঠা গোন্ধ থাকে।
গলনাংক আৰু উতলাংক
মিথাইল ক্ল’ৰাইড, মিথাইল ব্ৰ’মাইড, ইথাইল ক্ল’ৰাইড আৰু কিছুমান ক্ল’ৰ’ফ্ল’ৰ’মিথেন কোঠাৰ উষ্ণতাত গেছ। উচ্চ সদস্যবোৰ তৰল বা কঠিন। আমি ইতিমধ্যে শিকিছোঁ, জৈৱিক হেল’জেন যৌগৰ অণুবোৰ সাধাৰণতে পোলাৰ। পিতৃ হাইড্ৰকাৰ্বনতকৈ অধিক পোলাৰিটি আৰু উচ্চ আণৱিক ভৰৰ বাবে, হেল’জেন ডেৰিভেটিভত আন্তঃআণৱিক আকৰ্ষণ বল (ডাইপ’ল-ডাইপ’ল আৰু ভেন ডাৰ ৱালছ) শক্তিশালী। সেয়েহে তুলনাযোগ্য আণৱিক ভৰৰ হাইড্ৰকাৰ্বনতকৈ ক্ল’ৰাইড, ব্ৰ’মাইড আৰু আয়’ডাইডৰ উতলাংক যথেষ্ট বেছি।
অণুবোৰ আকাৰত ডাঙৰ হ’লে আৰু অধিক ইলেক্ট্ৰন থাকিলে আকৰ্ষণবোৰ শক্তিশালী হয়। বিভিন্ন হেলাইডৰ উতলাংকৰ ভিন্নতাৰ ধৰণ চিত্ৰ 10.1-ত চিত্ৰিত কৰা হৈছে। একে এলকাইল গোটৰ বাবে, এলকাইল হেলাইডৰ উতলাংক ক্ৰমত হ্ৰাস পায়: $\mathrm{RI}>\mathrm{RBr}>\mathrm{RCl}>\mathrm{RF}$। এইটো কাৰণ হেল’জেন পৰমাণুৰ আকাৰ আৰু ভৰ বৃদ্ধিৰ সৈতে ভেন ডাৰ ৱালছ বলৰ পৰিমাণ বৃদ্ধি পায়।
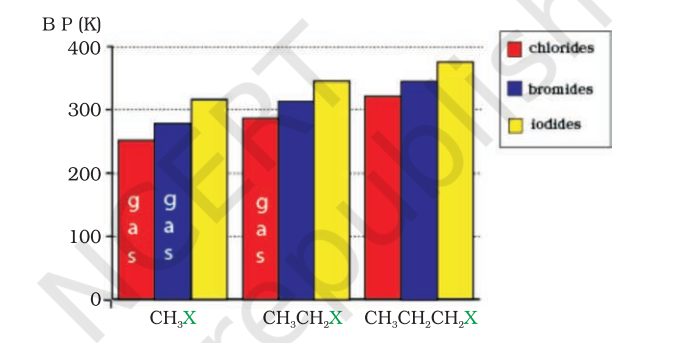
চিত্ৰ 10.1: কিছুমান এলকাইল হেলাইডৰ উতলাংকৰ তুলনা
আইছ’মাৰিক হেল’এলকেনৰ উতলাংক শাখাবিহীনতা বৃদ্ধিৰ সৈতে হ্ৰাস পায় (একক 12, শ্ৰেণী XI)। উদাহৰণস্বৰূপে, 2-ব্ৰ’ম’-2-মিথাইলপ্ৰ’পেনৰ তিনিটা সমাবয়বৰ ভিতৰত আটাইতকৈ কম উতলাংক আছে।
$\mathrm{CH_3} \mathrm{CH_2} \mathrm{CH_2} \mathrm{CH_2} \mathrm{Br}$
আইছ’মাৰিক ডাইহেল’বেনজিনৰ উতলাংক প্ৰায় একে। কিন্তু পাৰা-সমাবয়ববোৰ অৰ্থ’-আৰু মেটা-সমাবয়বতকৈ উচ্চ গলনাংকযুক্ত। ই পাৰা-সমাবয়বৰ সমমিতিৰ বাবে হয় যি অৰ্থ’- আৰু মেটা-সমাবয়বতকৈ ভালদৰে স্ফটিক জালীত খাপ খায়।

ঘনত্ব
হাইড্ৰকাৰ্বনৰ ব্ৰ’ম’, আয়’ড’ আৰু পলিক্ল’ৰ’ ডেৰিভেটিভবোৰ পানীতকৈ গধুৰ। কাৰ্বন পৰমাণুৰ সংখ্যা, হেল’জেন পৰমাণুৰ সংখ্যা আৰু হেল’জেন পৰমাণুৰ পাৰমাণৱিক ভৰ বৃদ্ধিৰ সৈতে ঘনত্ব বৃদ্ধি পায় (তালিকা 10.3)।
তালিকা 10.3: কিছুমান হেল’এলকেনৰ ঘনত্ব
| যৌগ | ঘনত্ব (g/mL) | যৌগ | ঘনত্ব (g/mL) |
|---|---|---|---|
| $\mathrm{n}-\mathrm{C}_3 \mathrm{H}_7 \mathrm{Cl}$ | 0.89 | $\mathrm{CH}_2 \mathrm{Cl}_2$ | 1.336 |
| $\mathrm{n}-\mathrm{C}_3 \mathrm{H}_7 \mathrm{Br}$ | 1.335 | $\mathrm{CHCl}_3$ | 1.489 |
| $\mathrm{n}-\mathrm{C}_3 \mathrm{H}_7 \mathrm{I}$ | 1.747 | $\mathrm{CCl}_4$ | 1.595 |
দ্ৰৱণীয়তা
হেল’এলকেনবোৰ পানীত অতি সামান্য দ্ৰৱণীয়। পানীত হেল’এলকেন দ্ৰৱীভূত কৰিবলৈ, হেল’এলকেন অণুবোৰৰ মাজৰ আকৰ্ষণ অতিক্ৰম কৰিবলৈ আৰু পানীৰ অণুবোৰৰ মাজৰ হাইড্ৰ’জেন বন্ধন ভাঙিবলৈ শক্তিৰ প্ৰয়োজন। নতুন আকৰ্ষণ স্থাপন কৰিলে কম শক্তি মুক্ত হয় যেতিয়া হেল’এলকেন আৰু পানীৰ অণুবোৰৰ মাজত নতুন আকৰ্ষণ স্থাপন কৰা হয় কাৰণ এইবোৰ পানীৰ মূল হাইড্ৰ’জেন বন্ধনতকৈ ইমান শক্তিশালী নহয়। ফলস্বৰূপে, পানীত হেল’এলকেনৰ দ্ৰৱণীয়তা কম। কিন্তু হেল’এলকেনবোৰ জৈৱিক দ্ৰাৱকত দ্ৰৱীভূত হ’বলৈ টানে কাৰণ হেল’এলকেন আৰু দ্ৰাৱক অণুবোৰৰ মাজৰ নতুন আন্তঃআণৱিক আকৰ্ষণবোৰ পৃথক হেল’এলকেন আৰু দ্ৰাৱক অণুবোৰত ভাঙি যোৱাবোৰৰ প্ৰায় একে শক্তিৰ।
10.7 ৰাসায়নিক বিক্ৰিয়া
10.7.1 হেল’এলকেনৰ বিক্ৰিয়া
হেল’এলকেনৰ বিক্ৰিয়াবোৰ নিম্নলিখিত শ্ৰেণীত বিভক্ত কৰিব পাৰি: 1. নিউক্লিফিলিক প্ৰতিস্থাপন 2. নিৰ্মূলণ বিক্ৰিয়া 3. ধাতুৰ সৈতে বিক্ৰিয়া।
(1) নিউক্লিফিলিক প্ৰতিস্থাপন বিক্ৰিয়া আপুনি শ্ৰেণী XI-ত শিকিছিল যে নিউক্লিফিলবোৰ ইলেক্ট্ৰন সমৃদ্ধ প্রজাতি। সেয়েহে, ইহঁতে আধাৰ অণুটোৰ সেই অংশত আক্ৰমণ কৰে যিটো ইলেক্ট্ৰনৰ অভাৱযুক্ত। যি বিক্ৰিয়াত এটা নিউক্লিফিলে অণু এটাত ইতিমধ্যে থকা নিউক্লিফিলক প্ৰতিস্থাপন কৰে তাক নিউক্লিফিলিক প্ৰতিস্থাপন বিক্ৰিয়া বুলি কোৱা হয়। হেল’এলকেনবোৰ এই বিক্ৰিয়াত








