অধ্যায় ০৩ মৌলৰ শ্ৰেণীবিভাজন আৰু ধৰ্মৰ পর্যায়তা
“পিৰিয়ডিক টেবুল হৈছে নিঃসন্দেহে ৰসায়ন বিজ্ঞানৰ আটাইতকৈ গুৰুত্বপূৰ্ণ ধাৰণা, তত্ত্ব আৰু প্ৰয়োগ দুয়োটা দিশতে। ইয়াৰ সহায়ত ছাত্ৰ-ছাত্ৰীয়ে দৈনন্দিন অধ্যয়ন কৰে, ই পেছাদাৰীসকলক গৱেষণাৰ নতুন দিশৰ সন্ধান দিয়ে আৰু সমগ্ৰ ৰসায়ন বিজ্ঞানক সংক্ষিপ্তভাৱে সজোৱাত সহায় কৰে। ই এনে এক উল্লেখযোগ্য প্ৰদৰ্শন যে ৰাসায়নিক মৌলবোৰ এটা উলমি-পালমি থকা সত্তাৰ সমষ্টি নহয়, বৰঞ্চ ইহঁতে একেধৰণৰ প্ৰৱণতা দেখুৱায় আৰু পৰিয়াল হিচাপে একেলগে থাকে। পিৰিয়ডিক টেবুলৰ জ্ঞান ৰসায়নৰ মৌলিক গঠন খণ্ড ৰাসায়নিক মৌলৰ পৰা বিশ্বখন কেনেকৈ গঠিত হৈছে বুজিব বিচৰা প্ৰত্যেকজনৰ বাবে অতি প্ৰয়োজনীয়।”
গ্লেন টি. চিবৰ্গ
এই এককত, আমি পিৰিয়ডিক টেবুলৰ ঐতিহাসিক বিকাশ, যিদৰে ই বৰ্তমান আছে, আৰু আধুনিক পিৰিয়ডিক সূত্ৰ অধ্যয়ন কৰিম। আমি ইয়াও শিকিম যে পৰমাণুৰ ইলেকট্ৰনীয় বিন্যাসৰ যুক্তিসংগত ফলাফল হিচাপে পিৰিয়ডিক শ্ৰেণীবিভাজন কেনেকৈ আহে। শেষত, আমি মৌলবোৰৰ ভৌতিক আৰু ৰাসায়নিক ধৰ্মৰ কিছুমান পিৰিয়ডিক প্ৰৱণতা পৰীক্ষা কৰিম।
৩.১ আমি মৌলবোৰক শ্ৰেণীবিভাজন কৰাৰ প্ৰয়োজনীয়তা কিয়? [৭৪]
আমি এতিয়ালৈকে জানো যে মৌলবোৰ সকলো ধৰণৰ পদাৰ্থৰ মৌলিক একক। ১৮০০ চনত, কেৱল ৩১টা মৌলহে জনা গৈছিল। ১৮৬৫ চনলৈকে, চিনাক্ত কৰা মৌলৰ সংখ্যা দুগুণতকৈও বাঢ়ি ৬৩ লৈ গৈছিল। বৰ্তমান ১১৪টা মৌল জনা গৈছে। ইয়াৰে, সদ্য আৱিষ্কাৰ কৰা মৌলবোৰ মানুহে তৈয়াৰ কৰা। নতুন মৌল সংশ্লেষণ কৰাৰ চেষ্টা অব্যাহত আছে। ইমান বেছি সংখ্যক মৌলৰ বাবে এই মৌলবোৰ আৰু ইহঁতৰ অসংখ্য যৌগৰ ৰসায়ন পৃথকভাৱে অধ্যয়ন কৰাটো অতি কঠিন। এই সমস্যা সহজ কৰিবলৈ, বিজ্ঞানীসকলে মৌলবোৰ শ্ৰেণীবিভাজন কৰি তেওঁলোকৰ জ্ঞানক প্ৰণালীবদ্ধভাৱে সংগঠিত কৰাৰ এক পদ্ধতিগত উপায়ৰ সন্ধান কৰিলে। ই কেৱল মৌলৰ বিষয়ে জনা ৰাসায়নিক তথ্যবোৰ যুক্তিসংগত কৰাই নহয়, বৰঞ্চ অধিক অধ্যয়নৰ বাবে নতুন তথ্যৰ ভৱিষ্যৎবাণীও কৰিব পাৰে।
৩.২ পিৰিয়ডিক শ্ৰেণীবিভাজনৰ উৎপত্তি [৭৫-৭৭]
মৌলবোৰক গোটত ভাগ কৰা আৰু পিৰিয়ডিক সূত্ৰ আৰু পিৰিয়ডিক টেবুলৰ বিকাশ হৈছে বহুতো বিজ্ঞানীৰ নিৰীক্ষণ আৰু পৰীক্ষণৰ জৰিয়তে অৰ্জিত জ্ঞানক প্ৰণালীবদ্ধ কৰাৰ ফলাফল। জাৰ্মান ৰসায়নবিদ জোহান ডবাৰেইনাৰে ১৮০০ চনৰ আৰম্ভণিতে মৌলৰ ধৰ্মৰ মাজত থকা প্ৰৱণতাৰ ধাৰণাটো প্ৰথমবাৰৰ বাবে বিবেচনা কৰিছিল। ১৮২৯ চনলৈকে তেওঁ কেইবাটাও তিনিটা মৌলৰ গোটৰ (ট্ৰায়াড) ভৌতিক আৰু ৰাসায়নিক ধৰ্মৰ মাজত সাদৃশ্য লক্ষ্য কৰিলে। প্ৰতিটো ক্ষেত্ৰতে, তেওঁ লক্ষ্য কৰিলে যে প্ৰতিটো ট্ৰায়াডৰ মাজৰ মৌলটোৰ পাৰমাণৱিক ভৰ আন দুটাৰ পাৰমাণৱিক ভৰৰ মাজৰ প্ৰায় মাজবিন্দুত থাকে (তালিকা ৩.১)। লগতে মাজৰ মৌলটোৰ ধৰ্মবোৰ আন দুটা সদস্যৰ মাজৰ ধৰ্মৰ মাজত থাকে।
তালিকা ৩.১ ডবাৰেইনাৰৰ ট্ৰায়াড
| মৌল | পাৰমাণৱিক ভৰ |
মৌল | পাৰমাণৱিক ভৰ |
মৌল | পাৰমাণৱিক ভৰ |
|---|---|---|---|---|---|
| $\mathbf{L i}$ | 7 | $\mathbf{C a}$ | 40 | $\mathbf{C l}$ | 35.5 |
| $\mathbf{N a}$ | 23 | $\mathbf{S r}$ | 88 | $\mathbf{B r}$ | 80 |
| $\mathbf{K}$ | 39 | $\mathbf{B a}$ | 137 | $\mathbf{I}$ | 127 |
ডবাৰেইনাৰৰ সম্পৰ্ক, যাক ট্ৰায়াডৰ সূত্ৰ বুলি কোৱা হয়, কেৱল কেইটামান মৌলৰ বাবেহে কাম কৰা যেন লাগিল, গতিকে ইয়াক কাকতালীয় বুলি ধৰা হ’ল। মৌলবোৰ শ্ৰেণীবিভাজন কৰাৰ পৰৱৰ্তী প্ৰচেষ্টা এজন ফৰাচী ভূতত্ত্ববিদ এ.ই.বি. ডি চেঙ্কুৰটোৱাই ১৮৬২ চনত কৰিছিল। তেওঁ তেতিয়াৰ জনা মৌলবোৰ পাৰমাণৱিক ভৰৰ উৰ্ধ্বক্ৰমত সজাই এক চিলিণ্ডাৰ আকৃতিৰ মৌলৰ তালিকা তৈয়াৰ কৰি ধৰ্মৰ পিৰিয়ডিক পুনৰাবৃত্তি প্ৰদৰ্শন কৰিলে। ইয়েও বেছি মনোযোগ আকৰ্ষণ কৰিব পৰা নাই। ইংৰাজ ৰসায়নবিদ জন আলেকজেণ্ডাৰ নিউলেণ্ডছে ১৮৬৫ চনত অষ্টকৰ সূত্ৰ প্ৰতিপাদন কৰিলে। তেওঁ মৌলবোৰ পাৰমাণৱিক ভৰৰ উৰ্ধ্বক্ৰমত সজাই লক্ষ্য কৰিলে যে প্ৰতিটো অষ্টম মৌলৰ ধৰ্ম প্ৰথম মৌলটোৰ দৰে একে (তালিকা ৩.২)। সম্পৰ্কটো আছিল ঠিক যেনেকৈ সংগীতৰ অষ্টকত প্ৰতিটো অষ্টম সুৰে প্ৰথম সুৰটোক স্মৰণ কৰায়। নিউলেণ্ডছৰ অষ্টকৰ সূত্ৰ কেৱল কেলছিয়ামলৈকে থকা মৌলবোৰৰ বাবেহে সঁচা যেন লাগিল। যদিও তেতিয়া তেওঁৰ ধাৰণাটো বহুলভাৱে গ্ৰহণ কৰা হোৱা নাছিল, তেওঁৰ কামৰ বাবে পিছত ১৮৮৭ চনত লণ্ডনৰ ৰয়েল ছ’চাইটিয়ে তেওঁক ডেভি পদক প্ৰদান কৰিছিল।
আমি আজি যেনেকৈ জানো, পিৰিয়ডিক সূত্ৰই ইয়াৰ বিকাশ ৰাছিয়ান ৰসায়নবিদ দিমিট্ৰি মেণ্ডেলিভ (১৮৩৪-১৯০৭) আৰু জাৰ্মান ৰসায়নবিদ লথাৰ মেয়াৰ (১৮৩০-১৮৯৫)ৰ ওচৰত ঋণী।
স্বাধীনভাৱে কাম কৰি, দুয়োজন ৰসায়নবিদে ১৮৬৯ চনত প্ৰস্তাৱ দিলে যে মৌলবোৰ পাৰমাণৱিক ভৰৰ উৰ্ধ্বক্ৰমত সজালে, নিয়মীয়া অন্তৰালত ভৌতিক আৰু ৰাসায়নিক ধৰ্মৰ সাদৃশ্য দেখা দিয়ে। লথাৰ মেয়াৰে পাৰমাণৱিক আয়তন, গলনাংক আৰু উতলাংকৰ দৰে ভৌতিক ধৰ্মবোৰ পাৰমাণৱিক ভৰৰ বিপৰীতে প্লট কৰি এক পিৰিয়ডিকভাৱে পুনৰাবৃত্তি হোৱা নমুনা পাইছিল। নিউলেণ্ডছৰ বিপৰীতে, লথাৰ মেয়াৰে সেই পুনৰাবৃত্তি হোৱা নমুনাৰ দৈৰ্ঘ্যৰ পৰিৱৰ্তন লক্ষ্য কৰিছিল। ১৮৬৮ চনলৈকে, লথাৰ মেয়াৰে মৌলৰ এটা তালিকা বিকশিত কৰিছিল যি আধুনিক পিৰিয়ডিক টেবুলৰ সৈতে বহুত মিল আছে। অৱশ্যে, দিমিট্ৰি মেণ্ডেলিভৰ কামৰ পিছতহে তেওঁৰ কাম প্ৰকাশিত হৈছিল, যিজন বিজ্ঞানীক সাধাৰণতে আধুনিক পিৰিয়ডিক টেবুলৰ বিকাশৰ বাবে কৃতিত্ব দিয়া হয়।
তালিকা ৩.২ নিউলেণ্ডছৰ অষ্টক
| মৌল | $\mathbf{L i}$ | $\mathbf{B e}$ | $\mathbf{B}$ | $\mathbf{C}$ | $\mathbf{N}$ | $\mathbf{O}$ | $\mathbf{F}$ |
|---|---|---|---|---|---|---|---|
| পাৰ. ভ. | 7 | 9 | 11 | 12 | 14 | 16 | 19 |
| মৌল | $\mathbf{N a}$ | $\mathbf{M g}$ | $\mathbf{A l}$ | $\mathbf{S i}$ | $\mathbf{P}$ | $\mathbf{S}$ | $\mathbf{C l}$ |
| পাৰ. ভ. | 23 | 24 | 27 | 29 | 31 | 32 | 35.5 |
| মৌল | $\mathbf{K}$ | $\mathbf{C a}$ | |||||
| পাৰ. ভ. | 39 | 40 |
ডবাৰেইনাৰে পিৰিয়ডিক সম্পৰ্কৰ অধ্যয়ন আৰম্ভ কৰাৰ সময়তে, মেণ্ডেলিভেই আছিল যিয়ে প্ৰথমবাৰৰ বাবে পিৰিয়ডিক সূত্ৰ প্ৰকাশ কৰাৰ দায়িত্ব লৈছিল। ইয়াক তলত দিয়া ধৰণে উল্লেখ কৰা হৈছে:
মৌলবোৰৰ ধৰ্মবোৰ হৈছে ইহঁতৰ পাৰমাণৱিক ভৰৰ এক পিৰিয়ডিক ফলন।
মেণ্ডেলিভে মৌলবোৰক তেওঁলোকৰ পাৰমাণৱিক ভৰৰ উৰ্ধ্বক্ৰমত এটা টেবুলৰ আনুভূমিক শাৰী আৰু উলম্ব স্তম্ভত এনেদৰে সজাইছিল যে একে ধৰ্মৰ মৌলবোৰে একে উলম্ব স্তম্ভ বা গোট অধিকাৰ কৰিছিল। মেণ্ডেলিভৰ মৌল শ্ৰেণীবিভাজন কৰাৰ পদ্ধতি লথাৰ মেয়াৰৰ পদ্ধতিতকৈ অধিক বিশদ আছিল। তেওঁ পিৰিয়ডিকতাৰ গুৰুত্ব সম্পূৰ্ণৰূপে চিনাক্ত কৰিছিল আৰু মৌলবোৰ শ্ৰেণীবিভাজন কৰিবলৈ ভৌতিক আৰু ৰাসায়নিক ধৰ্মৰ এক বিস্তৃত পৰিসৰ ব্যৱহাৰ কৰিছিল। বিশেষকৈ, মেণ্ডেলিভে মৌলবোৰে গঠন কৰা যৌগৰ অভিজ্ঞতামূলক সূত্ৰ আৰু ধৰ্মৰ সাদৃশ্যৰ ওপৰত নিৰ্ভৰ কৰিছিল। তেওঁ উপলব্ধি কৰিলে যে যদি পাৰমাণৱিক ভৰৰ ক্ৰম কঠোৰভাৱে অনুসৰণ কৰা হয়, তেন্তে কিছুমান মৌলে তেওঁৰ শ্ৰেণীবিভাজনৰ পদ্ধতিৰ সৈতে খাপ নাখায়। তেওঁ পাৰমাণৱিক ভৰৰ ক্ৰমক উপেক্ষা কৰি, ভাবিলে যে পাৰমাণৱিক জোখবোৰ ভুল হ’ব পাৰে, আৰু একে ধৰ্মৰ মৌলবোৰ একেলগে ৰাখিলে। উদাহৰণস্বৰূপে, টেলুৰিয়াম (গোট VI)তকৈ কম পাৰমাণৱিক ভৰ থকা আয়’ডিনক ধৰ্মৰ সাদৃশ্যৰ বাবে ফ্লুৰিন, ক্ল’ৰিন, ব্ৰ’মিনৰ সৈতে গোট VII ত ৰখা হৈছিল (চিত্ৰ ৩.১)। একে সময়তে, একে গোটত একে ধৰ্মৰ মৌলবোৰ সজোৱাৰ তেওঁৰ প্ৰাথমিক লক্ষ্য ৰাখি, তেওঁ প্ৰস্তাৱ দিলে যে কিছুমান মৌল এতিয়াও আৱিষ্কাৰ হোৱা নাই আৰু সেয়েহে তালিকাত কেইবাটাও খালী ঠাই এৰি দিলে। উদাহৰণস্বৰূপে, গেলিয়াম আৰু জাৰ্মেনিয়াম দুয়োটাই মেণ্ডেলিভে তেওঁৰ পিৰিয়ডিক টেবুল প্ৰকাশ কৰাৰ সময়ত অজ্ঞাত আছিল। তেওঁ এলুমিনিয়ামৰ তলত আৰু চিলিকনৰ তলত খালী ঠাই এৰি দিলে, আৰু এই মৌলবোৰক একা-এলুমিনিয়াম আৰু একা-চিলিকন বুলি নামকৰণ কৰিলে। মেণ্ডেলিভে কেৱল গেলিয়াম আৰু জাৰ্মেনিয়ামৰ অস্তিত্বৰ ভৱিষ্যৎবাণী কৰাই নহয়, বৰঞ্চ ইহঁতৰ কিছুমান সাধাৰণ ভৌতিক ধৰ্মৰ বৰ্ণনাও দিছিল। এই মৌলবোৰ পিছত আৱিষ্কাৰ কৰা হৈছিল। মেণ্ডেলিভে এই মৌলবোৰৰ বাবে ভৱিষ্যৎবাণী কৰা কিছুমান ধৰ্ম আৰু পৰীক্ষামূলকভাৱে পোৱা ধৰ্মবোৰ তালিকা ৩.৩ ত তালিকাভুক্ত কৰা হৈছে।
মেণ্ডেলিভৰ পৰিমাণগত ভৱিষ্যৎবাণীৰ সাহস আৰু ইয়াৰ অন্তিম সফলতাই তেওঁক আৰু তেওঁৰ পিৰিয়ডিক টেবুলক বিখ্যাত কৰি তুলিলে। ১৯০৫ চনত প্ৰকাশিত মেণ্ডেলিভৰ পিৰিয়ডিক টেবুল চিত্ৰ ৩.১ ত দেখুওৱা হৈছে।
তালিকা ৩.৩ একা-এলুমিনিয়াম (গেলিয়াম) আৰু একা-চিলিকন (জাৰ্মেনিয়াম) মৌলৰ বাবে মেণ্ডেলিভৰ ভৱিষ্যৎবাণী
| ধৰ্ম | একা-এলুমিনিয়াম (ভৱিষ্যৎবাণী) |
গেলিয়াম (পোৱা) |
একা-চিলিকন (ভৱিষ্যৎবাণী) |
জাৰ্মেনিয়াম (পোৱা) |
|---|---|---|---|---|
| পাৰমাণৱিক ভৰ | 68 | 70 | 72 | 72.6 |
| ঘনত্ব/(g/cm $\mathbf{)}$ | 5.9 | 5.94 | 5.5 | 5.36 |
| গলনাংক/K | $\mathrm{Low}$ | 302.93 | $\mathrm{High}$ | 1231 |
| অক্সাইডৰ সূত্ৰ | $\mathrm{E}_2 \mathrm{O}_3$ | $\mathrm{Ga}_2 \mathrm{O}_3$ | $\mathrm{EO}_{2}$ | $\mathrm{GeO}_{2}$ |
| ক্ল’ৰাইডৰ সূত্ৰ | $\mathrm{E} \mathrm{Cl}_{3}$ | $\mathrm{GaCl}_{3}$ | $\mathrm{ECl}_{4}$ | $\mathrm{GeCl}_{4}$ |
গোট আৰু শৃংখলাত মৌলৰ পিৰিয়ডিক ব্যৱস্থা

চিত্ৰ ৩.১ আগতে প্ৰকাশিত মেণ্ডেলিভৰ পিৰিয়ডিক টেবুল
৩.৩ আধুনিক পিৰিয়ডিক সূত্ৰ আৰু পিৰিয়ডিক টেবুলৰ বৰ্তমান ৰূপ [৭৮]
আমি মনত ৰাখিব লাগিব যে যেতিয়া মেণ্ডেলিভে তেওঁৰ পিৰিয়ডিক টেবুল বিকশিত কৰিছিল, তেতিয়া ৰসায়নবিদসকলে পৰমাণুৰ আভ্যন্তৰীণ গঠনৰ বিষয়ে একো নাজানিছিল। অৱশ্যে, $20^{\text {th }}$ শতিকাৰ আৰম্ভণিতে উপ-পাৰমাণৱিক কণাৰ তত্ত্বৰ বিষয়ে গভীৰ বিকাশ ঘটিছিল। ১৯১৩ চনত, ইংৰাজ পদাৰ্থবিজ্ঞানী হেনৰী ম’জলিয়ে মৌলবোৰৰ বৈশিষ্ট্যপূৰ্ণ $X$-ৰশ্মি বৰ্ণালীত নিয়মীয়তা লক্ষ্য কৰিলে। $\sqrt{v}$ (য’ত $V$ হৈছে $X$-ৰশ্মিৰ কম্পনাংক) বনাম পাৰমাণৱিক সংখ্যা $(Z)$ৰ প্লটে এডাল সৰল ৰেখা দিলে আৰু $\sqrt{v}$ বনাম পাৰমাণৱিক ভৰৰ প্লটে নিদিলে। তেওঁ তেনেদৰে দেখুৱালে যে পাৰমাণৱিক সংখ্যা হৈছে এটা মৌলৰ ইয়াৰ পাৰমাণৱিক ভৰতকৈ অধিক মৌলিক ধৰ্ম। মেণ্ডেলিভৰ পিৰিয়ডিক সূত্ৰ সেয়েহে তদনুযায়ী সংশোধন কৰা হ’ল। ইয়াক আধুনিক পিৰিয়ডিক সূত্ৰ বুলি জনা যায় আৰু তলত দিয়া ধৰণে উল্লেখ কৰিব পাৰি:
মৌলবোৰৰ ভৌতিক আৰু ৰাসায়নিক ধৰ্মবোৰ হৈছে ইহঁতৰ পাৰমাণৱিক সংখ্যাৰ পিৰিয়ডিক ফলন।
পিৰিয়ডিক সূত্ৰই ৯৪টা প্ৰাকৃতিকভাৱে পোৱা মৌলৰ মাজত গুৰুত্বপূৰ্ণ সাদৃশ্য প্ৰকাশ কৰিলে (নেপচুনিয়াম আৰু প্লুটোনিয়াম যেনেকৈ এক্টিনিয়াম আৰু প্ৰট’এক্টিনিয়াম ইউৰেনিয়ামৰ এটা আকৰ পিচ ব্লেণ্ডতো পোৱা যায়)। ই অজৈৱিক ৰসায়নত নতুনকৈ আগ্ৰহ সৃষ্টি কৰিলে আৰু কৃত্ৰিমভাৱে উৎপাদিত চমু জীৱনকালৰ মৌলৰ সৃষ্টিৰ সৈতে বৰ্তমানলৈকে আহিছে।
আপুনি মনত পেলাব পাৰে যে পাৰমাণৱিক সংখ্যা নিউক্লীয় আধানৰ (অৰ্থাৎ, প্ৰটনৰ সংখ্যা) বা এটা নিৰপেক্ষ পৰমাণুত ইলেকট্ৰনৰ সংখ্যাৰ সমান। তেতিয়া মৌলৰ পিৰিয়ডিকতাত কোৱাণ্টাম সংখ্যা আৰু ইলেকট্ৰনীয় বিন্যাসৰ গুৰুত্ব কল্পনা কৰাটো সহজ হয়। প্ৰকৃততে, এতিয়া স্বীকৃত যে পিৰিয়ডিক সূত্ৰ মূলতঃ ইলেকট্ৰনীয় বিন্যাসৰ পিৰিয়ডিক পৰিৱৰ্তনৰ ফলাফল, যিয়ে প্ৰকৃততে মৌল আৰু ইহঁতৰ যৌগৰ ভৌতিক আৰু ৰাসায়নিক ধৰ্ম নিৰ্ধাৰণ কৰে।
পিৰিয়ডিক টেবুলৰ বহুতো ৰূপ সময়ে সময়ে উদ্ভাৱন কৰা হৈছে। কিছুমান ৰূপে ৰাসায়নিক বিক্ৰিয়া আৰু যোজ্যতাৰ ওপৰত গুৰুত্ব দিয়ে, আনহাতে আনবোৰে মৌলৰ ইলেকট্ৰনীয় বিন্যাসৰ ওপৰত গুৰুত্ব দিয়ে। এটা আধুনিক সংস্কৰণ, যাক মৌলৰ পিৰিয়ডিক টেবুলৰ “দীঘল ৰূপ” বুলি কোৱা হয় (চিত্ৰ ৩.২), আটাইতকৈ সুবিধাজনক আৰু বহুলভাৱে ব্যৱহৃত। আনুভূমিক শাৰীবোৰ (যাক মেণ্ডেলিভে শৃংখলা বুলি কৈছিল)ক পিৰিয়ড বুলি কোৱা হয় আৰু উলম্ব স্তম্ভবোৰক গোট বুলি কোৱা হয়। যিবোৰ মৌলৰ পৰমাণুত একে বহিঃস্থ ইলেকট্ৰনীয় বিন্যাস থাকে, সেইবোৰ উলম্ব স্তম্ভত সজোৱা হয়, যাক গোট বা পৰিয়াল বুলি কোৱা হয়। আন্তঃৰাষ্ট্ৰীয় বিশুদ্ধ আৰু প্ৰয়োগিক ৰসায়ন সংঘ (আইউপিএচি)ৰ পৰামৰ্শ অনুসৰি, গোটবোৰক ১ ৰ পৰা ১৮ লৈ সংখ্যক কৰা হৈছে, যিয়ে গোট IA … VIIA, VIII, IB … VIIB আৰু ০ ৰ পুৰণি নোটেচনক প্ৰতিস্থাপিত কৰিছে।
মুঠ সাতটা পিৰিয়ড আছে। পিৰিয়ড নম্বৰে পিৰিয়ডত থকা মৌলবোৰৰ সৰ্বোচ্চ মুখ্য কোৱাণ্টাম সংখ্যা $(n)$ৰ সৈতে মিল খায়। প্ৰথম পিৰিয়ডত ২টা মৌল থাকে। পৰৱৰ্তী পিৰিয়ডবোৰত ক্ৰমে $8,8,18,18$ আৰু ৩২টা মৌল থাকে। সপ্তম পিৰিয়ডটো অসম্পূৰ্ণ আৰু ষষ্ঠ পিৰিয়ডৰ দৰে ইয়াৰ তাত্ত্বিক সৰ্বোচ্চ সীমা (কোৱাণ্টাম সংখ্যাৰ ভিত্তিত) ৩২টা মৌল হ’ব। পিৰিয়ডিক টেবুলৰ এই ৰূপত, ষষ্ঠ আৰু সপ্তম পিৰিয়ডৰ ১৪টা মৌল (ক্ৰমে লেঞ্থেনয়েড আৰু এক্টিনয়েড) তলত পৃথক পেনেলত ৰখা হৈছে[^0]।
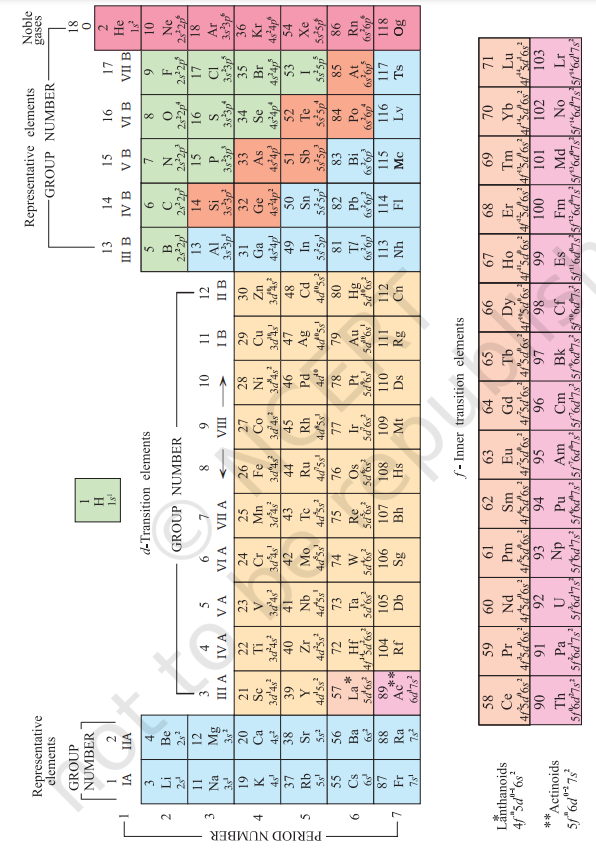
চিত্ৰ ৩.২ মৌলৰ পিৰিয়ডিক টেবুলৰ দীঘল ৰূপ, ইহঁতৰ পাৰমাণৱিক সংখ্যা আৰু ভূমি অৱস্থাৰ বহিঃস্থ ইলেকট্ৰনীয় বিন্যাসৰ সৈতে। গোটবোৰক ১৯৮৪ চনৰ আইউপিএচিৰ পৰামৰ্শ অনুসৰি ১-১৮ লৈ সংখ্যক কৰা হৈছে। এই নোটেচনে মৌলবোৰৰ বাবে IA–VIIA, VIII, IB–VIIB আৰু ০ ৰ পুৰণি সংখ্যক কৰাৰ পদ্ধতিক প্ৰতিস্থাপিত কৰিছে।
৩.৪ পাৰমাণৱিক সংখ্যা > ১০০ থকা মৌলৰ নামকৰণ [৭৮-৮১]
নতুন মৌলৰ নামকৰণ পৰম্পৰাগতভাৱে আৱিষ্কাৰক (বা আৱিষ্কাৰকসকল)ৰ বিশেষাধিকাৰ আছিল আৰু প্ৰস্তাৱিত নামটো আইউপিএচিয়ে অনুমোদন কৰিছিল। সৰু কালত ইয়াই কিছু বিতৰ্কৰ সৃষ্টি কৰিছিল। অতি উচ্চ পাৰমাণৱিক সংখ্যা থকা নতুন মৌলবোৰ ইমানেই অস্থিৰ যে কেৱল অতি সূক্ষ্ম পৰিমাণ, কেতিয়াবা কেৱল কেইটামান পৰমাণুহে পোৱা যায়। সেয়েহে ইহঁতৰ সংশ্লেষণ আৰু বৈশিষ্ট্যায়নৰ বাবে অতি অত্যাধুনিক ব্যয়বহুল সঁজুলি আৰু পৰীক্ষাগাৰৰ প্ৰয়োজন। এনে কাম পৃথিৱীৰ কেৱল কেইটামান পৰীক্ষাগাৰত প্ৰতিযোগিতামূলক ভাৱে কৰা হয়। বিজ্ঞানীসকলে, নতুন মৌলটোৰ নিৰ্ভৰযোগ্য তথ্য সংগ্ৰহ কৰাৰ আগতে, কেতিয়াবা ইয়াৰ আৱিষ্কাৰৰ দাবী কৰাৰ প্ৰলোভনত পৰে। উদাহৰণস্বৰূপে, আমেৰিকান আৰু ছ’ভিয়েট বিজ্ঞানী দুয়োজনে ১০৪ নং মৌল আৱিষ্কাৰ কৰাৰ কৃতিত্বৰ দাবী কৰিছিল। আমেৰিকানসকলে ইয়াক ৰাদাৰফৰ্ডিয়াম বুলি নামকৰণ কৰিছিল আনহাতে ছ’ভিয়েটসকলে ইয়াক কুৰ্চাটভিয়াম বুলি নামকৰণ কৰিছিল। এনে সমস্যা এৰাবলৈ, আইউপিএচিয়ে পৰামৰ্শ দিছে যে যেতিয়ালৈকে নতুন মৌলৰ আৱিষ্কাৰ প্ৰমাণিত নহয়, আৰু ইয়াৰ নাম আনুষ্ঠানিকভাৱে স্বীকৃত নহয়, তেতিয়ালৈকে মৌলটোৰ পাৰমাণৱিক সংখ্যাৰ পৰা পোনপটীয়াকৈ সংখ্যামূলক মূল ব্যৱহাৰ কৰি এক প্ৰণালীবদ্ধ নামকৰণ কৰা হওক। এইবোৰ তালিকা ৩.৪ ত দেখুওৱা হৈছে। মূলবোৰ পাৰমাণৱিক সংখ্যা গঠন কৰা অংকবোৰৰ ক্ৰমত একেলগে লগোৱা হয় আৰু শেষত “ইয়াম” যোগ কৰা হয়। $Z$ ১০০ তকৈ বেছি থকা মৌলবোৰৰ বাবে আইউপিএচি নামবোৰ তালিকা ৩.৫ ত দেখুওৱা হৈছে।
তালিকা ৩.৪ মৌলৰ আইউপিএচি নামকৰণৰ বাবে নোটেচন
| অংক | নাম | সংক্ষিপ্ত ৰূপ |
|---|---|---|
| 0 | nil | $\mathrm{n}$ |
| 1 | un | $\mathrm{u}$ |
| 2 | bi | $\mathrm{b}$ |
| 3 | tri | $\mathrm{t}$ |
| 4 | quad | $\mathrm{q}$ |
| 5 | pent | $\mathrm{p}$ |
| 6 | hex | $\mathrm{h}$ |
| 7 | sept | $\mathrm{s}$ |
| 8 | oct | $\mathrm{o}$ |
| 9 | enn | $\mathrm{e}$ |
তালিকা ৩.৫ পাৰমাণৱিক সংখ্যা ১০০ তকৈ বেছি থকা মৌলৰ নামকৰণ
| পাৰমাণৱিক সংখ্যা |
আইউপিএচি নামকৰণ অনুসৰি নাম |
চিহ্ন | আইউপিএচি আনুষ্ঠানিক নাম |
আইউপিএচি চিহ্ন |
|---|---|---|---|---|
| 101 | Unnilunium | Unu | Mendelevium | $\mathrm{Md}$ |
| 102 | Unnilbium | Unb | Nobelium | No |
| 103 | Unniltrium | Unt | Lawrencium | $\mathrm{Lr}$ |
| 104 | Unnilquadium | Unq | Rutherfordium | $\mathrm{Rf}$ |
| 105 | Unnilpentium | Unp | Dubnium | $\mathrm{Db}$ |
| 106 | Unnilhexium | Unh | Seaborgium | $\mathrm{Sg}$ |
| 107 | Unnilseptium | Uns | Bohrium | $\mathrm{Bh}$ |
| 108 | Unniloctium | Uno | Hassium | $\mathrm{Hs}$ |
| 109 | Unnilennium | Une | Meitnerium | $\mathrm{Mt}$ |
| 110 | Ununnillium | Uun | Darmstadtium | $\mathrm{Ds}$ |
| 111 | Unununnium | Uuu | Rontgenium | $\mathrm{Rg}$ |
| 112 | Ununbium | Uub | Copernicium | $\mathrm{Cn}$ |
| 113 | Ununtrium | Uut | Nihonium | $\mathrm{Nh}$ |
| 114 | Ununquadium | Uuq | Flerovium | $\mathrm{Fl}$ |
| 115 | Ununpentium | Uup | Moscovium | $\mathrm{Mc}$ |
| 116 | Ununhexium | Uuh | Livermorium | $\mathrm{Lv}$ |
| 117 | Ununseptium | Uus | Tennessine | $\mathrm{Ts}$ |
| 118 | Ununoctium | Uuo | Oganesson | $\mathrm{Og}$ |
এইদৰে, নতুন মৌলটোৱে প্ৰথমে এটা অস্থায়ী নাম পায়, য’ত চিহ্নটো তিনিটা আখৰৰে গঠিত। পিছত স্থায়ী নাম আৰু চিহ্ন প্ৰতিটো দেশৰ আইউপিএচি প্ৰতিনিধিৰ ভোটৰ দ্বাৰা দিয়া হয়। স্থায়ী নামটোৱে সেই দেশক (বা দেশৰ ৰাজ্যক) প্ৰতিফলিত কৰিব পাৰে য’ত মৌলটো আৱিষ্কাৰ কৰা হৈছিল, বা এজন উল্লেখযোগ্য বিজ্ঞানীক শ্ৰদ্ধাঞ্জলি জনাব পাৰে। এতিয়ালৈকে, ১১৮ লৈকে পাৰমাণৱিক সংখ্যা থকা মৌলবোৰ আৱিষ্কাৰ কৰা হৈছে। সকলো মৌলৰ আনুষ্ঠানিক নাম আইউপিএচিয়ে ঘোষণা কৰিছে।
সমস্যা ৩.১
পাৰমাণৱিক সংখ্যা ১২০ থকা মৌলটোৰ বাবে আইউপিএচি নাম আৰু চিহ্ন কি হ’ব?
সমাধান
তালিকা ৩.৪ ৰ পৰা, ১, ২ আৰু ০ ৰ মূলবোৰ হৈছে ক্ৰমে un, bi আৰু nil। গতিকে, চিহ্ন আৰু নাম ক্ৰমে Ubn আৰু unbinilium হ’ব।
৩.৫ মৌলৰ ইলেকট্ৰনীয় বিন্যাস আৰু পিৰিয়ডিক টেবুল [৮১-৮২]
আগৰ এককত আমি শিকিছো যে পৰমাণুত এটা ইলেকট্ৰনক চাৰিটা কোৱাণ্টাম সংখ্যাৰ এক সমষ্টিৰ দ্বাৰা চৰিত্ৰায়িত কৰা হয়, আৰু মুখ্য কোৱাণ্টাম সংখ্যাই ( $n$ ) শেল নামেৰে জনা মুখ্য শক্তি স্তৰ নিৰ্ধাৰণ কৰে। আমি ইলেকট্ৰনবোৰ পৰমাণুৰ বিভিন্ন উপশেলত,












