অধ্যায় ০৮ ৰেডক্স বিক্ৰিয়া
“য’ত জাৰণ হয়, তাত সদায়ই বিজাৰণ হয়। ৰসায়ন বিজ্ঞান মূলতঃ ৰেডক্স ব্যৱস্থাৰ এক অধ্যয়ন।”
ৰসায়ন বিজ্ঞানে বিভিন্ন ধৰণৰ পদাৰ্থ আৰু এটা ধৰণৰ পদাৰ্থৰ পৰা আন এটা ধৰণৰ পদাৰ্থলৈ ৰূপান্তৰৰ সৈতে সম্পৰ্ক ৰাখে। পদাৰ্থৰ এটা ধৰণৰ পৰা আন এটা ধৰণলৈ ৰূপান্তৰ বিভিন্ন ধৰণৰ বিক্ৰিয়াৰ জৰিয়তে সংঘটিত হয়। এনে বিক্ৰিয়াবোৰৰ এক গুৰুত্বপূৰ্ণ শ্ৰেণী হৈছে ৰেডক্স বিক্ৰিয়া। বহুতো পৰিঘটনা, যেনে ভৌতিক আৰু জৈৱিক দুয়োটাতে, ৰেডক্স বিক্ৰিয়া জড়িত হৈ থাকে। এই বিক্ৰিয়াবোৰৰ ঔষধ শিল্প, জৈৱিক, উদ্যোগিক, ধাতুবিদ্যা আৰু কৃষি ক্ষেত্ৰত বহুল ব্যৱহাৰ হয়। এই বিক্ৰিয়াবোৰৰ গুৰুত্ব বিভিন্ন ধৰণৰ ইন্ধন দহন কৰি ঘৰুৱা, যাতায়াত আৰু অন্যান্য বাণিজ্যিক উদ্দেশ্যৰ বাবে শক্তি উৎপাদন, অতি সক্ৰিয় ধাতু আৰু অধাতু নিষ্কাশনৰ বাবে ইলেক্ট্ৰ’কেমিকেল প্ৰক্ৰিয়া, কষ্টিক ছ’ডাৰ দৰে ৰাসায়নিক যৌগ উৎপাদন, শুকান আৰু ভিজা বেটাৰীৰ কাৰ্য্য আৰু ধাতুৰ ক্ষয় আদি ৰেডক্স প্ৰক্ৰিয়াৰ অন্তৰ্গত হোৱাৰ পৰাই স্পষ্ট হৈ পৰে। সৰহ দিন নহয়, হাইড্ৰ’জেন ইক’নমি (ইন্ধন হিচাপে তৰল হাইড্ৰ’জেনৰ ব্যৱহাৰ) আৰু ‘অ’জন গাঁত’ৰ বিকাশৰ দৰে পৰিৱেশগত বিষয়বোৰে ৰেডক্স পৰিঘটনাৰ অধীনত স্থান পাবলৈ আৰম্ভ কৰিছে।
৮.১ ৰেডক্স বিক্ৰিয়াৰ শাস্ত্ৰীয় ধাৰণা - জাৰণ আৰু বিজাৰণ বিক্ৰিয়া [২৩৫-২৩৭]
মূলতঃ, জাৰণ শব্দটো এটা মৌল বা যৌগত অক্সিজেন যোগ হোৱাক বুজাবলৈ ব্যৱহাৰ কৰা হৈছিল। বায়ুমণ্ডলত ডাইঅক্সিজেনৰ উপস্থিতিৰ বাবে (২০%), বহুতো মৌলে ইয়াৰ সৈতে সংযুক্ত হয় আৰু এইটোৱেই প্ৰধান কাৰণ যে সিহঁত সাধাৰণতে পৃথিৱীত নিজৰ অক্সাইডৰ ৰূপত পোৱা যায়। জাৰণৰ সীমিত সংজ্ঞা অনুসৰি তলৰ বিক্ৰিয়াবোৰে জাৰণ প্ৰক্ৰিয়াক প্ৰতিনিধিত্ব কৰে:
$$2 \mathrm{Mg}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{MgO}(\mathrm{s}) \tag{8.1}$$
$$\mathrm{S}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow \mathrm{SO_2}(\mathrm{~g}) \tag{8.2}$$
(৮.১) আৰু (৮.২) বিক্ৰিয়াত, মেগনেছিয়াম আৰু গন্ধক মৌলবোৰ অক্সিজেন যোগ হোৱাৰ বাবে জাৰিত হয়। একেদৰে, মিথেনো অক্সিজেন যোগ হোৱাৰ বাবে জাৰিত হয়।
$$\mathrm{CH} _{4}(\mathrm{~g})+2 \mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g})+2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{7.3}$$
(৮.৩) বিক্ৰিয়াটোৰ সাৱধানী পৰীক্ষণ, য’ত হাইড্ৰ’জেনক অক্সিজেনে সলনি কৰিছে, ৰসায়নবিদসকলক ইয়াৰ পৰা হাইড্ৰ’জেন আঁতৰোৱাৰ দিশত জাৰণক পুনৰ ব্যাখ্যা কৰিবলৈ উৎসাহিত কৰিলে, আৰু সেয়েহে জাৰণ শব্দটোৰ পৰিসৰ এটা পদাৰ্থৰ পৰা হাইড্ৰ’জেন আঁতৰোৱাকো অন্তৰ্ভুক্ত কৰিবলৈ বহল কৰা হ’ল। তলৰ উদাহৰণটো আন এটা বিক্ৰিয়া য’ত হাইড্ৰ’জেন আঁতৰোৱাকো জাৰণ বিক্ৰিয়া হিচাপে উল্লেখ কৰিব পাৰি।
$$ \begin{equation*} 2 \mathrm{H_2} \mathrm{~S}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{~S}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \tag{8.4} \end{equation*} $$
ৰসায়নবিদসকলৰ জ্ঞান বৃদ্ধি হোৱাৰ লগে লগে, (৭.১ ৰ পৰা ৭.৪)ৰ দৰে বিক্ৰিয়াবোৰৰ বাবে জাৰণ শব্দটো সম্প্ৰসাৰিত কৰাটো স্বাভাৱিক আছিল, যিবোৰত অক্সিজেন নাথাকিলেও আন ইলেক্ট্ৰ’নেগেটিভ মৌল থাকে। মেগনেছিয়ামৰ ফ্লুৰিন, ক্ল’ৰিন আৰু গন্ধক আদিৰ সৈতে জাৰণ তলৰ বিক্ৰিয়াবোৰ অনুসৰি সংঘটিত হয়:
$$\operatorname{Mg}(\mathrm{s})+\mathrm{F_2} (\mathrm{~g}) \rightarrow \operatorname{MgF_2} (s) \tag{8.5}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{Cl_2} (g) \rightarrow \mathrm{MgCl_2} (s) \tag{8.6}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{S} (s) \rightarrow \operatorname{MgS}(\mathrm{s}) \tag{8.7}$$
(৭.৫ ৰ পৰা ৭.৭) বিক্ৰিয়াবোৰ জাৰণ বিক্ৰিয়াৰ শ্ৰেণীত অন্তৰ্ভুক্ত কৰাটোৱে ৰসায়নবিদসকলক কেৱল হাইড্ৰ’জেন আঁতৰোৱাক নহয়, ইলেক্ট্ৰ’পজিটিভ মৌল আঁতৰোৱাকো জাৰণ হিচাপে বিবেচনা কৰিবলৈ উৎসাহিত কৰিলে। এইদৰে বিক্ৰিয়াটো:
$$ 2 \mathrm{~K_4} \left[ \mathrm{Fe} ( \mathrm{CN})_{6} \right] ( \mathrm{aq}) + \mathrm{H_2} \mathrm{O_2} ( \mathrm{aq}) \rightarrow 2 \mathrm{~K_3} \left[\mathrm{Fe}( \mathrm{CN})_6 \right] ( \mathrm{aq}) + 2 \mathrm{KOH} ( \mathrm{aq}) $$
ইয়াক পটেছিয়াম ফেৰ’চায়ানাইডে পটেছিয়াম ফেৰিচায়ানাইডলৈ ৰূপান্তৰ হোৱাৰ আগতে ইলেক্ট্ৰ’পজিটিভ মৌল পটেছিয়াম আঁতৰোৱাৰ বাবে জাৰণ হিচাপে ব্যাখ্যা কৰা হয়। সংক্ষিপ্তকৈ, “জাৰণ” শব্দটো এটা পদাৰ্থত অক্সিজেন/ইলেক্ট্ৰ’নেগেটিভ মৌল যোগ হোৱা বা এটা পদাৰ্থৰ পৰা হাইড্ৰ’জেন/ইলেক্ট্ৰ’পজিটিভ মৌল আঁতৰোৱা বুলি সংজ্ঞায়িত কৰা হয়।
আৰম্ভণিতে, বিজাৰণক এটা যৌগৰ পৰা অক্সিজেন আঁতৰোৱা বুলি বিবেচনা কৰা হৈছিল। অৱশ্যে, বিজাৰণ শব্দটো বৰ্তমান এটা পদাৰ্থৰ পৰা অক্সিজেন/ইলেক্ট্ৰ’নেগেটিভ মৌল আঁতৰোৱা বা পদাৰ্থত হাইড্ৰ’জেন/ইলেক্ট্ৰ’পজিটিভ মৌল যোগ হোৱাকো অন্তৰ্ভুক্ত কৰিবলৈ বহল কৰা হৈছে।
ওপৰত দিয়া সংজ্ঞা অনুসৰি, তলৰবোৰ বিজাৰণ প্ৰক্ৰিয়াৰ উদাহৰণ:
$$2 \mathrm{HgO}(\mathrm{s}) \xrightarrow{\Delta} 2 \mathrm{Hg}(\mathrm{l})+\mathrm{O_2}(\mathrm{~g}) \tag{8.8}$$
(মাৰ্কিউৰিক অক্সাইডৰ পৰা অক্সিজেন আঁতৰোৱা)
$$2 \mathrm{FeCl_3}(\mathrm{aq})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{FeCl_2}(\mathrm{aq})+2 \mathrm{HCl}(\mathrm{aq}) \tag{8.9}$$
(ইলেক্ট্ৰ’নেগেটিভ মৌল, ক্ল’ৰিন ফেৰিক ক্ল’ৰাইডৰ পৰা আঁতৰোৱা)
$$\mathrm{CH_2}=\mathrm{CH_2}(\mathrm{~g})+\mathrm{H_2}(\mathrm{~g}) \rightarrow \mathrm{H_3} \mathrm{C}-\mathrm{CH_3}(\mathrm{~g})\tag{8.10}$$
(হাইড্ৰ’জেন যোগ হোৱা)
$$2 \mathrm{HgCl_2}(\mathrm{aq})+\mathrm{SnCl_2}(\mathrm{aq}) \rightarrow \mathrm{Hg_2} \mathrm{Cl_2}(\mathrm{~s})+\mathrm{SnCl_4}(\mathrm{aq})\tag{8.11}$$
(মাৰ্কিউৰিক ক্ল’ৰাইডত পাৰা যোগ হোৱা)
(৮.১১) বিক্ৰিয়াত, ষ্টেনাছ ক্ল’ৰাইডৰ ষ্টেনিক ক্ল’ৰাইডলৈ একে সময়তে জাৰণো সংঘটিত হৈছে কাৰণ ইলেক্ট্ৰ’নেগেটিভ মৌল ক্ল’ৰিন ইয়াত যোগ হৈছে। সোনকালেই অনুভৱ কৰা হ’ল যে জাৰণ আৰু বিজাৰণ সদায় একে সময়তে সংঘটিত হয় (ওপৰত দিয়া সকলো সমীকৰণ পুনৰ পৰীক্ষা কৰিলে স্পষ্ট হ’ব), সেয়েহে, ৰাসায়নিক বিক্ৰিয়াৰ এই শ্ৰেণীৰ বাবে “ৰেডক্স” শব্দটো সৃষ্টি কৰা হ’ল।
সমস্যা ৮.১
তলত দিয়া বিক্ৰিয়াবোৰত, জাৰিত আৰু বিজাৰিত হোৱা species চিনাক্ত কৰক:
(i) $\mathrm{H_2} \mathrm{~S}$ (g) $+\mathrm{Cl_2}$ (g) $\rightarrow 2 \mathrm{HCl}$ (g) $+\mathrm{S}$ (s)
(ii) $3 \mathrm{Fe_3} \mathrm{O_4}$ (s) $+8 \mathrm{Al}$ (s) $\rightarrow 9 \mathrm{Fe}$ (s) $+4 \mathrm{Al_2} \mathrm{O_3}(\mathrm{~s})$
(iii) $2 \mathrm{Na}$ (s) $+\mathrm{H_2}$ (g) $\rightarrow 2 \mathrm{NaH}$ (s)
সমাধান
(i) $\mathrm{H_2} \mathrm{~S}$ জাৰিত হয় কাৰণ অধিক ইলেক্ট্ৰ’নেগেটিভ মৌল, ক্ল’ৰিন হাইড্ৰ’জেনত যোগ হয় (বা অধিক ইলেক্ট্ৰ’পজিটিভ মৌল, হাইড্ৰ’জেন S ৰ পৰা আঁতৰোৱা হৈছে)। ক্ল’ৰিন বিজাৰিত হয় কাৰণ ইয়াত হাইড্ৰ’জেন যোগ হয়।
(ii) এলুমিনিয়াম জাৰিত হয় কাৰণ অক্সিজেন ইয়াত যোগ হয়। ফেৰাছ ফেৰিক অক্সাইড $\left(\mathrm{Fe_3} \mathrm{O_4}\right)$ বিজাৰিত হয় কাৰণ ইয়াৰ পৰা অক্সিজেন আঁতৰোৱা হৈছে।
(iii) ইলেক্ট্ৰ’নেগেটিভিটীৰ ধাৰণাটোৰ সাৱধানী প্ৰয়োগৰ দ্বাৰাহে আমি অনুমান কৰিব পাৰো যে ছ’ডিয়াম জাৰিত হয় আৰু হাইড্ৰ’জেন বিজাৰিত হয়।
ইয়াত বাছনি কৰা বিক্ৰিয়া (iii)ই আমাক ৰেডক্স বিক্ৰিয়া সংজ্ঞায়িত কৰাৰ আন এটা পদ্ধতিৰ বিষয়ে চিন্তা কৰিবলৈ উৎসাহিত কৰে।
৮.২ ইলেক্ট্ৰন স্থানান্তৰ বিক্ৰিয়াৰ দিশত ৰেডক্স বিক্ৰিয়া [২৩৭-২৩৯]
আমি ইতিমধ্যে শিকিছো যে বিক্ৰিয়াবোৰ ৰেডক্স বিক্ৰিয়া কাৰণ এই বিক্ৰিয়াবোৰৰ প্ৰতিটোত ছ’ডিয়াম জাৰিত হয় কাৰণ ছ’ডিয়ামত অক্সিজেন বা অধিক ইলেক্ট্ৰ’নেগেটিভ মৌল যোগ হয়।
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaCl}(\mathrm{s})\tag{8.12}$$
$$4 \mathrm{Na}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na_2} \mathrm{O}(\mathrm{s})\tag{8.13}$$
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{S}(\mathrm{s}) \rightarrow \mathrm{Na_2} \mathrm{~S}(\mathrm{~s}) \tag{8.14}$$
একে সময়তে, ক্ল’ৰিন, অক্সিজেন আৰু গন্ধক বিজাৰিত হয় কাৰণ এইবোৰৰ প্ৰতিটোত ইলেক্ট্ৰ’পজিটিভ মৌল ছ’ডিয়াম যোগ হৈছে। ৰাসায়নিক বন্ধনৰ আমাৰ জ্ঞানৰ পৰা আমি ইয়াও জানো যে ছ’ডিয়াম ক্ল’ৰাইড, ছ’ডিয়াম অক্সাইড আৰু ছ’ডিয়াম ছালফাইড আয়নিক যৌগ আৰু সম্ভৱতঃ $\mathrm{Na}^{+} \mathrm{Cl}^{-}( \mathrm{s}),\left(\mathrm{Na}^{+} \right)_2 \mathrm{O}^{2-}( \mathrm{s})$, আৰু $ \left(\mathrm{Na}^{+} \right)_2$ $\mathrm{S}^{2-}( \mathrm{s})$ হিচাপে লিখা ভাল। উৎপন্ন species বোৰত আধানৰ বিকাশে আমাক (৮.১২ ৰ পৰা ৮.১৪) বিক্ৰিয়াবোৰ তলৰ ধৰণেৰে পুনৰ লিখিবলৈ পৰামৰ্শ দিয়ে:
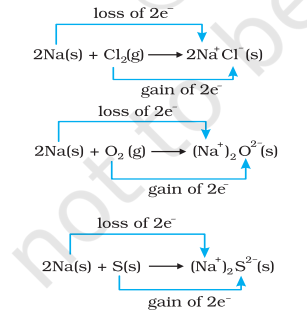
সুবিধাৰ বাবে, ওপৰৰ প্ৰতিটো প্ৰক্ৰিয়াক দুটা পৃথক পদক্ষেপ হিচাপে বিবেচনা কৰিব পাৰি, এটাই ইলেক্ট্ৰন হেৰুওৱাটো জড়িত কৰে আৰু আনটোৱে ইলেক্ট্ৰন লাভ কৰাটো জড়িত কৰে। উদাহৰণস্বৰূপে, আমি এইবোৰৰ এটা, যেনে, ছ’ডিয়াম ক্ল’ৰাইড গঠন, আৰু বিশদভাৱে বৰ্ণনা কৰিব পাৰো।
$2 \mathrm{Na}(\mathrm{s}) \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
$\mathrm{Cl_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{Cl}^{-}(\mathrm{g})$
ওপৰৰ প্ৰতিটো পদক্ষেপক half reaction বোলা হয়, যিয়ে স্পষ্টভাৱে ইলেক্ট্ৰনৰ জড়িততা দেখুৱায়। half reaction বোৰৰ যোগফলে সামগ্ৰিক বিক্ৰিয়াটো দিয়ে:
$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na}^{+} \mathrm{Cl}^{-}(\mathrm{s})$ বা $2 \mathrm{NaCl}(\mathrm{s})$
বিক্ৰিয়া ৮.১২ ৰ পৰা ৮.১৪ লে সূচায় যে ইলেক্ট্ৰন হেৰুওৱা half reaction বোৰক জাৰণ বিক্ৰিয়া বোলা হয়। একেদৰে, ইলেক্ট্ৰন লাভ কৰা half reaction বোৰক বিজাৰণ বিক্ৰিয়া বোলা হয়। ইয়াত উল্লেখ কৰাটো অসম্পৰ্কীয় নহ’ব যে জাৰণ আৰু বিজাৰণ সংজ্ঞায়িত কৰাৰ নতুন পদ্ধতিটো শাস্ত্ৰীয় ধাৰণা অনুসৰি species বোৰৰ আচৰণ আৰু ইলেক্ট্ৰন-স্থানান্তৰ পৰিৱৰ্তনত সিহঁতৰ আন্তঃক্ৰিয়াৰ মাজত এক সম্বন্ধ স্থাপন কৰিহে অৰ্জন কৰা হৈছে। (৮.১২ ৰ পৰা ৮.১৪) বিক্ৰিয়াত ছ’ডিয়াম, যিটো জাৰিত হয়, এটা বিজাৰক এজেণ্ট হিচাপে কাম কৰে কাৰণ ই ইয়াৰ সৈতে আন্তঃক্ৰিয়া কৰা প্ৰতিটো মৌলক ইলেক্ট্ৰন দান কৰে আৰু এনেদৰে সিহঁতক বিজাৰিত কৰাত সহায় কৰে। ক্ল’ৰিন, অক্সিজেন আৰু গন্ধক বিজাৰিত হয় আৰু জাৰক এজেণ্ট হিচাপে কাম কৰে কাৰণ এইবোৰে ছ’ডিয়ামৰ পৰা ইলেক্ট্ৰন গ্ৰহণ কৰে। সংক্ষিপ্তকৈ, আমি উল্লেখ কৰিব পাৰো যে
জাৰণ: যিকোনো species ৰ দ্বাৰা ইলেক্ট্ৰন(বোৰ) হেৰুওৱা।
বিজাৰণ: যিকোনো species ৰ দ্বাৰা ইলেক্ট্ৰন(বোৰ) লাভ কৰা।
জাৰক এজেণ্ট: ইলেক্ট্ৰন(বোৰ) গ্ৰহণকাৰী।
বিজাৰক এজেণ্ট: ইলেক্ট্ৰন(বোৰ) দাতা।
সমস্যা ৮.২
যুক্তি দৰ্শাওক যে বিক্ৰিয়াটো: $2 \mathrm{Na}(\mathrm{s})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaH}$ (s) এটা ৰেডক্স পৰিৱৰ্তন।
সমাধান
ওপৰৰ বিক্ৰিয়াত যৌগটো এটা আয়নিক যৌগ গঠন হোৱাৰ পৰা, যাক $\mathrm{Na}^{+} \mathrm{H}^{-}$(s) হিচাপেও প্ৰতিনিধিত্ব কৰিব পাৰি, ই সূচায় যে এই প্ৰক্ৰিয়াটোৰ এটা half reaction হৈছে:
$2 \mathrm{Na}(\mathrm{s}) \quad \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
আৰু আন half reaction টো হৈছে:
$\mathrm{H_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{H}^{-}(\mathrm{g})$
পৰীক্ষাধীন বিক্ৰিয়াটোক দুটা half reaction ত বিভক্ত কৰাটোৱে স্বয়ংক্ৰিয়ভাৱে প্ৰকাশ কৰে যে ইয়াত ছ’ডিয়াম জাৰিত হয় আৰু হাইড্ৰ’জেন বিজাৰিত হয়, সেয়েহে, সম্পূৰ্ণ বিক্ৰিয়াটো এটা ৰেডক্স পৰিৱৰ্তন।
৮.২.১ প্ৰতিযোগিতামূলক ইলেক্ট্ৰন স্থানান্তৰ বিক্ৰিয়া [২৩৮-২৩৯]
চিত্ৰ ৮.১ ত দেখুওৱাৰ দৰে কপাৰ নাইট্ৰেটৰ জলীয় দ্ৰৱত ধাতৱ জিংকৰ এটা ফিতাপাত প্ৰায় এক ঘণ্টাৰ বাবে ৰাখক। আপুনি লক্ষ্য কৰিব পাৰে যে পাতটো ৰঙচুৱা ধাতৱ তামেৰে আৱৰি পৰে আৰু দ্ৰৱৰ নীলা ৰং আঁতৰি যায়। $\mathrm{Zn}^{2+}$ আয়নবোৰৰ গঠন উৎপাদনসমূহৰ মাজত সহজে বিচাৰ কৰিব পাৰি যেতিয়া $\mathrm{Cu}^{2+}$ ৰ বাবে দ্ৰৱৰ নীলা ৰং আঁতৰি গৈছে। যদি হাইড্ৰ’জেন ছালফাইড গেছ $\mathrm{Zn}^{2+}$ আয়ন থকা বৰণহীন দ্ৰৱটোৰ মাজেৰে পাৰ কৰোৱা হয়, বগা জিংক ছালফাইড, $\mathrm{ZnS}$ দ্ৰৱটোক এম’নিয়াৰে ক্ষাৰকীয় কৰিলে দেখা পাব পাৰি।
ধাতৱ জিংক আৰু কপাৰ নাইট্ৰেটৰ জলীয় দ্ৰৱৰ মাজৰ বিক্ৰিয়াটো হৈছে:
$$\mathrm{Zn}(\mathrm{s})+\mathrm{Cu}^{2+}(\mathrm{aq}) \rightarrow \mathrm{Zn}^{2+}(\mathrm{aq})+\mathrm{Cu}(\mathrm{s}) \tag{8.15}$$
(৮.১৫) বিক্ৰিয়াত, জিংকে $Zn^{2+}$ গঠন কৰিবলৈ ইলেক্ট্ৰন হেৰুৱাইছে আৰু সেয়েহে জিংক জাৰিত হয়। স্পষ্টতঃ, এতিয়া যদি জিংক জাৰিত হয়, ইলেক্ট্ৰনবোৰ মুকলি কৰি দিয়ে, তেন্তে কিবা এটা বিজাৰিত হ’ব লাগিব, জিংকে হেৰুওৱা ইলেক্ট্ৰনবোৰ গ্ৰহণ কৰি। কপাৰ আয়ন জিংকৰ পৰা ইলেক্ট্ৰন লাভ কৰি বিজাৰিত হয়।
বিক্ৰিয়া (৮.১৫)ক এনেদৰে পুনৰ লিখিব পাৰি:
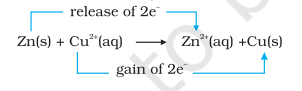
এই স্তৰত আমি সমীকৰণ (৮.১৫) ৰ দ্বাৰা প্ৰতিনিধিত্ব কৰা বিক্ৰিয়াটোৰ বাবে সমতাৱস্থাৰ তদন্ত কৰিব পাৰো। এই উদ্দেশ্যে, এটা জিংক ছালফেট দ্ৰৱত ধাতৱ তামৰ এটা ফিতাপাত ৰাখক। কোনো দৃশ্যমান বিক্ৰিয়া লক্ষ্য কৰা নাযায় আৰু $\mathrm{Cu}^{2+}$ আয়নৰ উপস্থিতি চিনাক্ত কৰাৰ চেষ্টা কৰি $\mathrm{H_2} \mathrm{~S}$ গেছ দ্ৰৱটোৰ মাজেৰে পাৰ কৰি কপ্ৰিক ছালফাইড, CuS ৰ ক’লা ৰং উৎপন্ন কৰিবলৈ সফল নহয়। কপ্ৰিক ছালফাইডৰ দ্ৰৱণীয়তা ইমান কম যে এইটো এক অতি সংবেদনশীল পৰীক্ষা; তথাপিও গঠন হোৱা $\mathrm{Cu}^{2+}$ ৰ পৰিমাণ চিনাক্ত কৰিব পৰা নাযায়। আমি এইদৰে সিদ্ধান্তত উপনীত হওঁ যে বিক্ৰিয়া (৮.১৫) ৰ বাবে সমতাৱস্থাই বিক্ৰিয়কতকৈ উৎপাদনসমূহক বহু পৰিমাণে পক্ষপাতিত্ব কৰে।
এতিয়া ইলেক্ট্ৰন স্থানান্তৰ বিক্ৰিয়াক পানীত তাম ধাতু আৰু চিলভাৰ নাইট্ৰেট দ্ৰৱলৈ সম্প্ৰসাৰিত কৰো আৰু চিত্ৰ ৮.২ ত দেখুওৱাৰ দৰে এটা ছেট-আপ সাজো। দ্ৰৱটোৱে নীলা ৰং বিকশিত কৰে কাৰণ বিক্ৰিয়াটোৰ বাবে $\mathrm{Cu}^{2+}$ আয়ন গঠন হয়:
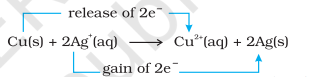
ইয়াত, $\mathrm{Cu}(\mathrm{s})$ জাৰিত হৈ $\mathrm{Cu}^{2+}(\mathrm{aq})$ হয় আৰু $\mathrm{Ag}^{+}(\mathrm{aq})$ বিজাৰিত হৈ $\mathrm{Ag}(\mathrm{s})$ হয়। সমতাৱস্থাই উৎপাদন $\mathrm{Cu}^{2+}(\mathrm{aq})$ আৰু $\mathrm{Ag}(\mathrm{s})$ ক বহু পৰিমাণে পক্ষপাতিত্ব কৰে।
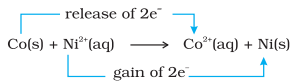
বিপৰীত দিশেৰে, নিকেল ছালফেট দ্ৰৱত ৰখা ধাতৱ কোবাল্টৰ বিক্ৰিয়াটোও তুলনা কৰো আহক। ইয়াত সংঘটিত হোৱা বিক্ৰিয়াটো হৈছে:
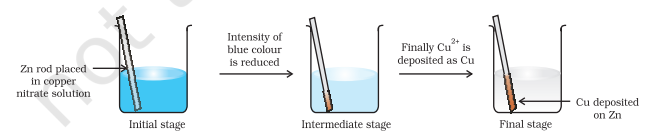
চিত্ৰ ৮.১ বিকাৰত সংঘটিত হোৱা জিংক আৰু কপাৰ নাইট্ৰেটৰ জলীয় দ্ৰৱৰ মাজৰ ৰেডক্স বিক্ৰিয়া।
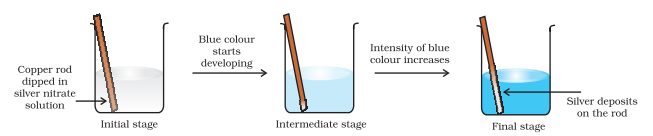
চিত্ৰ ৮.২ বিকাৰত সংঘটিত হোৱা কপাৰ আৰু চিলভাৰ নাইট্ৰেটৰ জলীয় দ্ৰৱৰ মাজৰ ৰেডক্স বিক্ৰিয়া।
সমতাৱস্থাত, ৰাসায়নিক পৰীক্ষাই প্ৰকাশ কৰে যে $\mathrm{Ni}^{2+}(\mathrm{aq})$ আৰু $\mathrm{Co}^{2+}(\mathrm{aq})$ দুয়োটাই মধ্যমীয়া ঘনত্বত উপস্থিত থাকে। এই ক্ষেত্ৰত, বিক্ৰিয়ক $\left[\mathrm{Co}(\mathrm{s})\right.$ আৰু $\left.\mathrm{Ni}^{2+}(\mathrm{aq})\right]$ বা উৎপাদন $\left[\mathrm{Co}^{2+}(\mathrm{aq})\right.$ আৰু $\left.\mathrm{Ni}(\mathrm{s})\right]$ কোনোটোকে বহু পৰিমাণে পক্ষপাতিত্ব কৰা নহয়।
ইলেক্ট্ৰন মুকলি কৰাৰ এই প্ৰতিযোগিতাই আমাক ঘটনাক্ৰমে এচিডসমূহৰ মাজত প্ৰটন মুকলি কৰাৰ প্ৰতিযোগিতাৰ কথা মনত পেলায়। সাদৃশ্যই সূচায় যে আমি এটা তালিকা বিকশিত কৰিব পাৰো য’ত ধাতু আৰু সিহঁতৰ আয়নবোৰ ইলেক্ট্ৰন মুকলি কৰাৰ প্ৰৱণতাৰ ভিত্তিত তালিকাভুক্ত কৰা হয় যেনেকৈ আমি এচিডৰ ক্ষেত্ৰত এচিডবোৰৰ শক্তি সূচাবলৈ কৰো। বাস্তৱতে আমি ইতিমধ্যে কিছুমান তুলনা কৰিছো। তুলনা কৰি আমি জানিব পাৰিছো যে জিংকে তামলৈ ইলেক্ট্ৰন মুকলি কৰে আৰু তামে চিলভাৰলৈ ইলেক্ট্ৰন মুকলি কৰে আৰু সেয়েহে, ধাতুবোৰৰ ইলেক্ট্ৰন মুকলি কৰাৰ প্ৰৱণতা ক্ৰমত আছে: $\mathrm{Zn}>\mathrm{Cu}>\mathrm{Ag}$। আমি আমাৰ তালিকাটো অধিক বিশাল কৰিবলৈ আৰু ধাতু ক্ৰিয়া শৃংখলা বা ইলেক্ট্ৰ’কেমিকেল শৃংখলা ডিজাইন কৰিবলৈ ভাল পাম। বিভিন্ন ধাতুৰ মাজত ইলেক্ট্ৰনৰ বাবে প্ৰতিযোগিতাই আমাক কোষৰ এটা শ্ৰেণী ডিজাইন কৰাত সহায় কৰে, যাক গেলভেনিক কোষ বুলি নামকৰণ কৰা হয় য’ত ৰাসায়নিক বিক্ৰিয়াবোৰ বিদ্যুৎ শক্তিৰ উৎস হয়। আমি দ্বাদশ শ্ৰেণীত এই কোষবোৰৰ বিষয়ে অধিক অধ্যয়ন কৰিম।
৮.৩ জাৰণ সংখ্যা [২৩৯-২৪৯]
ইলেক্ট্ৰন স্থানান্তৰৰ এক কম স্পষ্ট উদাহৰণ উপলব্ধি কৰা হয় যেতিয়া হাইড্ৰ’জেন অক্সিজেনৰ সৈতে সংযুক্ত হৈ পানী গঠন কৰে বিক্ৰিয়াৰ দ্বাৰা:
$$2 \mathrm{H_2}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{H_2} \mathrm{O}(\mathrm{l})\tag{8.18}$$
ইয়াৰ পদ্ধতিটো সৰল নহ’লেও, আমি $\mathrm{H}$ পৰমাণুটোক $\mathrm{H_2}$ ত এক নিৰপেক্ষ (শূন্য) অৱস্থাৰ পৰা $\mathrm{H_2} \mathrm{O}$ ত এক ধনাত্মক অৱস্থালৈ যোৱা হিচাপে কল্পনা কৰিব পাৰো, $\mathrm{O}$ পৰমাণুটো $\mathrm{O_2}$ ত শূন্য অৱস্থাৰ পৰা $\mathrm{H_2} \mathrm{O}$ ত ডাইনেগেটিভ অৱস্থালৈ যায়। ইয়াত ধৰা হয় যে $\mathrm{H}$ ৰ পৰা $\mathrm{O}$ লৈ ইলেক্ট্ৰন স্থানান্তৰ হয় আৰু ফলত $\mathrm{H_2}$ জাৰিত হয় আৰু $\mathrm{O_2}$ বিজাৰিত হয়।
অৱশ্যে, যিদৰে আমি পাছত দেখিম, আধান স্থানান্তৰটো কেৱল আংশিক আৰু সম্ভৱতঃ $\mathrm{H}$ ৰ দ্বাৰা সম্পূৰ্ণ ইলেক্ট্ৰন হেৰুওৱা আৰু O ৰ দ্বাৰা লাভ কৰাতকৈ ইলেক্ট্ৰন স্থানান্তৰ হিচাপে ভালদৰে বৰ্ণনা কৰা হয়। সমীকৰণ (৮.১৮) ৰ সৈতে ইয়াত যি কৈছে সেয়া সমযোজী যৌগ জড়িত আন বহুতো বিক্ৰিয়াৰ বাবে সঁচা হ’ব পাৰে। এই শ্ৰেণীৰ বিক্ৰিয়াৰ দুটা এনে উদাহৰণ হৈছে:
$$\mathrm{H_2}(\mathrm{~s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{HCl}(\mathrm{g})\tag{8.19}$$
আৰু,
$$\mathrm{CH_4}(\mathrm{~g})+4 \mathrm{Cl_2}(\mathrm{~g}) \rightarrow \mathrm{CCl_4}(\mathrm{l})+4 \mathrm{HCl}(\mathrm{g})\tag{8.20}$$
সমযোজী যৌগ গঠন জড়িত ৰাসায়নিক বিক্ৰিয়াত ইলেক্ট্ৰন স্থানান্তৰৰ খতিয়ান ৰখাৰ বাবে, জাৰণ সংখ্যা ব্যৱহাৰ কৰাৰ এক অধিক ব্যৱহাৰিক পদ্ধতি বিকশিত হৈছে। এই পদ্ধতিত, সদায় ধৰা হয় যে কম ইলেক্ট্ৰ’নেগেটিভ পৰমাণুৰ পৰা অধিক ইলেক্ট্ৰ’নেগেটিভ পৰমাণুলৈ সম্পূৰ্ণ ইলেক্ট্ৰন স্থানান্তৰ হয়। উদাহৰণস্বৰূপে, আমি (৮.১৮ ৰ পৰা ৮.২০) সমীকৰণবোৰ পুনৰ লিখো বিক্ৰিয়াটোৰ অংশ গঠন কৰা প্ৰতিটো পৰমাণুত আধান দেখুৱাবলৈ:
$$ \begin{array}{cccc} 2 \stackrel{0}{\mathrm{H_2}}(\mathrm{~g}) + \stackrel{0}{\mathrm{O_2}}(\mathrm{~g}) & \rightarrow & 2 \stackrel{+1}{\mathrm{H_2}} \stackrel{-2}{\mathrm{O}}(\mathrm{l}) \tag{8.21} \end{array} $$
$$ \begin{array}{llll} \stackrel {0}{\mathrm{H_2}}(\mathrm{~s}) + \stackrel{0}{\mathrm{Cl_2}}(\mathrm{~g}) & \rightarrow & 2 \stackrel{+1-1}{\mathrm{HCl}}(\mathrm{g}) \tag{8.22} \end{array} $$
$$ \begin{array}{cccc} \stackrel{-4 +1}{\mathrm{CH_4}}(\mathrm{~g}) + & 4 \stackrel{0}{\mathrm{Cl_2}}(\mathrm{~g}) \rightarrow & \stackrel{+4 -1}{\mathrm{C}\mathrm{Cl_4}} (\mathrm{l})+4 \stackrel{+1 -1 }{\mathrm{H } \mathrm{Cl}} (\mathrm{g})\tag{8.23} \end{array} $$
ইয়াত গুৰুত্ব দিব পাৰি যে ইলেক্ট্ৰন স্থানান্তৰৰ ধাৰণাটো কেৱল খতিয়ান ৰখাৰ উদ্দেশ্যৰ বাবেহে কৰা হয় আৰু এই এককৰ পাছৰ স্তৰত স্পষ্ট হ’ব যে ই ৰেডক্স বিক্ৰিয়াবোৰৰ সৰল বৰ্ণনালৈ নিয়ে।
জাৰণ সংখ্যাই যৌগত এটা মৌলৰ জাৰণ অৱস্থা সূচায় যাক এক গোট নিয়মৰ ভিত্তিত নিশ্চিত কৰা হয় যি এই ভিত্তিত ৰচনা কৰা হয় যে সমযোজী বন্ধনত ইলেক্ট্ৰন যোৰ সম্পূৰ্ণৰূপে অধিক ইলেক্ট্ৰ’নেগেটিভ মৌলৰ হয়।
যৌগ/আয়নত কোনটো মৌল আনটোতকৈ অধিক ইলেক্ট্ৰ’নেগেটিভ সদায় মনত ৰখাটো বা সহজে বুজাটো সম্ভৱ নহয়। সেয়েহে, যৌগ/আয়নত এটা মৌলৰ জাৰণ সংখ্যা নিৰ্ধাৰণ কৰিবলৈ এক গোট নিয়ম ৰচনা কৰা হৈছে। যদি এটা মৌলৰ দুটা বা তাতোধিক পৰমাণু অণু/আয়নত উপস্থিত থাকে যেনে $\mathrm{Na_2} \mathrm{~S_2} \mathrm{O_3} / \mathrm{Cr_2} \mathrm{O_7}^{2-}$, তেন্তে সেই মৌলৰ পৰমাণুটোৰ জাৰণ সংখ্যা তেতিয়া সেই মৌলৰ সকলো পৰমাণুৰ জাৰণ সংখ্যাৰ গড় হ’ব। আমি এই স্তৰত, জাৰণ সংখ্যা গণনাৰ নিয়মবোৰ উল্লেখ কৰিব পাৰো। এই নিয়মবোৰ হৈছে:
১. মৌলবোৰত, মুক্ত বা অসংযুক্ত অৱস্থাত, প্ৰতিটো পৰমাণুৱে শূন্য জাৰণ সংখ্যা বহন কৰে। স্পষ্টতঃ $\mathrm{H_2}, \mathrm{O_2}, \mathrm{Cl_2}, \mathrm{O_3}, \mathrm{P_4}, \mathrm{~S_8}, \mathrm{Na}, \mathrm{Mg}, \mathrm{Al}$ ত প্ৰতিটো পৰমাণুৰ জাৰণ সংখ্যা শূন্য।
২. কেৱল এটা পৰমাণুৰে গঠিত আয়নবোৰৰ বাবে, জাৰণ সংখ্যা আয়নটোৰ আধানৰ সমান। এইদৰে $\mathrm{Na}^{+}$ আয়নৰ জাৰণ সংখ্যা $+1, \mathrm{Mg}^{2+}$ আয়ন, $+2, \mathrm{Fe}^{3+}$ আয়ন, +৩ , $\mathrm{Cl}^{-}$ আয়ন, $-1, \mathrm{O}^{2-}$ আয়ন, -২ ; আৰু আনকি। সিহঁতৰ যৌগবোৰত সকলো ক্ষাৰ ধাতুৰ জাৰণ সংখ্যা +১ , আৰু সকলো ক্ষাৰকীয় মৃত্তিকা ধাতুৰ জাৰণ সংখ্যা +২ । এলুমিনিয়ামক ইয়াৰ সকলো যৌগত +৩ জাৰণ সংখ্যা থকা বুলি গণ্য কৰা হয়।
৩. বেছিভাগ যৌগত অক্সিজেনৰ জাৰণ সংখ্যা -২ । অৱশ্যে, আমি ইয়াত দুয়ো ধৰণৰ ব্যতিক্ৰমৰ সন্মুখীন হওঁ। এটা হৈছে পাৰ’ক্সাইড আৰু ছুপাৰ’ক্সাইডৰ ক্ষেত্ৰত, অক্সিজেনৰ যৌগবোৰ য’ত অক্সিজেন পৰমাণুবোৰ পৰস্পৰৰ সৈতে প্ৰত্যক্ষভাৱে সংযুক্ত। পাৰ’ক্সাইডত (যেনে, $\mathrm{H_2} \mathrm{O_2}$, $\mathrm{Na_2} \mathrm{O_2}$, প্ৰতিটো অক্সিজেন পৰমাণুক -১ জাৰণ সংখ্যা দিয়া হয়, ছুপাৰ’ক্সাইডত (যেনে, $\mathrm{KO_2}, \mathrm{RbO_2}$ ) প্ৰতিটো অক্সিজেন পৰমাণুক $-(1 / 2)$ জাৰণ সংখ্যা দিয়া হয়। দ্বিতীয় ব্যতিক্ৰমটো কেতিয়াবাহে দেখা দিয়ে, অৰ্থাৎ যেতিয়া অক্সিজেন ফ্লুৰিনৰ সৈতে বন্ধন গঠন কৰে। এনে যৌগত যেনে, অক্সিজেন ডাইফ্লুৰাইড $\left(\mathrm{OF_2}\right)$ আৰু ডাইঅক্সিজেন ডাইফ্লুৰাইড $\left(\mathrm{O_2} \mathrm{~F_2}\right)$, অক্সিজেনক ক্ৰমে +২ আৰু +১ জাৰণ সংখ্যা দিয়া হয়। অক্সিজেনলৈ দিয়া সংখ্যাটো অক্সিজেনৰ বন্ধন অৱস্থাৰ ওপৰত নিৰ্ভৰ কৰিব কিন্তু এই সংখ্যাটো এতিয়া কেৱল এটা ধনাত্মক অংক হ’ব।
৪. হাইড্ৰ’জেনৰ জাৰণ সংখ্যা +১ , যেতিয়া ই ধাতুৰ সৈতে বাইনেৰী যৌগত (অৰ্থাৎ দুটা মৌল থকা যৌগ) বন্ধন গঠন কৰে তেতিয়া বাদে। উদাহৰণস্বৰূপে, $\mathrm{LiH}, \mathrm{NaH}$, আৰু $\mathrm{CaH_2}$ ত, ইয়াৰ জাৰণ সংখ্যা -১ ।
৫. ইয়াৰ সকলো যৌগত, ফ্লুৰিনৰ জাৰণ সংখ্যা -১ । আন হেল’জেনবোৰৰ ($(\mathrm{Cl}$, $\mathrm{Br}$, আৰু I) জাৰণ সংখ্যাও -১ , যেতিয়া সিহঁত সিহঁতৰ যৌগত হেলাইড আয়ন হিচাপে উপস্থিত হয়। ক্ল’ৰিন, ব্ৰ’মিন আৰু আয়’ডিন যেতিয়া অক্সিজেনৰ সৈতে সংযুক্ত হয়, উদাহৰণস্বৰূপে অক্স’এচিড আৰু অক্স’এনায়নত, ধনাত্মক জাৰণ সংখ্যা থাকে।
৬. যৌগত থকা সকলো পৰমাণুৰ জাৰণ সংখ্যাৰ বীজগণিতীয় যোগফল শূন্য হ’ব লাগিব। বহুপৰমাণুক আয়নত, আয়নটোৰ সকলো পৰমাণুৰ জাৰণ সংখ্যাৰ বীজগণিতীয় যোগফল আয়নটোৰ আধানৰ সমান হ’ব লাগিব। এইদৰে, কাৰ্বনেট আয়ন, $\left(\mathrm{CO_3}\right)^{2-}$ ত থকা তিনিটা অক্সিজেন পৰমাণু আৰু এটা কাৰ্বন পৰমাণুৰ জাৰণ সংখ্যাৰ যোগফল -২ ৰ সমান হ’ব লাগিব।
ওপৰৰ নিয়মবোৰ প্ৰয়োগ কৰি, আমি অণু বা আয়নত ইচ্ছিত মৌলটোৰ জাৰণ সংখ্যা












