অধ্যায় ১২ যন্ত্রপাতি ও প্রযুক্তি
১২.১ অণুবীক্ষণ যন্ত্র
জৈবিক গবেষণা ও অনুসন্ধান অণুবীক্ষণ যন্ত্র ছাড়া কল্পনা করা যায় না কারণ এটি আমাদের চোখের সীমার বাইরের কিছু দেখতে সক্ষম করে। আজ, অণুবীক্ষণ যন্ত্রের কৌশল এতটাই উন্নত হয়েছে যে একজন গবেষণাকারী কেবল একটি অতি ক্ষুদ্র কাঠামোর অত্যন্ত বিবর্ধিত চিত্রই দেখতে পারেন না, বরং এমন বস্তুর ত্রিমাত্রিক কাঠামোও দৃশ্যমান করতে পারেন। শক্তিশালী ইলেকট্রন অণুবীক্ষণ যন্ত্রের কৌশল ব্যবহার করে, এমনকি ব্যাকটেরিয়া এবং ভাইরাসের DNA অণুকেও দৃশ্যমান করা হয়েছে।
প্রথম অণুবীক্ষণ যন্ত্রের ব্যবহার ১৬৬৫ সালের দিকে, যখন ব্রিটিশ পদার্থবিদ রবার্ট হুক বিবর্ধক লেন্সের সমন্বয়ে একটি সরল অণুবীক্ষণ যন্ত্র ডিজাইন করেন (চিত্র ১২.১) এবং কর্কের পাতলা টুকরো পর্যবেক্ষণ করেন, এবং সেই মৌচাকের মতো কাঠামোর জন্য ‘সেলুলি’ বা কোষ শব্দটি উদ্ভাবন করেন। আপনি জানেন যে ম্যাথিয়াস জ্যাকব শ্লাইডেন এবং থিওডোর শোয়ান ১৮৩৮ সালে উদ্ভিদ ও প্রাণীর কোষ পর্যবেক্ষণের ভিত্তিতে কোষ তত্ত্ব প্রস্তাব করেছিলেন।
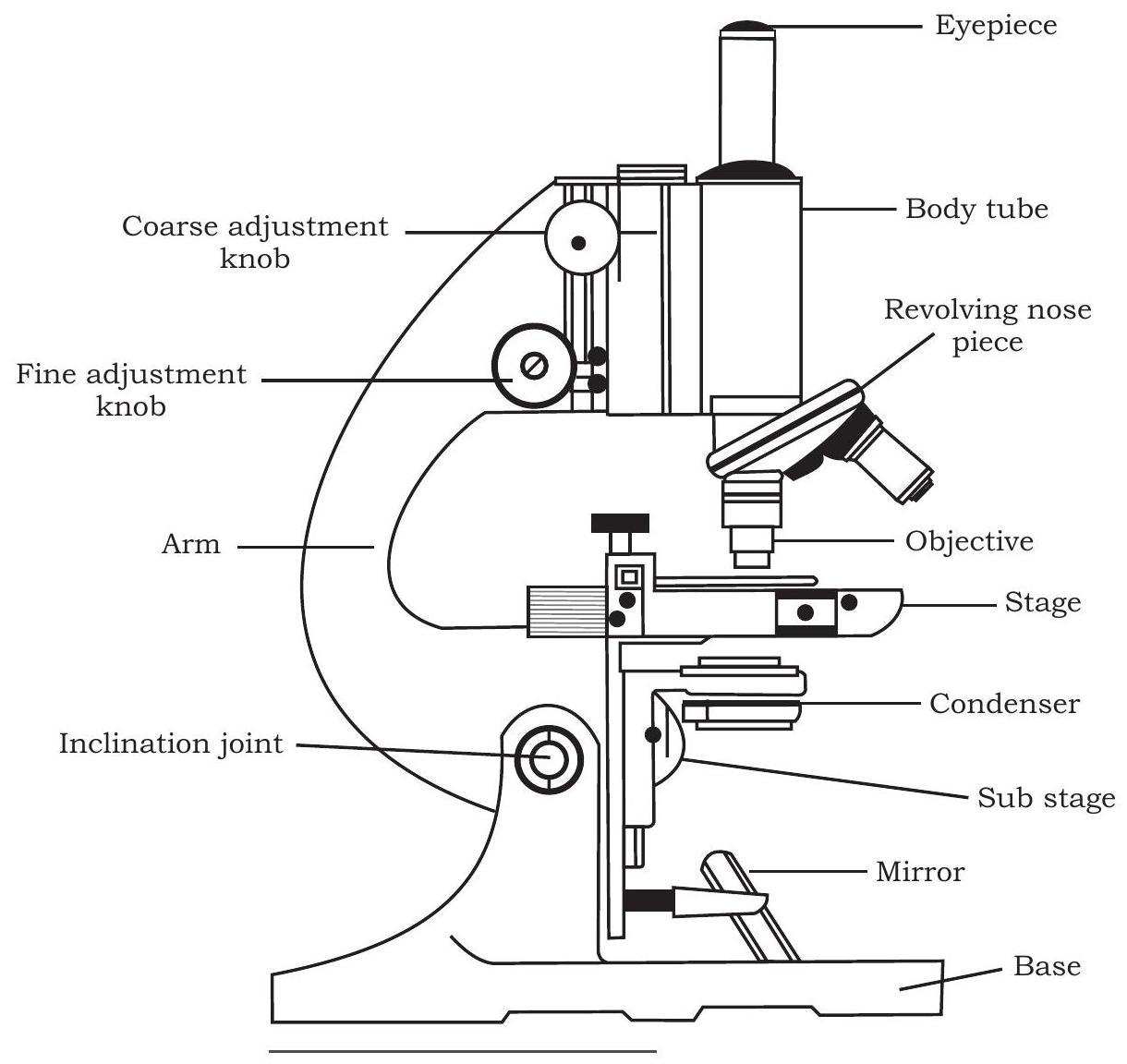
চিত্র ১২.১: অণুবীক্ষণ যন্ত্র
১২.১.১ বিবর্ধন ও রেজোলিউশন
এখন আসুন আমরা সেই নীতির দিকে মনোনিবেশ করি যার উপর অণুবীক্ষণ যন্ত্রের কৌশলটি ভিত্তি করে। অণুবীক্ষণ যন্ত্রের মতো একটি আলোকিক যন্ত্রের জন্য দুটি আলোকিক বৈশিষ্ট্য অত্যন্ত গুরুত্বপূর্ণ। একটি হল বিবর্ধন করার ক্ষমতা এবং অন্যটি হল রেজোলিউশন করার ক্ষমতা।
একটি অণুবীক্ষণ যন্ত্রের বিবর্ধন বা বিবর্ধন ক্ষমতা হল সেই ক্ষমতা যার দ্বারা রেটিনার চিত্রের আকার বৃদ্ধি করা যায়। সুতরাং সহজ কথায় বিবর্ধন হল -
অণুবীক্ষণ যন্ত্রের সাহায্যে রেটিনার চিত্রের আকার / অণুবীক্ষণ যন্ত্র ব্যবহার না করে রেটিনার চিত্রের আকার
আপনি পদার্থবিদ্যায় পড়ে থাকতে পারেন যে একটি লেন্সের বিবর্ধন (M) নিম্নলিখিত সূত্র অনুসারে পরিমাপ করা হয় (যেখানে $f$ হল লেন্সের ফোকাল দৈর্ঘ্য এবং $d$ হল লেন্স থেকে বস্তুর দূরত্ব)।
$$ M=\frac{f}{f-d} $$
সাধারণত, পরীক্ষাগারে যে অণুবীক্ষণ যন্ত্র ব্যবহার করা হয় তা একটি যৌগিক অণুবীক্ষণ যন্ত্র যাতে দুটি সেট লেন্স থাকে। একটিকে বলা হয় অবজেক্টিভ লেন্স, যা দেখা যাবে এমন বস্তুর কাছাকাছি থাকে, এবং অন্যটি হল আইপিস যার মাধ্যমে পর্যবেক্ষক দেখেন। এটা বলার অপেক্ষা রাখে না যে বস্তু, অবজেক্টিভ লেন্স, আইপিস এবং পর্যবেক্ষকের চোখ আলোর যাত্রাপথের জন্য একই সরলরেখায় থাকতে হবে যাতে বস্তুর বিবর্ধিত চিত্র দেখা যায়। সহজ কথায়, একটি অণুবীক্ষণ যন্ত্রের বিবর্ধন হল অবজেক্টিভ লেন্সের বিবর্ধন ক্ষমতা এবং আইপিসের বিবর্ধন ক্ষমতার গুণফল $\left(\mathrm{M} _{\mathrm{o}} \times \mathrm{M} _{\mathrm{e}}\right)$।
রেজোলিউশন ক্ষমতা হল অণুবীক্ষণ যন্ত্রের আরেকটি গুরুত্বপূর্ণ বৈশিষ্ট্য, যা একে অপরের খুব কাছাকাছি অবস্থিত দুটি বস্তুর পৃথক চিত্র গঠনের ক্ষমতা। এটি দুটি বিন্দুর মধ্যে ক্ষুদ্রতম দূরত্ব দ্বারা পরিমাপ করা যেতে পারে।
১২.১.২ একটি আলোক অণুবীক্ষণ যন্ত্রের কার্যকারিতা
আপনি আগের শ্রেণীতে একটি যৌগিক অণুবীক্ষণ যন্ত্রের গঠন সম্পর্কে ইতিমধ্যেই পড়েছেন, তবুও পুনরাবৃত্তি করার জন্য, যেমন আপনি চিত্র ১২.১-এ দেখতে পাচ্ছেন, একটি যৌগিক অণুবীক্ষণ যন্ত্রে একটি বেস থাকে যার উপর একটি মঞ্চ লাগানো থাকে যার কেন্দ্রে একটি ছিদ্র থাকে। বেসের সাথে একটি বাহু সংযুক্ত থাকে যার সাথে একটি বডি টিউব এমনভাবে লাগানো থাকে যে এটি মঞ্চের ছিদ্রের সাথে সারিবদ্ধ হয়। বডি টিউবের নিচের প্রান্তে একটি নোজ পিস লাগানো থাকে যার উপর দুই থেকে চারটি অবজেক্টিভ লেন্স থাকতে পারে। নোজ পিসটি ঘুরিয়ে, অবজেক্টিভ লেন্সগুলোর মধ্যে একটি মঞ্চের উপরে থাকা ছিদ্রের উপর স্থাপন করা যেতে পারে যেখানে দেখা যাবে এমন বস্তুটি একটি কাচের স্লাইডের উপর রাখা হয়। বডি টিউবের উপরের প্রান্তে একটি আইপিস লাগানো থাকে যার মাধ্যমে একজন পর্যবেক্ষক অণুবীক্ষণ যন্ত্রের নিচে দেখতে পারেন। বাহুতে সমন্বয় স্ক্রু (মোটা এবং সূক্ষ্ম) থাকে যা মঞ্চের উপর উপস্থিত বস্তু থেকে অবজেক্টিভ লেন্সের দূরত্ব সামঞ্জস্য করতে সহায়তা করে। মঞ্চের নিচে, আলোর একটি উৎস থাকে (যা একটি প্রতিফলক দর্পণ বা একটি বাল্ব হতে পারে যা বস্তুকে আলোকিত করে এবং অবজেক্টিভ লেন্স ও আইপিসের মাধ্যমে চিত্র গঠনে সহায়তা করে)। এছাড়াও, আলোর উৎস এবং মঞ্চের মধ্যে একটি কনডেন্সার থাকে, যা বস্তুর উপর আলো ফোকাস করার জন্য গুরুত্বপূর্ণ। চিত্র ১২.২ একটি যৌগিক অণুবীক্ষণ যন্ত্রে আলোর পথও দেখায়। আপনি লক্ষ্য করে থাকতে পারেন যে অবজেক্টিভ লেন্স এবং আইপিস উভয়েরই বিবর্ধন ক্ষমতা ভিন্ন। একটি শিক্ষার্থীর অণুবীক্ষণ যন্ত্রে আইপিসের বিবর্ধন ক্ষমতা $10 \times$ বা $15 x$ এবং নোজ পিসে লাগানো বিভিন্ন অবজেক্টিভ লেন্সগুলোর বিবর্ধন ক্ষমতা হল $4 \times$, $10 x, 40 / 45 x$ এবং $100 x$। আলোচিত অণুবীক্ষণ যন্ত্রের কৌশলটিকে ব্রাইট ফিল্ড মাইক্রোস্কোপিও বলা হয় কারণ দেখা যাবে এমন বস্তুকে আলোকিত করতে আলো ব্যবহার করা হয়। তাই, বস্তুর বিভিন্ন অঞ্চলকে আলাদা করার জন্য, একে নির্দিষ্ট রঞ্জক বা দাগ দিয়ে রঞ্জিত করা হয়। কারমিন, ইওসিন, সাফ্রানিন, মিথিলিন ব্লু, গিমসা ইত্যাদি হল কয়েকটি এমন দাগ যা সাধারণত আলোক অণুবীক্ষণ যন্ত্রের জন্য ব্যবহৃত হয়।
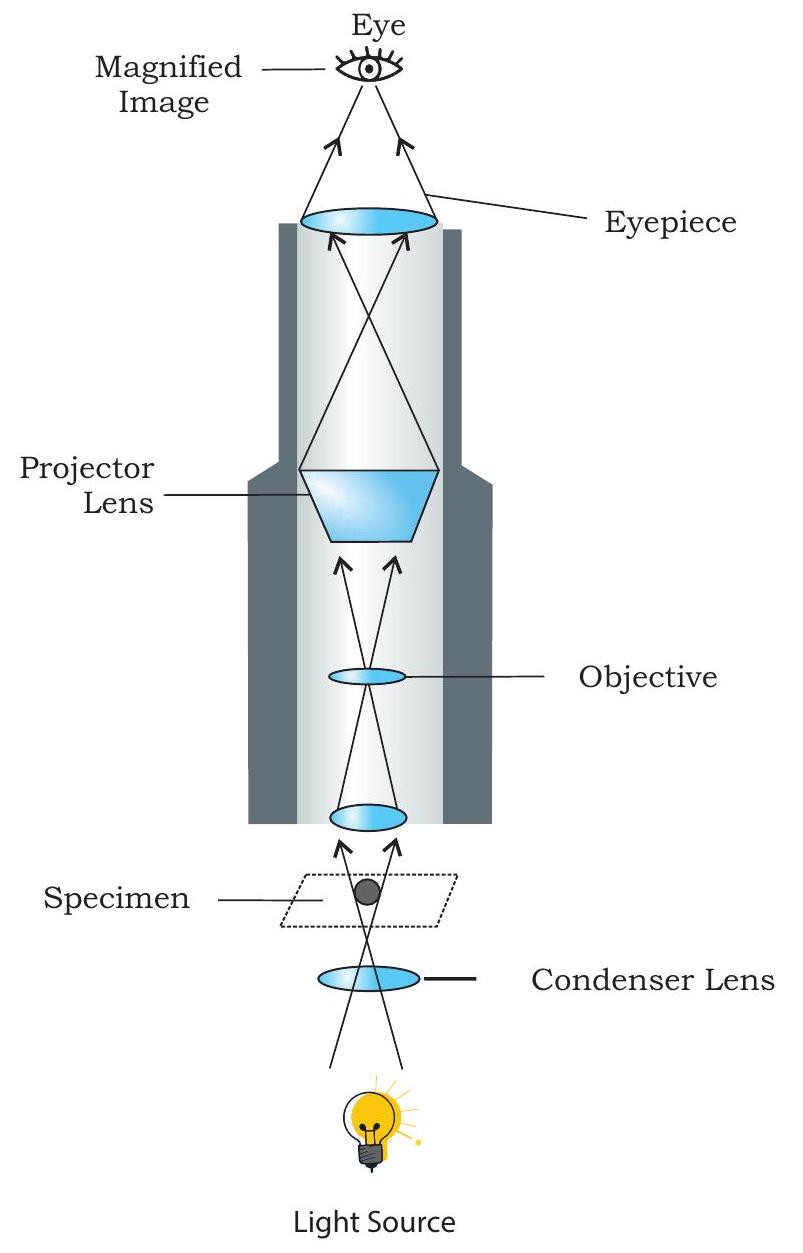
চিত্র ১২.২: আলোক অণুবীক্ষণ যন্ত্র
১২.১.৩ অণুবীক্ষণ যন্ত্রের বিভিন্ন রূপ
কলা/কোষের অভ্যন্তরীণ সংগঠনের ক্ষুদ্রাতিক্ষুদ্র বিবরণ অধ্যয়ন এতই বৈচিত্র্যময় যে তা শুধুমাত্র আলোক অণুবীক্ষণ যন্ত্র দ্বারা অর্জন করা যায় না। তাই, এক বা অন্য ধরনের কৌশল প্রয়োগ করে, বেশ বৈচিত্র্যময় অণুবীক্ষণ যন্ত্রের রূপ ব্যবহার করা হয়। এক ধরনের এমন কৌশলে, কেন্দ্রীয় কনডেন্সার থেকে বস্তুর উপর পড়া আলো একটি ডিস্ক দ্বারা অবরুদ্ধ করা হয় এবং বস্তুর আলোকিতকরণ একটি তির্যক আলোক রশ্মি দ্বারা করা হয়, যা স্লাইড থেকে প্রতিফলিত হয় এবং চিত্রটি অন্ধকার পটভূমির বিপরীতে আলোকিত হয়। তাই, এমন অণুবীক্ষণ যন্ত্রকে ডার্ক ফিল্ড মাইক্রোস্কোপি বলে জানা যায়। মাইটোকন্ড্রিয়া, নিউক্লিয়াস, রসধার ইত্যাদি এটি ব্যবহার করে সহজেই সনাক্ত করা যায়। একইভাবে, ফেজ কনট্রাস্ট মাইক্রোস্কোপি নামক একটি ভিন্ন রূপে, স্বচ্ছ বস্তুর মধ্য দিয়ে যাওয়া আলোর তরঙ্গ বিস্তার এবং দশা পরিবর্তিত হয়। এই পরিবর্তন বস্তু বা নমুনার অংশের ঘনত্বের উপর নির্ভর করে। এমন পরিবর্তন সেই অঞ্চলে বেশি হয় যেখানে ঘনত্ব তুলনামূলকভাবে বেশি এবং ফলস্বরূপ, বস্তুর বিভিন্ন অঞ্চলের বিভিন্ন কনট্রাস্ট দেখা যায়। এটি বিশেষ করে কোষ অঙ্গাণু এবং ক্রোমোজোম অধ্যয়নে সহায়ক। বস্তু বা নমুনাকে কিছু নির্দিষ্ট রঞ্জক দিয়ে রঞ্জিত করা নিয়মিতভাবে করা হয়। কিছু বিশেষ ধরনের রঞ্জক আছে যেমন অ্যাক্রিডিন অরেঞ্জ, বিসবেনজিমাইড, মেরোসায়ানিন (ফ্লুরোফোরও বলা হয়)। এই রঞ্জকগুলি আলোকিত হওয়ার পর দীর্ঘ তরঙ্গদৈর্ঘ্যের আলো নির্গত করতে সক্ষম, একটি বৈশিষ্ট্য যাকে ফ্লুরোসেন্স বলে। এর ফলস্বরূপ, ফ্লুরোফোর দ্বারা রঞ্জিত বস্তুটি বেশি আলোকিত এবং ব্যবহৃত রঞ্জকের উপর নির্ভর করে ভিন্ন রঙের দেখায়। ফ্লুরোসেন্স মাইক্রোস্কোপিতে, একই নীতি প্রয়োগ করা হয়। দেখা যাবে এমন বস্তুকে একটি নির্দিষ্ট অঙ্গাণু বা অণুর অংশ অধ্যয়নের জন্য ফ্লুরোফোর দিয়ে রঞ্জিত করা হয়। ফ্লুরোসেন্স অণুবীক্ষণ যন্ত্রের নিচে বস্তুকে আলোকিত করার পর, নির্দিষ্টভাবে রঞ্জিত অঞ্চলটি সহজেই দেখা বা পর্যবেক্ষণ করা যায়। এটি সংক্রমণের কারণ জানতে এবং ইমিউনোডায়াগনোসিসে ব্যাকটেরিয়া বা ভাইরাস শনাক্ত করতে সহায়ক।
ইলেকট্রন অণুবীক্ষণ যন্ত্র একটি অত্যন্ত পরিশীলিত কৌশল যাতে অধ্যয়ন করা যাবে এমন বস্তুকে ইলেকট্রন রশ্মি দ্বারা আঘাত করা হয় যা দৃশ্যমান আলোর চেয়ে প্রায় $1,00,000$ গুণ কম তরঙ্গদৈর্ঘ্যের। একটি ইলেকট্রন অণুবীক্ষণ যন্ত্রে ইলেকট্রন রশ্মি চৌম্বকীয় লেন্সের সাহায্যে চিত্রকে বিবর্ধিত করে। ইলেকট্রনের সম্পূর্ণ যাত্রা শূন্যতায় হয় এবং উৎপন্ন চিত্রটি একটি ফ্লুরোসেন্ট স্ক্রিনে দেখা হয় এবং আইপিসের মাধ্যমে নয়। ইলেকট্রনের খুব কম তরঙ্গদৈর্ঘ্যের কারণে, একটি ইলেকট্রন অণুবীক্ষণ যন্ত্র দ্বারা উৎপন্ন চিত্রের রেজোলিউশন খুব বেশি। দুই ধরনের ইলেকট্রন অণুবীক্ষণ যন্ত্র ব্যবহার করা হয়; ট্রান্সমিশন ইলেকট্রন মাইক্রোস্কোপি এবং স্ক্যানিং ইলেকট্রন মাইক্রোস্কোপি। ট্রান্সমিশন ইলেকট্রন মাইক্রোস্কোপিতে, বস্তু বা নমুনার অতিপাতলা ভারী ধাতব লবণ (সীসা, টাংস্টেন ইত্যাদির) দ্বারা আবৃত অংশ এমনভাবে স্থাপন করা হয় যে ইলেকট্রন রশ্মি এর মধ্য দিয়ে গিয়ে চিত্র তৈরি করে। ইলেকট্রন অণুবীক্ষণ যন্ত্রের অন্য কৌশলে, বস্তুর সোনা বা প্লাটিনাম দ্বারা আবৃত পৃষ্ঠ থেকে প্রতিফলিত ইলেকট্রন রশ্মি চিত্র তৈরি করে। এই কৌশলে, বস্তুর পৃষ্ঠের অত্যন্ত বিবর্ধিত এবং উচ্চ রেজোলিউশনের চিত্র তৈরি হয়, তাই, একে স্ক্যানিং ইলেকট্রন মাইক্রোস্কোপি বলা হয়।
গত দুই তিন দশকে, আরও একটি পরিশীলিত অণুবীক্ষণ যন্ত্রের ইমেজিং কৌশল উন্নত এবং ব্যবহার করা হয়েছে যাকে কনফোকাল মাইক্রোস্কোপি বলা হয়। কনফোকাল মাইক্রোস্কোপি স্থির কোষ/কলার মধ্যে বিস্তারিত কাঠামো রেজোলিউশন করতে এবং বস্তুর স্পষ্ট চিত্র দিতে উপযোগী। কনফোকাল মাইক্রোস্কোপি ব্যবহার করে একটি বস্তু পরীক্ষা করতে, এটি প্রথমে ফ্লুরোসেন্ট লেবেল করা হয় এবং তারপর উচ্চ রেজোলিউশনে একটি কনফোকাল অণুবীক্ষণ যন্ত্রের নিচে বিশ্লেষণ করা হয়।
১২.২ অপকেন্দ্রীকরণ
আপনি সমস্ত জীবন্ত জীবের কোষে উপস্থিত প্রোটিন, নিউক্লিক অ্যাসিড ইত্যাদির মতো বিভিন্ন জৈব অণু সম্পর্কে পড়েছেন। এই জৈব অণুগুলি অধ্যয়ন করতে, আপনাকে এক বা একাধিক পৃথকীকরণ কৌশল ব্যবহার করে এগুলিকে পৃথক করতে হবে। অপকেন্দ্রীকরণ হল এমন একটি কৌশল যাতে কণা বা অণুগুলিকে তাদের ঘনত্বের ভিত্তিতে মহাকর্ষীয় বলের (g) প্রভাবে, কেন্দ্রাতিগ বল ব্যবহার করে উচ্চ গতিতে একটি অক্ষের চারপাশে একটি দ্রবণে ঘুরিয়ে পৃথক করা হয়। ব্যবহৃত যন্ত্রটিকে সেন্ট্রিফিউজ বলা হয় (চিত্র ১২.৩), যা এর ব্যবহারের উপর নির্ভর করে বিভিন্ন ধরনের হয়। এটি একটি বেস, একটি ঘূর্ণায়মান পাত্র (স্পিনিং ভেসেল/রোটর) এবং একটি ঢাকনা নিয়ে গঠিত।
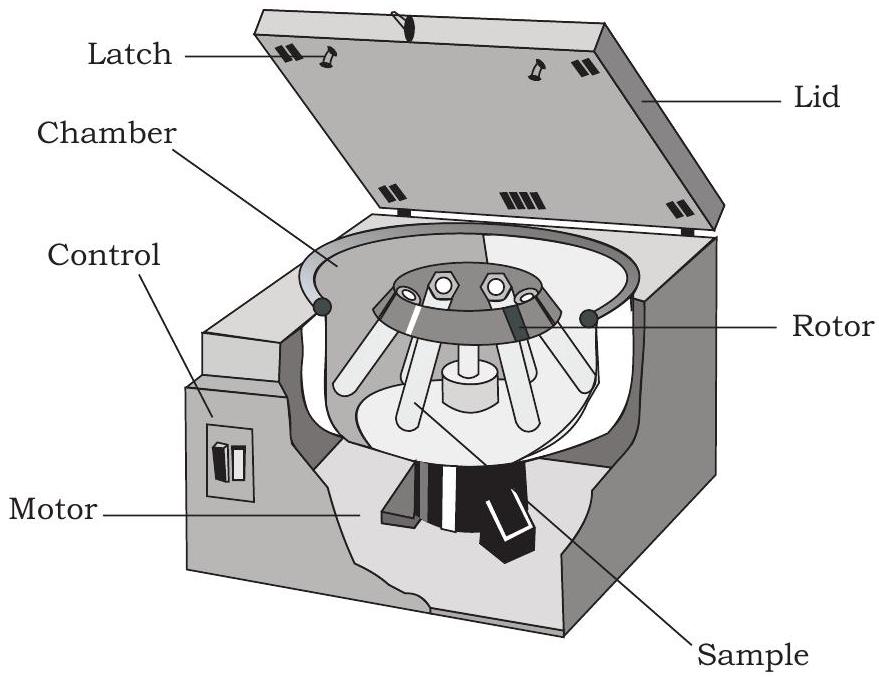
চিত্র ১২.৩: সেন্ট্রিফিউজের মৌলিক গঠন
স্পিনিং ভেসেলে বেশ কয়েকটি সেন্ট্রিফিউজ টিউব থাকে। কোষের নির্যাস বা মিশ্রণটি সেন্ট্রিফিউজ টিউবে নেওয়া হয় এবং একটি নির্দিষ্ট সময়ের জন্য কাঙ্ক্ষিত গতিতে (প্রতি মিনিটে ঘূর্ণন; rpm) ঘুরতে দেওয়া হয় যার ফলে কণিক পদার্থ সেন্ট্রিফিউজ টিউবের নীচে জমা হয়।
১২.২.১ অবক্ষেপণের মৌলিক নীতি
অবক্ষেপণ হল নিলম্বনে থাকা কণাগুলির প্রবণতা যে তরল থেকে তারা বেরিয়ে আসে এবং একটি বাধার বিরুদ্ধে স্থির হয়। এটি তাদের উপর ক্রিয়াশীল শক্তির প্রতিক্রিয়ায় তরলের মধ্য দিয়ে তাদের গতির কারণে হয়। এই শক্তিগুলি মহাকর্ষ এবং কেন্দ্রাতিগ শক্তির কারণে হতে পারে।
১২.২.২ সেন্ট্রিফিউজের প্রকারভেদ
বিভিন্ন ধরনের সেন্ট্রিফিউজ বাণিজ্যিকভাবে পাওয়া যায়। গবেষণার উদ্দেশ্যে সাধারণত ব্যবহৃত সেন্ট্রিফিউজগুলি হল:
- টেবিল টপ/ক্লিনিক্যাল সেন্ট্রিফিউজ বা মাইক্রোফিউজ
- উচ্চ-গতির সেন্ট্রিফিউজ
- আল্ট্রাসেন্ট্রিফিউজ
- ডিফারেনশিয়াল সেন্ট্রিফিউজ
বৃহৎ-ক্ষমতার প্রস্তুতিমূলক সেন্ট্রিফিউজ, উচ্চ গতির রেফ্রিজারেটেড সেন্ট্রিফিউজ এবং আল্ট্রাসেন্ট্রিফিউজ হল সেন্ট্রিফিউজের প্রধান প্রকার।
নীতি এবং প্রয়োগের ভিত্তিতে, নিম্নলিখিত ধরনের অপকেন্দ্রীকরণ করা হয়-
ডিফারেনশিয়াল অপকেন্দ্রীকরণ- এটি বিভিন্ন আকার এবং ঘনত্বের কণার অবক্ষেপণ হার (কেন্দ্রাতিগ বল) এর পার্থক্যের উপর ভিত্তি করে। এটি বড় কোষীয় কাঠামো, নিউক্লিয়ার ভগ্নাংশ, মাইটোকন্ড্রিয়া, ক্লোরোপ্লাস্ট বা বড় প্রোটিন পৃথক করতে ব্যবহৃত হয়।
ঘনত্ব-গ্রেডিয়েন্ট অপকেন্দ্রীকরণ- একই আকার কিন্তু ভিন্ন ঘনত্বের জৈবিক কণা পৃথক করার জন্য, কেউ ঘনত্ব-গ্রেডিয়েন্ট অপকেন্দ্রীকরণ ব্যবহার করতে পারেন। এই ধরনের অপকেন্দ্রীকরণে, সেন্ট্রিফিউজ টিউবগুলিতে একটি ঘনত্ব গ্রেডিয়েন্ট তৈরি করা হয়। তাদের ঘনত্বের উপর নির্ভর করে, বিভিন্ন অণু বিভিন্ন স্তরে জমা হয়। ভারী অণুগুলি বাইরের দিকে চলে যায় এবং হালকা অণুগুলি সেন্ট্রিফিউজ টিউবগুলির ভিতরের অংশে থাকে। ঘনত্বের পার্থক্য যত বেশি, তারা তত দ্রুত চলে।
আল্ট্রাসেন্ট্রিফিউজেশন- যখন অণুগুলি পৃথক করার জন্য খুব উচ্চ গতিতে অপকেন্দ্রীকরণ করা হয়, অর্থাৎ $100,000 \mathrm{x} / \mathrm{g}$ বা তার বেশি, তখন তাকে আল্ট্রাসেন্ট্রিফিউজেশন বলে। আল্ট্রাসেন্ট্রিফিউজে, ঘনত্ব বণ্টনের সঠিক পরিমাপের জন্য কোষকে জৈবিক কণার মধ্য দিয়ে আলোর যাত্রার অনুমতি দিতে হয়।
১২.৩ ইলেক্ট্রোফোরেসিস
ইলেক্ট্রোফোরেসিস হল একটি বৈদ্যুতিক ক্ষেত্রের প্রভাবে ম্যাক্রোঅণুর আধান থেকে ভর অনুপাতের ভিত্তিতে পৃথকীকরণের একটি পদ্ধতি। ইলেক্ট্রোফোরেসিস একটি গ্রীক শব্দ যার অর্থ ‘ইলেকট্রন বহন করা’। উপসর্গ ইলেক্ট্রো বিদ্যুতের দিকে ইঙ্গিত করে যা অণুগুলিকে স্থানান্তরিত করার জন্য প্রয়োজনীয় এবং প্রত্যয় ফোরেসিস মানে ‘স্থানান্তর’ বা ‘চলাচল’। এটি প্রথমবার ১৮০৭ সালে রাশিয়ান অধ্যাপক পিটার ইভানোভিচ স্ট্রাকভ এবং ফার্ডিনান্ড ফ্রেডেরিক রিউস দ্বারা পর্যবেক্ষণ করা হয়েছিল। তারা ধ্রুবক বৈদ্যুতিক ক্ষেত্রের উপস্থিতিতে জলে বিচ্ছুরিত কাদার কণার স্থানান্তর লক্ষ্য করেছিলেন।
নীতি
অনেক গুরুত্বপূর্ণ জৈব অণু যেমন নিউক্লিওটাইড, DNA, RNA, পেপটাইড এবং প্রোটিন আয়নিত গ্রুপ বহন করে, এবং তাই যে কোনও প্রদত্ত $\mathrm{pH}$ এ তারা ক্যাটায়ন বা অ্যানায়ন হিসাবে বৈদ্যুতিকভাবে আধানযুক্ত প্রজাতি হিসাবে দ্রবণে বিদ্যমান থাকে। একটি বৈদ্যুতিক ক্ষেত্রের প্রভাবে, এই কণাগুলি তাদের নেট আধানের উপর নির্ভর করে ক্যাথোড বা অ্যানোডের দিকে স্থানান্তরিত হবে।
একটি অণুর গতিশীলতা তার আকারের ব্যস্তানুপাতিক এবং তার আধানের সরাসরি সমানুপাতিক, যা তাদের একে অপরের থেকে আলাদা করতে দেয়।
১২.৩.১ অ্যাগারোজ জেল ইলেক্ট্রোফোরেসিস
এই ধরনের ইলেক্ট্রোফোরেসিসে, জেলটি অ্যাগারোজ অণুর একটি ম্যাট্রিক্স যা হাইড্রোজেন বন্ধন দ্বারা একসাথে ধরে রাখা হয় এবং ক্ষুদ্র ছিদ্র গঠন করে। DNA পৃথকীকরণের জন্য জেলগুলি প্রায়শই অ্যাগারোজ নামক একটি পলিস্যাকারাইড দিয়ে তৈরি করা হয়, যা শুকনো, গুঁড়া ফ্লেক্স হিসাবে আসে। যখন অ্যাগারোজ একটি বাফারে গরম করা হয় এবং ঠান্ডা হতে দেওয়া হয়, তখন এটি একটি কঠিন, কিছুটা নরম জেল গঠন করবে।
জেল হল জেলি-জাতীয় পদার্থের একটি স্ল্যাব, একটি জেল বক্সে স্থাপন করা। বক্সের এক প্রান্ত একটি ধনাত্মক ইলেক্ট্রোডের সাথে সংযুক্ত, অন্যদিকে অন্য প্রান্তটি একটি ঋণাত্মক ইলেক্ট্রোডের সাথে সংযুক্ত। জেল বক্সটি একটি লবণ-যুক্ত বাফার দ্রবণ দিয়ে পূর্ণ করা হয় যা তড়িৎ পরিবহন করতে পারে। কূপ সহ জেলের প্রান্তটি ঋণাত্মক ইলেক্ট্রোডের দিকে স্থাপন করা হয়। জেলের অন্য প্রান্তটি ধনাত্মক ইলেক্ট্রোডের দিকে স্থাপন করা হয় যার দিকে DNA খণ্ডগুলি স্থানান্তরিত হবে (চিত্র ১২.৪)।
DNA অণুগুলি ঋণাত্মকভাবে আধানযুক্ত। DNA খণ্ডের জেল ইলেক্ট্রোফোরেসিস শুধুমাত্র আকারের ভিত্তিতে তাদের আলাদা করে। ইলেক্ট্রোফোরেসিস ব্যবহার করে, আমরা একটি নমুনায় উপস্থিত বিভিন্ন DNA খণ্ড পরীক্ষা করতে পারি এবং তাদের পরম আকার নির্ধারণ করতে পারি।

চিত্র ১২.৪: অ্যাগারোজ জেল ইলেক্ট্রোফোরেসিস ইউনিট যা পরিচিত আকারের DNA খণ্ড দ্বারা তৈরি DNA ল্যাডারের সাহায্যে নিউক্লিক অ্যাসিড পৃথক করতে।
যখন শক্তি চালু করা হয়, তড়িৎ জেলের মধ্য দিয়ে প্রবাহিত হতে শুরু করে। DNA অণুগুলির ঋণাত্মক আধান থাকে তাদের শর্করা-ফসফেট ব্যাকবোনে ফসফেট গ্রুপের উপস্থিতির কারণে; তাই, তারা ধনাত্মক ইলেক্ট্রোড (অ্যানোড) এর দিকে জেলের ম্যাট্রিক্সের মধ্য দিয়ে চলে।
একটি অ্যাগারোজ DNA জেল চালানোর জন্য ভোল্টেজ $80-120 \mathrm{~V}$ এর মধ্যে থাকে। বৈদ্যুতিক প্রবাহ প্রয়োগ করা হলে, DNA-এর ছোট টুকরোগুলি দীর্ঘগুলির চেয়ে দ্রুত জেল ম্যাট্রিক্সের ছিদ্রের মধ্য দিয়ে চলে। এইভাবে DNA-এর দীর্ঘতম টুকরোগুলি কূপের কাছাকাছি থাকে যখন DNA-এর সংক্ষিপ্ততম টুকরোগুলি জেলের ধনাত্মক প্রান্তের কাছাকাছি থাকে।
১২.৩.২ DNA খণ্ডগুলিকে দৃশ্যমান করা
লক্ষ্য DNA দৃশ্যমান করার জন্য ব্যবহৃত যন্ত্র হল আল্ট্রা-ভায়োলেট (UV) ট্রান্স-ইলুমিনেটর। ইথিডিয়াম ব্রোমাইড (EtBr) সম্ভবত DNA দৃশ্যমান করার জন্য ব্যবহৃত সবচেয়ে সুপরিচিত দাগ। এই দাগটি জেল মিশ্রণে, ইলেক্ট্রোফোরেসিস বাফারে মেশানো যেতে পারে বা জেলটি চালানোর পরে রঞ্জিত করা হয়। EtBr-এর অণুগুলি DNA ক্ষারের মধ্যে আন্তঃপ্রবেশ করে এবং UV আলোর নিচে ফ্লুরোস করে। এর সুবিধা থাকা সত্ত্বেও, ইথিডিয়াম ব্রোমাইড একটি সম্ভাব্য কার্সিনোজেন, তাই এটি অবশ্যই খুব সাবধানে পরিচালনা করতে হবে (চিত্র ১২.৫)।
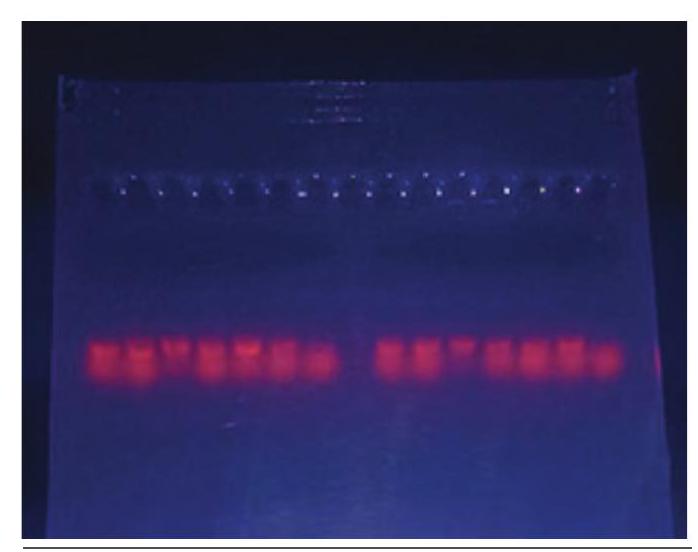
চিত্র ১২.৫: অতিসাবধানতার সাথে UV আলোর নিচে DNA ব্যান্ডগুলির দৃশ্যমানকরণ
১২.৩.৩ পলিঅ্যাক্রিলামাইড জেল ইলেক্ট্রোফোরেসিস (PAGE)
PAGE হল একটি বিশ্লেষণাত্মক পদ্ধতি যা প্রোটিন মিশ্রণের উপাদানগুলিকে তাদের আকারের ভিত্তিতে আলাদা করতে ব্যবহৃত হয়। প্রোটিন অণুগুলিতে অভিন্ন আধান প্রদান করতে, সোডিয়াম ডোডেসিল সালফেট (SDS) নামক একটি অ্যানায়নিক ডিটারজেন্ট ব্যবহার করা হয় প্রোটিনগুলিকে আবদ্ধ করতে এবং তাদের ঋণাত্মক আধান দিতে। তারপর প্রোটিনগুলিকে একটি বৈদ্যুতিক ক্ষেত্রে পলিঅ্যাক্রিলামাইড দিয়ে তৈরি একটি জেল ম্যাট্রিক্স ব্যবহার করে তাদের আকার অনুসারে ইলেক্ট্রোফোরেটিকভাবে আলাদা করা হয়।
পলিঅ্যাক্রিলামাইড অ্যাক্রিলামাইড এবং $\mathrm{N}, \mathrm{N}^{\prime}-$ মিথাইলিন-বিস-অ্যাক্রিলামাইড (BIS) এর মধ্যে পলিমারকরণ বিক্রিয়ার ফলস্বরূপ উৎপন্ন হয় একটি অনুঘটক ব্যবহার করে। পলিমারকরণ বা ক্রস-লিঙ্কিংয়ের মাত্রা অ্যাক্রিলামাইড এবং BIS-এর ঘনত্ব সামঞ্জস্য করে নিয়ন্ত্রণ করা যেতে পারে। ক্রস-লিঙ্কিং যত বেশি, জেল তত শক্ত। জেলের কাঠিন্য, ঘুরে, PAGE-এর সময় জেলের মধ্য দিয়ে ভ্রমণ করার সময় ম্যাক্রোঅণুগুলির দ্বারা অনুভূত ঘর্ষণ নিয়ন্ত্রণ করে, এইভাবে পৃথকীকরণের রেজোলিউশনকে প্রভাবিত করে। আলগা জেল (4-8% অ্যাক্রিলামাইড) উচ্চ আণবিক ওজনের অণুগুলিকে দ্রুত জেলের মধ্য দিয়ে স্থানান্তরিত হতে দেয় যখন শক্ত জেল $(12-20 %$ অ্যাক্রিলামাইড) বড় অণুগুলির স্থানান্তরকে সীমাবদ্ধ করে এবং নির্বাচনভাবে ছোটগুলিকে জেলের মধ্য দিয়ে যেতে দেয়।
১২.৩.৪ ট্র্যাকিং ডাই
যেহেতু DNA, RNA এবং প্রোটিন বেশিরভাগই বর্ণহীন, তাই ইলেক্ট্রোফোরেসিসের সময় জেলের মধ্য দিয়ে তাদের অগ্রগতি সহজে অনুসরণ করা যায় না। তাই, পরিচিত ইলেক্ট্রোফোরেটিক গতিশীলতার অ্যানায়নিক রঞ্জকগুলি সাধারণত নমুনা বাফারে অন্তর্ভুক্ত করা হয়। একটি খুব সাধারণ ট্র্যাকিং ডাই হল ব্রোমোফেনল ব্লু। এই রঞ্জকটি ক্ষারীয় এবং নিরপেক্ষ $\mathrm{pH}$ এ রঙিন, এবং এটি একটি ছোট ঋণাত্মক আধানযুক্ত অণু যা অ্যানোডের দিকে চলে এবং এটি ক্ষারীয় এবং নিরপেক্ষ $\mathrm{pH}$ এ রঙিন। অত্যন্ত গতিশীল অণু হওয়ায় এটি বেশিরভাগ প্রোটিন এবং নিউক্লিক অ্যাসিডের আগে চলে যায়। এটি ইলেক্ট্রোফোরেসিস মাধ্যমের অ্যানোডিক প্রান্তে পৌঁছালে, ইলেক্ট্রোফোরেসিস বন্ধ করা হয়। অন্যান্য সাধারণ ট্র্যাকিং ডাই হল জাইলিন সায়ানল, যার গতিশীলতা কম, এবং অরেঞ্জ জি, যার গতিশীলতা বেশি। জেলে প্রোটিনের দৃশ্যমানকরণ-কুমাসি ব্রিলিয়েন্ট ব্লু $\mathrm{R}-250$ হল সবচেয়ে জনপ্রিয় প্রোটিন দাগ। এটি একটি অ্যানায়নিক রঞ্জক, যা অ-নির্দিষ্টভাবে প্রোটিনের সাথে আবদ্ধ হয়। জেলে প্রোটিনগুলি অ্যাসিটিক অ্যাসিড দ্বারা স্থির করা হয় এবং একই সাথে রঞ্জিত করা হয়। জেলে অন্তর্ভুক্ত অতিরিক্ত রঞ্জকটি একই দ্রবণ দিয়ে রঞ্জক ছাড়াই ডিস্টেইনিং করে অপসারণ করা যেতে পারে। প্রোটিনগুলি একটি পরিষ্কার পটভূমিতে নীল ব্যান্ড হিসাবে সনাক্ত করা হয়। একটি রঞ্জন (প্রোটিন-নির্দিষ্ট) কৌশল দ্বারা দৃশ্যমান করার পরে, একটি প্রোটিনের আকার একটি পরিচিত আণবিক ওজন ল্যাডারের সাথে এর স্থানান্তর দূরত্ব তুলনা করে গণনা করা যেতে পারে।
বক্স ১
জেলি বৈশিষ্ট্যের বিস্ময়কর আবিষ্কার
একজন জাপানি সম্রাট এবং তার রাজকীয় দল তুষার ঝড়ের সময় পাহাড়ে হারিয়ে গিয়েছিলেন এবং একটি ছোট সরাইখানায় পৌঁছেছিলেন; তাদের সাথে তাদের রাতের খাবারের জন্য একটি সামুদ্রিক শৈবাল জেলি খাবার পরিবেশন করা হয়েছিল। সম্ভবত সরাইখানার মালিক খুব বেশি জেলি তৈরি করেছিলেন বা স্বাদ এতটা সুস্বাদু ছিল না কিন্তু কিছু জেলি ফেলে দেওয়া হয়েছিল, রাতে জমে যায় এবং পরে গলে এবং নিষ্কাশন করে ভেঙে যায়, কম ঘনত্বের একটি ফাটা পদার্থ রেখে যায়। সরাইখানার মালিক অবশিষ্টাংশটি নিলেন এবং, তার বিস্ময়ের জন্য, দেখলেন যে আরও জল দিয়ে সিদ্ধ করে, জেলিটি পুনরায় তৈরি করা যেতে পারে।
আগার
কোচ নামে একজন বিজ্ঞানী ব্যাকটেরিয়া চাষ করতে ব্যবহার করতেন কাটা, সিদ্ধ আলুর নির্বীজিত পৃষ্ঠে। এটি অসন্তোষজনক ছিল কারণ ব্যাকটেরিয়া সবসময় আলুতে ভালভাবে বৃদ্ধি পায় না। তারপর তিনি জেলাটিন যোগ করে নিয়মিত তরল মিডিয়া কঠিন করার চেষ্টা করেছিলেন কিন্তু এটি অনেক ব্যাকটেরিয়া দ্বারা হজম হয় এবং তাপমাত্রা $28^{\circ} \mathrm{C}$ এর উপরে উঠলে গলে যায়। একটি ভাল বিকল্প প্রদান করেছিলেন ফ্যানি আইলশেমিয়াস হেসে, ওয়ালথার হেসের স্ত্রী, যিনি কোচের একজন সহকারী ছিলেন। তিনি একটি কঠিনীভবন এজেন্ট হিসাবে আগার ব্যবহারের পরামর্শ দিয়েছিলেন- তিনি কিছু সময়ের জন্য জেলি তৈরি করতে সফলভাবে এটি ব্যবহার করছিলেন। আগার বেশিরভাগ ব্যাকটেরিয়া দ্বারা আক্রান্ত হয়নি এবং $42^{\circ} \mathrm{C}$ এর বেশি তাপমাত্রায় পৌঁছানো পর্যন্ত গলে যায়নি। অ্যাগারোজ হল আগারের দুটি প্রধান উপাদানের একটি, এবং আগারের অন্য উপাদান, অ্যাগারোপেকটিন অপসারণ করে আগার থেকে শুদ্ধ করা হয়।
১২.৪ এনজাইম-লিঙ্কড ইমিউনোসরবেন্ট অ্যাসে (ELISA)
এনজাইম-লিঙ্কড ইমিউনোসরবেন্ট অ্যাসে (ELISA) আবিষ্কার করেছিলেন দুই সুইডিশ বিজ্ঞানী, ইভা এঙ্গভাল এবং পিটার পার্লম্যান ১৯৭১ সালে। ELISA হল একটি পরিমাণগত পদ্ধতি যা একটি প্রদত্ত নমুনায় অ্যান্টিজেন এবং অ্যান্টিবডির ঘনত্ব পরিমাপের জন্য ব্যবহৃত হয়। এটি একটি এনজাইম-উত্প্রেরিত বিক্রিয়ার সাহায্যে অ্যান্টিজেন-অ্যান্টিবডি মিথস্ক্রিয়া পর্যবেক্ষণ করে করা হয়। এই সনাক্তকরণ ব্যবস্থা (একটি এনজাইম-কনজুগেট) একটি নির্দিষ্ট অ্যান্টিবডির সাথে সমযোজীভাবে সংযুক্ত থাকে যা একটি লক্ষ্য অ্যান্টিজেনকে চিনতে পারে। উৎপাদিত রঙের তীব্রতা ELISA রিডার বা স্পেকট্রোফটোমিটার দ্বারা সনাক্ত করা হয়। ELISA অনেক অন্যান্য ইমিউনোলজিকাল অ্যাসের তুলনায় একটি নিরাপদ এবং কম ব্যয়বহুল অ্যাসে।
ELISA-এর বেশ কয়েকটি পরিবর্তন বিকশিত হয়েছে, যা অ্যান্টিজেন বা অ্যান্টিবডির গুণগত সনাক্তকরণ বা পরিমাণগত পরিমাপের অনুমতি দেয়। এই বিভিন্ন ধরনের ELISA গুণগতভাবে অ্যান্টিবডি বা অ্যান্টিজেনের উপস্থিতি সনাক্ত করতে নিয়োজিত করা যেতে পারে। অ্যান্টিবডি বা অ্যান্টিজেনের পরিচিত ঘনত্ব ব্যবহার করে, একটি নমুনার অজানা ঘনত্ব নির্ধারণ করতে একটি স্ট্যান্ডার্ড কার্ভ প্রস্তুত করা হয়।
“
চিত্র ১২.৬. পরোক্ষ ELISA

চিত্র ১২.৭ স্যান্ডউইচ ELISA

চিত্র ১২.৮: প্রতিযোগিতামূলক ELISA
সরাসরি ELISA - সরাসরি ELISA-তে, অ্যান্টিজেন বা নমুনাটি মাইক্রোটিটার প্লেটের কূপগুলিতে আবৃত করা হয় এবং এনজাইম-কনজুগেটেড অ্যান্টিবডি সরাসরি অ্যান্টিজেনের সাথে আবদ্ধ হয়। অ্যান্টিবডির সাথে সংযুক্ত এনজাইমটি তার সাবস্ট্রেটের সাথে বিক্রিয়া করে একটি রঙিন পণ








