অধ্যায় 08 রিডক্স প্রতিক্রিয়াগুলি
“যেখানে অক্সিডেশন ঘটে, সেখানে সর্বদা রিডাকশন ঘটে। বিজ্ঞান প্রায়ই রিডক্স সিস্টেমের অধ্যয়নের মাধ্যমে প্রকাশিত হয়।”
বিজ্ঞান বিভিন্ন ধরনের পদার্থ এবং এক ধরনের পদার্থকে অন্য ধরনের পদার্থে রূপান্তর ঘটানোর বিষয়টি নিয়ে কাজ করে। পদার্থের এক ধরন থেকে অন্য ধরনে রূপান্তর ঘটে যা বিভিন্ন ধরনের প্রতিক্রিয়ার মাধ্যমে ঘটে। এই প্রতিক্রিয়াগুলির মধ্যে একটি গুরুত্বপূর্ণ শ্রেণী হল রিডক্স প্রতিক্রিয়াগুলি। প্রতিবেশী এবং জীববৈজ্ঞানী প্রজন্মের বিভিন্ন ঘটনাই রিডক্স প্রতিক্রিয়াগুলির সাথে যুক্ত। এই প্রতিক্রিয়াগুলি ওষুধ, জীববৈজ্ঞানী, শিল্প, পদার্থবিজ্ঞান এবং কৃষি ক্ষেত্রে ব্যাপকভাবে ব্যবহৃত হয়। এই প্রতিক্রিয়াগুলির গুরুত্ব তথ্য থেকে প্রকাশিত হয় যে বিভিন্ন ধরনের জ্বালানি জ্বালিয়ে ঘরোয়া, পরিবহন এবং অন্যান্য বাণিজ্যিক উদ্দেশ্যে শক্তি পাওয়ার জন্য, উচ্চ প্রতিক্রিয়াশীল ধাতু এবং অ-ধাতু উদ্ভাবন করার জন্য ইলেক্ট্রোকেমিক্যাল প্রক্রিয়া, ক্ষতিকর সোডা তৈরি, সংকুচিত এবং আর্দ্র ব্যাটারির কাজ এবং ধাতুর ক্ষয় সবই রিডক্স প্রক্রিয়ার অধীনে। সাম্প্রতিকভাবে, পরিবেশ সম্পর্কিত বিষয়গুলি যেমন হাইড্রজেন অর্থনীতি (জলাশ্বায়ী হাইড্রজেন জ্বালানি হিসাবে ব্যবহার) এবং ‘অজয় ফোলা’ এর উন্নয়ন রিডক্স ঘটনার অধীনে আরো গুরুত্ব পাচ্ছে।
8.1 রিডক্স প্রতিক্রিয়াগুলির প্রাচীন ধারণা - অক্সিডেশন এবং রিডাকশন প্রতিক্রিয়াগুলি
প্রাথমিকভাবে, অক্সিডেশন শব্দটি একটি উপাদান বা যৌগে অক্সিজেন যোগ করার বর্ণনা করার জন্য ব্যবহৃত হয়েছিল। আবহশক্তির অক্সিজেনের (20%) উপস্থিতির কারণে অনেক উপাদান এর সাথে যুক্ত হয় এবং এটি হল এগুলি প্রায়শই তাদের অক্সাইডের আকারে পৃথিবীতে ঘটে আসার প্রধান কারণ। নিম্নলিখিত প্রতিক্রিয়াগুলি অক্সিডেশন প্রক্রিয়াগুলি হিসাবে প্রকাশ করে যা অক্সিডেশনের সীমিত সংজ্ঞার অনুযায়ী:
$$2 \mathrm{Mg}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{MgO}(\mathrm{s}) \tag{8.1}$$
$$\mathrm{S}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow \mathrm{SO_2}(\mathrm{~g}) \tag{8.2}$$
প্রতিক্রিয়া (8.1) এবং (8.2) এতে অক্সিজেনের যোগস্থানে অক্সিজেন যোগ করার কারণে ম্যাগনেসিয়াম এবং সালফার উপাদানগুলি অক্সিডাইজ হয়েছে। একইভাবে ম্যাথান অক্সিজেনের যোগস্থানে অক্সিডাইজ হয়েছে।
$$\mathrm{CH} _{4}(\mathrm{~g})+2 \mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g})+2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{7.3}$$
প্রতিক্রিয়া (8.3) এতে হাইড্রজেনের পরিবর্তে অক্সিজেন যোগ করার সময় হাইড্রজেন উপাদানটি অপসারিত হয়েছে এমন একটি সাবধানপূর্বক পর্যালোচনা করলে বৈজ্ঞানীদের অক্সিডেশনকে একটি উপাদান থেকে হাইড্রজেন অপসারণের পক্ষে পুনর্ব্যাখ্যা করতে উৎসাহিত হয়েছিল। এই শব্দটির পরিমাপ বৃদ্ধি করে অক্সিডেশন শব্দটি একটি উপাদান থেকে হাইড্রজেন অপসারণের বিষয়টিও অন্তর্ভুক্ত করা হয়েছে। নিম্নলিখিত উদাহরণটি অন্য একটি প্রতিক্রিয়া যেখানে হাইড্রজেন অপসারণ অন্যভাবেও অক্সিডেশন প্রতিক্রিয়া হিসাবে উল্লেখ করা যেতে পারে।
$$ \begin{equation*} 2 \mathrm{H_2} \mathrm{~S}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{~S}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \tag{8.4} \end{equation*} $$
বৈজ্ঞানীদের জ্ঞান বৃদ্ধির সাথে সাথে এই শব্দটি অক্সিডেশনের জন্য প্রতিক্রিয়াগুলির জন্য ব্যবহার করা হয়েছে যা (7.1 থেকে 7.4) অক্সিজেন ছাড়াই অন্য ক্ষতিকর উপাদানগুলি নিয়ে ঘটে। ম্যাগনেসিয়ামের ফ্লুরাইড, ক্লোরাইড এবং সালফারের অক্সিডেশন নিম্নলিখিত প্রতিক্রিয়াগুলি অনুসরণ করে ঘটে:
$$\operatorname{Mg}(\mathrm{s})+\mathrm{F_2} (\mathrm{~g}) \rightarrow \operatorname{MgF_2} (s) \tag{8.5}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{Cl_2} (g) \rightarrow \mathrm{MgCl_2} (s) \tag{8.6}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{S} (s) \rightarrow \operatorname{MgS}(\mathrm{s}) \tag{8.7}$$
প্রতিক্রিয়া 7.5 থেকে 7.7 অক্সিডেশন প্রতিক্রিয়াগুলির অধীনে অন্তর্ভুক্ত করা বৈজ্ঞানীদের হাইড্রজেন অপসারণ ছাড়াই অন্যান্য উপাদানগুলি অপসারণের জন্য অক্সিডেশন হিসাবে বিবেচনা করতে উৎসাহিত করেছে। এই কারণে প্রতিক্রিয়াটি অক্সিডেশন হিসাবে ব্যাখ্যা করা হয়েছে যেখানে পটাসিয়াম ফেরোসায়ানেট থেকে পটাসিয়াম ফেরিসায়ানেটে পরিবর্তিত হওয়ার আগে পটাসিয়াম উপাদানটি অপসারিত হয়েছে। সংক্ষেপে, “অক্সিডেশন” শব্দটি একটি উপাদানে অক্সিজেন/ক্ষতিকর উপাদান যোগ করা বা একটি উপাদান থেকে হাইড্রজেন/অন্যান্য উপাদান অপসারণ হিসাবে সংজ্ঞায়িত হয়েছে।
শুরুতে রিডাকশন একটি যৌগ থেকে অক্সিজেন অপসারণ হিসাবে বিবেচিত হতো। কিন্তু এই শব্দটি বর্তমানে একটি উপাদান থেকে অক্সিজেন/ক্ষতিকর উপাদান অপসারণ বা একটি উপাদানে হাইড্রজেন/অন্যান্য উপাদান যোগ করা অন্তর্ভুক্ত করে ব্যাপক করা হয়েছে।
উপর্যুক্ত সংজ্ঞার অনুযায়ী, নিম্নলিখিতগুলি রিডাকশন প্রক্রিয়ার উদাহরণ:
$$2 \mathrm{HgO}(\mathrm{s}) \xrightarrow{\Delta} 2 \mathrm{Hg}(\mathrm{l})+\mathrm{O_2}(\mathrm{~g}) \tag{8.8}$$
(মারকুরিয়াস অক্সাইড থেকে অক্সিজেন অপসারণ)
$$2 \mathrm{FeCl_3}(\mathrm{aq})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{FeCl_2}(\mathrm{aq})+2 \mathrm{HCl}(\mathrm{aq}) \tag{8.9}$$
(ফেরি ক্লোরাইড থেকে ক্লোরাইড উপাদান অপসারণ)
$$\mathrm{CH_2}=\mathrm{CH_2}(\mathrm{~g})+\mathrm{H_2}(\mathrm{~g}) \rightarrow \mathrm{H_3} \mathrm{C}-\mathrm{CH_3}(\mathrm{~g})\tag{8.10}$$
(হাইড্রজেন যোগ)
$$2 \mathrm{HgCl_2}(\mathrm{aq})+\mathrm{SnCl_2}(\mathrm{aq}) \rightarrow \mathrm{Hg_2} \mathrm{Cl_2}(\mathrm{~s})+\mathrm{SnCl_4}(\mathrm{aq})\tag{8.11}$$
(মারকুরিয়াস ক্লোরাইডে মারকুরি যোগ)
প্রতিক্রিয়া (8.11) এতে স্ট্যানোস ক্লোরাইডের স্ট্যাননিক ক্লোরাইডে অক্সিডেশন ঘটেছে কারণ এতে ক্লোরাইড উপাদানটি যোগ করা হয়েছে। শীঘ্রই এটি স্পষ্ট হয়ে গেল যে অক্সিডেশন এবং রিডাকশন সর্বদা একই সময়ে ঘটে (যেহেতু উপরে দেওয়া সব সমীকরণগুলি পুনরায় পর্যালোচনা করলে এটি প্রকাশিত হবে), তাই এই ধরনের রাসায়নিক প্রতিক্রিয়াগুলির জন্য “রিডক্স” শব্দটি তৈরি করা হয়েছে।
সমস্যা 8.1
নিম্নলিখিত প্রতিক্রিয়াগুলিতে অক্সিডেশন এবং রিডাকশনের জন্য উপস্থিত উপাদানগুলি সনাক্ত করুন:
(i) $\mathrm{H_2} \mathrm{~S}$ (g) $+\mathrm{Cl_2}$ (g) $\rightarrow 2 \mathrm{HCl}$ (g) $+\mathrm{S}$ (s)
(ii) $3 \mathrm{Fe_3} \mathrm{O_4}$ (s) $+8 \mathrm{Al}$ (s) $\rightarrow 9 \mathrm{Fe}$ (s) $+4 \mathrm{Al_2} \mathrm{O_3}(\mathrm{~s})$
(iii) $2 \mathrm{Na}$ (s) $+\mathrm{H_2}$ (g) $\rightarrow 2 \mathrm{NaH}$ (s)
সমাধান
(i) $\mathrm{H_2} \mathrm{~S}$ অক্সিডাইজ হয়েছে কারণ এতে একটি আরও ক্ষতিকর উপাদান, ক্লোরাইড যোগ করা হয়েছে হাইড্রজেনের বাইরে (বা একটি আরও অন্যান্য উপাদান, হাইড্রজেন সালফার থেকে অপসারিত হয়েছে)। ক্লোরাইড রিডাকশন হয়েছে কারণ এতে হাইড্রজেন যোগ করা হয়েছে।
(ii) অ্যালুমিনিয়াম অক্সিডাইজ হয়েছে কারণ এতে অক্সিজেন যোগ করা হয়েছে। ফেরো ফেরি অক্সাইড $\left(\mathrm{Fe_3} \mathrm{O_4}\right)$ রিডাকশন হয়েছে কারণ এতে অক্সিজেন অপসারিত হয়েছে।
(iii) ক্ষতিকরতার ধারণার সাবধানপূর্বক ব্যবহার করে আমরা মনে করতে পারি যে সোডিয়াম অক্সিডাইজ হয়েছে এবং হাইড্রজেন রিডাকশন হয়েছে।
এই প্রতিক্রিয়া (iii) এখানে নির্বাচিত হয়েছে যাতে আমাদের রিডক্স প্রতিক্রিয়াগুলি ব্যাখ্যা করার আরেকটি উপায় নিয়ে চিন্তা করতে হয়।
8.2 ইলেক্ট্রন ট্রান্সফার প্রতিক্রিয়াগুলির মাধ্যমে রিডক্স প্রতিক্রিয়াগুলি
আমরা ইতিমধ্যে জানতাম যে প্রতিক্রিয়াগুলি রিডক্স প্রতিক্রিয়াগুলি কারণ এই প্রতিক্রিয়াগুলিতে সোডিয়াম অক্সিডাইজ হয়েছে কারণ সোডিয়ামে অক্সিজেন বা আরও ক্ষতিকর উপাদান যোগ করা হয়েছে।
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaCl}(\mathrm{s})\tag{8.12}$$
$$4 \mathrm{Na}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na_2} \mathrm{O}(\mathrm{s})\tag{8.13}$$
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{S}(\mathrm{s}) \rightarrow \mathrm{Na_2} \mathrm{~S}(\mathrm{~s}) \tag{8.14}$$
একইভাবে ক্লোরাইড, অক্সিজেন এবং সালফার রিডাকশন হয়েছে কারণ এগুলিতে অন্যান্য উপাদান সোডিয়াম যোগ করা হয়েছে। আমাদের রাসায়নিক বন্ধনের জ্ঞান থেকে আমরা জানি যে সোডিয়াম ক্লোরাইড, সোডিয়াম অক্সাইড এবং সোডিয়াম সালফাইড ইলেক্ট্রোনিক যৌগ এবং সম্ভবত আরও ভাল হয় যেমন $\mathrm{Na}^{+} \mathrm{Cl}^{-}( \mathrm{s}),\left(\mathrm{Na}^{+} \right)_2 \mathrm{O}^{2-}( \mathrm{s})$, $ \left(\mathrm{Na}^{+} \right)_2$ $\mathrm{S}^{2-}( \mathrm{s})$। উত্পন্ন উপাদানগুলিতে চার্জের উপস্থিতি প্রতিক্রিয়া (8.12 থেকে 8.14) একই ভাবে নিম্নলিখিত উপায়ে পুনর্লিখিত করতে উৎসাহিত করে:
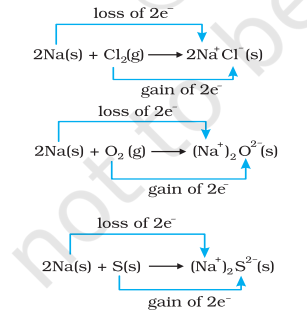
সুবিধার জন্য, উপরের প্রতিটি প্রক্রিয়া দুটি আলাদা ধাপের মধ্যে বিবেচনা করা যেতে পারে, একটি ইলেক্ট্রন হারানোর এবং অন্যটি ইলেক্ট্রন পাওয়ার। উদাহরণ হিসাবে, আমরা এই উদাহরণগুলি আরও বিস্তারিত করতে পারি যেমন, সোডিয়াম ক্লোরাইডের গঠন।
$2 \mathrm{Na}(\mathrm{s}) \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
$\mathrm{Cl_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{Cl}^{-}(\mathrm{g})$
উপরের প্রতিটি ধাপকে হাফ প্রতিক্রিয়া বলা হয়, যা স্পষ্টভাবে ইলেক্ট্রনের অংশগ্রহণ দেখায়। হাফ প্রতিক্রিয়াগুলির যোগফল সামগ্রিক প্রতিক্রিয়া দেয়:
$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na}^{+} \mathrm{Cl}^{-}(\mathrm{s})$ বা $2 \mathrm{NaCl}(\mathrm{s})$
প্রতিক্রিয়া 8.12 থেকে 8








