અધ્યાય 04 રાસાયણિક બંધન અને આણ્વીય રચના
“વૈજ્ઞાનિકો સતત નવા સંયોજનો શોધી રહ્યા છે, તેમના વિશેના તથ્યોને વ્યવસ્થિત રીતે ગોઠવી રહ્યા છે, હાલના જ્ઞાનથી સમજાવવાનો પ્રયાસ કરી રહ્યા છે, અગાઉના મંતવ્યોમાં સુધારો કરવા અથવા નવા અવલોકિત તથ્યોને સમજાવવા માટે સિદ્ધાંતો વિકસાવવા માટે સંગઠિત કરી રહ્યા છે.”
દ્રવ્ય એક અથવા વિવિધ પ્રકારના તત્ત્વોથી બનેલું છે. સામાન્ય પરિસ્થિતિઓમાં, કુલીન વાયુઓ સિવાય, કોઈપણ અન્ય તત્ત્વ પ્રકૃતિમાં સ્વતંત્ર પરમાણુ તરીકે અસ્તિત્વમાં નથી. જો કે, પરમાણુઓનું એક સમૂહ એક જાતિ તરીકે લાક્ષણિક ગુણધર્મો સાથે સાથે અસ્તિત્વમાં રહેતું જોવા મળે છે. આવા પરમાણુઓના સમૂહને અણુ કહેવામાં આવે છે. દેખીતી રીતે, આ ઘટક પરમાણુઓને અણુઓમાં એકસાથે રાખતું કોઈક બળ હોવું જોઈએ. વિવિધ રાસાયણિક જાતિઓમાં વિવિધ ઘટકો (પરમાણુઓ, આયનો, વગેરે)ને એકસાથે રાખતું આકર્ષક બળને રાસાયણિક બંધ કહેવામાં આવે છે. રાસાયણિક સંયોજનોની રચના વિવિધ તત્ત્વોના પરમાણુઓના વિવિધ રીતે સંયોજનના પરિણામે થાય છે, તેથી ઘણા પ્રશ્નો ઊભા થાય છે. પરમાણુઓ શા માટે જોડાય છે? ફક્ત ચોક્કસ સંયોજનો શા માટે શક્ય છે? કેટલાક પરમાણુઓ જોડાય છે જ્યારે અમુક અન્ય શા માટે જોડાતા નથી? અણુઓ ચોક્કસ આકારો ધરાવે છે શા માટે? આવા પ્રશ્નોના જવાબ આપવા માટે સમયાંતરે વિવિધ સિદ્ધાંતો અને ખ્યાલો રજૂ કરવામાં આવ્યા છે. આ છે કોસેલ-લુઇસ અભિગમ, વેલેન્સ શેલ ઇલેક્ટ્રોન પેર રિપલ્શન (VSEPR) સિદ્ધાંત, વેલેન્સ બોન્ડ (VB) સિદ્ધાંત અને મોલેક્યુલર ઑર્બિટલ (MO) સિદ્ધાંત. વેલેન્સના વિવિધ સિદ્ધાંતોની ઉત્ક્રાંતિ અને રાસાયણિક બંધનોની પ્રકૃતિનું અર્થઘટન પરમાણુની રચના, તત્ત્વોની ઇલેક્ટ્રોનિક રચના અને આવર્ત કોષ્ટકની સમજણમાં થયેલી પ્રગતિઓ સાથે નજીકથી સંબંધિત છે. દરેક સિસ્ટમ વધુ સ્થિર થવાનું વલણ ધરાવે છે અને બંધન સ્થિરતા પ્રાપ્ત કરવા માટે સિસ્ટમની ઊર્જા ઘટાડવાની પ્રકૃતિની રીત છે.
4.1 રાસાયણિક બંધન માટે કોસેલ-લુઇસ અભિગમ
ઇલેક્ટ્રોનના સંદર્ભમાં રાસાયણિક બંધનની રચનાને સમજાવવા માટે ઘણા પ્રયાસો કરવામાં આવ્યા હતા, પરંતુ તે 1916માં જ ત્યારે હતું જ્યારે કોસેલ અને લુઇસ સ્વતંત્ર રીતે સંતોષકારક સમજૂતી આપવામાં સફળ થયા હતા. તેઓ કુલીન વાયુઓની નિષ્ક્રિયતા પર આધારિત વેલેન્સની કેટલીક તાર્કિક સમજૂતી આપનારા પ્રથમ હતા.
લુઇસે પરમાણુને ધન વીજભારિત ‘કર્નલ’ (ન્યુક્લિયસ અને આંતરિક ઇલેક્ટ્રોન) અને બાહ્ય કક્ષ તરીકે ચિત્રિત કર્યું જે વધુમાં વધુ આઠ ઇલેક્ટ્રોન ધરાવી શકે છે. તેણે આગળ ધારણા કરી કે આ આઠ ઇલેક્ટ્રોન ‘કર્નલ’ને ઘેરતા ઘનના ખૂણાઓ પર કબજો કરે છે. આમ, સોડિયમનો એક બાહ્ય કક્ષ ઇલેક્ટ્રોન ઘનના એક ખૂણા પર કબજો કરશે, જ્યારે કુલીન વાયુના કિસ્સામાં તમામ આઠ ખૂણા કબજે કરવામાં આવશે. ઇલેક્ટ્રોનનું આ અષ્ટક ખાસ કરીને સ્થિર ઇલેક્ટ્રોનિક ગોઠવણીનું પ્રતિનિધિત્વ કરે છે. લુઇસે અનુમાન કર્યું કે જ્યારે પરમાણુઓ રાસાયણિક બંધનો દ્વારા જોડાયેલા હોય ત્યારે તેઓ સ્થિર અષ્ટક પ્રાપ્ત કરે છે. સોડિયમ અને ક્લોરિનના કિસ્સામાં, આ સોડિયમમાંથી ક્લોરિનમાં એક ઇલેક્ટ્રોનના સ્થાનાંતરણ દ્વારા થઈ શકે છે જે $\mathrm{Na}^+$ અને $\mathrm{Cl}^{-}$ આયનો આપે છે. $ \mathrm{Cl}_2, \mathrm{H}_2, \mathrm{~F}_2 $, વગેરે જેવા અન્ય અણુઓના કિસ્સામાં, બંધન પરમાણુઓ વચ્ચે ઇલેક્ટ્રોનની જોડીના વહેંચણી દ્વારા રચાય છે. આ પ્રક્રિયામાં દરેક પરમાણુ ઇલેક્ટ્રોનના સ્થિર બાહ્ય અષ્ટક પ્રાપ્ત કરે છે.
લુઇસ સંકેતો: અણુની રચનામાં, ફક્ત બાહ્ય કક્ષના ઇલેક્ટ્રોન જ રાસાયણિક સંયોજનમાં ભાગ લે છે અને તેમને વેલેન્સ ઇલેક્ટ્રોન તરીકે ઓળખવામાં આવે છે. આંતરિક કક્ષના ઇલેક્ટ્રોન સારી રીતે સુરક્ષિત હોય છે અને સામાન્ય રીતે સંયોજન પ્રક્રિયામાં સામેલ હોતા નથી. અમેરિકન રસાયણશાસ્ત્રી જી.એન. લુઇસે પરમાણુમાં વેલેન્સ ઇલેક્ટ્રોનનું પ્રતિનિધિત્વ કરવા માટે સરળ સંકેતો રજૂ કર્યા. આ સંકેતોને લુઇસ સંકેતો કહેવામાં આવે છે. ઉદાહરણ તરીકે, બીજા આવર્તના તત્ત્વો માટે લુઇસ સંકેતો નીચે પ્રમાણે છે:

લુઇસ સંકેતોનું મહત્વ: સંકેતની આસપાસના બિંદુઓની સંખ્યા વેલેન્સ ઇલેક્ટ્રોનની સંખ્યાનું પ્રતિનિધિત્વ કરે છે. વેલેન્સ ઇલેક્ટ્રોનની આ સંખ્યા તત્ત્વના સામાન્ય અથવા સમૂહ વેલેન્સની ગણતરી કરવામાં મદદ કરે છે. તત્ત્વોનો સમૂહ વેલેન્સ સામાન્ય રીતે લુઇસ સંકેતોમાં બિંદુઓની સંખ્યા અથવા 8 ઓછા બિંદુઓ અથવા વેલેન્સ ઇલેક્ટ્રોનની સંખ્યા જેટલો હોય છે.
રાસાયણિક બંધન સંબંધિત, કોસેલે નીચેના તથ્યો તરફ ધ્યાન દોર્યું:
- આવર્ત કોષ્ટકમાં, ખૂબ જ વિદ્યુતઋણાત્મક હેલોજન અને ખૂબ જ વિદ્યુતધનાત્મક ક્ષાર ધાતુઓ કુલીન વાયુઓ દ્વારા અલગ પડે છે;
- હેલોજન પરમાણુમાંથી ઋણ આયન અને ક્ષાર ધાતુ પરમાણુમાંથી ધન આયનની રચના સંબંધિત પરમાણુઓ દ્વારા ઇલેક્ટ્રોનના લાભ અને ખોય સાથે સંકળાયેલી છે;
- આ રીતે રચાયેલા ઋણ અને ધન આયનો સ્થિર કુલીન વાયુ ઇલેક્ટ્રોનિક રચનાઓ પ્રાપ્ત કરે છે. કુલીન વાયુઓ (હીલિયમ સિવાય જે ઇલેક્ટ્રોનનું દ્વિગુણ ધરાવે છે) આઠ (અષ્ટક) ઇલેક્ટ્રોનની ખાસ કરીને સ્થિર બાહ્ય કક્ષ રચના ધરાવે છે, $n s^{2} n p^{6}$.
- ઋણ અને ધન આયનો વિદ્યુતસ્થિતિક આકર્ષણ દ્વારા સ્થિર થાય છે.
ઉદાહરણ તરીકે, ઉપરોક્ત યોજના અનુસાર, સોડિયમ અને ક્લોરિનમાંથી $\mathrm{NaCl}$ ની રચનાને નીચે પ્રમાણે સમજાવી શકાય છે:
| $\mathrm{Na}$ | $\rightarrow$ | $\mathrm{Na}^{+}+\mathrm{e}^{-}$ |
| $[\mathrm{Ne}] 3 \mathrm{~s}^{1}$ | $[\mathrm{Ne}]$ | |
| $\mathrm{Cl}+\mathrm{e}^{-}$ | $\rightarrow$ | $\mathrm{Cl}^{-}$ |
| $[\mathrm{Ne}] 3 s^{2} 3 p^{5}$ | $[\mathrm{Ne}] 3 s^{2} 3 p^{6}$ અથવા $[\mathrm{Ar}]$ | |
| $\mathrm{Na}^{+}+\mathrm{Cl}^{-}$ | $\rightarrow$ | $\mathrm{NaCl}$ અથવા $\mathrm{Na}^{+} \mathrm{Cl}^{-}$ |
એ જ રીતે $\mathrm{CaF}_{2}$ ની રચના નીચે પ્રમાણે દર્શાવી શકાય છે:
| $\mathrm{Ca}$ | $\rightarrow$ | $\mathrm{Ca}^{2+}+2 \mathrm{e}^{-}$ |
| $[\mathrm{Ar}] 4 s^{2}$ | $[\mathrm{Ar}]$ | |
| $\mathrm{F}+\mathrm{e}^{-}$ | $\rightarrow$ | $\mathrm{F}^{-}$ |
| $[\mathrm{He}] 2 s^{2} 2 p^{5}$ | $[\mathrm{He}] 2 s^{2} 2 p^{6}$ અથવા $[\mathrm{Ne}]$ | |
| $\mathrm{Ca}^{2+}+2 \mathrm{~F}^{-}$ | $\rightarrow$ | $\mathrm{CaF}_2$ અથવા $\mathrm{Ca}^{2+}\left(\mathrm{F}^{-}\right)_2$ |
ધન અને ઋણ આયનો વચ્ચેના વિદ્યુતસ્થિતિક આકર્ષણના પરિણામે રચાયેલા બંધને વિદ્યુતસંયોજક બંધ તરીકે ઓળખવામાં આવે છે. આમ, વિદ્યુતસંયોજકતા આયન પરના એકમ વીજભાર(ઓ)ની સંખ્યા જેટલી હોય છે. આમ, કેલ્શિયમને બેનો ધન વિદ્યુતસંયોજકતા અસાઇન કરવામાં આવે છે, જ્યારે ક્લોરિનને એકની ઋણ વિદ્યુતસંયોજકતા અસાઇન કરવામાં આવે છે.
કોસેલના અનુમાનો ઇલેક્ટ્રોન સ્થાનાંતરણ દ્વારા આયન-રચના અને આયનિક સ્ફટિકીય સંયોજનોની રચના સંબંધિત આધુનિક ખ્યાલો માટે આધાર પૂરો પાડે છે. આયનિક સંયોજનોની સમજણ અને વ્યવસ્થિતીકરણમાં તેના મંતવ્યો મહાન મૂલ્યના સાબિત થયા છે. તે જ સમયે તેણે એ હકીકતને પણ સ્વીકારી કે મોટી સંખ્યામાં સંયોજનો આ ખ્યાલોમાં ફિટ થતા ન હતા.
4.1.1 અષ્ટક નિયમ
કોસેલ અને લુઇસે 1916માં રાસાયણિક બંધનની ઇલેક્ટ્રોનિક સિદ્ધાંત તરીકે ઓળખાતા પરમાણુઓ વચ્ચેના રાસાયણિક સંયોજનનો એક મહત્વપૂર્ણ સિદ્ધાંત વિકસાવ્યો. આ મુજબ, પરમાણુઓ તેમની વેલેન્સ કક્ષમાં અષ્ટક ધરાવવા માટે એક પરમાણુમાંથી બીજા પરમાણુમાં વેલેન્સ ઇલેક્ટ્રોનના સ્થાનાંતરણ (લાભ અથવા ખોય) અથવા વેલેન્સ ઇલેક્ટ્રોનના વહેંચણી દ્વારા જોડાઈ શકે છે. આને અષ્ટક નિયમ તરીકે ઓળખવામાં આવે છે.
4.1.2 સહસંયોજક બંધ
લેંગમુયર (1919) ને અષ્ટકની સ્થિર ઘનાકાર ગોઠવણીના ખ્યાલને છોડીને અને સહસંયોજક બંધ શબ્દ રજૂ કરીને લુઇસના અનુમાનોને શુદ્ધ કર્યા. લુઇસ-લેંગમુયર સિદ્ધાંતને ક્લોરિન અણુ, $\mathrm{Cl}_2$ ની રચનાને ધ્યાનમાં લઈને સમજી શકાય છે. ઇલેક્ટ્રોનિક રચના $[\mathrm{Ne}] 3 s^2 3 p^5$ સાથેનો $\mathrm{Cl}$ પરમાણુ, આર્ગોન રચનાથી એક ઇલેક્ટ્રોન ઓછો છે. $\mathrm{Cl}_2$ અણુની રચનાને બે ક્લોરિન પરમાણુઓ વચ્ચે ઇલેક્ટ્રોનની જોડીના વહેંચણીના સંદર્ભમાં સમજી શકાય છે, દરેક ક્લોરિન પરમાણુ વહેંચાયેલી જોડીમાં એક ઇલેક્ટ્રોન ફાળો આપે છે. આ પ્રક્રિયામાં બંને ક્લોરિન પરમાણુઓ નજીકના કુલીન વાયુ (એટલે કે, આર્ગોન) ના બાહ્ય કક્ષ અષ્ટક પ્રાપ્ત કરે છે.

બે Cl પરમાણુઓ વચ્ચે સહસંયોજક બંધ
બિંદુઓ ઇલેક્ટ્રોનનું પ્રતિનિધિત્વ કરે છે. આવી રચનાઓને લુઇસ ડોટ સ્ટ્રક્ચર તરીકે ઓળખવામાં આવે છે.
લુઇસ ડોટ સ્ટ્રક્ચર અન્ય અણુઓ માટે પણ લખી શકાય છે, જેમાં જોડાતા પરમાણુઓ સમાન અથવા અલગ હોઈ શકે છે. મહત્વપૂર્ણ શરતો નીચે મુજબ છે:
- દરેક બંધ પરમાણુઓ વચ્ચે ઇલેક્ટ્રોન જોડીના વહેંચણીના પરિણામે રચાય છે.
- દરેક જોડાતા પરમાણુ વહેંચાયેલી જોડીમાં ઓછામાં ઓછો એક ઇલેક્ટ્રોન ફાળો આપે છે.
- ઇલેક્ટ્રોનના વહેંચણીના પરિણામે જોડાતા પરમાણુઓ બાહ્ય કક્ષ કુલીન વાયુ રચનાઓ પ્રાપ્ત કરે છે.
- આમ પાણી અને કાર્બન ટેટ્રાક્લોરાઇડ અણુઓમાં, સહસંયોજક બંધની રચનાને નીચે પ્રમાણે દર્શાવી શકાય છે:

આમ, જ્યારે બે પરમાણુઓ એક ઇલેક્ટ્રોન જોડી વહેંચે છે ત્યારે તેઓ એક સિંગલ સહસંયોજક બંધ દ્વારા જોડાયેલા હોવાનું કહેવાય છે. ઘણા સંયોજનોમાં આપણી પાસે પરમાણુઓ વચ્ચે બહુવિધ બંધ હોય છે. બહુવિધ બંધની રચના બે પરમાણુઓ વચ્ચે એક કરતાં વધુ ઇલેક્ટ્રોન જોડીના વહેંચણીની કલ્પના કરે છે. જો બે પરમાણુઓ બે જોડી ઇલેક્ટ્રોન વહેંચે છે, તો તેમની વચ્ચેના સહસંયોજક બંધને ડબલ બંધ કહેવામાં આવે છે. ઉદાહરણ તરીકે, કાર્બન ડાયોક્સાઇડ અણુમાં, આપણી પાસે કાર્બન અને ઓક્સિજન પરમાણુઓ વચ્ચે બે ડબલ બંધ હોય છે. એ જ રીતે ઇથીન અણુમાં બે કાર્બન પરમાણુઓ ડબલ બંધ દ્વારા જોડાયેલા હોય છે..

$\mathrm{C} _{2} \mathrm{H} _{4}$ અણુ
જ્યારે જોડાતા પરમાણુઓ ત્રણ ઇલેક્ટ્રોન જોડી વહેંચે છે જેમ કે $N_{2}$ અણુમાં બે નાઇટ્રોજન પરમાણુઓના કિસ્સામાં અને ઇથાઇન અણુમાં બે કાર્બન પરમાણુઓ, ત્યારે ટ્રિપલ બંધ રચાય છે.
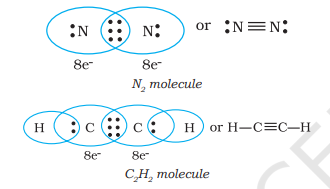
4.1.3 સરળ અણુઓનું લુઇસ પ્રતિનિધિત્વ (લુઇસ સ્ટ્રક્ચર)
લુઇસ ડોટ સ્ટ્રક્ચર અણુઓ અને આયનોમાં બંધનની તસ્વીર વહેંચાયેલી ઇલેક્ટ્રોન જોડી અને અષ્ટક નિયમના સંદર્ભમાં પૂરી પાડે છે. જ્યારે આવી તસ્વીર અણુના બંધન અને વર્તનને સંપૂર્ણ રીતે સમજાવી શકતી નથી, તો પણ તે મોટા પ્રમાણમાં અણુની રચના અને ગુણધર્મોને સમજવામાં મદદ કરે છે. આમ, અણુઓના લુઇસ ડોટ સ્ટ્રક્ચર લખવા ખૂબ જ ઉપયોગી છે. નીચેના પગલાં અપનાવીને લુઇસ ડોટ સ્ટ્રક્ચર લખી શકાય છે:
- સ્ટ્રક્ચર લખવા માટે જરૂરી ઇલેક્ટ્રોનની કુલ સંખ્યા જોડાતા પરમાણુઓના વેલેન્સ ઇલેક્ટ્રોન ઉમેરીને મેળવવામાં આવે છે. ઉદાહરણ તરીકે, $\mathrm{CH}_{4}$ અણુમાં બંધન માટે આઠ વેલેન્સ ઇલેક્ટ્રોન ઉપલબ્ધ છે (કાર્બનમાંથી 4 અને ચાર હાઇડ્રોજન પરમાણુઓમાંથી 4).
- ઋણ આયનો માટે, દરેક ઋણ વીજભારનો અર્થ એક ઇલેક્ટ્રોનનો ઉમેરો થાય છે. ધન આયનો માટે, દરેક ધન વીજભાર વેલેન્સ ઇલેક્ટ્રોનની કુલ સંખ્યામાંથી એક ઇલેક્ટ્રોનની બાદબાકી પરિણમે છે. ઉદાહરણ તરીકે, $CO_3^{2-}$ આયન માટે, બે ઋણ વીજભારો સૂચવે છે કે તટસ્થ પરમાણુઓ દ્વારા પૂરા પાડવામાં આવેલા ઇલેક્ટ્રોન કરતાં બે વધારાના ઇલેક્ટ્રોન છે. $\mathrm{NH}_{4}^{+}$ આયન માટે, એક ધન વીજભાર તટસ્થ પરમાણુઓના સમૂહમાંથી એક ઇલેક્ટ્રોનની ખોય સૂચવે છે.
- જોડાતા પરમાણુઓના રાસાયણિક સંકેતો જાણીને અને સંયોજનની કંકાલ રચના (જાણીતી અથવા બુદ્ધિપૂર્વક અનુમાનિત) નું જ્ઞાન ધરાવીને, કુલ બંધોના પ્રમાણમાં પરમાણુઓ વચ્ચે બંધન વહેંચાયેલી જોડી તરીકે કુલ ઇલેક્ટ્રોન વિતરિત કરવાનું સરળ છે.
- સામાન્ય રીતે, ઓછામાં ઓછો વિદ્યુતઋણાત્મક પરમાણુ અણુ/આયનમાં કેન્દ્રીય સ્થાન ધરાવે છે. ઉદાહરણ તરીકે $\mathrm{NF}_3$ અને $CO_3^{2-}$ માં, નાઇટ્રોજન અને કાર્બન કેન્દ્રીય પરમાણુઓ છે જ્યારે ફ્લોરિન અને ઓક્સિજન ટર્મિનલ સ્થાનો ધરાવે છે.
- સિંગલ બંધ માટે વહેંચાયેલી ઇલેક્ટ્રોન જોડીનું હિસાબ કાઢ્યા પછી, બાકીની ઇલેક્ટ્રોન જોડી બહુવિધ બંધ માટે ઉપયોગમાં લેવાય છે અથવા એકલ જોડી તરીકે રહે છે. મૂળભૂત આવશ્યકતા એ છે કે દરેક બંધિત પરમાણુને ઇલેક્ટ્રોનનું અષ્ટક મળે.
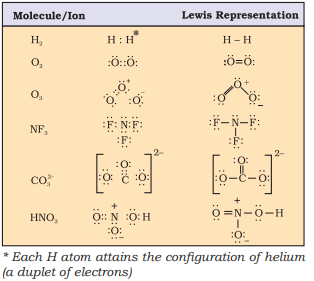
થોડા અણુઓ/આયનોના લુઇસ પ્રતિનિધિત્વ કોષ્ટક 4.1 માં આપવામાં આવ્યા છે.
કોષ્ટક 4.1 કેટલાક અણુઓનું લુઇસ પ્રતિનિધિત્વ
સમસ્યા 4.1
$\mathrm{CO}$ અણુનું લુઇસ ડોટ સ્ટ્રક્ચર લખો.
ઉકેલ
પગલું 1. કાર્બન અને ઓક્સિજન પરમાણુઓના વેલેન્સ ઇલેક્ટ્રોનની કુલ સંખ્યા ગણો. કાર્બન અને ઓક્સિજન પરમાણુઓની બાહ્ય (વેલેન્સ) કક્ષ રચનાઓ છે: $2 s^{2} 2 p^{2}$ અને $2 s^{2} 2 p^{4}$, અનુક્રમે. ઉપલબ્ધ વેલેન્સ ઇલેક્ટ્રોન $4+6=10$ છે.
પગલું 2. $\mathrm{CO}$ ની કંકાલ રચના આ રીતે લખવામાં આવે છે: C O
પગલું 3. $\mathrm{C}$ અને $\mathrm{O}$ વચ્ચે એક સિંગલ બંધ (એક વહેંચાયેલી ઇલેક્ટ્રોન જોડી) દોરો અને $\mathrm{O}$ પર અષ્ટક પૂર્ણ કર








