અધ્યાય 08 રેડોક્સ પ્રક્રિયાઓ
“જ્યાં ઑક્સિડેશન હોય છે, ત્યાં હંમેશા રિડક્શન હોય છે રસાયણવિજ્ઞાન અનિવાર્યપણે રેડોક્સ પ્રણાલીઓનો અભ્યાસ છે.”
રસાયણવિજ્ઞાન પદાર્થોની વિવિધતાઓ અને એક પ્રકારના પદાર્થનું બીજા પ્રકારના પદાર્થમાં રૂપાંતર સાથે વ્યવહાર કરે છે. પદાર્થનું એક પ્રકારથી બીજા પ્રકારમાં રૂપાંતરણ વિવિધ પ્રકારની પ્રક્રિયાઓ દ્વારા થાય છે. આવી પ્રક્રિયાઓની એક મહત્વપૂર્ણ શ્રેણી રેડોક્સ પ્રક્રિયાઓ છે. અસંખ્ય ઘટનાઓ, ભૌતિક તેમજ જૈવિક બંને, રેડોક્સ પ્રક્રિયાઓ સાથે સંકળાયેલી છે. આ પ્રક્રિયાઓને ફાર્માસ્યુટિકલ, જૈવિક, ઔદ્યોગિક, ધાતુશાસ્ત્રીય અને કૃષિ ક્ષેત્રોમાં વ્યાપક ઉપયોગ મળે છે. આ પ્રક્રિયાઓનું મહત્વ એ હકીકતથી સ્પષ્ટ છે કે ઘરેલું, પરિવહન અને અન્ય વ્યાપારી હેતુઓ માટે ઊર્જા મેળવવા માટે વિવિધ પ્રકારના ઇંધણનું બળવું, અત્યંત પ્રતિક્રિયાશીલ ધાતુઓ અને અધાતુઓના નિષ્કર્ષણ માટે વિદ્યુતરાસાયણિક પ્રક્રિયાઓ, કૉસ્ટિક સોડા જેવા રાસાયણિક સંયોજનોનું ઉત્પાદન, શુષ્ક અને ભીના બેટરીઓનું સંચાલન અને ધાતુઓનું ક્ષય રેડોક્સ પ્રક્રિયાઓના ક્ષેત્રમાં આવે છે. તાજેતરમાં, હાઇડ્રોજન ઇકોનોમી (ઇંધણ તરીકે પ્રવાહી હાઇડ્રોજનનો ઉપયોગ) અને ‘ઓઝોન હોલ’ નો વિકાસ જેવા પર્યાવરણીય મુદ્દાઓ રેડોક્સ ઘટના હેઠળ આવવા લાગ્યા છે.
8.1 રેડોક્સ પ્રક્રિયાઓની શાસ્ત્રીય કલ્પના - ઑક્સિડેશન અને રિડક્શન પ્રક્રિયાઓ
મૂળભૂત રીતે, ઑક્સિડેશન શબ્દનો ઉપયોગ કોઈ તત્વ અથવા સંયોજનમાં ઑક્સિજનની ઉમેરણીને વર્ણવવા માટે થતો હતો. વાતાવરણમાં ડાયોક્સિજનની હાજરી (20%)ને કારણે, ઘણાં તત્વો તેની સાથે જોડાય છે અને આ એક મુખ્ય કારણ છે કે શા માટે તેઓ સામાન્ય રીતે પૃથ્વી પર તેમના ઑક્સાઇડના રૂપમાં જોવા મળે છે. ઑક્સિડેશનની મર્યાદિત વ્યાખ્યા અનુસાર નીચેની પ્રક્રિયાઓ ઑક્સિડેશન પ્રક્રિયાઓનું પ્રતિનિધિત્વ કરે છે:
$$2 \mathrm{Mg}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{MgO}(\mathrm{s}) \tag{8.1}$$
$$\mathrm{S}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow \mathrm{SO_2}(\mathrm{~g}) \tag{8.2}$$
પ્રક્રિયાઓ (8.1) અને (8.2) માં, મેગ્નેશિયમ અને સલ્ફર તત્વો તેમમાં ઑક્સિજનની ઉમેરણીને કારણે ઑક્સિડાઇઝ થાય છે. તે જ રીતે, મિથેન તેમાં ઑક્સિજનની ઉમેરણીને કારણે ઑક્સિડાઇઝ થાય છે.
$$\mathrm{CH} _{4}(\mathrm{~g})+2 \mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g})+2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{7.3}$$
પ્રક્રિયા (8.3)ની સૂક્ષ્મ તપાસ, જેમાં હાઇડ્રોજનને ઑક્સિજન દ્વારા બદલવામાં આવ્યું છે, તે રસાયણશાસ્ત્રીઓને તેમાંથી હાઇડ્રોજનના દૂર થવાના સંદર્ભમાં ઑક્સિડેશનની પુનઃવ્યાખ્યા કરવા પ્રેરિત કરી, અને તેથી, ઑક્સિડેશન શબ્દનો વ્યાપ હાઇડ્રોજનને પદાર્થમાંથી દૂર કરવાનો સમાવેશ કરવા માટે વિસ્તૃત કરવામાં આવ્યો. નીચેનું ઉદાહરણ એક બીજી પ્રક્રિયા છે જ્યાં હાઇડ્રોજનનું દૂર થવું પણ ઑક્સિડેશન પ્રક્રિયા તરીકે ગણી શકાય.
$$ \begin{equation*} 2 \mathrm{H_2} \mathrm{~S}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{~S}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \tag{8.4} \end{equation*} $$
રસાયણશાસ્ત્રીઓનું જ્ઞાન વધતાં, (7.1 થી 7.4) જેવી પ્રક્રિયાઓ માટે ઑક્સિડેશન શબ્દને વિસ્તૃત કરવું સ્વાભાવિક હતું, જેમાં ઑક્સિજન સિવાય અન્ય વિદ્યુતઋણાત્મક તત્વોનો સમાવેશ થતો નથી. મેગ્નેશિયમનું ફ્લોરિન, ક્લોરિન અને સલ્ફર વગેરે સાથે ઑક્સિડેશન નીચેની પ્રક્રિયાઓ અનુસાર થાય છે:
$$\operatorname{Mg}(\mathrm{s})+\mathrm{F_2} (\mathrm{~g}) \rightarrow \operatorname{MgF_2} (s) \tag{8.5}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{Cl_2} (g) \rightarrow \mathrm{MgCl_2} (s) \tag{8.6}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{S} (s) \rightarrow \operatorname{MgS}(\mathrm{s}) \tag{8.7}$$
પ્રક્રિયાઓ (7.5 થી 7.7) ને ઑક્સિડેશન પ્રક્રિયાઓના વર્ગમાં સમાવવાથી રસાયણશાસ્ત્રીઓને માત્ર હાઇડ્રોજનના દૂર થવાને જ નહીં, પરંતુ વિદ્યુતધનાત્મક તત્વોના દૂર થવાને પણ ઑક્સિડેશન તરીકે ગણવા પ્રેરિત કર્યા. આમ પ્રક્રિયા:
$$ 2 \mathrm{~K_4} \left[ \mathrm{Fe} ( \mathrm{CN})_{6} \right] ( \mathrm{aq}) + \mathrm{H_2} \mathrm{O_2} ( \mathrm{aq}) \rightarrow 2 \mathrm{~K_3} \left[\mathrm{Fe}( \mathrm{CN})_6 \right] ( \mathrm{aq}) + 2 \mathrm{KOH} ( \mathrm{aq}) $$
ને પોટેશિયમ ફેરોસાયનાઇડમાંથી વિદ્યુતધનાત્મક તત્વ પોટેશિયમના દૂર થવાને કારણે ઑક્સિડેશન તરીકે અર્થઘટન કરવામાં આવે છે, તે પોટેશિયમ ફેરિક્યાનાઇડમાં બદલાય તે પહેલાં. સારાંશમાં, “ઑક્સિડેશન” શબ્દને પદાર્થમાં ઑક્સિજન/વિદ્યુતઋણાત્મક તત્વની ઉમેરણી અથવા પદાર્થમાંથી હાઇડ્રોજન/વિદ્યુતધનાત્મક તત્વના દૂર થવા તરીકે વ્યાખ્યાયિત કરવામાં આવે છે.
શરૂઆતમાં, રિડક્શનને સંયોજનમાંથી ઑક્સિજનના દૂર થવા તરીકે ગણવામાં આવતું હતું. જોકે, રિડક્શન શબ્દને આજકાલ પદાર્થમાંથી ઑક્સિજન/વિદ્યુતઋણાત્મક તત્વના દૂર થવા અથવા પદાર્થમાં હાઇડ્રોજન/વિદ્યુતધનાત્મક તત્વની ઉમેરણી તરીકે સમાવવા માટે વિસ્તૃત કરવામાં આવ્યો છે.
ઉપર આપેલી વ્યાખ્યા અનુસાર, નીચેના રિડક્શન પ્રક્રિયાઓના ઉદાહરણો છે:
$$2 \mathrm{HgO}(\mathrm{s}) \xrightarrow{\Delta} 2 \mathrm{Hg}(\mathrm{l})+\mathrm{O_2}(\mathrm{~g}) \tag{8.8}$$
(મર્ક્યુરિક ઑક્સાઇડમાંથી ઑક્સિજનનું દૂર થવું)
$$2 \mathrm{FeCl_3}(\mathrm{aq})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{FeCl_2}(\mathrm{aq})+2 \mathrm{HCl}(\mathrm{aq}) \tag{8.9}$$
(વિદ્યુતઋણાત્મક તત્વ, ક્લોરિનનું ફેરિક ક્લોરાઇડમાંથી દૂર થવું)
$$\mathrm{CH_2}=\mathrm{CH_2}(\mathrm{~g})+\mathrm{H_2}(\mathrm{~g}) \rightarrow \mathrm{H_3} \mathrm{C}-\mathrm{CH_3}(\mathrm{~g})\tag{8.10}$$
(હાઇડ્રોજનની ઉમેરણી)
$$2 \mathrm{HgCl_2}(\mathrm{aq})+\mathrm{SnCl_2}(\mathrm{aq}) \rightarrow \mathrm{Hg_2} \mathrm{Cl_2}(\mathrm{~s})+\mathrm{SnCl_4}(\mathrm{aq})\tag{8.11}$$
(મર્ક્યુરિક ક્લોરાઇડમાં પારાની ઉમેરણી)
પ્રક્રિયા (8.11) માં, સ્ટેનસ ક્લોરાઇડનું સ્ટેનિક ક્લોરાઇડમાં એક સાથે ઑક્સિડેશન પણ થઈ રહ્યું છે કારણ કે તેમાં વિદ્યુતઋણાત્મક તત્વ ક્લોરિનની ઉમેરણી થાય છે. ટૂંક સમયમાં જ સમજાયું કે ઑક્સિડેશન અને રિડક્શન હંમેશા એક સાથે થાય છે (જે ઉપર આપેલી તમામ સમીકરણોને ફરીથી તપાસીને સ્પષ્ટ થશે), તેથી, રાસાયણિક પ્રક્રિયાઓની આ શ્રેણી માટે “રેડોક્સ” શબ્દ ઘડવામાં આવ્યો.
સમસ્યા 8.1
નીચે આપેલી પ્રક્રિયાઓમાં, ઑક્સિડેશન અને રિડક્શન પામતી સ્પીસીઝને ઓળખો:
(i) $\mathrm{H_2} \mathrm{~S}$ (g) $+\mathrm{Cl_2}$ (g) $\rightarrow 2 \mathrm{HCl}$ (g) $+\mathrm{S}$ (s)
(ii) $3 \mathrm{Fe_3} \mathrm{O_4}$ (s) $+8 \mathrm{Al}$ (s) $\rightarrow 9 \mathrm{Fe}$ (s) $+4 \mathrm{Al_2} \mathrm{O_3}(\mathrm{~s})$
(iii) $2 \mathrm{Na}$ (s) $+\mathrm{H_2}$ (g) $\rightarrow 2 \mathrm{NaH}$ (s)
ઉકેલ
(i) $\mathrm{H_2} \mathrm{~S}$ ઑક્સિડાઇઝ થાય છે કારણ કે વધુ વિદ્યુતઋણાત્મક તત્વ, ક્લોરિન હાઇડ્રોજનમાં ઉમેરવામાં આવે છે (અથવા વધુ વિદ્યુતધનાત્મક તત્વ, હાઇડ્રોજન S માંથી દૂર કરવામાં આવ્યું છે). ક્લોરિન તેમાં હાઇડ્રોજનની ઉમેરણીને કારણે રિડ્યુસ થાય છે.
(ii) એલ્યુમિનિયમ ઑક્સિડાઇઝ થાય છે કારણ કે તેમાં ઑક્સિજન ઉમેરવામાં આવે છે. ફેરસ ફેરિક ઑક્સાઇડ $\left(\mathrm{Fe_3} \mathrm{O_4}\right)$ રિડ્યુસ થાય છે કારણ કે તેમાંથી ઑક્સિજન દૂર કરવામાં આવ્યું છે.
(iii) વિદ્યુતઋણાત્મકતાની કલ્પનાનો સૂક્ષ્મ ઉપયોગ કરીને જ આપણે અનુમાન કરી શકીએ કે સોડિયમ ઑક્સિડાઇઝ થાય છે અને હાઇડ્રોજન રિડ્યુસ થાય છે.
અહીં પસંદ કરેલી પ્રક્રિયા (iii) આપણને રેડોક્સ પ્રક્રિયાઓને વ્યાખ્યાયિત કરવાની બીજી રીત વિશે વિચારવા પ્રેરિત કરે છે.
8.2 ઇલેક્ટ્રૉન સ્થાનાંતરણ પ્રક્રિયાઓના સંદર્ભમાં રેડોક્સ પ્રક્રિયાઓ
આપણે પહેલાથી જ શીખ્યા છીએ કે આ પ્રક્રિયાઓ રેડોક્સ પ્રક્રિયાઓ છે કારણ કે આ દરેક પ્રક્રિયાઓમાં સોડિયમમાં ઑક્સિજન અથવા વધુ વિદ્યુતઋણાત્મક તત્વની ઉમેરણીને કારણે સોડિયમ ઑક્સિડાઇઝ થાય છે.
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaCl}(\mathrm{s})\tag{8.12}$$
$$4 \mathrm{Na}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na_2} \mathrm{O}(\mathrm{s})\tag{8.13}$$
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{S}(\mathrm{s}) \rightarrow \mathrm{Na_2} \mathrm{~S}(\mathrm{~s}) \tag{8.14}$$
સાથે સાથે, ક્લોરિન, ઑક્સિજન અને સલ્ફર રિડ્યુસ થાય છે કારણ કે આ દરેકમાં વિદ્યુતધનાત્મક તત્વ સોડિયમ ઉમેરવામાં આવ્યું છે. રાસાયણિક બંધનના આપણા જ્ઞાન પરથી આપણે એ પણ જાણીએ છીએ કે સોડિયમ ક્લોરાઇડ, સોડિયમ ઑક્સાઇડ અને સોડિયમ સલ્ફાઇડ આયનિક સંયોજનો છે અને કદાચ વધુ સારી રીતે $\mathrm{Na}^{+} \mathrm{Cl}^{-}( \mathrm{s}),\left(\mathrm{Na}^{+} \right)_2 \mathrm{O}^{2-}( \mathrm{s})$, અને $ \left(\mathrm{Na}^{+} \right)_2$ $\mathrm{S}^{2-}( \mathrm{s})$ તરીકે લખી શકાય. ઉત્પન્ન થયેલી સ્પીસીઝ પર ચાર્જનો વિકાસ આપણને પ્રક્રિયાઓ (8.12 થી 8.14) નીચેની રીતે ફરીથી લખવા સૂચવે છે:
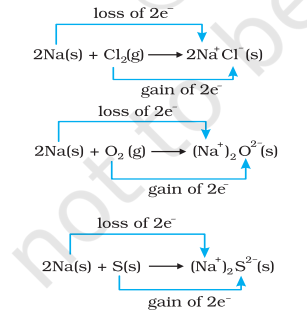
સગવડ માટે, ઉપરોક્ત દરેક પ્રક્રિયાઓને બે અલગ-અલગ પગલાં તરીકે ગણી શકાય, એકમાં ઇલેક્ટ્રૉનની હાનિ અને બીજામાં ઇલેક્ટ્રૉનનો લાભ સામેલ છે. ઉદાહરણ તરીકે, આપણે આમાંથી એકને, કહીએ તો, સોડિયમ ક્લોરાઇડની રચનાને વધુ વિગતવાર સમજાવી શકીએ.
$2 \mathrm{Na}(\mathrm{s}) \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
$\mathrm{Cl_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{Cl}^{-}(\mathrm{g})$
ઉપરોક્ત દરેક પગલાને અર્ધ-પ્રક્રિયા કહેવામાં આવે છે, જે ઇલેક્ટ્રૉનની સામેલગીરીને સ્પષ્ટ રીતે દર્શાવે છે. અર્ધ-પ્રક્રિયાઓનો સરવાળો સમગ્ર પ્રક્રિયા આપે છે:
$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na}^{+} \mathrm{Cl}^{-}(\mathrm{s})$ અથવા $2 \mathrm{NaCl}(\mathrm{s})$
પ્રક્રિયાઓ 8.12 થી 8.14 સૂચવે છે કે જે અર્ધ-પ્રક્રિયાઓમાં ઇલેક્ટ્રૉનની હાનિ સામેલ હોય તેને ઑક્સિડેશન પ્રક્રિયાઓ કહેવામાં આવે છે. તે જ રીતે, જે અર્ધ-પ્રક્રિયાઓમાં ઇલેક્ટ્રૉનનો લાભ સામેલ હોય તેને રિડક્શન પ્રક્રિયાઓ કહેવામાં આવે છે. અહીં એ ઉલ્લેખ કરવો અસંગત ન હોઈ શકે કે ઑક્સિડેશન અને રિડક્શનને વ્યાખ્યાયિત કરવાની નવી રીત શાસ્ત્રીય કલ્પના અનુસાર સ્પીસીઝના વર્તન અને ઇલેક્ટ્રૉન-સ્થાનાંતરણ ફેરફારમાં તેમની આંતરક્રિયા વચ્ચે સહસંબંધ સ્થાપિત કરીને જ પ્રાપ્ત થઈ છે. પ્રક્રિયાઓ (8.12 થી 8.14) માં સોડિયમ, જે ઑક્સિડાઇઝ થાય છે, તે રિડ્યુસિંગ એજન્ટ તરીકે કાર્ય કરે છે કારણ કે તે તેની સાથે આંતરક્રિયા કરતા દરેક તત્વને ઇલેક્ટ્રૉન દાન કરે છે અને આમ તેમને રિડ્યુસ કરવામાં મદદ કરે છે. ક્લોરિન, ઑક્સિજન અને સલ્ફર રિડ્યુસ થાય છે અને ઑક્સિડાઇઝિંગ એજન્ટ તરીકે કાર્ય કરે છે કારણ કે આ સોડિયમ પરથી ઇલેક્ટ્રૉન સ્વીકારે છે. સારાંશમાં, આપણે ઉલ્લેખ કરી શકીએ કે
ઑક્સિડેશન: કોઈ પણ સ્પીસીઝ દ્વારા ઇલેક્ટ્રૉન(ની)ની હાનિ.
રિડક્શન: કોઈ પણ સ્પીસીઝ દ્વારા ઇલેક્ટ્રૉન(ની)નો લાભ.
ઑક્સિડાઇઝિંગ એજન્ટ: ઇલેક્ટ્રૉન(નો) સ્વીકર્તા.
રિડ્યુસિંગ એજન્ટ: ઇલેક્ટ્રૉન(નો) દાતા.
સમસ્યા 8.2
યથાર્થ ઠેરવો કે પ્રક્રિયા: $2 \mathrm{Na}(\mathrm{s})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaH}$ (s) એ રેડોક્સ ફેરફાર છે.
ઉકેલ
ઉપરોક્ત પ્રક્રિયામાં રચાયેલું સંયોજન આયનિક સંયોજન હોવાથી, જેને $\mathrm{Na}^{+} \mathrm{H}^{-}$(s) તરીકે પણ દર્શાવી શકાય છે, આ સૂચવે છે કે આ પ્રક્રિયામાં એક અર્ધ-પ્રક્રિયા છે:
$2 \mathrm{Na}(\mathrm{s}) \quad \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
અને બીજી અર્ધ-પ્રક્રિયા છે:
$\mathrm{H_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{H}^{-}(\mathrm{g})$
પરીક્ષણ હેઠળની પ્રક્રિયાનું આ બે અર્ધ-પ્રક્રિયાઓમાં વિભાજન આપમેળે જ દર્શાવે છે કે અહીં સોડિયમ ઑક્સિડાઇઝ થાય છે અને હાઇડ્રોજન રિડ્યુસ થાય છે, તેથી, સંપૂર્ણ પ્રક્રિયા એક રેડોક્સ ફેરફાર છે.
8.2.1 સ્પર્ધાત્મક ઇલેક્ટ્રૉન સ્થાનાંતરણ પ્રક્રિયાઓ
કોપર નાઇટ્રેટના જલીય દ્રાવણમાં ધાત્વીય ઝિંકની એક પટ્ટી મૂકો જેમ કે આકૃતિ 8.1 માં દર્શાવેલ છે, લગભગ એક કલાક માટે. તમે નોંધ શકો છો કે પટ્ટી લાલ રંગની ધાત્વીય તાંબા સાથે લેપિત થાય છે અને દ્રાવણનો વાદળી રંગ અદૃશ્ય થઈ જાય છે. $\mathrm{Zn}^{2+}$ આયનોની રચના ઉત્પાદનોમાં સરળતાથી નક્કી કરી શકાય છે જ્યારે $\mathrm{Cu}^{2+}$ ને કારણે દ્રાવણનો વાદળી રંગ અદૃશ્ય થઈ જાય છે. જો હાઇડ્રોજન સલ્ફાઇડ વાયુને $\mathrm{Zn}^{2+}$ આયનો ધરાવતા રંગહીન દ્રાવણમાંથી પસાર કરવામાં આવે, તો સફેદ ઝિંક સલ્ફાઇડ, $\mathrm{ZnS}$ ની દ્રશ્યતા એમોનિયા સાથે દ્રાવણને ક્ષારીય બનાવવા પર જોઈ શકાય છે.
ધાત્વીય ઝિંક અને કોપર નાઇટ્રેટના જલીય દ્રાવણ વચ્ચેની પ્રક્રિયા છે:
$$\mathrm{Zn}(\mathrm{s})+\mathrm{Cu}^{2+}(\mathrm{aq}) \rightarrow \mathrm{Zn}^{2+}(\mathrm{aq})+\mathrm{Cu}(\mathrm{s}) \tag{8.15}$$
પ્રક્રિયા (8.15) માં, ઝિંકે $Zn^{2+}$ બનાવવા માટે ઇલેક્ટ્રૉન ગુમાવ્યા છે અને તેથી, ઝિંક ઑક્સિડાઇઝ થાય છે. સ્પષ્ટ છે, હવે જો ઝિંક ઑક્સિડાઇઝ થાય છે, ઇલેક્ટ્રૉન મુક્ત કરે છે, તો કંઈક રિડ્યુસ થવું જોઈએ, ઝિંક દ્વારા ગુમાવેલા ઇલેક્ટ્રૉનને સ્વીકારીને. કોપર આયન ઝિંક પરથી ઇલેક્ટ્રૉન મેળવીને રિડ્યુસ થાય છે.
પ્રક્રિયા (8.15) નીચે પ્રમાણે ફરીથી લખી શકાય:
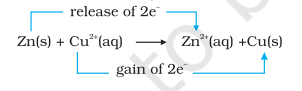
આ તબક્કે આપણે સમીકરણ (8.15) દ્વારા દર્શાવેલ પ્રક્રિયા માટે સંતુલનની સ્થિતિની તપાસ કરી શકીએ. આ હેતુ માટે, ચાલો ઝિંક સલ્ફેટ દ્રાવણમાં ધાત્વીય તાંબાની એક પટ્ટી મૂકીએ. કોઈ દૃશ્યમાન પ્રક્રિયા જોવા મળતી નથી અને $\mathrm{Cu}^{2+}$ આયનોની હાજરી શોધવાનો પ્રયાસ $\mathrm{H_2} \mathrm{~S}$ વાયુને દ્રાવણમાંથી પસાર કરીને કપ્રિક સલ્ફાઇડ, CuS નો કાળો રંગ ઉત્પન્ન કરવા માટે સફળ થતો નથી. કપ્રિક સલ્ફાઇડની દ્રાવ્યતા એટલી ઓછી છે કે આ એક અત્યંત સંવેદનશીલ પરીક્ષણ છે; છતાં પણ રચાયેલ $\mathrm{Cu}^{2+}$ ની માત્રા શોધી શકાતી નથી. આમ આપણે નિષ્કર્ષ પર આવીએ છીએ કે પ્રક્રિયા (8.15) માટે સંતુલનની સ્થિતિ પ્રક્રિયકો કરતાં ઉત્પાદનોને મોટા પ્રમાણમાં પસંદ કરે છે.
ચાલો હવે ઇલેક્ટ્રૉન સ્થાનાંતરણ પ્રક્રિયાને તાંબાની ધાતુ અને પાણીમાં સિલ્વર નાઇટ્રેટ દ્રાવણ સુધી વિસ્તૃત કરીએ અને આકૃતિ 8.2 માં દર્શાવ્યા પ્રમાણે એક સેટ-અપ ગોઠવીએ. પ્રક્રિયાને કારણે $\mathrm{Cu}^{2+}$ આયનોની રચના થવાથી દ્રાવણ વાદળી રંગ વિકસાવે છે:
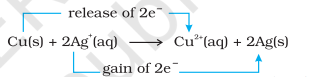
અહીં, $\mathrm{Cu}(\mathrm{s})$ નું $\mathrm{Cu}^{2+}(\mathrm{aq})$ માં ઑક્સિડેશન થાય છે અને $\mathrm{Ag}^{+}(\mathrm{aq})$ નું $\mathrm{Ag}(\mathrm{s})$ માં રિડક્શન થાય છે. સંતુલન $\mathrm{Cu}^{2+}(\mathrm{aq})$ અને $\mathrm{Ag}(\mathrm{s})$ ઉત્પાદનોને મોટા પ્રમાણમાં પસંદ કરે છે.
તુલના માટે, ચાલો નિકલ સલ્ફેટ દ્રાવણમાં મૂકેલી ધાત્વીય કોબાલ્ટની પ્રક્રિયાની પણ તુલના કરીએ. અહીં થતી પ્રક્રિયા છે:
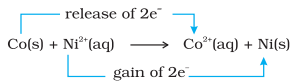
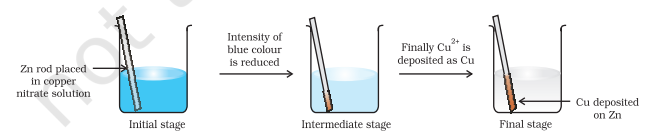
આકૃતિ 8.1 બીકરમાં થતી ઝિંક અને કોપર નાઇટ્રેટના જલીય દ્રાવણ વચ્ચેની રેડોક્સ પ્રક્રિયા.
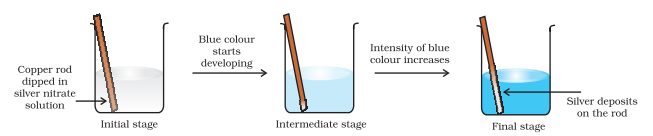
આકૃતિ 8.2 બીકરમાં થતી તાંબા અને સિલ્વર નાઇટ્રેટના જલીય દ્રાવણ વચ્ચેની રેડોક્સ પ્રક્રિયા
સંતુલન પર, રાસાયણિક પરીક્ષણો દર્શાવે છે કે $\mathrm{Ni}^{2+}(\mathrm{aq})$ અને $\mathrm{Co}^{2+}(\mathrm{aq})$ બંને મધ્યમ સાંદ્રતા પર હાજર છે. આ કિસ્સામાં, ન તો પ્રક્રિયકો $\left[\mathrm{Co}(\mathrm{s})\right.$ અને $\left.\mathrm{Ni}^{2+}(\mathrm{aq})\right]$ અને ન તો ઉત્પાદનો $\left[\mathrm{Co}^{2+}(\mathrm{aq})\right.$ અને $\left.\mathrm{Ni}(\mathrm{s})\right]$ મોટા પ્રમાણમાં પસંદ કરવામાં આવે છે.
ઇલેક્ટ્રૉન મુક્ત કરવા માટેની આ સ્પર્ધા આકસ્મિક રીતે આપણને એસિડ્સ વચ્ચે પ્રોટોન મુક્ત કરવા માટેની સ્પર્ધાની યાદ અપાવે છે. સમાનતા સૂચવે છે કે આપણે એક કોષ








