अध्याय 05 भौतिक एवं रासायनिक परिवर्तन
दैनिक जीवन में हमें अपने आस-पास बहुत से परिवर्तन दिखाई देते हैं। इन परिवर्तनों में एक या अधिक पदार्थ सम्मिलित हो सकते हैं। उदाहरण के लिए, आपकी माताजी आपसे शीतल पेय बनाने के लिए पानी में शक्कर घोलने के लिए कहती हैं। शक्कर का विलयन बनाना एक परिवर्तन है। इसी प्रकार दूध से दही जमाना एक अन्य परिवर्तन है। कभी-कभी दूध खट्टा हो जाता है। दूध का खट्टा होना भी एक परिवर्तन है। खींचा हुआ रबड़ बैंड भी किसी परिवर्तन को प्रदर्शित करता है।
ऐसे दस परिवर्तनों की सूची बनाइए, जिन्हें आप अपने आस-पास देखते हैं।
इस अध्याय में हम कुछ क्रियाकलाप करके इन परिवर्तनों की प्रकृति का अध्ययन करेंगे। व्यापक रूप से, ये परिवर्तन दो प्रकार के होते हैं- भौतिक और रासायनिक।
5.1 भौतिक परिवर्तन
क्रियाकलाप (5.1)
कागज़ के एक टुकड़े को चार वर्गाकार टुकड़ों में काटिए। अब प्रत्येक वर्ग को पुनः चार टुकड़ों में काटिए। इन टुकड़ों को फ़र्श अथवा किसी मेज़ पर इस प्रकार लगाइए, जिससे ये टुकड़े परस्पर जुड़कर कागज़ के टुकड़े का मूल आकार ले लें (चित्र 5.1)।
स्पष्ट रूप से, आप टुकड़ों को पुनः जोड़कर मूल टुकड़ा नहीं बना सकते, लेकिन क्या कागज़ के गुण में कोई परिवर्तन हुआ है?

चित्र 5.1 कागज़ के टुकड़े
क्रियाकलाप (5.2)
अपनी कक्षा के चॉकबोर्ड के आस-पास फ़र्श पर गिरे चॉक पाउडर को एकत्रित कर लें अथवा चॉक के एक छोटे टुकड़े का चूर्ण (पाउडर) बना लें। इस पाउडर में थोड़ा जल मिलाकर पेस्ट बना लें। इसे चॉक के आकार में बेलकर सूखने दें।
क्या आप चॉक के चूर्ण से फिर चॉक बना सकते हैं?
क्रियाकलाप (5.3)
काँच या प्लास्टिक के कटोरे में थोड़ी बर्फ़ लीजिए। बर्फ़ के थोड़े-से भाग के पिघलने तक बर्तन को धूप में रखें। अब आपके पास बर्फ़ और जल का मिश्रण होगा। अब कटोरे को हिमकारी मिश्रण (बर्फ़ और नमक) में रख दें।
क्या जल फिर से ठोस बर्फ़ बन गया?
क्रियाकलाप (5.4)
एक पात्र में थोड़ा-सा जल लेकर उसे उबालिए। क्या आपको जल की सतह से भाप निकलती दिखाई देती है? उबलते हुए जल से कुछ दूरी पर भाप के ऊपर किसी बर्तन को उलटा करके रखिए। बर्तन की भीतरी सतह को देखिए।
क्या आपको वहाँ जल की कोई बूँद दिखाई देती है?
क्रियाकलाप (5.5)
सावधानी ज्वाला पर कार्य करते समय सावधानी बरतें।
उपयोग किए जा चुके लोहे की आरी के ब्लेड को चिमटे से पकड़िए। ब्लेड के मुक्त सिरे के अग्र (अगले) भाग को गैस स्टोव की ज्वाला पर रखिए। कुछ मिनट तक प्रतीक्षा कीजिए।
क्या ब्लेड के अग्र भाग के रंग में कोई परिवर्तन होता है?
ब्लेड को ज्वाला से हटाइए। कुछ समय बाद अग्र भाग को पुनः देखिए।
क्या इसका पहले वाला रंग वापस आ जाता है?
क्रियाकलाप 5.1 और 5.2 में आपने देखा कि कागज़ तथा चॉक के आमाप (साइज़) में परिवर्तन हो जाता है। क्रियाकलाप 5.3 और 5.4 में जल की अवस्था परिवर्तित हो जाती है (ठोस से द्रव अथवा गैस से द्रव)। क्रियाकलाप 5.5 में आरी के ब्लेड का रंग गर्म करने पर परिवर्तित हो जाता है।
पदार्थ के आकार, आमाप (साइज़), रंग और अवस्था जैसे गुण उसके भौतिक गुण कहलाते हैं। वह परिवर्तन, जिसमें किसी पदार्थ के भौतिक गुणों में परिवर्तन हो जाता है, भौतिक परिवर्तन कहलाता है। भौतिक परिवर्तन सामान्यतः उत्क्रमणीय होता है। ऐसे परिवर्तन में कोई नया पदार्थ नहीं बनता है।
अब हम दूसरे प्रकार के परिवर्तन पर विचार करते हैं।
5.2 रासायनिक परिवर्तन
लोहे में जंग लगना एक ऐसा परिवर्तन है, जिससे आप भली-भाँति परिचित हैं। यदि आप लोहे के एक टुकड़े को कुछ दिनों के लिए खुले में छोड़ दें, तो इस पर भूरे रंग के पदार्थ की परत जम जाती है। यह पदार्थ जंग कहलाता है और यह प्रक्रम जंग लगना कहलाता है (चित्र 5.2)। पार्क अथवा लॉन आदि के लोहे के दरवाज़े अथवा बगीचों या पार्क आदि में रखी लोहे की बैंच और लोहे की लगभग कोई भी वस्तु, जो खुले में रखी रहती हैं, में जंग लग जाती है। आपने देखा होगा

चित्र 5.2 लोहे की कुछ जंग लगी वस्तुएँ
कि घर में रखी कुल्हाड़ी, हथौड़ा आदि को वायु में कुछ दिनों तक खुला रख देने पर उनमें जंग लग जाती है। रसोई में लोहे का गीला तवा कुछ समय तक खुला छोड़ देने पर उसमें जंग लग जाती है। जंग लोहा नहीं है। जंग उस पदार्थ (लौह) से भिन्न होती है, जिस पर यह लगती है।
आइए, हम कुछ ऐसे और परिवर्तनों पर विचार करें जिनमें नए पदार्थ निर्मित होते हैं।
क्रियाकलाप (5.6)
(शिक्षक द्वारा निदर्शित किए जाने के लिए)
| सावधानी |
|---|
| मैग्नीशियम के जलते हुए फीते (अथवा तार) की ओर लंबी अवधि तक देखना हानिकारक होता है। शिक्षकों को बच्चों को बताना चाहिए कि वे जलते हुए मैग्नीशियम की ओर अधिक समय तक टकटकी लगाकर न देखें। |
मैग्नीशियम की पतली पट्टी (फीता) अथवा तार का टुकड़ा लीजिए। इसके सिरों को रेगमाल से साफ़ कर लीजिए। सिरे को मोमबत्ती की लौ के पास लाइए। यह चमकदार श्वेत (सफ़ेद) प्रकाश देती हुई जलने लगेगी (चित्र 5.3)। पूरी तरह जलने के बाद कुछ श्वेत भस्म (पाउडर) शेष रह जाती है।

चित्र 5.3 मैग्नीशियम का जलता हुआ फीता
क्या भस्म मैग्नीशियम के फ़ीते जैसी लगती है?
इस परिवर्तन को निम्नलिखित समीकरण द्वारा व्यक्त किया जा सकता है-
मैग्नीशियम $(\mathrm{Mg})+$ ऑक्सीजन $\left(\mathrm{O}_{2}\right) \rightarrow$ मैग्नीशियम ऑक्साइड (MgO)
ध्यान दें कि यहाँ लिखी समीकरण गणित में प्रयुक्त समीकरणों से भिन्न है। इस प्रकार के समीकरणों में तीर का अर्थ है ‘बनना’ या ‘हो जाता है’। इस पुस्तक में रासायनिक समीकरणों को संतुलित करने का कोई प्रयास नहीं किया जा रहा है और न ही यह छात्रों से अपेक्षित है।
भस्म को एकत्रित करके इसमें जल की कुछ मात्रा मिलाइए। मिश्रण (जलीय विलयन) को अच्छी तरह हिलाइए। मिश्रण का लाल और नीले लिटमस पत्र से परीक्षण कीजिए।
क्या मिश्रण लाल लिटमस को नीला कर देता है?
क्या मिश्रण नीले लिटमस को लाल कर देता है?
इस परीक्षण के आधार पर आप जलीय विलयन को किस रूप में वर्गीकृत करेंगे, अम्लीय अथवा क्षारकीय?
भस्म को जल में घोलने पर यह नया पदार्थ बनाती है। इस परिवर्तन को निम्नलिखित समीकरण के द्वारा लिखा जा सकता है
मैग्नीशियम ऑक्साइड $(\mathrm{MgO})+$ जल $\left(\mathrm{H}_2 \mathrm{O}\right) \rightarrow$ मैग्नीशियम हाइड्रॉक्साइड $\left[\mathrm{Mg}(\mathrm{OH})_2\right]$
जैसा कि आपने अध्याय 4 में पढ़ा था, मैग्नीशियम हाइड्रॉक्साइड एक क्षारक है। अतः, मैग्नीशियम ऑक्साइड एक नया पदार्थ है, जो मैग्नीशियम के जलने पर बनता है। मैग्नीशियम हाइड्रॉक्साइड एक अन्य नया पदार्थ है, जो मैग्नीशियम ऑक्साइड को जल में घोलने पर बनता है।
क्रियाकलाप (5.7)
(शिक्षक द्वारा निदर्शित किए जाने के लिए)
काँच के एक गिलास या कटोरे अथवा चौड़े मुँह की बोतल में लगभग आधा कप पानी लेकर उसमें एक चम्मच कॉपर सल्फेट (नीला थोथा) घोल लीजिए। इस विलयन में तनु सल्फ्यूरिक अम्ल की कुछ बूँदें मिलाइए। आपको नीले रंग का विलयन मिल जाएगा। एक परखनली अथवा काँच की छोटी बोतल में विलयन का थोड़ा-सा नमूना बचा लीजिए। शेष विलयन में एक कील अथवा उपयोग किए जा चुके ब्लेड का टुकड़ा डाल दीजिए। लगभग आधे घंटे तक प्रतीक्षा कीजिए। अब विलयन के रंग को देखिए। इसकी तुलना अलग से बचाए गए नमूने वाले विलयन के रंग से कीजिए (चित्र 5.4)।

चित्र 5.4 लोहे के साथ अभिक्रिया के कारण कॉपर सल्फेट विलयन के रंग में परिवर्तन
क्या आपको विलयन के रंग में कोई परिवर्तन दिखाई देता है?
कील अथवा ब्लेड को बाहर निकाल लीजिए।
क्या इसमें कोई परिवर्तन दिखाई देता है?
आपको जो परिवर्तन दिखाई देते हैं, वे कॉपर सल्फेट और लोहे के बीच अभिक्रिया के कारण होते हैं। विलयन के रंग का नीले से हरा हो जाना, एक नए पदार्थ आयरन सल्फेट के बनने के कारण होता है। लोहे की कील पर भूरा निक्षेप कॉपर या ताँबे की परत के कारण होता है, जो एक अन्य नया पदार्थ है। हम इस अभिक्रिया को निम्न प्रकार से व्यक्त कर सकते हैं:
कॉपर सल्फेट विलयन $(\mathrm{CuSO})_4$ (नीला थोथा $)+$ लोहा $(\mathrm{Fe}) \rightarrow$ आयरन सल्फेट विलयन $(\mathrm{FeSO})_4$ (हरा) + कॉपर (Cu) (भूरा निक्षेप)
क्रियाकलाप (5.8)
किसी परखनली में लगभग एक चम्मच सिरका लीजिए। इसमें चुटकी भर खाने का सोडा डालिए। आपको एक बुदबुदाहट की ध्वनि सुनाई देगी और गैस के बुलबुले बाहर निकलते दिखाई देंगे। इस गैस को चित्र 5.5 में दिखाई गई व्यवस्था के अनुसार ताजे बने चूने के पानी में से गुजारिए (चूने का पानी तैयार करने की विधि अध्याय 4 में बताई गई है)।
चूने के पानी में क्या परिवर्तन होता है?
परखनली में परिवर्तन निम्न प्रकार से होते हैं:
सिरका (ऐसीटिक अम्ल)+खाने का सोडा (सोडियम हाइड्रोजन कार्बोनेट) $\rightarrow$ कार्बन डाइऑक्साइड $\left(\mathrm{CO}_{2}\right)+$ अन्य पदार्थ
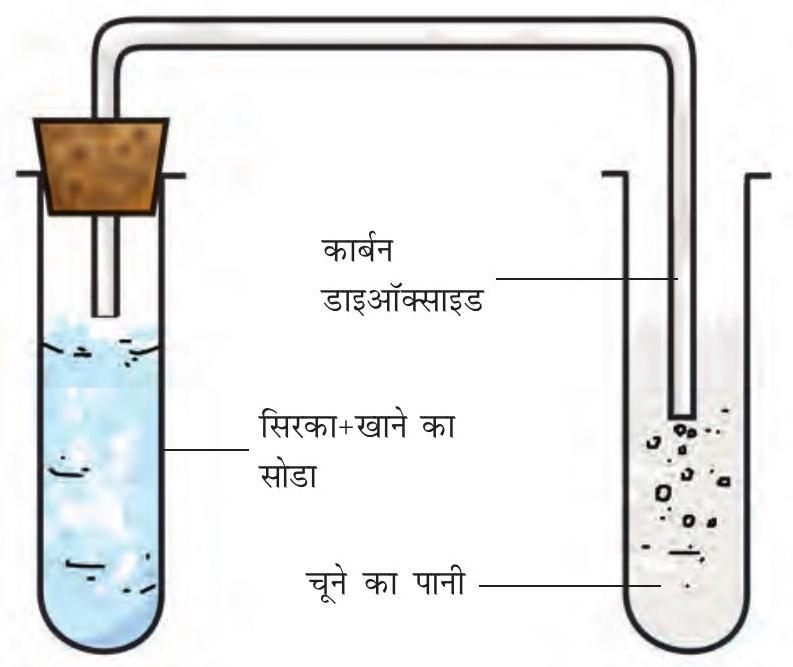
चित्र 5.5 चूने के पानी में से गैस को गुजारने के लिए व्यवस्था
कार्बन डाइऑक्साइड और चूने के पानी के बीच अभिक्रिया निम्न प्रकार से होती है:
कार्बन डाइऑक्साइड $\left(\mathrm{CO}_2\right)$ +चूने का पानी $\left[\mathrm{Ca}(\mathrm{OH})_2\right] \rightarrow$ कैल्सियम कार्बोनेट $\left(\mathrm{CaCO}_3\right)+$ जल $\left(\mathrm{H}_2 \mathrm{O}\right)$
जब कार्बन डाइऑक्साइड को चूने के पानी में प्रवाहित किया जाता है, तो कैल्सियम कार्बोनेट बनता है, जिससे चूने का पानी दूधिया हो जाता है। चूने के पानी का दूधिया हो जाना कार्बन डाइऑक्साइड का मानक परीक्षण है। आप इसका उपयोग अध्याय 6 में यह दिखाने के लिए करेंगे कि हम श्वसन में जो वायु बाहर निकालते हैं उसमें कार्बन डाइऑक्साइड की मात्रा अधिक होती है।
क्रियाकलाप 5.6 से 5.8 में आपने देखा कि प्रत्येक परिवर्तन में एक या अधिक नए पदार्थ बने थे। क्रियाकलाप 5.6 में मैग्नीशियम को वायु की उपस्थिति में जलाने पर बनने वाली भस्म एक नया पदार्थ थी। क्रियाकलाप 5.7 में कॉपर सल्फेट की लोहे के साथ अभिक्रिया से आयरन सल्फेट और कॉपर बने थे। ये दोनों नए पदार्थ थे। कॉपर, लोहे के ब्लेड पर निक्षेपित हो गया था। क्रियाकलाप 5.8 में सिरका और खाने के सोडे की अभिक्रिया से कार्बन डाइऑक्साइड बनी थी, जिसने चूने के पानी को दूधिया कर दिया था। क्या आप इस अभिक्रिया में बनने वाले नए पदार्थ का नाम बता सकते हैं?
वह परिवर्तन, जिसमें एक अथवा एक-से अधिक नए पदार्थ बनते हैं, रासायनिक परिवर्तन कहलाता है। रासायनिक परिवर्तन को रासायनिक अभिक्रिया भी कहते हैं।
रासायनिक परिवर्तन हमारे जीवन में अत्यधिक महत्वपूर्ण हैं। सभी नए पदार्थ रासायनिक परिवर्तनों के परिणामस्वरूप ही बनते हैं। उदाहरण के लिए, भोजन का पाचन, फलों का पकना, अंगूरों का किण्वन आदि विभिन्न रासायनिक परिवर्तनों के कारण होता है। औषधि भी रासायनिक अभिक्रियाओं की शृंखला का अन्त्योउत्पाद होती है। उपयोगी नए पदार्थ जैसे, प्लास्टिक और अपमार्जकों (डिटर्जेंट्स) को रासायनिक अभिक्रियाओं द्वारा ही बनाया जाता है। वास्तव में, प्रत्येक नए पदार्थ की खोज रासायनिक परिवर्तनों का अध्ययन करके की गई है।
हमने देखा कि रासायनिक परिवर्तन में एक या एक-से अधिक नए पदार्थ निर्मित होते हैं। नए उत्पादों (पदार्थों) के अतिरिक्त, रासायनिक परिवर्तन में निम्न घटनाएँ भी हो सकती हैं।
- ऊष्मा, प्रकाश अथवा किसी अन्य प्रकार के विकिरण (उदाहरण के लिए, पराबैंगनी) का निर्मुक्त (बाहर निकलना) अथवा उनका अवशोषित होना।
- ध्वनि का उत्पन्न होना।
- गंध में परिवर्तन होना अथवा किसी नई गंध का बनना।
- रंग में परिवर्तन होना।
- किसी गैस का बनना।
आइए, अब हम कुछ अन्य उदाहरणों पर विचार करते हैं।
आपने देखा कि मैग्नीशियम के फीते का जलना एक रासायनिक परिवर्तन है। कोयला, लकड़ी अथवा पत्तियों का जलना भी रासायनिक परिवर्तन है। वास्तव में, किसी भी पदार्थ का जलना एक रासायनिक परिवर्तन है। जलने के साथ सदैव ऊष्मा का उत्पादन होता है।
पटाखों का विस्फोट एक अन्य रासायनिक परिवर्तन है। आप जानते हैं कि ऐसे विस्फोट से ऊष्मा, प्रकाश, ध्वनि और अरुचिकर गैसें उत्पन्न होती हैं, जो वायुमंडल को प्रदूषित करती हैं। इसलिए आपको पटाखे न जलाने की सलाह दी जाती है।
जब भोजन-सामग्री बासी हो जाती है अथवा सड़-गल जाती है, तो उसमें से दुर्गंध आने लगती है। क्या हम इस परिवर्तन को रासायनिक परिवर्तन कह सकते हैं?
सुरक्षात्मक आवरण
आपने वायुमंडल में ओजोन की परत के बारे में अवश्य सुना होगा। यह हमें सूर्य के प्रकाश में उपस्थित हानिकारक पराबैंगनी विकिरण से बचाती है। ओजोन पराबैंगनी विकिरण को अवशोषित कर लेती है और ऑक्सीजन में परिणत हो जाती है। ऑक्सीजन ओजोन से भिन्न होती है। क्या हम ओजोन के अपघटन को रासायनिक परिवर्तन कह सकते हैं?
यदि ओजोन द्वारा पराबैंगनी विकिरण अवशोषित नहीं होती तो वह पृथ्वी की सतह पर पहुँचकर हमें और अन्य जीवों को हानि पहुँचाती। ओजोन इस विकिरण से हमें सुरक्षा प्रदान करने में प्राकृतिक आवरण की तरह कार्य करती है।
संभवतः आपने देखा होगा कि यदि सेब को काटने के बाद तत्काल न खा लिया जाए, तो उसके कटे हुए टुकड़े भूरे रंग के हो जाते हैं। यदि आपने रंग में यह परिवर्तन नहीं देखा है, तो किसी सेब का एक टुकड़ा काटिए और उसे कुछ देर तक ऐसा ही छोड़ दीजिए। इसी प्रकार का क्रियाकलाप आलू अथवा बैंगन के टुकड़े के साथ दोहराइए। ऐसी प्रत्येक स्थिति में रंग का परिवर्तन, वास्तव में किसी नए पदार्थ अथवा पदार्थों के बनने के कारण होता है। क्या यह परिवर्तन रासायनिक परिवर्तन नहीं है?
अध्याय 1 में हमने पढ़ा कि पादप (पौधे) अपना भोजन प्रकाश संश्लेषण नामक प्रक्रम द्वारा स्वयं बनाते हैं। क्या हम प्रकाश संश्लेषण को रासायनिक परिवर्तन कह सकते हैं? पहेली ने कहा कि पाचन भी एक रासायनिक परिवर्तन है।
अध्याय 4 में, आपने अम्ल और क्षारक को परस्पर मिलाकर उदासीन किया था। क्या उदासीनीकरण की अभिक्रिया रासायनिक परिवर्तन है?
5.3 लोहे में जंग लगना
आइए, हम जंग लगने की घटना पर पुन: विचार करते हैं। यह एक ऐसा परिवर्तन है, जो लोहे की वस्तुओं को प्रभावित करता है और धीरे-धीरे उन्हें नष्ट कर देता है। चूँकि लोहे का उपयोग सेतु (पुल), जहाज़, कार, ट्रक आदि का ढाँचा बनाने और अन्य कई वस्तुओं को बनाने के लिए किया जाता है, अतः जंग लगने के कारण होने वाली आर्थिक हानि बहुत अधिक होती है।
जंग लगने की प्रक्रिया को निम्नलिखित समीकरण द्वारा व्यक्त किया जा सकता है:
लोहा $(\mathrm{Fe})+$ ऑक्सीजन $\left(\mathrm{O}_2\right.$, वायु से $)+$ जल $\left(\mathrm{H}_2 \mathrm{O}\right) \rightarrow$ जंग (आयरन ऑक्साइड, $\mathrm{Fe}_2 \mathrm{O}_3$ )
जंग लगने के लिए ऑक्सीजन और जल (अथवा जलवाष्प) दोनों की उपस्थिति अनिवार्य है।
वास्तव में, यदि वायु में आर्द्रता की मात्रा अधिक हो, अर्थात् नमी अधिक हो, तो जंग जल्दी लगती है।
ओह! इसलिए मेरी सहेली रीता सदैव लोहे की वस्तुओं में जल्दी जंग लगने < की शिकायत करती है, क्योंकि वह समुद्रतट के निकट रहती है।
हम जंग लगने से रोकथाम कैसे करते हैं? लोहे की वस्तुओं को ऑक्सीजन अथवा जल अथवा दोनों के संपर्क में आने से बचाकर ही ऐसा किया जा सकता है। इसका एक सरल उपाय उन पर पेंट अथवा ग्रीज़ की एक परत चढ़ाना है। वास्तव में, लोहे की सभी वस्तुओं पर नियमित रूप से पेंट अथवा ग्रीज़ की परत चढ़ाते रहना चाहिए, जिससे उनमें जंग लगने को रोका जा सके। एक अन्य उपाय लोहे के ऊपर क्रोमियम अथवा जस्ता (जिंक) जैसी किसी धातु की परत चढ़ाना है। लोहे पर जिंक की परत चढ़ाने का प्रक्रम यशद्-लेपन (गैल्वेनाइजेशन) कहलाता है। अपने घरों में पानी की आपूर्ति के लिए उपयोग होने वाले लोहे के पाइप यशद्-लेपित होते हैं, जिससे उनमें जंग नहीं लगता।
क्या आप जानते हैं कि पानी के ज़हाज लोहे के बने होते हैं और उनका एक भाग हमेशा पानी में डूबा रहता है। पानी के ऊपर के भाग पर भी जल की बूँदें गिरती रहती हैं। यही नहीं, समुद्र के पानी में अनेक लवण भी पाए जाते हैं। लवणयुक्त जल, जंग लगने के प्रक्रम की दर को बढ़ा देते हैं। अतः, जहाज़ों पर पेंट करने के बाद भी उन्हें जंग लगने से काफी क्षति होती है। यही नहीं, जहाज़ों के लोहे के कुछ भाग को बदलना प्रतिवर्ष आवश्यक हो जाता है। क्या आप विश्व में जंग लगने से होने वाली कुल आर्थिक हानि की कल्पना कर सकते हैं?
स्टेनलेस स्टील लोहे में कार्बन और क्रोमियम, निकैल तथा मैंगनीज जैसी धातुओं को मिलाकर बनाया जाता है। इसमें जंग नहीं लगती है।
5.4 क्रिस्टलीकरण
कक्षा 6 में आपने पढ़ा था कि साधारण नमक (लवण) को समुद्रजल के वाष्पन द्वारा प्राप्त किया जा सकता है। इस प्रकार प्राप्त होने वाला नमक शुद्ध नहीं होता है और उसके क्रिस्टलों के आकार को स्पष्ट रूप से नहीं देखा जा सकता है। तथापि, किसी पदार्थ के शुद्ध क्रिस्टल उनके विलयन से प्राप्त किए जा सकते हैं। यह प्रक्रिया क्रिस्टलीकरण कहलाती है। यह भौतिक परिवर्तन का एक उदाहरण है।
| सावधानी |
|---|
| केवल तनु सल्फ्यूरिक अम्ल का ही उपयोग करें। जल को उबालते समय सतर्क रहें। |
क्रियाकलाप (5.9)
क्रियाकलाप 5.9 में अम्ल का उपयोग किया जाना है। अतः इसे शिक्षक की उपस्थिति में किया जाए।
किसी बीकर में लगभग एक कप जल लीजिए और उसमें तनु सल्फ्यूरिक अम्ल की कुछ बूँदें मिलाइए। जल को गर्म कीजिए। जब जल उबलना आरंभ कर दे, तो इसमें धीरे-धीरे कॉपर सल्फेट का चूर्ण निरंतर चलाते हुए मिलाएँ (चित्र 5.6)। कॉपर सल्फेट का चूर्ण मिलाना तब तक जारी रखें, जब तक कि उसमें और कॉपर सल्फेट घोलना संभव न हो। विलयन को फिल्टर पेपर की सहायता से छान लीजिए। इसे ठंडा होने दीजिए। जब विलयन ठंडा हो रहा हो, तो उसे हिला-डुलाकर या अन्य किसी प्रकार न छेड़ें। कुछ समय बाद विलयन को देखिए। क्या आपको कॉपर सल्फेट के क्रिस्टल दिखाई देते हैं? यदि नहीं, तो कुछ और समय तक प्रतीक्षा कीजिए।
आपने भौतिक और रासायनिक परिवर्तनों के बारे में पढ़ा। अपने आस-पास दिखाई देने वाले परिवर्तनों को भौतिक अथवा रासायनिक परिवर्तनों के रूप में पहचानने का प्रयास कीजिए।

चित्र 5.6 कॉपर सल्फेट के क्रिस्टल
प्रमुख शब्द
| रासायनिक परिवर्तन | क्रिस्टलीकरण | भौतिक परिवर्तन |
| रासायनिक अभिक्रिया | यशद्-लेपन | जंग लगना |
आपने क्या सीखा
- परिवर्तन दो प्रकार के हो सकते हैं, भौतिक अथवा रासायनिक।
- भौतिक परिवर्तन में पदार्थों के भौतिक गुणों में कुछ परिवर्तन होते हैं। इन परिवर्तनों में कोई नए पदार्थ नहीं बनते हैं। ये परिवर्तन उत्क्रमणीय हो सकते हैं।
- रासायनिक परिवर्तनों में नए पदार्थ बनते हैं।
- कुछ पदार्थों को क्रिस्टलीकरण के द्वारा उनके विलयनों से शुद्ध अवस्था में प्राप्त किया जा सकता है।
अभ्यास
1. निम्नलिखित प्रक्रमों के अंतर्गत होने वाले परिवर्तनों को भौतिक अथवा रासायनिक परिवर्तन के रूप में वर्गीकृत कीजिए।
(क) प्रकाश संश्लेषण
(ख) जल में शक्कर को घोलना
(ग) कोयले को जलाना
(घ) मोम को पिघलाना
(च) ऐलुमिनियम के टुकड़े को पीटकर उसका पतला पत्र (फॉइल) बनाना।
(छ) भोजन का पाचन
2. बताइए कि निम्नलिखित कथन सत्य हैं अथवा असत्य। यदि कथन असत्य हो तो, अपनी अभ्यास पुस्तिका में उसे सही करके लिखिए।
(क) लकड़ी के लट्ठे को टुकड़ों में काटना एक रासायनिक परिवर्तन है। (सत्य/असत्य)
(ख) पत्तियों से खाद का बनना एक भौतिक परिवर्तन है। (सत्य/असत्य)
(ग) जस्ते (जिंक) लेपित लोहे के पाइपों में आसानी से जंग नहीं लगती है। (सत्य/असत्य)
(घ) लोहा और जंग एक ही पदार्थ हैं। (सत्य/असत्य)
(च) भाप का संघनन रासायनिक परिवर्तन नहीं है। (सत्य/असत्य)
3. निम्नलिखित कथनों में रिक्त स्थानों को भरिए-
(क) जब कार्बन डाइऑक्साइड को चूने के पानी में प्रवाहित किया जाता है, तो यह के बनने के कारण दूधिया हो जाता है।
(ख) खाने के सोडे का रासायनिक नाम है।
(ग) ऐसी दो विधियाँ, जिनके द्वारा लोहे को जंग लगने से बचाया जा सकता है और हैं।
(घ) ऐसे परिवर्तन भौतिक परिवर्तन कहलाते हैं, जिनमें किसी पदार्थ के केवल गुणों में परिवर्तन होता है।
(च) ऐसे परिवर्तन जिनमें नए पदार्थ बनते हैं, परिवर्तन कहलाते हैं।
4. जब नींबू के रस में खाने का सोडा मिलाया जाता है, तो बुलबुले बनते हैं और गैस निकलती है। यह किस प्रकार का परिवर्तन है? समझाइए।
5. जब कोई मोमबत्ती जलती है, तो भौतिक और रासायनिक परिवर्तन दोनों होते हैं। इन परिवर्तनों की पहचान कीजिए। ऐसे ही किसी ज्ञात प्रक्रम का एक और उदाहरण दीजिए, जिसमें भौतिक और रासायनिक परिवर्तन दोनों होते हैं।
6. आप यह कैसे दिखाएँगे कि दही का जमना एक रासायनिक परिवर्तन है।
7. समझाइए कि लकड़ी के जलने और उसे छोटे टुकड़ों में काटने को दो भिन्न प्रकार के परिवर्तन क्यों माना जाता है।
8. कॉपर सल्फेट के क्रिस्टल कैसे बनाते हैं, इसका वर्णन कीजिए।
9. समझाइए कि लोहे के गेट को पेन्ट करने से उसका जंग लगने से बचाव किस कारण से होता है।
10. समझाइए कि रेगिस्तानी क्षेत्रों की अपेक्षा समुद्रतटीय क्षेत्रों में लोहे की वस्तुओं में जंग अधिक क्यों लगती है।
11. हम रसोई में जिस गैस का उपयोग करते हैं, वह द्रवित पेट्रोलियम गैस (एल.पी.जी. या LPG) कहलाती है। सिलिंडर में LPG द्रव के रूप में होती है। सिलिंडर से बाहर आते ही यह गैस में परिवर्तित हो जाती है (परिवर्तन $\mathrm{A}$ ); फिर यही गैस जलती है (परिवर्तन B)। निम्नलिखित कथन इन परिवर्तनों से संबंधित हैं। सही कथन का चयन कीजिए।
(क) प्रक्रम-A एक रासायनिक परिवर्तन है।
(ख) प्रक्रम-B एक रासायनिक परिवर्तन है।
(ग) प्रक्रम-A और प्रक्रम-B दोनों ही रासायनिक परिवर्तन हैं।
(घ) इनमें से कोई भी प्रक्रम रासायनिक परिवर्तन नहीं है।
12. अवायवीय जीवाणु जैविक अपशिष्ट पदार्थों को अपघटित कर जैव गैस (बायोगैस) बनाते हैं (परिवर्तन-A)। फिर जैव गैस ईंधन के रूप में जलाई जाती है (परिवर्तन-B)। निम्नलिखित कथन इन परिवर्तनों से संबंधित हैं। सही कथन चुनिए।
(क) प्रक्रम-A एक रासायनिक परिवर्तन है।
(ख) प्रक्रम-B एक रासायनिक परिवर्तन है।
(ग) प्रक्रम-A और प्रक्रम-B दोनों ही रासायनिक परिवर्तन हैं।
(घ) इनमें से कोई भी प्रक्रम रासायनिक परिवर्तन नहीं है।
विस्तारित अधिगम - क्रियाकलाप और परियोजना कार्य
1. ऐसे दो परिवर्तनों का वर्णन कीजिए, जो हानिकारक हों। समझाइए कि आप उन्हें हानिकारक क्यों मानते हैं। आप उनकी रोक-थाम कैसे कर सकते हैं?
2. चौडे मुँह वाली काँच की तीन बोतलें लीजिए। उन पर $\mathrm{A}, \mathrm{B}$, तथा $\mathrm{C}$ का चिह्न लगाइए। बोतल $\mathrm{A}$ को सामान्य नल के पानी से लगभग आधा भर लीजिए। बोतल $\mathrm{B}$ को उसी स्तर तक कुछ मिनट तक उबाले हुए जल से भर लीजिए, जहाँ तक बोतल A को भरा था। बोतल $\mathrm{C}$ में उसी उबले हुए जल को उसी मात्रा में लीजिए, जितनी अन्य बोतलों में ली थी। प्रत्येक बोतल में लोहे की एक जैसी कुछ कीलों को डाल दीजिए, ताकि वे पूरी तरह से पानी में डूबी रहें। बोतल $\mathrm{C}$ के जल में एक चम्मच खाना पकाने का तेल डाल दें, ताकि पानी के ऊपर उसकी एक परत बन जाए। बोतलों को कुछ दिनों तक ऐसे ही रखा रहने दें। प्रत्येक बोतल में से कीलों को निकालकर उनका अवलोकन करें। अपने प्रेक्षणों का कारण समझाएँ।
3. फिटकरी के क्रिस्टल बनाइए।
4. अपने क्षेत्र में खाना पकाने के लिए उपयोग किए जाने वाले विभिन्न किस्म के ईंधनों के बारे में जानकारी एकत्रित कीजिए। अपने शिक्षकों, माता-पिता अथवा किसी व्यक्ति से इस बारे में चर्चा कीजिए कि कौन से ईंधन कम प्रदूषणकारी हैं और क्यों?
क्या आप जानते हैं?
दिल्ली में कुतुबमीनार के पास एक लौह स्तम्भ (चित्र 5.7) है, जो सात मीटर से अधिक ऊँचा है। इसका भार $6000 \mathrm{~kg}$ से अधिक है। इसे 1600 वर्ष से भी अधिक पहले बनवाया गया था। इतने वर्षों में भी इस पर जंग नहीं लगी है। इसके जंग प्रतिरोधक गुण और इसके आमाप की वजह से विश्व भर के सभी भागों के वैज्ञानिकों के द्वारा इसका परीक्षण किया गया है। इससे यह जानकारी मिलती है कि अब से 1600 वर्ष पूर्व भारत में धातु प्रौद्योगिकी में कितना विकास हो चुका था।
चित्र 5.7 लौह स्तंभ का चित्र






