अध्याय 03 परमाणु एवं अणु
प्राचीन भारतीय एवं ग्रीक दार्शनिक द्रव्य के अज्ञात एवं अदृश्य रूपों से सदैव चकित होते रहे। पदार्थ की विभाज्यता के मत के बारे में भारत में बहुत पहले, लगभग 500 ईसा पूर्व विचार व्यक्त किया गया था। भारतीय दार्शनिक महर्षि कनाड (Maharshi Kanad) ने प्रतिपादित किया था कि यदि हम द्रव्य (पदार्थ) को विभाजित करते जाएँ तो हमें छोटे-छोटे कण प्राप्त होते जाएँगे तथा अंत में एक सीमा आएगी जब प्राप्त कण को पुनः विभाजित नहीं किया जा सकेगा अर्थात् वह सूक्ष्मतम कण अविभाज्य रहेगा। इस अविभाज्य सूक्ष्मतम कण को उन्होंने परमाणु कहा। एक अन्य भारतीय दार्शनिक पकुधा कात्यायाम (Pakudha Katyayama) ने इस मत को विस्तृत रूप से समझाया तथा कहा कि ये कण सामान्यतः संयुक्त रूप में पाए जाते हैं, जो हमें द्रव्यों के भिन्न-भिन्न रूपों को प्रदान करते हैं।
लगभग इसी समय ग्रीक दार्शनिक डेमोक्रिटस (Democritus) एवं लियुसीपस (Leucippus) ने सुझाव दिया था कि यदि हम द्रव्य को विभाजित करते जाएँ, तो एक ऐसी स्थिति आएगी जब प्राप्त कण को पुनः विभाजित नहीं किया जा सकेगा। उन्होंने इन अविभाज्य कणों को परमाणु (अर्थात् अविभाज्य) कहा था। ये सभी सुझाव दार्शनिक विचारों पर आधारित थे। इन विचारों की वैधता सिद्ध करने के लिए 18 वीं शताब्दी तक कोई अधिक प्रयोगात्मक कार्य नहीं हुए थे।
18 वों शताब्दी के अंत तक वैज्ञानिकों ने तत्वों एवं यौगिकों के बीच भेद को समझा तथा स्वाभाविक रूप से यह पता करने के इच्छुक हुए कि तत्व कैसे तथा क्यों संयोग करते हैं? जब तत्व परस्पर संयोग करते हैं, तब क्या होता है?
वैज्ञानिक आंतवाँ एल. लवाइजिए (Antonie L. Lavoisier) ने रासायनिक संयोजन के दो महत्वपूर्ण नियमों को स्थापित किया जिसने रसायन विज्ञान को महत्वपूर्ण आधार प्रदान किया।
3.1 रासायनिक संयोजन के नियम
लवाइजिए एवं जोजफ एल. प्राउस्ट (Joseph L. Proust) ने बहुत अधिक प्रायोगिक कार्यों के पश्चात् रासायनिक संयोजन के निम्नलिखित दो नियम प्रतिपादित किए।
3.1.1 द्रव्यमान संरक्षण का नियम
जब रासायनिक परिवर्तन (रासायनिक अभिक्रिया) संपन्न होता है, तब क्या द्रव्यमान में कोई परिवर्तन होता है?
क्रियाकलाप 3.1
निम्न $X$ एवं $Y$ रसायनों का एक युगल लीजिए। $\boldsymbol{X}$
$\text{X}$ $\text{Y}$ (i) कॉपर सल्फेट $Y$ सोडियम कार्बोनेट (ii) बेरियम क्लोराइड सोडियम सल्फेट सोडियम सल्फेट (iii) लेड नाइट्रेट सोडियम क्लोराइड सोडियम क्लोराइड $X$ एवं $Y$ युगलों की सूची में से किसी एक युगल के रसायनों के अलग-अलग विलयन $10 \mathrm{~mL}$ जल में तैयार कीजिए।
उपरोक्त तैयार युगल विलयनों में से $\mathrm{Y}$ के विलयन को एक शंक्वाकार फ्लास्क में लीजिए एवं $\mathrm{X}$ के विलयन को एक छोटी परख नली में लीजिए।
छोटी परख नली को विलय युक्त फ्लास्क में इस प्रकार लटकाइए ताकि दोनों विलयन परस्पर मिश्रित न हों। तत्पश्चात् फ्लास्क के मुख पर एक कार्क चित्र 3.1 की भाँति लगाइए।
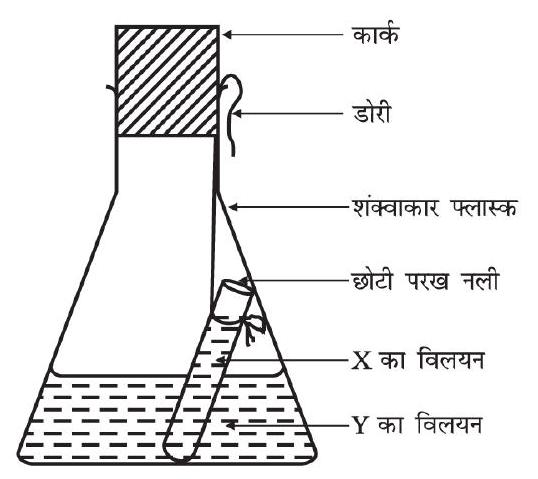
चित्र 3.1: $Y$ के विलयन युक्त शंक्वाकार फ्लास्क में डूबी हुई $X$ के विलयन युक्त छोटी परख नली।
अंर्तवस्तु युक्त फ्लास्क को सावधानीपूर्वक तौल लीजिए।
अब फ्लास्क को झुकाकर इस प्रकार घुमाएँ जिससे $X$ एवं $Y$ के विलयन परस्पर मिश्रित हो जाएँ।
अब इस फ्लास्क को पुनः तौल लीजिए।
शंक्वाकार फ्लास्क में क्या अभिक्रिया हुई?
क्या आप सोचते हैं कि कोई रासायनिक अभिक्रिया हुई?
फ्लास्क के मुख पर कार्क क्यों लगाते हैं?
क्या फ्लास्क के द्रव्यमान एवं अंतर्वस्तुओं में कोई परिवर्तन हुआ?
द्रव्यमान संरक्षण के नियम के अनुसार किसी रासायनिक अभिक्रिया में द्रव्यमान का न तो सृजन किया जा सकता है न ही विनाश।
3.1.2 स्थिर अनुपात का नियम
लवाइजिए एवं अन्य वैज्ञानिकों ने इस बात पर प्रकाश डाला कि कोई भी यौगिक दो या दो से अधिक तत्वों से निर्मित होता है। इस प्रकार प्राप्त यौगिकों में, इन तत्वों का अनुपात स्थिर होता है चाहे इसे किसी स्थान से प्राप्त किया गया हो अथवा किसी ने भी इसे बनाया हो।
यौगिक जल में हाइड्रोजन एवं ऑक्सीजन के द्रव्यमानों का अनुपात सदैव $1: 8$ होता है चाहे जल का स्रोत कोई भी हो। इसी प्रकार यदि $9 \mathrm{~g}$ जल का अपघटन करें तो सदैव $1 \mathrm{~g}$ हाइड्रोजन तथा $8 \mathrm{~g}$ ऑक्सीजन ही प्राप्त होगी। इसी प्रकार अमोनिया $\left(\mathrm{NH} _{3}\right)$ में, नाइट्रोजन एवं हाइड्रोजन द्रव्यमानों के अनुसार सदैव $14: 3$ के अनुपात में विद्यमान रहते हैं, चाहे अमोनिया किसी भी प्रकार से निर्मित हुई हो अथवा किसी भी स्रोत से ली गई हो।
उपरोक्त उदाहरणों से स्थिर अनुपात के नियम की व्याख्या होती है जिसे निश्चित अनुपात का नियम भी कहते हैं। प्राउस्ट ने इस नियम को इस प्रकार से व्यक्त किया था “किसी भी यौगिक में तत्व सदैव एक निश्चित द्रव्यमानों के अनुपात में विद्यमान होते हैं”।
वैज्ञानिकों की अगली समस्या इन नियमों की उचित व्याख्या करने की थी। अंग्रेज रसायनज्ञ, जॉन डाल्टन ने द्रव्यों की प्रकृति के बारे में एक आधारभूत सिद्धांत प्रस्तुत किया। डाल्टन ने द्रव्यों की विभाज्यता का विचार प्रदान किया जिसे उस समय तक दार्शनिकता माना जाता था। ग्रीक दार्शनिकों के द्वारा द्रव्यों के सूक्ष्मतम अविभाज्य कण, जिसे परमाणु नाम दिया था, उसे डाल्टन ने भी परमाणु नाम दिया। डाल्टन का यह सिद्धांत रासायनिक संयोजन के नियमों पर आधारित था। डाल्टन के परमाणु सिद्धांत ने द्रव्यमान के संरक्षण के नियम एवं निश्चित अनुपात के नियम की युक्तिसंगत व्याख्या की।
जॉन डाल्टन का जन्म सन् 1766 में इंग्लैंड के एक गरीब जुलाहा परिवार में हुआ था। बारह वर्ष की आयु में उन्होंने एक शिक्षक के रूप में अपनी जीविका शुरू की। सात साल बाद वह एक जॉन डाल्टन स्कूल के प्रिंसिपल बन गए। सन् 1793 में जॉन डाल्टन एक कॉलेज में गणित, भौतिकी एवं रसायन शास्त्र पढ़ाने के लिए मैनचेस्टर चले गए।

वहाँ पर उन्होंने अपने जीवन का अधिकांश समय शिक्षण एवं शोधकार्य में व्यतीत किया। सन् 1808 में इन्होंने अपने परमाणु सिद्धांत को प्रस्तुत किया, जो द्रव्यों के अध्ययन के लिए एक महत्वपूर्ण सिद्धांत साबित हुआ।
डाल्टन के परमाणु सिद्धांत के अनुसार सभी द्रव्य चाहे तत्व, यौगिक या मिश्रण हो, सूक्ष्म कणों से बने होते हैं जिन्हें परमाणु कहते हैं। डाल्टन के सिद्धांत की विवेचना निम्न प्रकार से कर सकते हैं :
(i) सभी द्रव्य परमाणुओं से निर्मित होते हैं, जो कि रासायनिक अभिक्रिया में भाग लेते हैं।
(ii) परमाणु अविभाज्य सूक्ष्मतम कण होते हैं जो रासायनिक अभिक्रिया में न तो सृजित होते हैं न ही उनका विनाश होता है।
(iii) दिए गए तत्व के सभी परमाणुओं का द्रव्यमान एवं रासायनिक गुणधर्म समान होते हैं।
(iv) भिन्न-भिन्न तत्वों के परमाणुओं के द्रव्यमान एवं रासायनिक गुणधर्म भिन्न-भिन्न होते हैं।
(v) भिन्न-भिन्न तत्वों के परमाणु परस्पर छोटी पूर्ण संख्या के अनुपात में संयोग कर यौगिक निर्मित करते हैं।
(vi) किसी भी यौगिक में परमाणुओं की सापेक्ष संख्या एवं प्रकार निश्चित होते हैं।
आप अगले अध्याय में यह अध्ययन करेंगे कि परमाणु में और भी छोटे-छोटे कण विद्यमान होते हैं।
प्रशन
1. एक अभिक्रिया में $5.3 \mathrm{~g}$ सोडियम कार्बोनेट एवं $6.0 \mathrm{~g}$ एसीटिक अम्ल अभिकृत होते हैं। $2.2 \mathrm{~g}$ कार्बन डाइऑक्साइड, $8.2 \mathrm{~g}$ सोडियम एसीटेट एवं $0.9 \mathrm{~g}$ जल उत्पाद के रूप में प्राप्त होते हैं। इस अभिक्रिया द्वारा दिखाइए कि यह परीक्षण द्रव्यमान संरक्षण के नियम के अनुरूप है।
सोडियम कार्बोनेट + एसीटिक अम्ल $\rightarrow$ सोडियम एसीटेट + कार्बन डाइऑक्साइड + जल
Show Answer
missing2. हाइड्रोजन एवं ऑक्सीजन द्रव्यमान के अनुसार $1: 8$ के अनुपात में संयोग करके जल निर्मित करते हैं। $3 \mathrm{~g}$ हाइड्रोजन गैस के साथ पूर्ण रूप से संयोग करने के लिए कितने ऑक्सीजन गैस के द्रव्यमान की आवश्यकता होगी?
Show Answer
missing3. डाल्टन के परमाणु सिद्धांत का कौन-सा अभिग्रहीत द्रव्यमान के संरक्षण के नियम का परिणाम है?
Show Answer
missing4. डाल्टन के परमाणु सिद्धांत का कौन-सा अभिग्रहीत निश्चित अनुपात के नियम की व्याख्या करता है?
Show Answer
missing3.2 परमाणु क्या होता है?
क्या आपने कभी किसी इमारत की दीवार बनते देखी है? इन दीवारों से एक कमरा एवं कई कमरों के समूह से एक इमारत निर्मित होती है। उस विशाल इमारत की रचनात्मक इकाई क्या है? किसी बाँबी (Ant-Hill) की रचनात्मक इकाई क्या होती है? यह रेत का छोटा-सा कण होता है। इसी प्रकार, सभी द्रव्यों की रचनात्मक इकाई परमाणु होती है।
परमाणु कितने बड़े होते हैं?
परमाणु बहुत छोटे होते हैं। ये किसी भी वस्तु, जिसकी हम कल्पना या तुलना कर सकते हैं, से भी छोटे होते हैं। लाखों परमाणुओं को जब एक के ऊपर एक चट्टे के रूप में रखें, तो बड़ी कठिनाई से कागज की एक शीट जितनी मोटी परत बन पाएगी।
परमाणु त्रिज्या को नेनोमीटर $(\mathrm{nm})$ में मापा जाता है।
$$ \begin{aligned} 1 / 10^{9} m & =1 nm \\ 1 m & =10^{9} nm \end{aligned} $$
सापेक्ष आकार
| त्रिज्या (मीटर में) | उदाहरण |
|---|---|
| $10^{-10}$ | हाइड्रोजन परमाणु |
| $10^{-9}$ | जल अणु |
| $10^{-8}$ | हीमोग्लोबिन अणु |
| $10^{-4}$ | रेत कण |
| $10^{-3}$ | चींटी |
| $10^{-1}$ | सेब |
जब परमाणु का आकार इतना सूक्ष्म है कि हम इसे नगण्य मान सकते हैं, तो हम इसके बारे में क्यों सोचें? हम इसके बारे में इसलिए सोचते हैं क्योंकि हमारा पूरा विश्व ही परमाणुओं से बना है। चाहे हम उन्हें देख नहीं सकें, फिर भी वे यहाँ विद्यमान हैं तथा हमारे प्रत्येक क्रियाकलापों पर उनका प्रभाव पड़ता रहता है। अब हम आधुनिक तकनीकों की सहायता से तत्वों की सतहों के आवर्धित प्रतिबिंबों को दिखा सकते हैं, जिनमें उपस्थित परमाणु स्पष्ट दिखाई देते हैं।

चित्र 3.2: सिलिकॉन सतह का प्रतिबिंब
3.2.1 विभिन्न तत्वों के परमाणुओं के आधुनिक प्रतीक क्या हैं?
डाल्टन ऐसे प्रथम वैज्ञानिक थे, जिन्होंने तत्वों के प्रतीकों का प्रयोग अत्यंत विशिष्ट अर्थ में किया। जब उन्होंने किसी तत्व के प्रतीक का प्रयोग किया, तो यह प्रतीक उस तत्व की एक निश्चित मात्रा की ओर इंगित करता था अर्थात् यह प्रतीक तत्व के एक परमाणु को प्रदर्शित करता था। बर्जिलियस ने तत्वों के ऐसे प्रतीकों का सुझाव दिया, जो उन तत्वों के नामों के एक या दो अक्षरों से प्रदर्शित होता था।
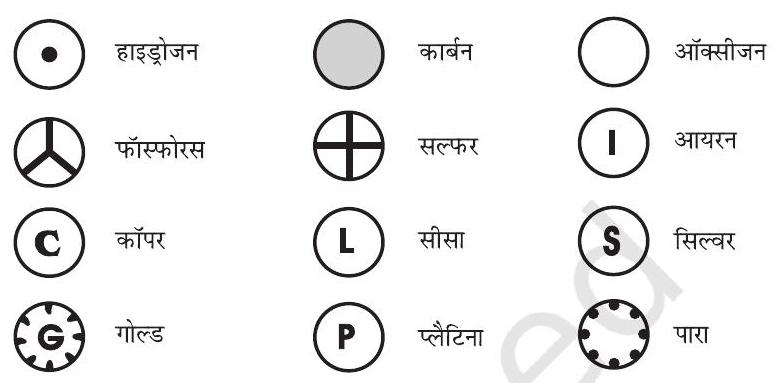
चित्र 3.3: डाल्टन द्वारा सुझाए गए कुछ तत्वों के प्रतीक
प्रारंभ में तत्वों के नामों की व्युत्पत्ति उन स्थानों के नामों से की गई, जहाँ वे सर्वप्रथम पाए गए थे। उदाहरणस्वरूप, कॉपर (Copper) का नाम साइप्रस (Cyprus) से व्युत्पन्न हुआ। कुछ तत्वों के नामों को विशिष्ट रंगों से लिया गया। उदाहरणस्वरूप, स्वर्ण (gold) का नाम अंग्रेजी के उस शब्द से लिया गया, जिसका अर्थ होता है पीला। इंटरनेशनल यूनियन ऑफ प्योर एंड एप्लाइड केमिस्ट्री (IUPAC) एक अर्न्तराष्ट्रीय वैज्ञानिक संस्था है जो तत्वों के नामों, प्रतीकों और मात्रकों को स्वीकृति प्रदान करती है। अधिकतर तत्वों के प्रतीक उन तत्वों के अंग्रेजी नामों के एक या दो अक्षरों से बने होते हैं। किसी प्रतीक के पहले अक्षर को सदैव बड़े अक्षर (capital letter) में तथा दूसरे अक्षर को छोटे अक्षर (small letter) में लिखा जाता है।
उदाहरणार्थ
(i) हाइड्रोजन, $\mathrm{H}$
(ii) ऐलुमिनियम, $\mathrm{Al}$ न कि $\mathrm{AL}$
(iii) कोबाल्ट, $\mathrm{Co}$ न कि $\mathrm{CO}$
कुछ तत्वों के प्रतीक उनके अंग्रेजी नामों के प्रथम अक्षर तथा बाद में आने वाले किसी एक अक्षर को संयुक्त करके बनाते हैं। उदाहरण : (i) क्लोरीन, $\mathrm{Cl}$, (ii) जिंक, $\mathrm{Zn}$ इत्यादि।
अन्य तत्वों के प्रतीकों को लैटिन, जर्मन या ग्रीक भाषाओं में उनके नामों से बनाया गया है। उदाहरणार्थ: लौह (Iron) का प्रतीक $\mathrm{Fe}$ है, जो उसके लैटिन नाम फेरम से व्युत्पन्न किया गया है। इसी प्रकार सोडियम का प्रतीक $\mathrm{Na}$ तथा पोटैशियम का प्रतीक $\mathrm{K}$ क्रमशः नैट्रियम एवं केलियम से व्युत्पन्न हैं। इस प्रकार प्रत्येक तत्व का एक नाम एवं एक अद्वितीय रासायनिक प्रतीक होता है।
3.2.2 परमाणु द्रव्यमान
डाल्टन के परमाणु सिद्धांत की सबसे विशिष्ट संकल्पना परमाणु द्रव्यमान की थी। उनके अनुसार प्रत्येक तत्व का एक अभिलाक्षणिक परमाणु द्रव्यमान होता है। डाल्टन का सिद्धांत स्थिर अनुपात के नियम को इतनी भली-भाँति समझाने में समर्थ था कि वैज्ञानिक इससे प्रेरित होकर परमाणु द्रव्यमान को मापने की ओर अग्रसर हुए। चूँकि एक परमाणु के द्रव्यमान को ज्ञात करना अपेक्षाकृत कठिन कार्य था इसलिए रासायनिक संयोजन के नियमों के उपयोग एवं उत्पन्न यौगिकों के द्वारा सापेक्ष परमाणु द्रव्यमानों को ज्ञात किया गया।(जब कभी आप तत्वों का अध्ययन करें, तो आपके संदर्भ के लिए उपरोक्त सारणी दी गई है। इस पूरी सारणी को एक बार में याद करने की आवश्यकता नहीं है। समय-समय पर एवं बार-बार उपयोग करते रहने से आप स्वतः ही इन प्रतीकों को निर्मित करना सीख जाएँगे।)
हम यहाँ पर एक यौगिक, कार्बन मोनोक्साइड $(\mathrm{CO})$ का उदाहरण लेते हैं, जो कार्बन एवं ऑक्सीजन द्वारा निर्मित होता है। प्रायोगिक तौर पर यह निरीक्षित किया गया कि $3 \mathrm{~g}$ कार्बन तथा $4 \mathrm{~g}$ ऑक्सीजन के संयोजन से कार्बन मोनोक्साइड निर्मित हुई है। दूसरे शब्दों में कहा जा सकता है कि कार्बन अपने $4 / 3$ गुणा अधिक द्रव्यमान वाले ऑक्सीजन के साथ संयुक्त होती है। मान लीजिए, हम परमाणु द्रव्यमान की इकाई को एक कार्बन परमाणु द्रव्यमान के बराबर मानते हैं
सारणी 3.1: कुछ तत्वों के प्रतीक
| तत्व | प्रतीक | तत्व | प्रतीक | तत्व | प्रतीक |
|---|---|---|---|---|---|
| ऐलुमिनियम | $\mathrm{Al}$ | कॉपर | $\mathrm{Cu}$ | नाइट्रोजन | $\mathrm{N}$ |
| आर्गन | $\mathrm{Ar}$ | फ्लुअं | $F$ | ऑक्सीजन | $\mathrm{O}$ |
| बेरियम | $\mathrm{Ba}$ | स्वर्ण | $\mathrm{u}$ | पोटैशियम | $\mathrm{K}$ |
| बोरॉन | B | हाइड्रो | $\mathrm{H}$ | सिलिकॉन | $\mathrm{Si}$ |
| ब्रोमीन | $\mathrm{Br}$ | आयो | I | चाँदी (सिल्वर) | $\mathrm{Ag}$ |
| कैल्सियम | $\mathrm{Ca}$ | आय | $\mathrm{Fe}$ | सोडियम | $\mathrm{Na}$ |
| कार्बन | $\mathrm{C}$ | सीसा | $\mathrm{Pb}$ | सल्फर | $\mathrm{S}$ |
| क्लोरीन | $\mathrm{Cl}$ | मैग्नीी | Mg | यूरेनियम | $\mathrm{U}$ |
| कोबाल्ट | Co | नियॉन | $\mathrm{Ne}$ | जिंक | $\mathrm{Zn}$ |
तो कार्बन परमाणु को $1.0 \mathrm{u}$ तथा ऑक्सीजन परमाणु द्रव्यमान को $1.33 \mathrm{u}$ निर्दिष्ट करेंगे। (प्रारंभ में परमाणु द्रव्यमान को $\mathrm{amu}$ द्वारा संक्षेप में लिखते थे, लेकिन आजकल IUPAC के नवीनतम अनुमोदन द्वारा इसको ’ $u$ ‘-यूनीफाइड द्रव्यमान द्वारा प्रदर्शित करते हैं।) लेकिन द्रव्यमानों की इकाई को यथासंभव पूर्णांक या लगभग पूर्णांक में व्यक्त करना अधिक सुविधाजनक होता है। आगे चलकर वैज्ञानिकों ने परमाणु द्रव्यमानों की भिन्न-भिन्न इकाइयों के बारे में विचार व्यक्त किए। वैज्ञानिक जब विभिन्न परमाणु द्रव्यमानों की इकाइयों के बारे में शोधरत थे तो उन्होंने प्रारंभ में प्रकृतिजन्य ऑक्सीजन परमाणु के द्रव्यमान के $1 / 16$ भाग को इकाई के रूप में लिया। दो कारणों से इसे सुसंगत समझा गया:
ऑक्सीजन अनेक तत्वों के साथ अभिक्रिया करके यौगिक बनाता है।
इस परमाणु द्रव्यमान इकाई द्वारा अधिकांश तत्वों के परमाणु द्रव्यमान पूर्णांक में प्राप्त होते हैं।
तथापि, 1961 में परमाणु द्रव्यमानों को ज्ञात करने के लिए परमाणु द्रव्यमान इकाई कार्बन-12 समस्थानिक (आइसोटोप) को मानक संदर्भ के रूप में सार्वभौमिक रूप से स्वीकार किया गया था। कार्बन- 12 समस्थानिक के एक परमाणु द्रव्यमान के $1 / 12$ वें भाग को मानक परमाणु द्रव्यमान इकाई के रूप में लेते हैं। कार्बन- 12 समस्थानिक के एक परमाणु द्रव्यमान के सापेक्ष सभी तत्वों के परमाणु द्रव्यमान प्राप्त किए गए।
कल्पना कीजिए कि एक फल विक्रेता बिना मानक भार के फल बेच रहा है। वह एक तरबूज लेकर कहता है कि “इसका द्रव्यमान 12 इकाई है” ( 12 तरबूजीय इकाई अथवा 12 फल द्रव्यमान इकाई )। वह तरबूज के 12 बराबर टुकड़े करता है तथा पाता है कि उसके द्वारा बेचे जा रहे प्रत्येक फल का द्रव्यमान तरबूज के एक टुकड़े के द्रव्यमान के सापेक्ष है। जैसा कि चित्र 3.4 में दिखाया गया है, अब वह फलों को सापेक्ष फल द्रव्यमान इकाई (fmu) में बेचता है।

चित्र 3.4 : (a) तरबूज (b) 12 टुकड़े (c) तरबूज का $1 / 12$ वाँ भाग (d) तरबूज के टुकड़ों का उपयोग करके वह फल विक्रेता फलों को कैसे तौल सकता है
किसी तत्व के सापेक्षिक परमाणु द्रव्यमान को उसके परमाणुओं के औसत द्रव्यमान का कार्बन-12 परमाणु के द्रव्यमान के $1 / 12$ वें भाग के अनुपात द्वारा परिभाषित किया जाता है।
सारणी 3.2: कुछ तत्वों के परमाणु द्रव्यमान
| तत्व | परमाणु द्रव्यमान (u) |
|---|---|
| हाइड्रोजन | 1 |
| कार्बन | 12 |
| नाइट्रोजन | 14 |
| ऑक्सीजन | 16 |
| सोडियम | 23 |
| मैग्नीशियम | 24 |
| सल्फर | 32 |
| क्लोरीन | 35.5 |
| कैल्सियम | 40 |
3.2.3 परमाणु किस प्रकार अस्तित्व में रहते हैं?
अधिकांश तत्वों के परमाणु स्वतंत्र रूप से अस्तित्व में नहीं रह पाते। परमाणु अणु एवं आयन बनाते हैं। ये अणु अथवा आयन अत्यधिक संख्या में पुंजित होकर वह द्रव्य बनाते हैं, जिसे हम देख सकते हैं, अनुभव कर सकते हैं अथवा छू सकते हैं।
प्रशन
1. परमाणु द्रव्यमान इकाई को परिभाषित कीजिए।
Show Answer
missing2. एक परमाणु को आँखों द्वारा देखना क्यों संभव नहीं होता है?
Show Answer
missing3.3. अणु क्या है?
साधारणतया अणु ऐसे दो या दो से अधिक परमाणुओं का समूह होता है जो आपस में रासायनिक बंध द्वारा जुड़े होते हैं अथवा वे परस्पर आकर्षण बल के द्वारा कसकर जुड़े होते हैं। अणु को किसी तत्व अथवा यौगिक के उस सूक्ष्मतम कण के रूप में परिभाषित कर सकते हैं जो स्वतंत्र रूप से अस्तित्व में रह सकता है तथा जो उस यौगिक के सभी गुणधर्म को प्रदर्शित करता है। एक ही तत्व के परमाणु अथवा भिन्न-भिन्न तत्वों के परमाणु परस्पर संयोग करके अणु निर्मित करते हैं।
3.3.1 तत्वों के अणु
किसी तत्व के अणु एक ही प्रकार के परमाणुओं द्वारा संरचित होते हैं। आर्गन $(\mathrm{Ar})$, हीलियम $(\mathrm{He})$ इत्यादि जैसे अनेक तत्वों के अणु उसी तत्व के केवल एक परमाणु द्वारा निर्मित होते हैं। लेकिन अधिकांश अधातुओं में ऐसा नहीं होता है। उदाहरणार्थ, ऑक्सीजन अणु दो ऑक्सीजन परमाणुओं से बनता है, इसलिए इसे द्वि-परमाणुक अणु, $\mathrm{O} _{2}$ कहते हैं। यदि सामान्यतः 2 के स्थान पर 3 ऑक्सीजन परमाणु परस्पर संयोग करते हैं तो हमें ओजोन, $\mathrm{O} _{3}$ प्राप्त होता है। किसी अणु की संरचना में प्रयुक्त होने वाले परमाणुओं की संख्या को उस अणु की परमाणुकता कहते हैं।
धातु अणुओं एवं कुछ अन्य तत्वों के अणुओं जैसे कि कार्बन के अणुओं की सरल संरचना नहीं होती है किंतु उनके अणुओं में असीमित परमाणु परस्पर बँधे होते हैं।
आइए, कुछ तत्वों की परमाणुकता का अवलोकन करें।
सारणी 3.3: कुछ तत्वों की परमाणुकता
| तत्वों के प्रकार | नाम | परमाणुकता |
|---|---|---|
| अधातु | आर्गन | एक परमाणुक |
| हीलियम | एक परमाणुक | |
| ऑक्सीजन | द्विपरमाणुक | |
| हाइड्रोजन | द्विपरमाणुक | |
| नाइट्रोजन | द्विपरमाणुक | |
| क्लोरीन | द्विपरमाणुक | |
| फॉस्फोरस | चतुर्परमाणुक | |
| सल्फर | बहुपरमाणुक |
3.3.2 यौगिकों के अणु
भिन्न-भिन्न तत्वों के परमाणु एक निश्चित अनुपात में परस्पर जुड़कर यौगिकों के अणु निर्मित करते हैं। सारणी 3.4 में कुछ उदाहरण दिए गए हैं।
सारणी 3.4: कुछ यौगिकों के अणु
| यौगिक | संयुक्त तत्व | द्रव्यमान अनुपात |
|---|---|---|
| जल | हाइड्रोजन, ऑक्सीजन | $1: 8$ |
| अमोनिया | नाइट्रोजन, हाइड्रोजन | $14: 3$ |
| कार्बन | ||
| डाइऑक्साइड | कार्बन, ऑक्सीजन | $3: 8$ |
क्रियाकलाप 3.2
अणुओं में विद्यमान परमाणुओं के द्रव्यमान अनुपातों के लिए सारणी 3.4 एवं तत्वों के परमाणु द्रव्यमानों के लिए सारणी 3.2 देखिए। सारणी 3.4 में दिए गए यौगिकों के अणुओं में प्रयुक्त तत्वों के परमाणुओं की संख्या के अनुपातों को ज्ञात कीजिए।
जल अणु में प्रयुक्त परमाणुओं की संख्याओं का अनुपात निम्न प्रकार से प्राप्त किया जा सकता है :
| तत्व | द्रव्यमान अनुपात | परमाणु द्रव्यमान (u) | द्रव्यमान अनु पात/ परमाणु द्र व्यमान | सरलतम अनुपात |
|---|---|---|---|---|
| H | 1 | 1 | $\frac{1}{1}=1$ | 2 |
| O | 8 | 16 | $\frac{8}{16}=\frac{1}{2}$ | 1 |
इस प्रकार, जल अणु में प्रयुक्त परमाणुओं की संख्याओं का अनुपात
$\mathrm{H}: \mathrm{O}=2: 1$
3.3.3 आयन क्या होता है?
धातु एवं अधातु युक्त यौगिक आवेशित कणों से बने होते हैं। इन आवेशित कणों को आयन कहते हैं। आयन एक आवेशित परमाणु अथवा परमाणुओं का एक ऐसा समूह होता है जिस पर नेट आवेश विद्यमान होता है। यह ऋण आवेश अथवा धन आवेश होता है। ऋण आवेशित आयन को ऋणायन (anion) तथा धन आवेशित आयन को धनायन (cation) कहते हैं। उदाहरण के लिए सोडियम क्लोराइड $(\mathrm{NaCl})$ को लीजिए। इसमें धनात्मक सोडियम आयन $\left(\mathrm{Na}^{+}\right)$तथा ॠणात्मक क्लोराइड आयन $\left(\mathrm{Cl}^{-}\right)$संघटक कण के रूप में विद्यमान होते हैं। परमाणुओं के समूह जिन पर नेट आवेश विद्यमान हो उसे बहुपरमाणुक आयन कहते हैं (सारणी 3.6)। हम आयनों के निर्माण के बारे में अध्याय-4 में और अधिक जानकारी प्राप्त करेंगे।
सारणी 3.5: कुछ आयनिक यौगिक
| आयनिक यौगिक | संघटक त्व | द्रव्यमान अनुपात |
|---|---|---|
| कैल्सियम ऑक्साइड | कैल्सियम एवं ऑक्सीजन | 5:2 |
| मैग्नीशियम सल्फाइड | मैग्नीशियम एवं सल्फर | 3:4 |
| सोडियम क्लोराइड | सोडियम एवं क्लोरीन | 23:35.5 |
3.4 रासायनिक सूत्र लिखना
किसी यौगिक का रासायनिक सूत्र उसके संघटक का प्रतीकात्मक निरूपण होता है। भिन्न-भिन्न यौगिकों के रासायनिक सूत्र सरलतापूर्वक लिखे जा सकते हैं। इस अभ्यास के लिए हमें तत्वों के प्रतीकों एवं उनकी संयोजन क्षमताएँ ज्ञात होनी चाहिए।
किसी तत्व की संयोजन शक्ति (अथवा क्षमता) उस तत्व की संयोजकता कहलाती है। किसी एक तत्व के परमाणु दूसरे तत्व के परमाणुओं के साथ किस प्रकार से संयुक्त होकर एक रासायनिक यौगिक का निर्माण करते हैं? इसको ज्ञात करने के लिए संयोजकता का उपयोग करते हैं। किसी तत्व के परमाणु की संयोजकता को उसके हाथ अथवा भुजा के रूप में विचार किया जा सकता है।
मानव की दो भुजाएँ तथा ऑक्टोपस की आठ भुजाएँ होती हैं। ऑक्टोपस की एक भुजा मानव की केवल एक भुजा पकड़ सकती है। यदि एक ऑक्टोपस को कुछ मानवों को इस प्रकार से पकड़ना है कि उसकी आठ भुजाएँ मानवों की दोनों भुजाओं के साथ प्रयुक्त हो जाएँ तो आपके विचार में ऑक्टोपस कुल कितने मानवों को पकड़ सकता है? अब ऑक्टोपस को $O$ तथा मानव को $H$ से निरूपित कीजिए। क्या आप इस संयोजन के लिए सूत्र लिख सकते हैं? क्या आप $\mathrm{OH} _{4}$ को सूत्र के रूप में प्राप्त करेंगे? पादांक 4 ऑक्टोपस द्वारा पकड़े गए मानवों की संख्या को प्रदर्शित करता है।
सारणी 3.6 में कुछ सरल एवं बहुपरमाणुक आयनों की संयोजकताएँ दी गई हैं। संयोजकता के बारे में हम और अधिक जानकारी अगले अध्याय में प्राप्त करेंगे।
सारणी 3.6: कुछ सामान्य, सरल एवं बहुपरमाणुक आयन
| संयोजकता | आयन का नाम | संकेत | अधात्विक तत्व | संकेत | बहुपरमाणुक आयन | संकेत |
|---|---|---|---|---|---|---|
| 1. | सोडियम पोटैशियम सिल्वर कॉपर (I)* | $Na^{+}$ $K^{+}$ $Ag^{+}$ $Cu^{+}$ | हाइड्रोजन हाइड्राइड क्लोराइड ब्रोमाइड आयोडाइड | $H^{+}$ $H^{-}$ $Cl^{-}$ $Br^{-}$ $I^{-}$ | अमोनियम हाइड्रॉक्साइड नाइट्रेट हाइड्रोजन कार्बोनेट | $NH_4^{+}$ $OH^{-}$ $NO_3^{-}$ $HCO_3^{-}$ |
| 2. | मैग्नीशियम कैल्सियम जिक आयरन (II)* कॉपर (II)* | $Mg^{2+}$ $Ca^{2+}$ $Zn^{2+}$ $Fe^{2+}$ $Cu^{2+}$ | ऑक्साइड सल्फाइड | $O^{2-}$ $S^{2-}$ | कार्बोनेट सल्फाइट सल्फेट | $CO_3{ }^{2-}$ $SO_3{ }^{2-}$ $SO_4{ }^{2-}$ |
| 3. | ऐलुमिनियम आयरन (III)* | $Al^{3+}$ $Fe^{3+}$ | नाइट्राइड | $N^{3-}$ | फॉस्फेट | $PO_4^{3-}$ |
कुछ तत्व एक से अधिक संयोजकता दर्शाते हैं। संयोजकता को कोष्ठकों में रोमन संख्यांक द्वारा प्रदर्शित करते हैं।
रासायनिक सूत्र लिखते समय आपको निम्न नियमों का पालन करना चाहिए:
आयन की संयोजकता अथवा आवेश संतुलित होना चाहिए।
जब एक यौगिक किसी धातु एवं अधातु के संयोग से निर्मित होता है तो धातु के नाम अथवा उसके प्रतीक को रासायनिक सूत्र में पहले लिखते हैं। उदाहरणार्थः कैल्सियम ऑक्साइड $(\mathrm{CaO})$, सोडियम क्लोराइड $(\mathrm{NaCl})$, आयरन सल्फाइड (FeS), कॉपर ऑक्साइड $(\mathrm{CuO}) \ldots$ इत्यादि, जहाँ पर ऑक्सीजन, क्लोरीन, सल्फर अधातुएँ हैं तथा उन्हें दायीं तरफ लिखते हैं, जबकि कैल्सियम, सोडियम, आयरन एवं कॉपर धातुएँ हैं तथा उन्हें बायीं तरफ लिखते हैं।
बहुपरमाणुक आयनों द्वारा निर्मित यौगिकों में आयनों की संख्या दर्शाने के लिए आयन को कोष्ठक में लिखकर आयनों की संख्या कोष्ठक के बाहर लिखते हैं उदाहरण $\mathrm{Mg}(\mathrm{OH}) _{2}$ है। यदि बहुपरमाणुक आयन की संख्या 1 हो तो कोष्ठक की आवश्यकता नहीं होती। उदाहरण के लिए $\mathrm{NaOH}$
3.4.1 सरल यौगिकों के सूत्र
दो भिन्न-भिन्न तत्वों से निर्मित सरलतम यौगिकों को द्विअंगी यौगिक कहते हैं। सारणी 3.6 में कुछ आयनों की संयोजकताएँ दी गई हैं। आप इनका उपयोग यौगिकों के सूत्रों को लिखने के लिए कर सकते हैं। आण्विक यौगिकों के रासायनिक सूत्र लिखते समय हम पहले संघटक तत्वों के प्रतीक लिखकर उनकी संयोजकताएँ लिखते हैं जैसा कि निम्न उदाहरणों में दर्शाया गया है। तत्पश्चात् संयोजित परमाणुओं की संयोजकताओं को क्रॉस करके (cross over) अणु सूत्र लिखते हैं।
उदाहरण
1. हाइड्रोजन क्लोराइड का सूत्र
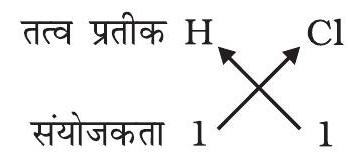
अतः हाइड्रोजन क्लोराइड का रासायनिक सूत्र $\mathrm{HCl}$ है।
2. हाइड्रोजन सल्फाइड के सूत्र
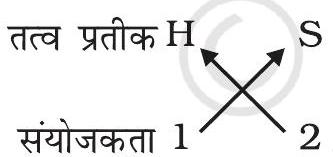
अतः हाइड्रोजन सल्फाइड का सूत्र : $\mathrm{H} _{2} \mathrm{~S}$ है।
3. कार्बन टेट्राक्लोराइड का सूत्र
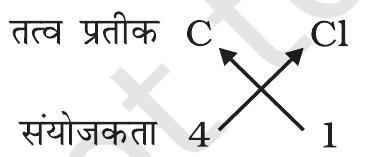
अतः कार्बन टेट्राक्लोराइड का सूत्र : $\mathrm{CCl} _{4}$ है।
मैग्नीशियम क्लोराइड का सूत्र ज्ञात करने के लिए पहले हम धनायन का संकेत $\left(\mathrm{Mg}^{2+}\right)$ लिखते हैं इसके पश्चात् ऋणायन क्लोराइड $\left(\mathrm{Cl}^{-}\right)$लिखते हैं। तत्पश्चात् इनके आवेशों को आड़ा-तिरछा (criss-cross) करके हम सूत्र प्राप्त करते हैं।
4. मैग्नीशियम क्लोराइड का सूत्र
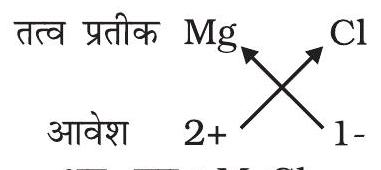
अतः सूत्र : $\mathrm{MgCl} _{2}$
इस प्रकार हम देखते हैं कि मैग्नीशियम क्लोराइड के अणु में दो क्लोराइड आयन $\left(\mathrm{Cl}^{-}\right)$प्रत्येक मैग्नीशियम आयन $\left(\mathrm{Mg}^{2+}\right)$ के लिए होता है। इस प्रकार के आयनिक यौगिकों में धनात्मक तथा ॠणात्मक आवेशों का संतुलन होना चाहिए तथा संपूर्ण संरचना उदासीन होनी चाहिए। ध्यान देने योग्य बात यह है कि इस प्रकार के सूत्रों में आयनों के आवेशों को नहीं दर्शाया जाता है।
यहाँ कुछ अधिक उदाहरण हैं
(a) ऐलुमिनियम ऑक्साइड का सूत्र:

अतः सूत्र : $Al_2 O_3$
(b) कैल्सियम ऑक्साइड का सूत्र:

यहाँ पर दोनों तत्वों की संयोजकताएँ समान हैं। अतः इसका सूत्र $\mathrm{Ca} _{2} \mathrm{O} _{2}$ प्राप्त होगा, किंतु हम इस सूत्र को $\mathrm{CaO}$ के रूप में सरलीकृत करते हैं।
(c) सोडियम नाइट्रेट का सूत्र:
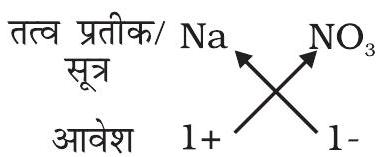
अतः सूत्र : $\mathrm{NaNO} _{3}$
(d) कैल्सियम हाइड्रॉक्साइड का सूत्र:
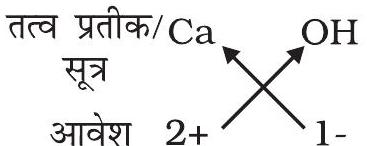
अतः सूत्र : $\mathrm{Ca}(\mathrm{OH}) _{2}$
ध्यान देने योग्य बात यह है कि कैल्सियम हाइड्रॉक्साइड का सूत्र $\mathrm{Ca}(\mathrm{OH}) _{2}$ है न कि $\mathrm{CaOH} _{2}$ । जब सूत्र में एक ही आयन के दो या दो से अधिक आयन होते हैं तो हम उनके लिए कोष्ठक का उपयोग करते हैं। यहाँ पर $\mathrm{OH}$ को कोष्ठक में रखकर पादांक 2 लगाते हैं जो यह निर्दिष्ट करता है कि एक कैल्सियम परमाणु के साथ दो हाइड्रोक्सील समूह जुड़े हैं। दूसरे शब्दों में, कैल्सियम हाइड्रॉक्साइड में ऑक्सीजन एवं हाइड्रोजन प्रत्येक के दो-दो परमाणु हैं।
(e) सोडियम कार्बोनेट का सूत्र:
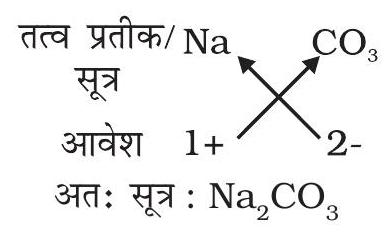
उपरोक्त उदाहरण में कोष्ठक के उपयोग की आवश्यकता नहीं है क्योंकि बहुपरमाणुक आयन कार्बोनेट का एक ही आयन विद्यमान है।
(f) अमोनियम सल्फेट का सूत्र:

अतः सूत्र : $(NH_4)_2 SO_4$
प्रशन
1. निम्न के सूत्र लिखिए:
(i) सोडियम ऑक्साइड
(ii) ऐलुमिनियम क्लोराइड
(iii) सोडियम सल्फाइड
(iv) मैग्नीशियम हाइड्रॉक्साइड
Show Answer
missing2. निम्नलिखित सूत्रों द्वारा प्रदर्शित यौगिकों के नाम लिखिए :
(i) $\mathrm{Al} _{2}\left(\mathrm{SO} _{4}\right) _{3}$
(ii) $\mathrm{CaCl} _{2}$
(iii) $\mathrm{K} _{2} \mathrm{SO} _{4}$
(iv) $\mathrm{KNO} _{3}$
(v) $\mathrm{CaCO} _{3}$
Show Answer
missing3. रासायनिक सूत्र का क्या तात्पर्य है?
Show Answer
missing4. निम्न में कितने परमाणु विद्यमान हैं?
(i) $\mathrm{H} _{2} \mathrm{~S}$ अणु एवं
(ii) $\mathrm{PO} _{4}^{3-}$ आयन?
Show Answer
missing3.5 आण्विक द्रव्यमान
3.5.1 आण्विक द्रव्यमान
अनुभाग 3.2.2 में हम परमाणु द्रव्यमान की अवधारणा की विवेचना कर चुके हैं। इस अवधारणा का विस्तार आण्विक द्रव्यमानों का परिकलन करने के लिए किया जा सकता है। किसी पदार्थ का आण्विक द्रव्यमान उसके सभी संघटक परमाणुओं के द्रव्यमानों का योग होता है। इस प्रकार यह अणु का वह सापेक्ष द्रव्यमान है जिसे परमाणु द्रव्यमान इकाई $(\mathrm{u})$ द्वारा व्यक्त किया जाता है।
उदाहरण 3.1 (a) जल $\left(\mathrm{H} _{2} \mathrm{O}\right)$ के सापेक्ष आण्विक द्रव्यमान का परिकलन कीजिए।
(b) नाइट्रिक अम्ल $\left(\mathrm{HNO} _{3}\right)$ के आण्विक द्रव्यमान का परिकलन कीजिए।
हल :
(a) हाइड्रोजन का परमाणु द्रव्यमान $=1 \mathrm{u}$ तथा ऑक्सीजन का परमाणु द्रव्यमान $=16 \mathrm{u}$ है।
अतः जल, जिसमें दो परमाणु हाइड्रोजन एवं एक परमाणु ऑक्सीजन होते हैं, का आण्विक द्रव्यमान $=2 \times 1+1 \times 16=18 \mathrm{u} \text { होगा। }$
(b) नाइट्रिक अम्ल $\left(\mathrm{HNO} _{3}\right)$ के आण्विक द्रव्यमान $=\mathrm{H}$ का परमाणु द्रव्यमान $+\mathrm{N}$ का परमाणु द्रव्यमान $+3 \times \mathrm{O}$ का परमाणु द्रव्यमान हाइड्रोजन का परमाणु द्रव्यमान $=1 \mathrm{u}$ ऑक्सीजन का परमाणु द्रव्यमान $=16 \mathrm{u}$ तथा नाइट्रोजन का परमाणु द्रव्यमान $=14 \mathrm{u}$ होता है। अतः $\mathrm{HNO} _{3}$ का आण्विक द्रव्यमान
$$ =1 \mathrm{u}+14 \mathrm{u}+3 \times 16 \mathrm{u}=63 \mathrm{u} \text { है। } $$
3.5.2 सूत्र इकाई द्रव्यमान
किसी पदार्थ का सूत्र इकाई द्रव्यमान उसके सभी संघटक परमाणुओं के परमाणु द्रव्यमानों का योग होता है। सूत्र द्रव्यमान का परिकलन उसी प्रकार से करते हैं जिस प्रकार से हमने आण्विक द्रव्यमान का परिकलन किया है। अंतर केवल इतना होता है कि यहाँ पर हम उस पदार्थ के लिए सूत्र इकाई का उपयोग करते हैं, जिसके संघटक आयन होते हैं। उदाहरणार्थः सोडियम क्लोराइड (इकाई सूत्र $\mathrm{NaCl}$ )। इसके इकाई सूत्र द्रव्यमान का परिकलन निम्न प्रकार से करते हैं:
$1 \times 23 \mathrm{u}+1 \times 35.5 \mathrm{u}=58.5 \mathrm{u}$
उदाहरण 3.2 $ \mathrm{CaCl} _{2}$ के सूत्र इकाई द्रव्यमान का परिकलन कीजिए
हल:
कैल्सियम क्लोराइड का सूत्र इकाई द्रव्यमान $\mathrm{CaCl} _{2}$ है। कैल्सियम (Ca) का परमाणु द्रव्यमान $=40 \mathrm{u}$ क्लोरीन (Cl) का परमाणु द्रव्यमान $=35.5 \mathrm{u}$ अत: $\mathrm{CaCl} _{2}$ का सूत्र इकाई द्रव्यमान
$=1 \times 40 \mathrm{u}+2 \times 35.5 \mathrm{u}=40 \mathrm{u}+71 \mathrm{u}$ $=111 \mathrm{u}$
प्रशन
1. निम्न यौगिकों के आण्विक द्रव्यमान का परिकलन कीजिए: $\mathrm{H} _{2}, \mathrm{O} _{2}, \mathrm{Cl} _{2}, \mathrm{CO} _{2}, \mathrm{CH} _{4}, \mathrm{C} _{2} \mathrm{H} _{6}, \mathrm{C} _{2} \mathrm{H} _{4}, \mathrm{NH} _{3}$ एवं $\mathrm{CH} _{3} \mathrm{OH}$
Show Answer
missing2. निम्न यौगिकों के सूत्र इकाई द्रव्यमान का परिकलन कीजिए: $\mathrm{ZnO}, \mathrm{Na} _{2} \mathrm{O}$ एवं $\mathrm{K} _{2} \mathrm{CO} _{3}$ दिया गया है: $\mathrm{Zn}$ का परमाणु द्रव्यमान $=65 \mathrm{u}$ $\mathrm{Na}$ का परमाणु द्रव्यमान $=23 \mathrm{u}$ $K$ का परमाणु द्रव्यमान $=39 \mathrm{u}$, $C$ का परमाणु द्रव्यमान $=12 \mathrm{u}$ एवं $O$ का परमाणु द्रव्यमान $=16 \mathrm{u}$ है।
Show Answer
missingआपने क्या सीखा

किसी भी अभिक्रिया में, अभिकारकों और उत्पादों के द्रव्यमानों का योग अपरिवर्तनीय होता है। यह द्रव्यमान के संरक्षण का नियम कहलाता है।
एक शुद्ध रासायनिक यौगिक में तत्व हमेशा द्रव्यमानों के निश्चित अनुपात में विद्यमान होते हैं, इसे निश्चित अनुपात का नियम कहते हैं।
तत्व का सूक्ष्मतम कण परमाणु होता है, जो स्वतंत्र रूप से प्रायः नहीं रह सकता है तथा उसके सभी रासायनिक गुणधर्मों को प्रदर्शित करता है।
अणु, किसी तत्व अथवा यौगिक का वह सूक्ष्मतम कण होता है जो सामान्य दशाओं में स्वतंत्र रह सकता है। यह पदार्थ के सभी गुणधर्मों को प्रदर्शित करता है।
किसी यौगिक का रासायनिक सूत्र उसके सभी संघटक तत्वों तथा संयोग करने वाले सभी तत्वों के परमाणुओं की संख्या को दर्शाता है।
परमाणुओं का वह पुंज जो आयन की तरह व्यवहार करता है, उसे बहुपरमाणुक आयन कहते हैं। उनके ऊपर एक निश्चित आवेश होता है।
आण्विक यौगिकों के रासायनिक सूत्र प्रत्येक तत्व की संयोजकता द्वारा निर्धारित होते हैं।
आयनिक यौगिकों में, प्रत्येक आयन के ऊपर आवेशों की संख्या द्वारा यौगिक के रासायनिक सूत्र ज्ञात करते हैं।
अभ्यास

1. $0.24 \mathrm{~g}$ ऑक्सीजन एवं बोरॉन युक्त यौगिक के नमूने में विश्लेषण द्वारा यह पाया गया कि उसमें $0.096 \mathrm{~g}$ बोरॉन एवं $0.144 \mathrm{~g}$ ऑक्सीजन है। उस यौगिक के प्रतिशत संघटन का भारात्मक रूप में परिकलन कीजिए।
Show Answer
missing2. $3.0 \mathrm{~g}$ कार्बन $8.00 \mathrm{~g}$ ऑक्सीजन में जलकर $11.00 \mathrm{~g}$ कार्बन डाइऑक्साइड निर्मित करता है। जब $3.00 \mathrm{~g}$ कार्बन को $50.00 \mathrm{~g}$ ऑक्सीजन में जलाएँगे तो कितने ग्राम कार्बन डाइऑक्साइड का निर्माण होगा? आपका उत्तर रासायनिक संयोजन के किस नियम पर आधारित होगा?
Show Answer
missing3. बहुपरमाणुक आयन क्या होते हैं? उदाहरण दीजिए।
Show Answer
missing4. निम्नलिखित के रासायनिक सूत्र लिखिए :
(a) मैग्नीशियम क्लोराइड
(b) कैल्सियम क्लोराइड
(c) कॉपर नाइट्रेट
(d) ऐलुमिनियम क्लोराइड
(e) कैल्सियम कार्बोनेट
Show Answer
missing5. निम्नलिखित यौगिकों में विद्यमान तत्वों का नाम दीजिए:
(a) बुझा हुआ चूना
(b) हाइड्रोजन ब्रोमाइड
(c) बेकिंग पाउडर (खाने वाला सोडा)
(d) पोटैशियम सल्फेट
Show Answer
missing6. निम्नलिखित पदार्थों के मोलर द्रव्यमान का परिकलन कीजिए:
(a) एथाइन, $\mathrm{C} _{2} \mathrm{H} _{2}$
(b) सल्फर अणु, $\mathrm{S} _{8}$
(c) फॉस्फोरस अणु, $\mathrm{P} _{4}$ (फॉस्फोरस का परमाणु द्रव्यमान = 31)
(d) हाइड्रोक्लोरिक अम्ल, $\mathrm{HCl}$
(e) नाइट्रिक अम्ल, $\mathrm{HNO} _{3}$
Show Answer
missingसमूह क्रियाकलाप

सूत्र लिखने के लिए एक खेल खेलिए
उदाहरण 1 : तत्वों के संकेतों एवं संयोजकताओं से युक्त अलग-अलग ताश के पत्ते बनाइए। प्रत्येक विद्यार्थी दो ताश के पत्तों को जिसमें से एक संकेत युक्त ताश के पत्ते को दाँए हाथ में तथा दूसरा संयोजकता युक्त ताश के पत्ते को बाँए हाथ में लीजिए। संकेतों को ध्यान में रखते हुए विद्यार्थी अपने ताश के पत्तों को अन्योन्य (crisscross) (तिर्यक) करके यौगिक का सूत्र बनाएँगे।
उदाहरण 2 : सूत्र लिखने का एक सस्ता मॉडलः दवाओं के उस पैक को जिसमें से गोलियाँ निकाल ली गई हों, लीजिए। जैसा कि चित्र में दिखाया गया है, तत्व की संयोजकता के अनुसार उसे समूह में काट लीजिए। अब आप एक प्रकार के आयन को दूसरे प्रकार के आयनों में लगाकर सूत्र बना सकते हैं।
उदाहरणार्थ :
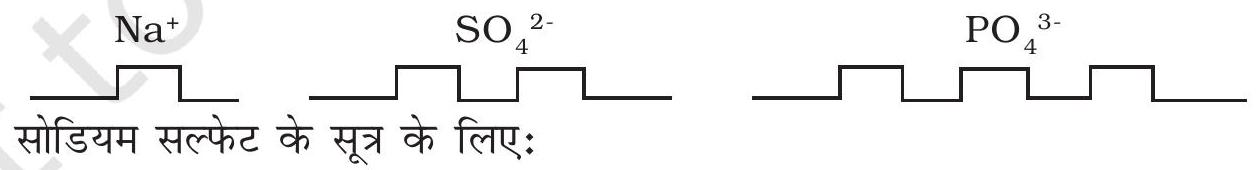
सोडियम सल्फेट का रासायनिक सूत्र है:
2 सोडियम आयनों को एक सल्फेट आयन पर लगाइए।
अतः सूत्र $\mathrm{Na} _{2} \mathrm{SO} _{4}$ होगा।
अपने आप कीजिए :
सोडियम फॉस्फेट का सूत्र लिखिए।





