इलेक्ट्रोकेमिस्ट्री एमडी
इकाई 3
विद्युतरसायन (Electrochemistry)
I. बहुविकल्पीय प्रश्न (प्रकार-I)
~~
- कॉपर इलेक्ट्रोड के मानक इलेक्ट्रोड विभव को कौन सा सेल मापेगा?
(i) $Pt$ (s) $\mid H_2$ (g,0.1 बार) $\mid H^{+}$(aq., $.1 M) | Cu^{2+}$ (aq., 1M) $\mid Cu$
(ii) $Pt$ (s) $\mid H_2$ (g, 1 बार) $\mid H^{+}$(aq., $1 M$ ) $| Cu^{2+}$ (aq., $2 M$ ) $\mid Cu$
(iii) $Pt$ (s) $\mid H_2$ (g, 1 बार) $\mid H^{+}$(aq., $1 M$ ) $| Cu^{2+}$ (aq., $1 M$ ) $\mid Cu$
(iv) $Pt(s) \mid H_2$ (g, 1 बार) $\mid H^{+}$(aq.,0.1 M) $| Cu^{2+}$ (aq., $.1 M) \mid Cu$
~~ 2. $Mg$ इलेक्ट्रोड का इलेक्ट्रोड विभव नर्न्स्ट समीकरण के अनुसार बदलता है
$E_{Mg^{2+} \mid Mg}=E_{Mg^{2+} \mid Mg}^{\ominus}-\frac{0.059}{2} \log \frac{1}{[Mg^{2+}]}$. $E_{Mg^{2+} \mid Mg}$ और $\log [Mg^{2+}]$ के ग्राफ़ का निर्माण है
(i)
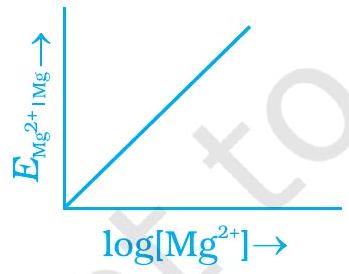
(iii)
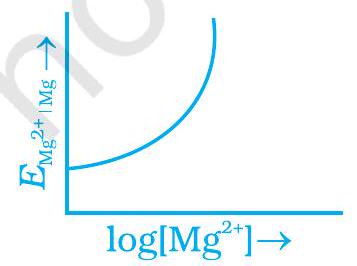
(ii)
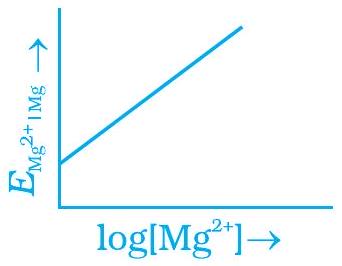
(iv)
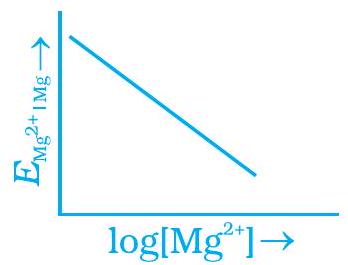
~~ 3. निम्नलिखित में से कौनसा कथन सही है?
(i) $E_{\text {सेल }}$ और $\Delta_{r} G$ सेल प्रतिक्रिया दोनों व्यापक गुण हैं।
(ii) $E_{\text {सेल }}$ और $\Delta_{r} G$ सेल प्रतिक्रिया दोनों सघन गुण हैं।
(iii) $\quad E_{\text {सेल }}$ एक सघन गुण है, जबकि $\Delta_{r} G$ सेल प्रतिक्रिया व्यापक गुण है।
(iv) $E_{\text {सेल }}$ एक व्यापक गुण है जबकि $\Delta_{r} G$ सेल प्रतिक्रिया एक सघन गुण है।
~~ 4. जब सेल से कोई विद्युत धारा नहीं ली जाती है तब दो इलेक्ट्रोडों के विभव के बीच के अंतर को कहते हैं
(i) सेल विभव
(ii) सेल विद्युत वाहक बल (EMF)
(iii) विभवांतर
(iv) सेल वोल्टेज
~~ 5. निम्नलिखित में से निष्क्रिय इलेक्ट्रोड के बारे में कौन सा कथन गलत है?
(i) यह सेल अभिक्रिया में भाग नहीं लेता है।
(ii) यह ऑक्सीकरण या अपचयन अभिक्रिया के लिए सतह प्रदान करता है।
(iii) यह इलेक्ट्रॉनों के स्थानांतरण के लिए सतह प्रदान करता है।
(iv) यह रेडॉक्स अभिक्रिया के लिए सतह प्रदान करता है।
~~ 6. गैल्वेनिक सेल, विद्युत अपघटनी सेल की तरह व्यवहार कर सकता है जब
(i) $E_{\text {सेल }}=0$
(ii) $E_{\text {सेल }} > E_{\text {बाह्य }}$
(iii) $E_{\text {बाह्य }} > E_{\text {सेल }}$
(iv) $E_{\text {सेल }}=E_{\text {बाह्य }}$
~~
नोट: यह प्रश्न NCERT Exemplar में विद्युतरसायन अध्याय के अंतर्गत दिया गया है, परन्तु इसकी विषय-वस्तु विलयन/रासायनिक बलगतिकी (Solutions/Chemical Kinetics) से संबंधित है। JEE विद्युतरसायन पाठ्यक्रम का भाग नहीं है।
- निम्नलिखित कथनों में से विलेय पदार्थों के विलयन की दर के बारे में कौन सा कथन सही नहीं है?
(i) विलयन की दर विलेय कणों के आकार पर निर्भर करती है।
(ii) विलयन की दर विलायक की प्रकृति पर निर्भर करती है।
(iii) विलयन की दर विलेय के सॉल्वेशन पर निर्भर नहीं होती है।
(iv) विलयन की दर तापमान के बढ़ने के साथ बढ़ती है।
~~ 8. नीचे दिए गए आँकड़ों का उपयोग करके सबसे प्रबल अपचायक (reducing agent) ज्ञात कीजिए।
$$E_{Cr_2 O_7^{2-} / Cr^{3+}}^{\ominus}=1.33 \text{ V}, \quad E_{Cl_2 / Cl^{-}}^{\ominus}=1.36 \text{ V}$$
$$E_{MnO_4^{-} / Mn^{2+}}^{\ominus}=1.51 \text{ V}, \quad E_{Cr^{3+} / Cr}^{\ominus}=-0.74 \text{ V}$$
(i) $Cl^{-}$
(ii) $Cr$
(iii) $Cr^{3+}$
(iv) $Mn^{2+}$
~~ 9. प्रश्न 8 में दिए गए आँकड़ों का उपयोग करें। निम्नलिखित में से सबसे प्रबल ऑक्सीकारक (oxidising agent) कौन सा है?
(i) $Cl^{-}$
(ii) $Mn^{2+}$
(iii) $MnO_4^{-}$
(iv) $Cr^{3+}$
~~ 10. प्रश्न 8 में दिए गए आँकड़ों का उपयोग करें। अपचयन क्षमता का निम्नलिखित में से कौन सा क्रम सही है?
(i) $Cr^{3+}<Cl^{-}<Mn^{2+}<Cr$
(ii) $Mn^{2+}<Cl^{-}<Cr^{3+}<Cr$
(iii) $Cr^{3+}<Cl^{-}<Cr_2 O_7^{2-}<MnO_4^{-}$
(iv) $Mn^{2+}<Cr^{3+}<Cl^{-}<Cr$
~~ 11. प्रश्न 8 में दिए गए आँकड़ों का उपयोग करके सबसे स्थिर ऑक्सीकृत स्पीशीज़ ज्ञात कीजिए।
(i) $Cl^{-}$
(ii) $Cr^{3+}$
(iii) $Cr$
(iv) $Mn^{2+}$
~~ 12. प्रश्न 8 में दिए गए आँकड़ों का उपयोग करके सबसे प्रबल ऑक्सीकारक ज्ञात कीजिए।
(i) $Cr^{3+}$
(ii) $MnO_4^{-}$
(iii) $Cr_2 O_7^{2-}$
(iv) $Mn^{2+}$
~~ 13. $Al_2 O_3$ से एक मोल एल्युमिनियम प्राप्त करने के लिए आवश्यक विद्युत की मात्रा है
(i) $1 F$
(ii) $6 F$
(iii) $3 F$
(iv) $2 F$
~~ 14. चालकता सेल का सेल स्थिरांक (cell constant)
(i) विद्युत अपघट्य बदलने पर बदलता है।
(ii) विद्युत अपघट्य की सांद्रता बदलने पर बदलता है।
(iii) विद्युत अपघट्य के तापमान बदलने पर बदलता है।
(iv) किसी दिए गए सेल के लिए स्थिर रहता है।
~~ 15. लेड संचायक बैटरी को चार्ज करते समय
(i) कैथोड पर $PbSO_4$ का अपचयन होकर $Pb$ बनता है।
(ii) एनोड पर $PbSO_4$ का अपचयन होकर $Pb$ बनता है।
(iii) कैथोड पर $PbSO_4$ का ऑक्सीकरण होकर $PbO_2$ बनता है।
(iv) एनोड पर $PbSO_4$ का ऑक्सीकरण होकर $PbO_2$ बनता है।
~~ 16. $\Lambda_{m(NH_4OH)}^{0}$ बराबर है
(i) $\quad \Lambda_{m(NH_4OH)}^{0} + \Lambda_{m(NH_4Cl)}^{0} - \Lambda_{m(HCl)}^{0}$
(ii) $\quad \Lambda_{m(NH_4Cl)}^{0} + \Lambda_{m(NaOH)}^{0} - \Lambda_{m(NaCl)}^{0}$
(iii) $\quad \Lambda_{m(NH_4Cl)}^{0} + \Lambda_{m(NaCl)}^{0} - \Lambda_{m(NaOH)}^{0}$
(iv) $\quad \Lambda_{m(NaOH)}^{0} + \Lambda_{m(NaCl)}^{0} - \Lambda_{m(NH_4Cl)}^{0}$
~~ 17. सोडियम क्लोराइड के जलीय विलयन के विद्युत अपघटन में, एनोड पर कौन सी अभिक्रिया होगी?
(i) $\quad Na^{+}(aq)+e^{-} \longrightarrow Na(s) ; \quad E_{\text {Cell }}^{\ominus}=-2.71 V$
(ii) $\quad 2 H_2 O(l) \longrightarrow O_2(g)+4 H^{+}(aq)+4 e^{-} ; E_{\text {Cell }}^{\ominus}=1.23 V$
(iii) $H^{+}(aq)+e^{-} \longrightarrow \frac{1}{2} H_2(g) ; \quad E_{\text {Cell }}^{\ominus}=0.00 V$
(iv) $\quad Cl^{-}(aq) \longrightarrow \frac{1}{2} Cl_2(g)+e^{-} ; \quad E_{\text {Cell }}^{\ominus}=1.36 V$
II. बहुविकल्पीय प्रश्न (प्रकार-II)
नोट: इसके बाद के प्रश्नों में दो या दो से अधिक विकल्प सही हो सकते हैं।
~~ 18. $Cu^{2+}/Cu$ के मानक इलेक्ट्रोड विभव का धनात्मक मान दर्शाता है कि
(i) यह रेडॉक्स युग्म, $H^{+}/H_2$ युग्म की तुलना में अधिक आसानी से अपचयित होता है।
(ii) यह रेडॉक्स युग्म, $H^{+}/H_2$ युग्म की तुलना में अधिक आसानी से ऑक्सीकृत होता है।
(iii) $Cu$ अम्ल से $H_2$ विस्थापित नहीं कर सकता।
(iv) $Cu$ अम्ल से $H_2$ विस्थापित कर सकता है।
~~
- कुछ अर्ध-अभिक्रियाओं के $E^{\ominus}$ मान नीचे दिए गए हैं। इनके आधार पर सही उत्तर चुनिए।
(a) $H^{+}(aq)+e^{-} \longrightarrow \frac{1}{2} H_2(g) ; \quad E^{\ominus}=0.00 \text{ V}$
(b) $2 H_2 O(l) \longrightarrow O_2(g)+4 H^{+}(aq)+4 e^{-} ; \quad E^{\ominus}=1.23 \text{ V}$
(c) $2 SO_4^{2-}(aq) \longrightarrow S_2 O_8^{2-}(aq)+2 e^{-} ; \quad E^{\ominus}=1.96 \text{ V}$
(i) तनु सल्फ्यूरिक अम्ल के विद्युत अपघटन में, कैथोड पर हाइड्रोजन अपचयित होगी।
(ii) सांद्र सल्फ्यूरिक अम्ल के विद्युत अपघटन में, एनोड पर जल ऑक्सीकृत होगा।
(iii) तनु सल्फ्यूरिक अम्ल के विद्युत अपघटन में, एनोड पर जल ऑक्सीकृत होगा।
(iv) तनु सल्फ्यूरिक अम्ल के विद्युत अपघटन में, एनोड पर $SO_4^{2-}$ आयन $S_2 O_8^{2-}$ में ऑक्सीकृत होगा।
- डेनियल सेल के लिए $E_{\text{सेल}}^{\ominus}=1.1 \text{ V}$। साम्यावस्था पर इस सेल का सही विवरण कौन सा है?
(i) $1.1=K_{c}$
(ii) $\frac{2.303 R T}{2 F} \log K_{c}=1.1$
(iii) $\log K_{c}=\frac{2.2}{0.059}$
(iv) $\log K_{c}=1.1$
- विद्युत अपघट्य विलयन की चालकता निम्नलिखित पर निर्भर करती है
(i) विद्युत अपघट्य की प्रकृति।
(ii) विलयन की सांद्रता।
(iii) आरोपित विभवांतर की शक्ति।
(iv) इलेक्ट्रोडों के बीच की दूरी।
- $\Lambda_m^{0}(H_2O)$ बराबर है
(i) $\quad \Lambda_{m(HCl)}^{0} + \Lambda_{m(NaOH)}^{0} - \Lambda_{m(NaCl)}^{0}$
(ii) $\quad \Lambda_{m(HNO_3)}^{0} + \Lambda_{m(NaNO_3)}^{0} - \Lambda_{m(NaOH)}^{0}$
(iii) $\quad \Lambda_{m(HNO_3)}^{0} + \Lambda_{m(NaOH)}^{0} - \Lambda_{m(NaNO_3)}^{0}$
(iv) $\quad \Lambda_{m(NH_4OH)}^{0} + \Lambda_{m(HCl)}^{0} - \Lambda_{m(NH_4Cl)}^{0}$
- प्लैटिनम इलेक्ट्रोडों का उपयोग करके $CuSO_4$ के जलीय विलयन के विद्युत अपघटन में क्या होगा?
(i) कैथोड पर कॉपर जमा होगा।
(ii) एनोड पर कॉपर जमा होगा।
(iii) एनोड पर ऑक्सीजन मुक्त होगी।
(iv) एनोड पर कॉपर विलीन होगा।
- $Cu$ इलेक्ट्रोडों का उपयोग करके $CuSO_4$ के जलीय विलयन के विद्युत अपघटन में क्या होगा?
(i) कैथोड पर कॉपर जमा होगा।
(ii) एनोड पर कॉपर विलीन होगा।
(iii) एनोड पर ऑक्सीजन मुक्त होगी।
(iv) एनोड पर कॉपर जमा होगा।
- विशिष्ट चालकता $\kappa$ बराबर है
(i) $\frac{1}{R} \cdot \frac{l}{A}$
(ii) $\frac{G^{*}}{R}$
(iii) $\Lambda_{m}$
(iv) $\frac{l}{A}$
- आयनिक विलयन की मोलर चालकता निर्भर करती है
(i) तापमान पर।
(ii) इलेक्ट्रोडों के बीच की दूरी पर।
(iii) विलयन की सांद्रता पर।
(iv) इलेक्ट्रोडों के पृष्ठ क्षेत्रफल पर।
- दिए गए सेल में, $Mg \mid Mg^{2+} | Cu^{2+} \mid Cu$
(i) $Mg$ कैथोड है
(ii) $Cu$ कैथोड है
(iii) सेल अभिक्रिया $Mg + Cu^{2+} \longrightarrow Mg^{2+} + Cu$ है
(iv) $Cu$ ऑक्सीकारक है
III. लघु उत्तरीय प्रश्न
- क्या किसी एकल इलेक्ट्रोड के निरपेक्ष इलेक्ट्रोड विभव को मापा जा सकता है?
- क्या $E_{\text{सेल}}^{\ominus}$ या $\Delta_{r} G^{\ominus}$ किसी सेल अभिक्रिया के लिए शून्य हो सकते हैं?
$E_{\text{सेल}} = 0$ या $\Delta_{r} G = 0$ होने की शर्त क्या है?
$E^{\ominus}$ के ऋणात्मक मान का क्या अर्थ होता है?
~~ 32. अलग-अलग विद्युत अपघटनी सेलों में 1 एम्पियर धारा 10 मिनट तक प्रवाहित करके जलीय कॉपर सल्फेट विलयन और जलीय सिल्वर नाइट्रेट विलयन का विद्युत अपघटन किया जाता है। क्या कैथोड पर कॉपर और सिल्वर का समान भार निक्षेपित होगा? अपने उत्तर की व्याख्या कीजिए।
~~ 33. उस सेल का सेल आरेख (cell notation) लिखिए जिसकी सेल अभिक्रिया $Cu + 2Ag^{+} \longrightarrow 2Ag + Cu^{2+}$ है।
~~ 34. $Cl^{-}$ आयनों के ऑक्सीकरण का मानक इलेक्ट्रोड विभव, जल के ऑक्सीकरण के मानक इलेक्ट्रोड विभव से अधिक धनात्मक है। फिर भी जलीय सोडियम क्लोराइड के विद्युत अपघटन में एनोड पर जल के स्थान पर $Cl^{-}$ का ऑक्सीकरण क्यों होता है?
~~ 35. इलेक्ट्रोड विभव (electrode potential) क्या है?
~~ 36. निम्नलिखित चित्र में एक विद्युतरसायनिक सेल को विद्युत अपघटनी सेल के साथ जोड़ा गया है। विद्युत अपघटनी सेल के इलेक्ट्रोड ‘A’ और ‘B’ की ध्रुवता क्या होगी?
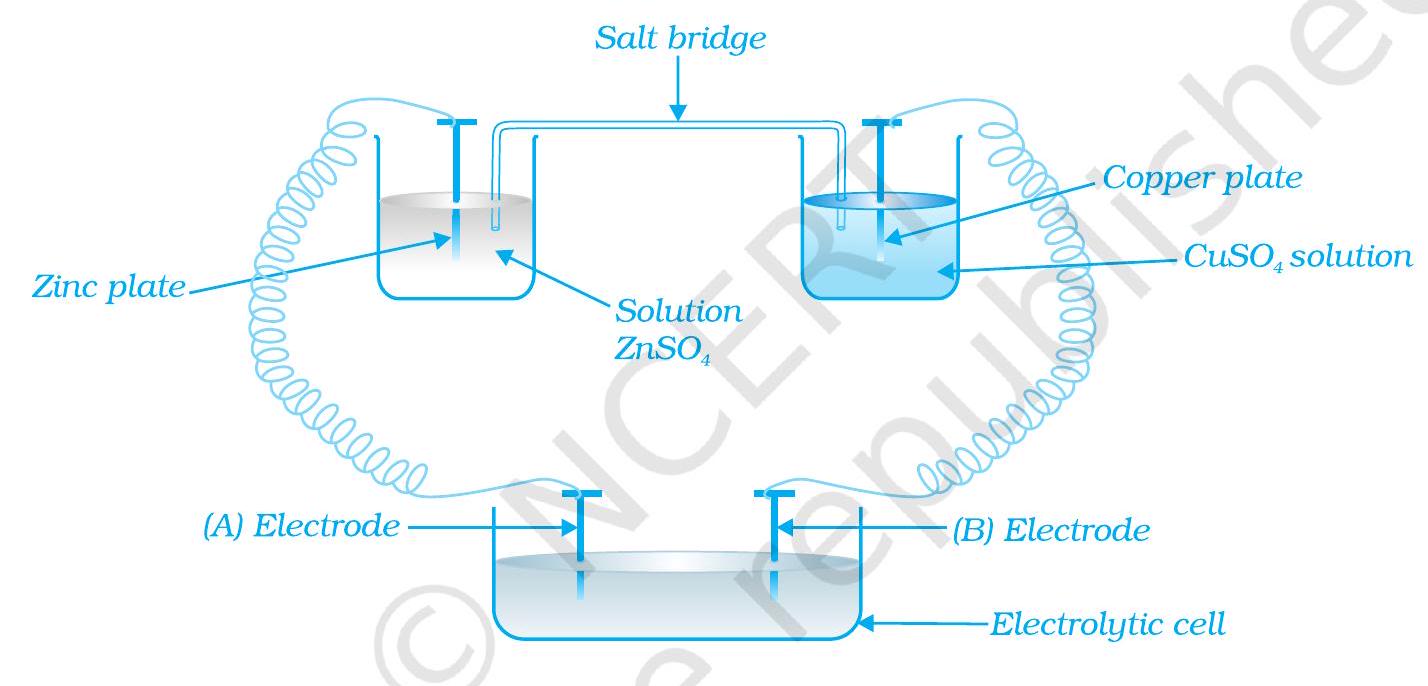
चित्र 3.1
~~ 37. आयनिक विलयन का प्रतिरोध मापने के लिए प्रत्यावर्ती धारा (AC) का उपयोग क्यों किया जाता है, दिष्ट धारा (DC) का नहीं?
~~ 38. एक गैल्वेनिक सेल का विद्युत वाहक बल (EMF) $1.1 \text{ V}$ है। यदि इस सेल पर $1.1 \text{ V}$ का विपरीत बाह्य विभव लगाया जाए, तो सेल अभिक्रिया और सेल में बहने वाली धारा पर क्या प्रभाव पड़ेगा?
~~ 39. जलीय $NaCl$ विलयन (ब्राइन) का विद्युत अपघटन करने पर कैथोड पर कौन से उत्पाद बनेंगे और विलयन का $pH$ कैसे प्रभावित होगा?
~~ 40. शुष्क सेल (dry cell) के विपरीत, मर्करी सेल अपने उपयोगी जीवनकाल में स्थिर विभव देता है। क्यों?
~~ 41. दो विद्युत अपघट्य ‘A’ और ‘B’ को तनु किया गया। तनुकरण पर ‘B’ का $\Lambda_m$ $1.5$ गुना बढ़ता है जबकि ‘A’ का $\Lambda_m$ $25$ गुना बढ़ता है। दोनों में से कौन सा प्रबल विद्युत अपघट्य है? अपने उत्तर की व्याख्या कीजिए।
~~ 42. जब अम्लीकृत जल (तनु $H_2SO_4$ विलयन) का विद्युत अपघटन किया जाता है, तो क्या विलयन का $pH$ प्रभावित होगा? अपने उत्तर की व्याख्या कीजिए।
~~ 43. जलीय विलयन में विद्युत अपघट्यों की विशिष्ट चालकता ($\kappa$) जल मिलाने पर कैसे बदलेगी?
~~ 44. अन्य इलेक्ट्रोडों का इलेक्ट्रोड विभव मापने के लिए किस संदर्भ इलेक्ट्रोड (reference electrode) का उपयोग किया जाता है?
~~ 45. निम्नलिखित सेल पर विचार कीजिए:
$Cu \mid Cu^{2+} | Cl^{-} \mid Cl_2, Pt$
एनोड और कैथोड पर होने वाली अभिक्रियाएँ लिखिए।
~~ 46. डेनियल सेल की सेल अभिक्रिया के लिए नर्न्स्ट समीकरण लिखिए। जब $Zn^{2+}$ आयनों की सांद्रता बढ़ती है, तो $E_{\text{सेल}}$ कैसे प्रभावित होगा?
~~ 47. प्राथमिक और द्वितीयक बैटरियों की तुलना में ईंधन सेलों (fuel cells) के क्या लाभ हैं?
~~ 48. लेड संचायक बैटरी की सेल अभिक्रिया लिखिए। जब बैटरी डिस्चार्ज होती है तो विलयन का घनत्व कैसे बदलता है?
~~ 49. तनुकरण पर $CH_3COOH$ का $\Lambda_m$ तेजी से बढ़ता है, जबकि $CH_3COONa$ का $\Lambda_m$ धीरे-धीरे बढ़ता है। क्यों?
IV. सुमेलन प्रकार (Matching Type)
~~ 50. स्तंभ I और स्तंभ II के पदों का मिलान कीजिए।
स्तंभ I
(i) $\Lambda_m$
(ii) $E_{\text{सेल}}$
(iii) $\kappa$
(iv) $G^{*}$
स्तंभ II
(a) $S \text{ cm}^{-1}$
(b) $m^{-1}$
(c) $S \text{ cm}^2 \text{ mol}^{-1}$
(d) $V$
~~ 51. स्तंभ I और स्तंभ II के पदों का मिलान कीजिए।
स्तंभ I
(i) $\Lambda_m$
(ii) $E_{\text{सेल}}^{\ominus}$
(iii) $\kappa$
(iv) $\Delta_r G_{\text{सेल}}$
स्तंभ II
(a) व्यापक गुण (extensive property)
(b) आयनों की संख्या / आयतन पर निर्भर
(c) सघन गुण (intensive property)
(d) तनुकरण पर बढ़ता है
~~ 52. स्तंभ I और स्तंभ II के पदों का मिलान कीजिए।
स्तंभ I
(i) लीड स्टोरेज बैटरी
(ii) मरकुरी सेल
(iii) फ्यूल सेल
(iv) संक्षारण (जंग लगना)
स्तंभ II
(a) अधिकतम दक्षता
(b) गैल्वेनीकरण से रोका जाता है
(c) स्थिर विभव देता है
(d) $Pb$ एनोड है, $PbO_2$ कैथोड है
~~ 53. स्तंभ I और स्तंभ II के पदों का मिलान कीजिए।
स्तंभ I
(i) $\kappa$
(ii) $\Lambda_{m}$
(iii) $\alpha$
(iv) $Q$
स्तंभ II
(a) $I \times t$
(b) $\Lambda_{m} / \Lambda_m^{0}$
(c) $\frac{\kappa}{c}$
(d) $\frac{G^{*}}{R}$
~~ 54. स्तंभ I और स्तंभ II के पदों का मिलान कीजिए।
स्तंभ I
(i) लेचलांच सेल
(ii) निकेल-कैड्मियम सेल
(iii) फ्यूल सेल
(iv) मरकुरी सेल
स्तंभ II
(a) सेल क्रिया $2 H_2+O_2 \longrightarrow 2 H_2 O$
(b) विलयन में कोई आयन सम्मिलित नहीं होता; श्रवण यंत्र (hearing aid) में उपयोग होता है।
(c) पुनर्भरण (recharge) किया जा सकता है
(d) एनोड पर अभिक्रिया: $Zn \longrightarrow Zn^{2+} + 2e^{-}$
(e) ईंधन की रासायनिक ऊर्जा को विद्युत ऊर्जा में परिवर्तित करता है
~~ 55. नीचे दिए गए आँकड़ों के आधार पर स्तंभ I और स्तंभ II का मिलान कीजिए:
$$E_{F_2/F^{-}}^{\ominus}=2.87 \text{ V}, \quad E_{Li^{+}/Li}^{\ominus}=-3.5 \text{ V}, \quad E_{Au^{3+}/Au}^{\ominus}=1.4 \text{ V}, \quad E_{Br_2/Br^{-}}^{\ominus}=1.09 \text{ V}$$
स्तंभ I
(i) $F_2$
(ii) $Li$
(iii) $Au^{3+}$
(iv) $Br^{-}$
(v) $Au$
(vi) $Li^{+}$
(vii) $F^{-}$
स्तंभ II
(a) सबसे प्रबल अपचायक धातु
(b) सबसे दुर्बल ऑक्सीकारक धातु आयन
(c) सबसे प्रबल ऑक्सीकारक अधातु
(d) उत्कृष्ट (noble) धातु
(e) $Au^{3+}$ द्वारा ऑक्सीकृत किया जा सकता है
(f) सबसे दुर्बल अपचायक अधातु आयन
(g) ऑक्सीकारक धातु आयन
V. अभिकथन और कारण प्रकार
नोट: निम्नलिखित प्रश्नों में एक अभिकथन (Assertion) के बाद एक कारण (Reason) दिया गया है। निम्नलिखित विकल्पों में से सही उत्तर चुनिए।
(i) कथन और कारण दोनों सत्य हैं और कारण कथन का सही स्पष्टीकरण है।
(ii) कथन और कारण दोनों सत्य हैं और कारण कथन का सही स्पष्टीकरण नहीं है।
(iii) कथन सत्य है, लेकिन कारण गलत है।
(iv) कथन और कारण दोनों गलत हैं।
(v) कथन गलत है, लेकिन कारण सत्य है।
~~ 56. अभिकथन : कॉपर हाइड्रोजन की तुलना में कम अभिक्रियाशील है।
कारण : $E_{Cu^{2+}/Cu}^{\ominus}$ ऋणात्मक है।
~~ 57. अभिकथन : सेल के स्वतः कार्य करने के लिए $E_{\text{सेल}}$ का मान धनात्मक होना चाहिए।
कारण : $E_{\text{कैथोड}} < E_{\text{एनोड}}$
~~ 58. अभिकथन : सभी विद्युत अपघट्यों की विशिष्ट चालकता ($\kappa$) तनुकरण पर घटती है।
कारण : तनुकरण पर प्रति इकाई आयतन में आयनों की संख्या कम हो जाती है।
~~
- अभिकथन : दुर्बल विद्युत अपघट्यों को तनु करने पर $\Lambda_m$ में तीव्र वृद्धि होती है।
कारण : दुर्बल विद्युत अपघट्यों में तनुकरण पर वियोजन की मात्रा बढ़ती है।
~~ 60. अभिकथन : मर्करी सेल अपने संपूर्ण जीवनकाल में स्थिर विभव देता है।
कारण : सेल अभिक्रिया में कोई आयन विलयन में सम्मिलित नहीं होता।
~~ 61. अभिकथन : $NaCl$ विलयन के विद्युत अपघटन में एनोड पर $O_2$ के स्थान पर $Cl_2$ मुक्त होती है।
कारण : एनोड पर ऑक्सीजन के निर्माण के लिए अतिविभव (overvoltage) की आवश्यकता होती है।
~~ 62. अभिकथन : आयनिक विलयन का विद्युत प्रतिरोध मापने के लिए AC स्रोत का उपयोग किया जाता है।
कारण : DC स्रोत का उपयोग करने पर विलयन की संघटना (composition) बदल जाएगी।
~~ 63. अभिकथन : $E_{\text{सेल}} = 0$ होने पर सेल में धारा प्रवाहित नहीं होती।
कारण : सेल अभिक्रिया साम्यावस्था में पहुँच जाती है।
~~ 64. अभिकथन : $Ag^{+}/Ag$ का $E_{Ag^{+}/Ag}$, $Ag^{+}$ आयनों की सांद्रता बढ़ने पर बढ़ता है।
कारण : $E_{Ag^{+}/Ag}^{\ominus}$ का मान धनात्मक है।
~~ 65. अभिकथन : कॉपर सल्फेट विलयन को तांबे के बर्तन में रखा जा सकता है।
कारण : कॉपर, $Cu^{2+}$ आयनों की तुलना में कम अभिक्रियाशील है।
VI. दीर्घ उत्तरीय प्रश्न
~~ 66. चित्र 3.2 को ध्यान से देखें और निम्नलिखित प्रश्नों का उत्तर दें।
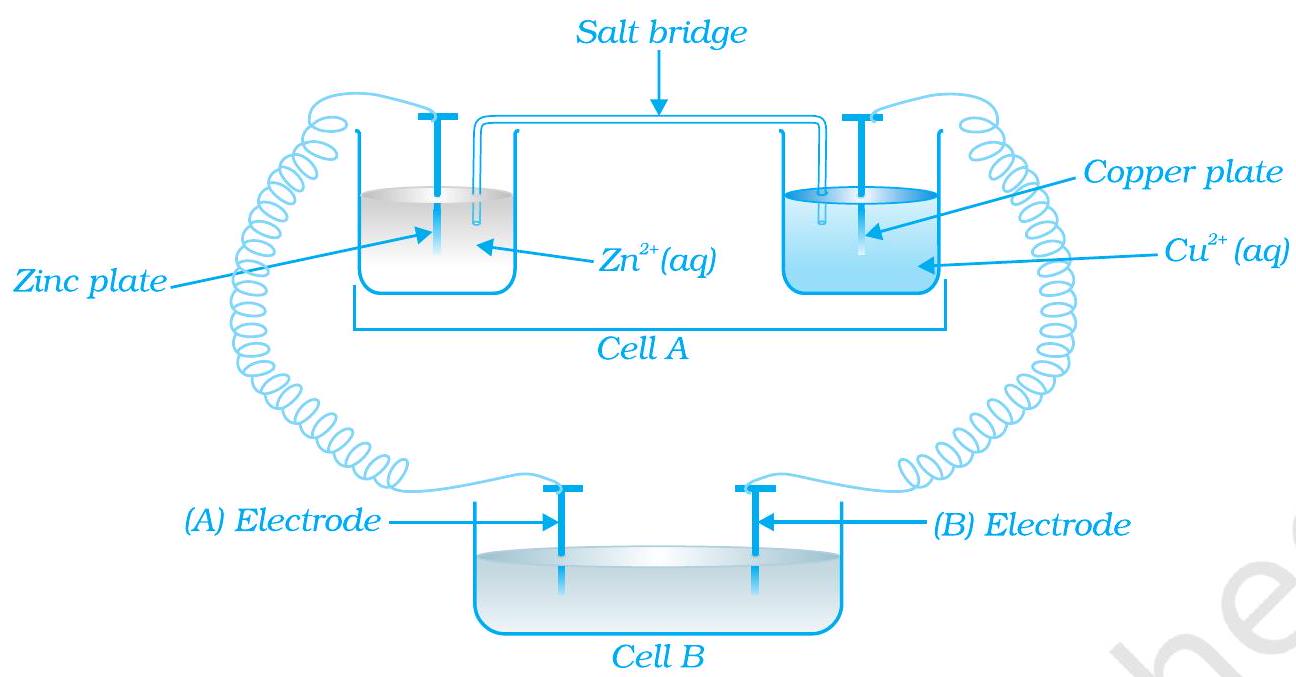
चित्र 3.2
(i) सेल ‘ए’ में $E_{\text {Cell }}=2 V$ है और सेल ‘B’ में $E_{\text {Cell }}=1.1 V$ है, इन दोनों सेलों में से कौन सेल ‘A’ या ‘B’ इलेक्ट्रोलिटिक सेल के रूप में कार्य करेगी। इस सेल में इलेक्ट्रोड अभिक्रियाएँ क्या होंगी?
(ii) अगर सेल ‘A’ में $E_{\text {Cell }}=0.5 V$ है और सेल ‘B’ में $E_{\text {Cell }}=1.1 V$ है तो एनोड और कैथोड पर कौन सी अभिक्रियाएँ होंगी?
~~ 67. चित्र 3.2 को ध्यान से देखें और निम्नलिखित प्रश्नों के उत्तर दें (i) से (vi) तक।
(i) इलेक्ट्रॉन प्रवाह के दिशा दिखाने के लिए चित्र फिर से बनाएँ।
(ii) क्या चांदी की प्लेट एनोड या कैथोड है?
(iii) यदि लवण सेतु (salt bridge) हटा दिया जाए तो क्या होगा?
(iv) सेल कब कार्य करना बंद कर देगी?
(v) सेल कार्य करने पर $Zn^{2+}$ आयनों और $Ag^{+}$ आयनों की घनता पर कैसा प्रभाव पड़ेगा?
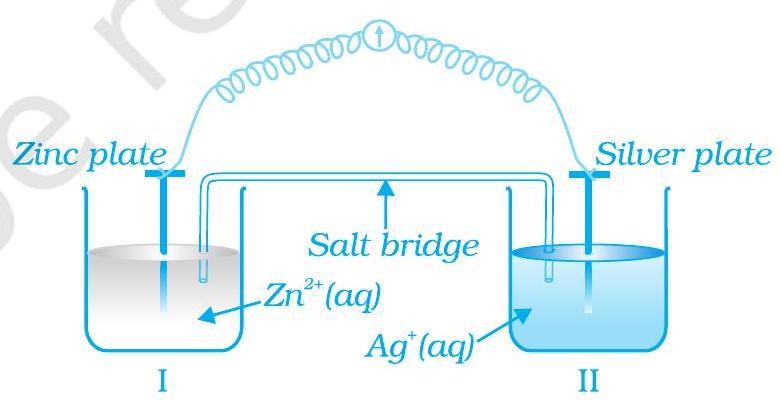
चित्र 3.3
(vi) सेल ‘मृत’ हो जाने के बाद $Zn^{2+}$ आयनों और $Ag^{+}$ आयनों की घनता पर कैसा प्रभाव पड़ेगा?
~~ 68. गैल्वेनिक सेल में सेल अभिक्रिया की गिब्स मुक्त ऊर्जा ($\Delta_r G$) और विद्युत वाहक बल ($E_{\text{सेल}}$) के बीच क्या संबंध है? गैल्वेनिक सेल से अधिकतम कार्य कब प्राप्त होगा?
उत्तर
I. बहुविकल्पीय प्रश्न (प्रकार-I)
~~
- (iii)
~~ 2. (ii)
~~ 3. (iii)
~~ 4. (ii)
~~ 5. (iv)
~~ 6. (iii)
~~ 7. (iii)
~~ 8. (ii)
~~ 9. (iii)
~~ 10. (ii)
~~ 11. (iv)
~~ 12. (i)
~~ 13. (iii)
~~ 14. (iv)
~~ 15. (i)
~~ 16. (ii)
~~ 17. (ii)
II. बहुविकल्पीय प्रश्न (प्रकार-II) ~~ 18. (ii), (iv)
~~ 19. (i), (iii)
~~ 20. (ii), (iii)
~~ 21. (i), (ii)
~~ 22. (i), (iv)
~~ 23. (i), (iii)
~~
- (i), (ii)
~~ 25. (i), (ii)
~~ 26. (i), (iii)
~~ 27. (ii), (iii)
III. लघु उत्तरीय प्रश्न
~~ 28. नहीं, किसी एकल इलेक्ट्रोड का निरपेक्ष विभव मापना संभव नहीं है।
~~ 29. नहीं, स्वतः अभिक्रिया के लिए $E_{\text{सेल}}^{\ominus}$ शून्य नहीं हो सकता।
~~ 30. जब सेल अभिक्रिया साम्यावस्था तक पहुँचती है।
~~ 31. $E^{\ominus}$ का ऋणात्मक मान दर्शाता है कि $Zn$, हाइड्रोजन से अधिक सक्रिय है। जब जस्ता इलेक्ट्रोड को SHE से जोड़ा जाएगा तो $Zn$ ऑक्सीकृत होगा और $H^{+}$ अपचयित होगा।
~~ 32. NCERT पाठ्यपुस्तक देखें, पृष्ठ संख्या 84।
~~ 33. $Cu \mid Cu^{2+} | Ag^{+} \mid Ag$
~~ 34. जलीय $NaCl$ के विद्युत अपघटन में एनोड पर $O_2$ के निर्माण के लिए उच्च अतिविभव (overvoltage) की आवश्यकता होती है, इसलिए $Cl^{-}$ जल के स्थान पर ऑक्सीकृत हो जाता है।
~~ 35. NCERT पाठ्यपुस्तक देखें, पृष्ठ संख्या 65।
~~ 36. ‘A’ की ध्रुवता ऋणात्मक होगी।
‘B’ की ध्रुवता धनात्मक होगी।
~~ 37. प्रत्यावर्ती धारा (AC) का उपयोग इसलिए किया जाता है ताकि विद्युत अपघटन न हो और विलयन की संघटना स्थिर रहे।
~~ 38. NCERT पाठ्यपुस्तक देखें, पृष्ठ संख्या 64।
~~ 39. कैथोड पर $H_2$ और $OH^{-}$ बनेंगे, $NaOH$ बनने से विलयन का $pH$ बढ़ जाएगा।
~~ 40. मर्करी सेल की कुल अभिक्रिया में विलयन में कोई आयन सम्मिलित नहीं होता, इसलिए विभव स्थिर रहता है।
~~ 41. ‘B’ प्रबल विद्युत अपघट्य है क्योंकि तनुकरण पर आयनों की संख्या वही रहती है, केवल अंतर-आयनिक आकर्षण कम होता है, इसलिए $\Lambda_m$ में वृद्धि अल्प होती है।
~~ 42. $[H^{+}]$ स्थिर रहने के कारण विलयन का $pH$ प्रभावित नहीं होगा।
एणोड पर : $2 H_2 O \longrightarrow O_2+4 H^{+}+4 e^{-}$
कैथोड पर $4 H^{+}+4 e^{-} \longrightarrow 2 H_2$
~~ 43. विशिष्ट चालकता ($\kappa$) कम होती है क्योंकि प्रति इकाई आयतन में आयनों की संख्या कम हो जाती है।
~~ 44. मानक हाइड्रोजन इलेक्ट्रोड (SHE) एक संदर्भ इलेक्ट्रोड है जिसका इलेक्ट्रोड विभव शून्य माना जाता है। अन्य इलेक्ट्रोडों का विभव इसकी तुलना में मापा जाता है।
~~ 45. एनोड: $Cu \longrightarrow Cu^{2+} + 2e^{-}$
कैथोड: $\quad Cl_2+2 e^{-} \longrightarrow 2 Cl^{-}$
$Cu$ एनोड है क्योंकि इसका ऑक्सीकरण हो रहा है।
$Cl_2$ कैथोड है क्योंकि इसका अपचयन हो रहा है।
~~ 46. $Zn + Cu^{2+} \longrightarrow Zn^{2+} + Cu$
$E_{\text{सेल}} = E_{\text{सेल}}^{\ominus} - \frac{0.059}{2} \log \frac{[Zn^{2+}]}{[Cu^{2+}]}$
$[Zn^{2+}]$ बढ़ने पर $E_{\text{सेल}}$ का मान घटेगा।
~~ 47. प्राथमिक बैटरियों में सीमित मात्रा में अभिकारक होते हैं और उपयोग के बाद समाप्त हो जाती हैं। द्वितीयक बैटरियों को पुनर्भरण किया जा सकता है, लेकिन चार्ज करने में समय लगता है। ईंधन सेल जब तक ईंधन और ऑक्सीकारक की आपूर्ति होती रहती है तब तक लगातार कार्य करता रहता है।
~~ 48. $Pb + PbO_2 + 2H_2SO_4 \longrightarrow 2PbSO_4 + 2H_2O$
डिस्चार्ज के दौरान $H_2SO_4$ की खपत होती है और $H_2O$ बनता है, जिससे विलयन का घनत्व कम होता है।
~~ 49. $CH_3COOH$ दुर्बल विद्युत अपघट्य है; तनुकरण पर वियोजन की मात्रा बढ़ने से आयनों की संख्या बढ़ती है, इसलिए $\Lambda_m$ तेजी से बढ़ता है।
$CH_3COOH + H_2O \rightarrow CH_3COO^{-} + H_3O^{+}$
$CH_3COONa$ प्रबल विद्युत अपघट्य है; आयनों की संख्या वही रहती है, केवल अंतर-आयनिक आकर्षण कम होता है, इसलिए $\Lambda_m$ धीरे-धीरे बढ़ता है।
IV. सुमेलन प्रकार
~~ 50. (i) $\rightarrow$ (c) (ii) $\rightarrow$ (d) (iii) $\rightarrow$ (a) (iv) $\rightarrow$ (b)
~~ 51. (i) $\rightarrow$ (d) (ii) $\rightarrow$ (a) (iii) $\rightarrow$ (b) (iv) $\rightarrow$ (c)
~~ 52. (i) $\rightarrow$ (d) (ii) $\rightarrow$ (c) (iii) $\rightarrow$ (a) (iv) $\rightarrow$ (b)
~~ 53. (i) $\rightarrow$ (d) (ii) $\rightarrow$ (c) (iii) $\rightarrow$ (b) (iv) $\rightarrow$ (a)
~~ 54. (i) $\rightarrow$ (d) (ii) $\rightarrow$ (c) (iii) $\rightarrow$ (a), (e) (iv) $\rightarrow$ (b)
~~ 55. (i) $\rightarrow$ (c) (ii) $\rightarrow$ (a) (iii) $\rightarrow$ (g) (iv) $\rightarrow$ (e) (v) $\rightarrow$ (d) (vi) $\rightarrow$ (b)
(vii) $\rightarrow$ (g) (f)
V. अभिकथन और कारण प्रकार
~~ 56. (iii)
~~ 57. (iii)
~~ 58. (i)
~~ 59. (i)
~~ 60. (i)
~~ 61. (i)
~~ 62. (i)
~~ 63. (i)
~~ 64. (ii)
~~ 65. (iv)
VI. दीर्घ उत्तरीय प्रश्न (उत्तर)
~~ 66. (i) सेल ‘B’ विद्युत अपघटनी सेल के रूप में कार्य करेगा क्योंकि इसका EMF कम है। इलेक्ट्रोड अभिक्रियाएँ होंगी:
कैथोड पर $Zn^{2+}+2 e^{-} \longrightarrow Zn$
एनोड पर $Cu \longrightarrow Cu^{2+}+2 e^{-}$
(ii) अब सेल ‘B’ गैल्वेनिक सेल के रूप में कार्य करेगा क्योंकि इसका EMF अधिक है, और यह सेल ‘A’ को विद्युत अपघटनी सेल की तरह चलाएगा।
इलेक्ट्रोड प्रतिक्रिया होगी:
एनोड पर: $Zn \longrightarrow Zn^{2+}+2 e^{-}$
कैथोड पर: $Cu^{2+}+2 e^{-} \longrightarrow Cu$
~~ 67. संकेत: (i) इलेक्ट्रॉन्स $Zn$ से Ag में चलते हैं।
(ii) Ag धातु कैथोड है।
(iii) लवण सेतु हटाने पर सेल कार्य करना बंद कर देगा।
(iv) जब $E_{\text{सेल}} = 0$ हो जाता है।
(v) $Zn^{2+}$ आयनों की सांद्रता बढ़ेगी और $Ag^{+}$ आयनों की सांद्रता घटेगी।
(vi) जब $E_{\text{सेल}} = 0$ हो जाता है तो साम्यावस्था प्राप्त होती है और $Zn^{2+}$ तथा $Ag^{+}$ आयनों की सांद्रता स्थिर हो जाती है।





