तालमेलि मद्देन्त
इकाई 7
संतुलन
I. बहुविकल्पी प्रश्न (प्रकार- I)
~~ 1. हम जानते हैं कि $K_c$ और $K_p$ के बीच का संबंध है
$ K_p=K_c(RT)^{\Delta n} $
प्रतिक्रिया के लिए $\Delta n$ का मान क्या होगा
$NH_4 Cl(s) \rightarrow NH_3(g)+HCl(g)$
(i) 1
(ii) 0.5
(iii) 1.5
(iv) 2
~~ 2. प्रतिक्रिया $H_2(g)+I_2(g) \rightarrow 2 HI(g)$ के लिए मानक मुक्त ऊर्जा $\Delta G^{\ominus}>0$ है। संतुलन स्थिरांक $(K)$ क्या होगा ———-.
(i) $K=0$
(ii) $K>1$
(iii) $K=1$
(iv) $K<1$
~~ 3. निम्नलिखित में से कौन सा भौतिक प्रक्रियाओं के संतुलन की आम विशेषता नहीं है?
(i) एक दिए गए तापमान पर एक बंद सिस्टम में संतुलन केवल संभव है।
(ii) प्रणाली की सभी मापनीय गुणधर्म स्थिर रहते हैं।
(iii) सभी भौतिक प्रक्रियाएँ संतुलन पर रुक जाती हैं।
(iv) प्रतिरोधी प्रक्रियाएँ एक ही दर से होती हैं और यह गतिशील लेकिन स्थिर स्थिति होती है।
~~ 4. $PCl_5, PCl_3$ और $Cl_2$ को $500 K$ पर एक बंद बरतन में संतुलन होता है और उनकी घनत्व $0.8 \times 10^{-3} mol L^{-1}, 1.2 \times 10^{-3} mol L^{-1}$ और $1.2 \times 10^{-3} mol L^{-1}$ क्रमशः होती हैं। प्रतिक्रिया $PCl_5(g) \rightarrow PCl_3(g)+Cl_2(g)$ के लिए $K_c$ का मान होगा
(i) $1.8 \times 10^{3} mol L^{-1}$
(ii) $1.8 \times 10^{-3}$
(iii) $1.8 \times 10^{-3} L mol^{-1}$
(iv) $0.55 \times 10^{4}$
~~ 5. निम्नलिखित में से कौन सा कथन गलत है?
(i) संतुलित जल के मिश्रण में समय के साथ बर्फ और पानी का भार नहीं बदलता।
(ii) लोहे में विद्यमान फेरी णिका एसिड युक्त समाधान में जब ऑक्सलिक रसायनिक धातु (III) नाइट्रेट और पोटेशियम थियोसियनेट मिलाए जाते हैं तो लाल रंग की तीव्रता बढ़ती है।
(iii) कैटलिस्ट को संघटन के मान को प्रभावित नहीं करता है।
(iv) एक प्रतिक्रिया के लिए नकारात्मक $\Delta H$ मान वाला संतुलन स्थिरांक तापमान बढ़ने पर कम होता है।
~~ 6. कोबाल्ट नाइट्रेट विलयन के लिए हाइड्रोक्लोरिक अम्ल को कमरे के तापमान पर जब जोड़ा जाता है, तो निम्न अभिक्रिया होती है और प्रतिक्रिया मिश्रण नीली हो जाती है। मिश्रण को शीतल करने पर यह गुलाबी हो जाती है। इस जानकारी के आधार पर सही उत्तर चिह्नित करें।
$[Co(H_2 O)_6]^{3+}(a q)+4 Cl^{-}(a q) \rightarrow[CoCl_4]^{2-}(a q)+6 H_2 O(l)$
(गुलाबी) (नीली)
(i) प्रतिक्रिया के लिए $\Delta H>0$
(ii) प्रतिक्रिया के लिए $\Delta H<0$
(iii) प्रतिक्रिया के लिए $\Delta H=0$
(iv) इस जानकारी के आधार पर $\Delta H$ की चिह्निता का पूर्वानुमान नहीं किया जा सकता है।
~~ 7. $25^{\circ} C$ पर न्यूट्रल पानी का $pH$ 7.0 होता है। जब तापमान बढ़ता है, पानी का आयनन बढ़ता है, हालांकि, $H^{+}$आयनों और $OH^{-}$आयनों की घनता समान होती है। पानी का $pH$ $60^{\circ} C$ पर क्या होगा?
(i) 7.0 के बराबर
(ii) 7.0 से अधिक
(iii) 7.0 से कम
(iv) शून्य के बराबर
~~
विषय: 8. एक एसिड का आयोनीकरण स्थिरता स्थिरता, K_a, एक एसिड की मजबूती का माप होता है। एसिटिक एसिड, हाइपोक्लोरस एसिड और फॉर्मिक एसिड के K_a मान $1.74 \times 10^{-5}, 3.0 \times 10^{-8}$ और $1.8 \times 10^{-4}$ हैं। इन एसिड के $0.1 मोल डीएम^{-3}$ हल के $pH$ के कौन से क्रम सही हैं?
(i) एसिटिक एसिड $>$ हाइपोक्लोरस एसिड $>$ फॉर्मिक एसिड
(ii) हाइपोक्लोरस एसिड $>$ एसिटिक एसिड $>$ फॉर्मिक एसिड
(iii) फॉर्मिक एसिड $>$ हाइपोक्लोरस एसिड $>$ एसिटिक एसिड
(iv) फॉर्मिक एसिड $>$ एसिटिक एसिड $>$ हाइपोक्लोरस एसिड
~~ 9. $K _{a_1}, K _{a_2}$ और $K _{a_3}$ निम्नलिखित प्रतिक्रियाओं के लिए संबंधित आयोनीकरण स्थिरताएं हैं।
$H_2 S \rightarrow H^{+}+HS$
$HS^{-} \rightarrow H^{+}+S^{2-}$
$H_2 S \rightarrow 2 H^{+}+S^{2-}$
$K _{a_1}, K _{a_2}$ और $K _{a_3}$ के बीच सही संबंध क्या है
(i) $K _{a_3}=K _{a_1} \times K _{a_2}$
(ii) $K _{a_3}=K _{a_1}+K _{a_2}$
(iii) $K _{a_3}=K _{a_1}-K _{a_2}$
(iv) $K _{a_3}=K _{a_1} / K _{a_2}$
~~ 10. $BF_3$ की अम्लता निम्नलिखित सिद्धांतों के आधार पर समझाई जा सकती है?
(i) आरेनियस सिद्धांत
(ii) ब्रॉन्स्टेड लौरी सिद्धांत
(iii) ल्यूइस सिद्धांत
(iv) ब्रॉन्स्टेड लौरी सिद्धांत और ल्यूइस सिद्धांत दोनों
~~ 11. निम्नलिखित में से बराबर मात्रा में मिश्रित करने पर कौन सा बफर द्वारा एक्सपरिमेंटिंग सुलझाया जाएगा?
(i) $0.1 मोल डीएम^{-3} NH_4 OH$ और $0.1 मोल डीएम^{-3} HCl$
(ii) $0.05 मोल डीएम^{-3} NH_4 OH$ और $0.1 मोल डीएम^{-3} HCl$
(iii) $0.1 मोल डीएम^{-3} NH_4 OH$ और $0.05 मोल डीएम^{-3} HCl$
(iv) $0.1 मोल डीएम^{-3} CH_4 COONa$ और $0.1 मोल डीएम^{-3} NaOH$
~~ 12. निम्नलिखित में से कौन से विलयनों में स्कोर्पियम क्लोराइड सबसे अधिक विलयनशील होगा?
(i) $0.1 मोल डीएम^{-3} AgNO_3$ के हल
(ii) $0.1 मोल डीएम^{-3} HCl$ के हल
(iii) $H_2 O$
(iv) जलीय नित्रोजन
~~ 13. $0.01 मोल डीएम^{-3} CH_3 COOH(K_a=1.74 \times 10^{-5})$ का $pH$ क्या होगा?
(i) 3.4
(ii) 3.6
(iv) 3.0
~~ 14. $CH_3 COOH$ के लिए $K_a$ $1.8 \times 10^{-5}$ है और $NH_4 OH$ के लिए $K_b$ $1.8 \times 10^{-5}$ है। अमोनियम एसेटेट का $pH$ होगा
(i) 7.005
(ii) 4.75
(iii) 7.0
(iv) 6 और 7 के बीच
~~ 15. प्रतिक्रिया $A \rightarrow B$ के आधी पूर्णता की अवस्था के लिए निम्नलिखित में से कौन सा विकल्प सही होगा।
(i) $\Delta G^{\ominus}=0$
(ii) $\Delta G^{\ominus}>0$
(iii) $\Delta G^{\ominus}<0$
(iv) $\Delta G^{\ominus}=-R T \ln 2$
~~ 16. दबाव को बढ़ाते हुए, गैस चरण प्रतिक्रिया की प्रतिष्ठान को पुनः स्थापित करने के लिए वाहनानुसार बढ़ाया जाएगा, इसे ले शाटलिए के सिद्धांत का उपयोग करके पूर्वानुमानित किया जाता है। संक्रमण को विचार करें।
$ N_2(g)+3 H_2(g) \rightarrow 2 NH_3(g) $
निम्नलिखित में से कौन सा सही है, अगर संपूर्ण दबाव बदले बिना तापमान को नहीं बदलते हुए स्थिरता की कुल दबावहीनता स्थापित हो जाए?
(i) $K$ पहले जैसा ही रहेगा
(ii) $K$ कम हो जाएगा
(iii) $K$ बढ़ जाएगा
(iv) पहली चरण में $K$ बढ़ेंगे और दबाव अत्यधिक होने पर कम हो जाएंगे
वस्तुनिष्ठ जपानी अनुवादक (हाई भाषा में अनुवाद करनेवाला कार्यक्रम),
उपस्थिति संख्या: 17. $30^{\circ} C$ पर पानी, ऐसेटोन और ईथर का वाष्प संचित्र दाब क्रम क्या होगा? इन एल्कोहलों में से पानी के पास अधिकतम उबलने का अंक है और ईथर के पास न्यूनतम उबलने का अंक है।
(अ) पानी $<$ ईथर $<$ ऐसेटोन
(b) पानी $<$ ऐसेटोन $<$ ईथर
(के) ईथर $<$ ऐसेटोन $<$ पानी
(iv) एसिटोन $<$ ईथर $<$ पानी
संख्या: 18. $500 केल्विन$ पर, संतुलन स्थिति व्यक्ति, $K_c$, निम्नलिखित प्रतिक्रिया के लिए 5 है।
$\frac{1}{2} H_2 गैस + \frac{1}{2} I_2 गैस \rightarrow HI गैस$
प्रतिक्रिया $2 HI गैस \rightarrow H_2 गैस + I_2 गैस$ के लिए संतुलन स्थिति मान $K_c$ क्या होगा।
(i) 0.04
(ii) 0.4
(के) 25
(iv) 2.5
संख्या: 19. किस इन प्रतिक्रिया में, संतुलन संख्या को अक्षरांतरण किए बिना रघु राशि आरगॉन के छोटे मात्रा के जोड़ाई को स्थिर रखता है?
(अ) $H_2 गैस + I_2 गैस \rightarrow 2 HI गैस$
(b) $PCl_5 गैस \rightarrow PCl_3 गैस + Cl_2 गैस$
(के) $\quad N_2 गैस + 3 H_2 गैस \rightarrow 2 NH_3 गैस$
(iv) संतुलन तीनों मामलों में प्रभावित नहीं होगा।
II. बहुविकल्पीय प्रश्न (प्रकार-II)
निम्नलिखित प्रश्नों में दो या अधिक विकल्प सही हो सकते हैं।
संख्या: 20. प्रतिक्रिया $N_2 O_4(g) \rightarrow 2 NO_2(g)$ के लिए $K$ का मूल्य $400 केल्विन$ पर 50 है और $500$ केल्विन$ के लिए 1700 है। निम्नलिखित में से कौन सा विकल्प सही है?
(अ) प्रतिक्रिया ऊष्मागारी है।
(ii) प्रतिक्रिया उष्मागारी है।
(के) यदि $NO_2$ (g) और $N_2 O_4$ (g) को $400 केल्विन$ पर अंशिक दाब में मिलाया जाता है, जहां तापछाप $20 \text{ बार}$ और $2 \text{ बार}$ होता है, तो अधिक $N_2 O_4(g)$ बनेगा।
(iv) प्रणो समीकरण की अव्यवस्था होती है।
संख्या: 21. एक विशेष तापमान और वायुमंडलीय दब के नीचे, एक शुद्ध पदार्थ के ठोस और तरल चरणों का स्थिरता में हो सकता है। निम्न में से कौन सा शब्द इस तापमान की परिभाषा के लिए उपयुक्त है?
(अ) सामान्य पिघलने का समय
(ii) संतुलन तापमान
(के) उबलने का समय
(iv) जमाव का समय
III. कम्पलेक्स उत्तर प्रकार
संख्या: 22. स्वच्छ जल में हाइड्रोक्लोरिक का आईसनीकरण नीचे दिया गया है:
$HCl(aq)+H_2 O(l) \rightarrow H_3 O^{+}(aq)+Cl^{-}(aq)$
इस आईसनीकरण में दो सम्बंधित अम्ल-आधार जोड़ों को लेबल करें।
संख्या: 23. शुगर का जलीय विलयन बिजली नहीं चलाता है। हालांकि, जब जल में सोडियम क्लोराइड जोड़ा जाता है, तो वह बिजली चलाता है। आप इस विधान को आधार पर कैसे समझाएंगे और इसे सोडियम क्लोराइड की घनत्व के प्रभावित किया जाता है?
संख्या: 24. $BF_3$ का प्रोटॉन नहीं होता है लेकिन फिर भी यह एक अम्ल के रूप में कार्य करता है और $NH_3$ के साथ प्रतिक्रिया करता है। ऐसा क्यों है? दोनों के बीच में कौन सा बंध होता है?
संख्या: 25. एक कमजोर आधार $MOH$ का आईसनीक मान निम्नलिखित व्यक्ति द्वारा दिया जाता है
$ K_b=\frac{[M^{+}][OH^{-}]}{[MOH]} $
कुछ निकटतम तापमान पर कुछ कमजोर आधारों के आयामी नागरिक नीचे दिए गए हैं।
| आधार | डाइमेथाइलएमिन | यूरिया | पिरिडीन | अम्मोनिया |
|---|---|---|---|---|
| $K_b$ | $5.4 \times 10^{-4}$ | $1.3 \times 10^{-14}$ | $1.77 \times 10^{-9}$ | $1.77 \times 10^{-5}$ |
स्थिरता में अपने आयामी की कम होने के आदानुक्रम सामयिक करें। उपरोक्त आधार में से कौन सा सबसे ताकतवर है?
26. एक कमजोर बेस का संधि अम्ल हमेशा अधिक मजबूत होता है। निम्नलिखित संघटना आधारों की बुनियादी शक्ति के अनुसार कम होने की क्रमशः क्या होगी?
$OH^{-}, RO^{-}, CH_3 COO^{-}, Cl^{-}$
~~ 27. निम्नलिखित को $pH$ की बढ़ती क्रम में व्यवस्थित कीजिए।
$ KNO_3(a q), CH_3 COONa(a q), NH_4 Cl(a q), C_6 H_5 COONH_4(a q) $
~~ 28. प्रतिक्रिया $2 HI(g) \rightarrow H_2(g)+I_2(g)$ के लिए $K_c$ का मान $1 \times 10^{-4}$ है।
एक दिए गए समय पर, प्रतिक्रिया मिश्रण का संघटन यह है
$[HI]=2 \times 10^{-5} mol, \quad[H_2]=1 \times 10^{-5} mol$ और $[I_2]=1 \times 10^{-5} mol$
प्रतिक्रिया किस दिशा में आगे बढ़ेगी?
~~ 29. मसले $pH=-\log [H^{+}]$ के समीकरण के आधार पर, $HCl$ के $10^{-8} mol dm^{-3}$ वाले विलयन के $pH$ का 8 होना चाहिए। हालांकि, यह 7.0 से कम माना जाता है। कारण का विवरण दीजिए।
~~ 30. एक मजबूत अम्ल के विलयन का $pH$ 5.0 है। दिए गए विलयन को 100 गुना पतला करने के बाद पाॅया जाने वाले विलयन का $pH$ क्या होगा?
~~ 31. एक थोड़ी-सी घुलनशील नमक की स्थिति सिर्फ तब होती है जब स्राव में यह योग्यता उत्तेजित होती है जब इसके आयनों की आपूर्ति का गुणनफल $(Q _{sp})$ इसकी विलयता उत्तेजितत्ता से अधिक होती है। यदि $BaSO_4$ की विलयता पानी में $8 \times 10^{-4} mol dm^{-3}$ है। तो $H_2 SO_4$ के $0.01 mol dm^{-3}$ में इसकी विलयता कीमत निर्धारित कीजिए।
~~ 32. $0.08 mol dm^{-3} HOCl$ विलयन का $pH$ 2.85 है। इसकी आयनिकता स्थिर कीमत गणना कीजिए।
~~ 33. एक दोनों $A$ और $B$ दोनों के समान औचित्य धारित विलयन से बनी समाधान की विलयन का $pH$ का गणना कीजिए, जहां $pH=6$ औचित्य और $pH=4$ अचीचिमितत्ता यहां का है।
~~ 34. $Al(OH)_3$ की विलयन उत्पाद क्षमता $2.7 \times 10^{-11}$ है। $gL^{-1}$ में इसकी विलयता गणना कीजिए और इस समाधान का $pH$ भी निर्धारित कीजिए। ($(Al=27 u)$ ).
~~ 35. एक संतृप्त समाधान प्राप्त करने के लिए $0.1 g$ लीड (द्विवर्षीय) क्लोराइड को घुलनशील करने के लिए जितना पानी की आवश्यकता होगी, इसकी गणना कीजिए। $(PbCl_2=3.2 \times 10^{-8}, Pb=207 u)$
~~ 36. एक अमोनिया और बोरॉन ट्रिफ्लोराइड के बीच एक प्रतिक्रिया नीचे दी गई है:
$: NH_3+BF_3 \longrightarrow H_3 N: BF_3$
इस प्रतिक्रिया में एसिड और बेस को पहचानें। इस प्रतिक्रिया को कौन सी सिद्धांत समझाती है? प्रतिक्रिया माध्यम में $B$ और $N$ का हाइब्रीडीकरण क्या होगा?
~~ 37. निम्नलिखित प्रतिक्रिया के लिए निम्नलिखित डेटा दिया गया है: $CaCO_3(s) \to CaO(s)+CO_2(g)$
$ \begin{aligned} & \Delta_f H^{\ominus}[CaO(s)]=-635.1 kJ mol^{-1} \\ & \Delta_f H^{\ominus}[CO_2(g)]=-393.5 kJ mol^{-1} \\ & \Delta_f H^{\ominus}[CaCO_3(s)]=-1206.9 kJ mol^{-1} \end{aligned} $
यहां प्रतिक्रिया की स्थिरता स्थिति के लिए तापमान का प्रभाव बताइए।
IV. मिलान के प्रकार
~~ 38. निम्नलिखित सभीयों को उपयुक्त स्थिति के साथ मिलाइए
| (i) तरल $\rightarrow$ वाष्प | (a) तृषित विलय |
|---|---|
| (ii) ठोस $\leftrightharpoons$ तरल | (b) उबालने का बिंदु |
| (iii) ठोस $\leftrightharpoons$ वाष्प | (c) उत्पादन बिंदु |
| (iv) विलयांक सामान (तरल विलय समाधान) $\leftrightharpoons$ विलयांक (समाधान) | (d) पिघलाने का बिंदु |
| (e) अअच्छीतताहीन समाधान |
39. प्रतिक्रिया के लिए: $एन_2(ग)+3 हा_2(ग) \leftrightharpoons 2 एन_एच_3(ग)$
संतुलन साधक $के_सी=\frac{[एन_एच_3]^{2}}{[एन_2][हा_2]^{3}}$
कुछ प्रतिक्रियाओं को नीचे संख्यागणित के माध्यम से लिखा गया है और उनके संतुलन साधकों को $के_सी$ के आधार पर लिखा गया है। निम्नलिखित प्रतिक्रियाओं को संबंधित संतुलन साधक के साथ मिलान करें
| स्तंभ I (प्रतिक्रिया) | स्तंभ II (संतुलन साधक) |
|---|---|
| (i) $2 एन_2(ग) + 6 हा_2(ग) \rightarrow 4 एन_एच_3(ग)$ | (a) $2 के_सी$ |
| (ii) $\quad 2 एन_एच_3(ग) \rightarrow एन_2(ग) + 3 हा_2(ग)$ | (b) $\quad के_सी^{\frac{1}{2}}$ |
| (iii) $\quad \frac{1}{2} एन_2(ग) + \frac{3}{2} हा_2(ग) \rightarrow एन_एच_3(ग)$ | (c) $\frac{1}{के_सी}$ |
| (d) $के_सी^{2}$ |
~~ 40. मिश्रण में सूचित गतिकीय संतुलन मान के आपसी संबंध को मिलाएं
| (i) $\Delta G^{\ominus}>0$ | (a) $K>1$ |
|---|---|
| (ii) $\Delta G^{\ominus}<0$ | (b) $K=1$ |
| (iii) $\Delta G^{\ominus}=0$ | (c) $K=0$ |
| (d) $K<1$ |
~~ 41. निम्नलिखित प्रजातियाँ के संबंधित संयुक्त अम्ल के साथ मिलाते हैं
| प्रजाति | संयुक्त अम्ल |
|---|---|
| (i) $एनएच_3$ | (a) $सीओ_3^{2-}$ |
| (ii) $एचसीओ_3^{-}$ | (b) $एनएच_4^{+}$ |
| (iii) $एच_2 ओ$ | (c) $एच_3ओ^{+}$ |
| (iv) $एचसीओ_4^{-}$ | (d) $एच_2 सीओ_3$ |
| (e) $एच_2 सीओ_3$ |
~~ 42. निम्नलिखित ग्राफिकल विविधता को उनकी विवरण के साथ मिलाएं
A
(i)
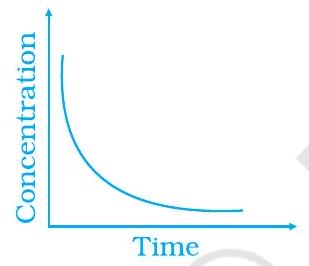
(ii)
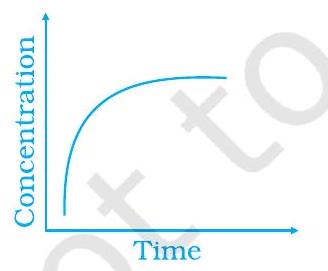
(iii)
(a) समय के साथ उत्पाद की उत्पादन की विविधता
(b) संतुलन में प्रतिक्रिया
(c) समय के साथ उत्पाद की उत्पादन की विविधता
~~ 43. स्तंभ (I) का स्तंभ (II) के साथ मिलाएं
| स्तंभ I | स्तंभ II |
|---|---|
| (i) संतुलन | (a) $\Delta G>0, K<1$ |
| (ii) स्वेच्छिक प्रक्रिया | (b) $\Delta G=0$ |
| (iii) निष्पाद्यात्मक प्रक्रिया | (c) $\Delta G^{\ominus}=0$ |
| (d) $\Delta G<0, K>1$ |
V. दावा और कारण प्रकार
निम्न प्रश्नों में एक दावा (ए) का बयान और एक कारण (आर) का बयान दिया गया है। प्रत्येक प्रश्न के नीचे दी गई विकल्पों में से सही विकल्प चुनें।
~~ 44. दावा (ए) : एसिडिटी की बढ़ती क्रमबध्दता है $एचएफ<एचसीएल<एचबीआर<एचआई$
कारण (आर) : प्राथमिकतापूर्वक तालिका के उन तत्वों द्वारा बनाए गए अम्लों की तुलना करते समय, $एच-ए$ बंध शक्ति अम्ल की एम्लता की तुलना में एक अधिक महत्वपूर्ण कारक होती है यह बंध के ध्रुवीकरण की तुलना में।
(i) दोनों $ए$ और $आर$ सही हैं और $आर$ द्वारा $ए$ का सही व्याख्यान है।
(ii) दोनों $ए$ और $आर$ सही हैं लेकिन $आर$ $ए$ का सही व्याख्यान नहीं है।
(iii) $ए$ सही है लेकिन $आर$ गलत है।
(iv) दोनों $ए$ और $आर$ गलत हैं।
~~ 45. दावा (ए) : एसिटिक अम्ल और सोडियम एसिटेट का मिश्रण छोटे मात्रा में अम्ल या तत्समक के योग में झूठा का निरंतर मान रखता है।
Reason (R) : Hydrogen sulphide is a weak acid.
(i) दोनों A और R सत्य हैं और R, A का सही स्पष्टीकरण है।
(ii) दोनों A और R सत्य हैं, लेकिन R A का सही स्पष्टीकरण नहीं है।
~~ 47. अभिकथन (A): किसी विशेष समय पर किसी केमिकल प्रतिक्रिया के लिए समतोच्चार स्थिरांक निर्धारित होता है और यह एक विशेषता गुण होती है।
Reason (R) : समतोच्चार स्थिरांक, तापमान से अपेक्षित नहीं होता है।
(i) दोनों A और R सत्य हैं और R, A का सही स्पष्टीकरण है।
(ii) दोनों A और R सत्य हैं, लेकिन R A का सही स्पष्टीकरण नहीं है।
(iii) A सत्य है, लेकिन R गलत है।
(iv) दोनों A और R गलत हैं।
~~ 48. अभिकथन (A) : अमोनियम कार्बोनेट का आकाशीय विलयन मात्र रहित होता है।
Reason (R) : एक अम्लीय / आकाशीय सौरभ और दुसरा अम्लीय / आकाशीय अधातु बनाने वाली अम्ल और आधातु के $K_a$ और $K_b$ नामक मान पर निर्भर करता है।
(i) दोनों A और R सत्य हैं और R, A का सही स्पष्टीकरण है।
(ii) दोनों A और R सत्य हैं, लेकिन R A का सही स्पष्टीकरण नहीं है।
(iii) A सत्य है, लेकिन R गलत है।
(iv) दोनों A और R गलत हैं।
~~ 49. अभिकथन (A): अमोनियम एसीटेट का उद्भावनीय विलयन एक बफर के रूप में कार्य कर सकता है।
Reason (R) : एसेटिक अम्ल एक कमजोर अम्ल है और $NH_4 OH$ एक कमजोर बेस है।
(i) दोनों A और R सत्य हैं और R, A का सही स्पष्टीकरण है।
(ii) दोनों A और R सत्य हैं, लेकिन R A का सही स्पष्टीकरण नहीं है।
(iii) A गलत है, लेकिन R सत्य है।
(iv) दोनों A और R गलत हैं।
~~ 50. अभिकथन (A): एक स्थिर दबाव और तापमान पर $PCl_5$ के विभाजन में साम और नियमित प्रक्रिया में हिलियम का जोड़ना $PCl_5$ के विभाजन को बढ़ाता है।
Reason (R) : हिलियम $Cl_2$ को क्रियाशीलता क्षेत्र से हटा देता है।
(i) दोनों A और R सत्य हैं और R, A का सही स्पष्टीकरण है।
(ii) दोनों A और R सत्य हैं, लेकिन R A का सही स्पष्टीकरण नहीं है।
(iii) A सत्य है, लेकिन R गलत है।
(iv) दोनों A और R गलत हैं।
VI. लंबा उत्तर टाइप
~~ 51. आप $K_c$ और $Q_c$ के माप का तुलनात्मक अध्ययन करके निम्नलिखित प्रतिक्रिया की निम्नलिखित चरणों की पूर्वानुमान हो सकती है?
(i) मुख्य प्रतिक्रिया प्रगति पथ में आगे करती है। (ii) मुख्य प्रतिक्रिया प्रगति पथ में पीछे जाती है।
(iii) कोई भी मुख्य प्रतिक्रिया नहीं होती है।
~~ 52. ले छेटेलियर सिद्धांत के आधार पर व्याख्या करें कि ऊष्मा और दबाव को कैसे समायोजित किया जा सकता है ताकि निम्नलिखित प्रतिक्रिया में अमोनिया का उत्पादन अधिक होगा।
$N_2(g)+3 H_2(g) \rightarrow 2 NH_3(g) \quad \Delta H=-92.38 kJ mol^{-1}$
स्थिरांकजनित वॉल्यूम पर नाइट्रोजन गैस के मिश्रण में आर्गॉन के जोड़ने का प्रभाव क्या होगा?
53. एक बचावी रूप में हलकी रूप से रंजक नमक का साधारण सूत्र $A_x^{p+} B_y^{q-}$ और मोलर उपलब्धता $S$ के साथ इसकी पूर्णता वाली विलयी में संतुलन में है। इस तरह के नमक के उपलब्धता और उपलब्धता उत्पाद के बीच एक संबंध प्रस्तुत कीजिए।
~~ 54. $\Delta G$ और $Q$ के बीच एक संबंध लिखिए और प्रत्येक शब्द के अर्थ की परिभाषा दीजिए और निम्नलिखित प्रश्नों का उत्तर दीजिए:
(अ) $Q<K$ होने पर एक प्रतिक्रिया आगे बढ़ती है और $Q=K$ होने पर कोई संकीर्ण प्रतिक्रिया नहीं होती है।
(ब) दबाव में वृद्धि के प्रभाव को विलयी अनुपात $Q$ के हिसाब से समझाइए। विलयी: $CO(g)+3 H_2(g) \rightarrow CH_4(g)+H_2 O(g)$
उत्तर
I. बहुविकल्पी प्रश्न (प्रकार-I)
~~ 1. (iv)
~~ 2. (iv)
~~ 3. (iii)
~~ 4. (ii)
~~ 5. (ii)
~~ 6. (i)
~~ 7. (iii)
~~ 8. (iv)
~~ 9. (i)
~~ 10. (iii)
~~ 11. (iii)
~~ 12. (iv)
~~ 13. (i)
~~ 14. (iii)
~~ 15. (i) $\Delta G^{\ominus}=0$
ब्याख्या: $\Delta G^{\ominus}=-R T \ln K$
प्रतिक्रिया के आधे में, $[A]=[B]$, इसलिए, $K=1$।
इस प्रकार, $\Delta G^{\ominus}=0$
~~ 16. (i), ब्याख्या: ले-चैटेलियर का सिद्धांत के अनुसार, स्थिर तापमान पर, संतुलन संगठन परिवर्तित होगा, लेकिन $K$ एक ही रहेगा।
~~ 17. (ii)
~~ 18. (i)
~~ 19. (iv)
II. बहुविकल्पी प्रश्न (प्रकार-II)
~~ 20. (i), (iii) और (iv)
ब्याख्या: (i) तापमान में वृद्धि के साथ किनेटिक बढ़ता है।
(iii) $Q>K$, इसलिए, प्रतिक्रिया पिछड़ी दिशा में बढ़ती है।
(iv) $\Delta n>0$, इसलिए, $\Delta S>0$।
~~ 21. (i) और (iv)
III. संक्षेप उत्तर प्रकार
~~ 22.
| $HCl$ | $Cl^{-}$ |
|---|---|
| एसिड | संयुक्त आधार |
| $H_2 O$ | $H_3 O^{+}$ |
| आधार | संयुक्त अम्ल |
~~ 23.
शक्कर पानी में आयनित नहीं होती है, लेकिन $NaCl$ पूर्णतः पानी में आयनित होती है और $Na^{+}$और $Cl^{-}$ आयनों को उत्पन्न करती है।
नमक के आदर्श मात्रा में वृद्धि से चालकता बढ़ती है क्योंकि अधिक आयनों को उत्पन्न होने के कारण।
~~ 24. $BF_3$ एक लुइस अम्ल के रूप में कार्य करता है क्योंकि यह इलेक्ट्रॉन क्षेत्री संयुक्त नहीं है और यहां दिए गए समन्वय बांध बनते हैं:
$H_3 N: \to BF_3$
~~ 25.
- संतुलन पर आयनन की गहराई का क्रम निम्नानुसार है:
डाइमेथलएमीन $>$ अमोनिया $>$ पाइरीडिन $>$ यूरिया
- क्योंकि डाइमेथलएमीन सर्वाधिक मात्रा में आयनन करेगी, इसलिए यह चारों दिए गए आधारों में सबसे शक्तिशाली आधार है।
~~ 26. $RO^{-}>OH^{-}>CH_3 COO^{-}>Cl^{-}$
~~ 27. $NH_4 Cl<C_6 H_5 COONH_4<KNO_3<CH_3 COONa$
~~ 28. एक निर्धारित समय पर, प्रतिक्रिया अनुपात $Q$ के लिए एक व्यक्ति स्वतः होगा द्वारा न्यूनतम मूल्य द्वारा दिया जाएगा।
$ \begin{aligned} Q & =\frac{[H_2][I_2]}{[H I]^{2}} \\ & =\frac{1 \times 10^{-5} \times 1 \times 10^{-5}}{(2 \times 10^{-5})^{2}}=\frac{1}{4} \\ & =0.25=2.5 \times 10^{-1} \end{aligned} $
प्रतिक्रिया अनुपात का मान $K_c$ के मान से अधिक होने के कारण, प्रतिक्रिया पिछड़ी दिशा में आगे बढ़ेगी।
~~
जबकि Solution $A$ में $pH=6$ है, इसलिए Solution $A$ में $[H^{+}]$ आयन की विचरण की एकाई $10^{-6} mol L^{-1}$ है।
Solution $B$ का $pH=4$ है, इसलिए Solution $B$ में $[H^{+}]$ आयन की विचरण की एकाई $10^{-4} mol L^{-1}$ है।
दोनों Solution का एक लीटर मिलाने पर, कुल आपूर्ति $=1 L+1 L=2 L$ हो जाती है।
Solution $A$ के $1 L$ में $H^{+}$ आयन की मात्रा $=$ विचरण $\times$ आयतन $V$ होती हैं। $
कंटेंट का हिंदी संस्करण क्या है: =10^{-6} मोल \times 1 लीटर $
सोल्यूशन $B$ में $1 लीटर$ के लिए $H^{+}$आयनों की मात्रा $=10^{-4} मोल \times 1 लीटर$
इसलिए मिश्रित सोल्यूशन $A$ और $B$ के द्वारा बने गए सोल्यूशन में कुल $H^{+}$आयनों की मात्रा $(10^{-6} मोल+10^{-4} मोल)$ होगी
यह मात्रा 2L सोल्यूशन में मौजूद होती है।
$ \begin{aligned} & \therefore \text{ कुल }[H^{+}]=\frac{10^{-4}(1+0.01)}{2}=\frac{1.01 \times 10^{-4}}{2} मोल L^{-1}=\frac{1.01 \times 10^{-4}}{2} मोल L^{-1} \\ & =0.5 \times 10^{-4} मोल L^{-1} \\ & =5 \times 10^{-5} मोल L^{-1} \\ & पीएच=-\log [H^{+}]=-\log (5 \times 10^{-5}) \\ & =-[\log 5+(-5 \log 10)] \\ & =-\log 5+5 \\ & =5-\log 5 \\ & =5-0.6990 \\ & =4.3010=4.3 \end{aligned} $
~~ 34. $S$ को $Al(OH)_3$ की सोल्यूबिलिटी मान लें।
$ Al(OH)_3 \leftrightharpoons Al^{3+}(aq)+30 H^{-}(aq) $
| आरम्भिक समय $t=0$ पर जीवस्थिति में विभिन्न प्रजातियों की घनत्व | 1 | 0 | 0 |
|---|---|---|---|
| संतुलन में विभिन्न प्रजातियों की घनत्व | 1-S | S | 3S |
$ \begin{aligned} & K _{s p}=[Al^{3+}][OH^{-}]^{3}=(S)(3 S)^{3}=27 S^{4} \\ & S^{4}=\frac{K _{s p}}{27}=\frac{27 \times 10^{-11}}{27 \times 10}=1 \times 10^{-12} \\ & S=1 \times 10^{-3} mol L^{-1} \end{aligned} $
(i) $Al(OH)_3$ की सोल्यूबिलिटी
$Al(OH)_3$ का मूलीय मास $78 ग्राम$ है। इसलिए,
$Al(OH)_3$ की सोल्यूबिलिटी, $ग्राम L^{-1}=1 \times 10^{-3} \times 78 ग्राम L^{-1}=78 \times 10^{-3} ग्राम L^{-1}$
$ =7.8 \times 10^{-2} ग्राम L^{-1} $
(ii) सोल्यूशन का $\mathbf{p H}$
$ \begin{aligned} & S=1 \times 10^{-3} mol L^{-1} \\ & {[OH^{-}]=3 S=3 \times 1 \times 10^{-3}=3 \times 10^{-3}} \\ & \text{ pOH }=3-\log 3 \\ & \text{ pH }=14-\text{ pOH }=11+\log 3=11.4771 \end{aligned} $
~~ 35. $PbCl_2$ की $K _{\text{sp }}=3.2 \times 10^{-8}$
$S$ को $PbCl_2$ की सोल्यूबिलिटी मान लें।
$ PbCl_2(s) \leftrightharpoons Pb^{2+}(aq)+2 Cl^{-}(aq) $
| आरम्भिक समय $t=0$ पर जीवस्थिति में विभिन्न प्रजातियों की घनत्व | 1 | 0 | 0 |
|---|---|---|---|
| संतुलन में विभिन्न प्रजातियों की घनत्व | 1-S | S | 2S |
$K _{\text{sp }}=[Pb^{2+}][Cl^{-}]^{2}=(S)(2 S)^{2}=4 S^{3}$
$K _{sp}=4 S^{3}$
$S^{3}=\frac{K _{sp}}{4}=\frac{3.2 \times 10^{-8}}{4} mol L^{-1}=8 \times 10^{-9} mol L^{-1}$
$S=\sqrt[3]{8 \times 10^{-9}}=2 \times 10^{-3} mol L^{-1} \quad \therefore S=2 \times 10^{-3} mol L^{-1}$
$PbCl_2$ का मूलीय मास $278$ है
$\therefore PbCl_2$ की सोल्यूबिलिटी, $ग्राम L^{-1}=2 \times 10^{-3} \times 278 ग्राम L^{-1}$
$ \begin{aligned} & =556 \times 10^{-3} ग्राम L^{-1} \\ & =0.556 ग्राम L^{-1} \end{aligned} $
संतुलित सोल्यूशन प्राप्त करने के लिए, $0.556 ग्राम$ $PbCl_2$ को $1 लीटर$ पानी में घुलाया जाता है।
$0.1 ग्राम PbCl_2$ को $\frac{0.1}{0.556} लीटर=0.1798 लीटर$ पानी में घुलाया जाता है।
संतुलित सोल्यूशन बनाने के लिए, $0.1 ग्राम PbCl_2$ को $0.1798 लीटर \approx 0.2 लीटर$ पानी में घुलाने की आवश्यकता होगी।
~~ 37. $\Delta_r H^{\ominus}=\Delta_f H^{\ominus}[CaO(s)]+\Delta_f H^{\ominus}[CO_2(g)]-\Delta_f H^{\ominus}[CaCO_3(s)]$
इसलिए $\Delta_r H^{\ominus}=178.3 kJ mol^{-1}$
प्रतिक्रिया उष्णीय है। इसलिए, ले-शाटेलिये के सिद्धांत के अनुसार, उष्णी को बढ़ाने पर प्रतिक्रिया आगे की दिशा में प्रसारित होगी।
IV. मिलने वाले प्रकार
~~ 38. (i) $\to$ (b) $\quad$ (ii) $\to$ (d) $\quad$ (iii) $\to$ (c) $\quad$ (iv) $\to$ (a)
~~ 39. (i) $\to$ (d) $\quad$ (ii) $\to$ (c) $\quad$ (iii) $\to$ (b)
~~ 40. (i) $\to$ (d) $\quad$ (ii) $\to$ (a) $\quad$ (iii) $\to$ (b)
~~ 41. (i) $\to$ (b) $\quad$ (ii) $\to$ (e) $\quad$ (iii) $\to$ (c) $\quad$ (iv) $\to$ (d)
~~ 42. (i) $\to$ (c) $\quad$ (ii) $\to$ (a) $\quad$ (iii) $\to$ (b)
~~ 43. (i) $\to$ (b) और (c) $\quad$ (ii) $\to$ (d) $\quad$ (iii) $\to$ (a)
V. कथन और कारण का प्रकार
~~ 44. (i)
~~ 45. (i)
~~ 46. (ii)
~~ 47. (iii)
~~ 48. (i)
~~ 49. (iii)
~~ 50. (iv)
~~ V. लंबे उत्तर के प्रकार
~~ 51. (i) G $ _{c}<K_c$
(ii) $Q_c>K_c$
(iii) $\beta_c=K_c$
यहाँ, $Q_c$ रिएक्शन उदाहरण की मात्रात्मक में और $K_c$ संतुलन स्थिरांक है।
~~ 53. $[.$ संकेतः $A_x^{p+} B_y^{q-} \rightarrow x A^{p+}(aq)+y B^{q-}(aq)$
$S$ मोल $A_x B_y$ घुलकर $x S$ मोल $A^{p+}$ और $y S$ मोल $B^{q}$ बनाते हैं।]
~~ 54. $\Delta G=\Delta G^{\ominus}+R T \ln Q$
$\Delta G^{\ominus}=$ बदलता हुआ मुक्त ऊर्जा कि रिएक्शन में
$\Delta G=$ मानक मुक्त ऊर्जा का बदलाव
$Q=$ रिएक्शन उच्चारण
$R=$ गैस स्थिरांक
$T=$ वास्तविक तापमान
क्योंकि $\Delta G^{\ominus}=-R T \ln K$
इसलिए $\Delta G=-R T \ln K+R T \ln Q=RT \ln \frac{Q}{K}$
अगर $Q<K$, तो $\Delta G$ नकारात्मक होगा। रिएक्शन आगे की ओर बढेगा।
अगर $Q=K$, तो $\Delta G=0$, कोई नेट रिएक्शन नहीं होगी।
[संकेतः अगली बार $CO, H_2, CH_4$ और $H_2 O$ की घनीभूतता के संबंध में $Q$ को गिनती में लाएं। दिखाएं कि $Q<K$ होगा और इसलिए रिएक्शन की आगे की ओर प्रगति होगी।]





