रासायनिक आबंधन एवं आणविक संरचना भाग 1
JEE में विषय का महत्व
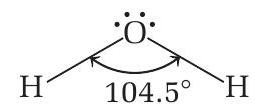
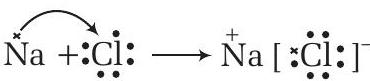
| मापदंड | मान | टिप्पणियाँ |
|---|---|---|
| कुल प्रश्न (2017-2024) | 13 | JEE में प्रत्येक वर्ष इस विषय से कम से कम एक प्रश्न शामिल किया गया है। |
| भारांक | 5.41% | इस विषय से प्रश्नों के अनुपात को दर्शाता है। |
वार्षिक प्रश्न वितरण
| वर्ष | विषय क्षेत्र | समाविष्ट अवधारणाएँ | प्रश्नों की संख्या | कठिनाई स्तर | प्रमुख फोकस क्षेत्र |
|---|---|---|---|---|---|
| 2024 | आबंध प्राचल / आणविक कक्षक सिद्धांत | आबंध ध्रुवता / आबंध क्रम | 2 | औसत | आबंध ध्रुवता का MO सिद्धांत और आबंध क्रम गणना से संबंध। |
| 2023 | रासायनिक आबंधन के लिए कोसेल-लुईस दृष्टिकोण / आबंध प्राचल / MOT | अष्टक नियम / आबंध एन्थैल्पी / द्विध्रुव आघूर्ण / आबंध क्रम / आणविक कक्षकों की ऊर्जा | 3 | औसत | लुईस संरचनाएँ, MO सिद्धांत, और विभिन्न आबंध गुण। |
| 2022 | VSEPR सिद्धांत और संकरण / संयोजकता आबंध और आणविक कक्षक सिद्धांत | संरचना और संकरण / VSEPR सिद्धांत / आणविक कक्षक सिद्धांत / आबंध क्रम | 1 | औसत | VSEPR, VB सिद्धांत, और MO सिद्धांत का उपयोग करके आणविक ज्यामिति की भविष्यवाणी। |
| 2021 | VSEPR सिद्धांत / VBT | आकार / संकरण | 1 | आसान | आणविक आकार और संकरण की भविष्यवाणी। |
| 2020 | आबंध प्राचल / आणविक कक्षक सिद्धांत | अंतराअणुक बल / द्विध्रुव आघूर्ण / आबंध क्रम | 1 | आसान | आबंध प्राचलों (द्विध्रुव आघूर्ण, आबंध क्रम) को अंतराअणुक बलों और MO सिद्धांत से जोड़ना। |
| 2019 | समपरमाणुक / द्विपरमाणुक अणुओं में आबंधन / आणविक कक्षक सिद्धांत / संयोजकता आबंध सिद्धांत | आणविक कक्षक विन्यास / अणु की संरचना | 2 | औसत | द्विपरमाणुक अणुओं पर MO और VB सिद्धांतों का अनुप्रयोग: संरचना और MO विन्यास। |
| 2018 | VSEPR सिद्धांत / आणविक कक्षक सिद्धांत / आयनिक / सहसंयोजक आबंध | अणु की संरचना / आबंध क्रम / आणविक कक्षक विन्यास | 2 | औसत/आसान | आबंध प्रकार, MO सिद्धांत, VSEPR, और संरचना भविष्यवाणी। |
| 2017 | आणविक कक्षक सिद्धांत / VSEPR सिद्धांत | आबंध क्रम / अनुचुंबकीय / प्रतिचुंबकीय / समइलेक्ट्रॉनिक / समसंरचनात्मक | 1 | औसत | चुंबकीय गुणों, आबंध क्रम, समइलेक्ट्रॉनिकता और समसंरचनात्मकता के लिए MO सिद्धांत का उपयोग। |
संबंधित वीडियो
रासायनिक आबंधन एवं आणविक संरचना अध्ययन नोट्स
विषय सूची
- संकरण
- द्विध्रुव आघूर्ण
- फजान का नियम
- जालक एन्थैल्पी
- अनुनाद
- सहसंयोजक आबंधन
- सारांश
1. संकरण
परिभाषा
संकरण नए संकर कक्षक बनाने के लिए परमाणु कक्षकों का मिश्रण है।
मुख्य बिंदु
- संकरण तब होता है जब परमाणु आबंध बनाते हैं।
- यह अणुओं की ज्यामिति की व्याख्या करता है।
- सामान्य प्रकारों में sp, sp², और sp³ संकरण शामिल हैं।
उदाहरण
- sp संकरण: रैखिक ज्यामिति (जैसे, CO₂)
- sp² संकरण: त्रिकोणीय समतलीय ज्यामिति (जैसे, BF₃)
- sp³ संकरण: चतुष्फलकीय ज्यामिति (जैसे, CH₄)
2. द्विध्रुव आघूर्ण
परिभाषा
द्विध्रुव आघूर्ण (μ) एक आबंध की ध्रुवता का माप है, जो सूत्र द्वारा दिया जाता है:
μ = q ⋅ r
- q: आवेश
- r: आवेशों के बीच की दूरी
मुख्य बिंदु
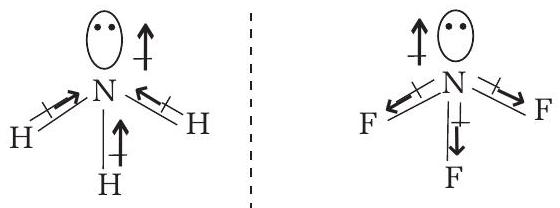
- द्विध्रुव आघूर्ण एक सदिश राशि है।
- इसका उपयोग अणुओं की ध्रुवता निर्धारित करने के लिए किया जाता है।
- ध्रुवीय अणुओं का एक शुद्ध द्विध्रुव आघूर्ण होता है।
3. फजान का नियम
परिभाषा
फजान का नियम आयनिक आबंधों में सहसंयोजक लक्षण की मात्रा की भविष्यवाणी करता है।
मुख्य बिंदु
- छोटे धनायन और बड़े ऋणायन अधिक सहसंयोजक लक्षण की ओर ले जाते हैं।
- आयनों का आकार ऋणायन के ध्रुवीकरण को प्रभावित करता है।
- ध्रुवीकरण क्षमता धनायन के आवेश के साथ बढ़ती है और उसके आकार के साथ घटती है।
उदाहरण
- NaCl, MgO की तुलना में अधिक आयनिक है, क्योंकि इसमें शामिल आयनों के आकार और आवेश के कारण।
4. जालक एन्थैल्पी
परिभाषा
जालक एन्थैल्पी वह ऊर्जा है जो गैसीय आयनों के एक आयनिक ठोस बनने पर मुक्त होती है।
मुख्य बिंदु
- यह एक आयनिक यौगिक की स्थिरता का माप है।
- यह एक आयनिक ठोस को गैसीय आयनों में विघटित करने की प्रक्रिया का विपरीत है।
- उच्च जालक एन्थैल्पी अधिक स्थिर आयनिक यौगिक को दर्शाती है।
5. अनुनाद
परिभाषा
अनुनाद वह घटना है जहाँ एक अणु को दो या दो से अधिक वैध लुईस संरचनाओं द्वारा दर्शाया जा सकता है।
मुख्य बिंदु
- अनुनाद संरचनाएँ समतुल्य होती हैं और इनमें कोई वरीयता नहीं होती।
- अनुनाद इलेक्ट्रॉनों को विस्थानीकृत करके अणुओं को स्थिर करता है।
- संयुग्मित तंत्रों में अनुनाद सामान्य है।
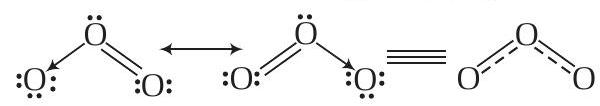
उदाहरण
- ओज़ोन (O₃) की दो अनुनाद संरचनाएँ होती हैं।
- बेंजीन अपनी सुगंधित वलयों में अनुनाद प्रदर्शित करते हैं।
6. सहसंयोजक आबंधन
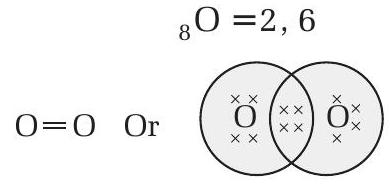
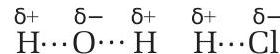
परिभाषा
सहसंयोजक आबंधन (या दाता आबंधन) एक प्रकार का सहसंयोजक आबंध है जहाँ दोनों इलेक्ट्रॉन एक ही परमाणु द्वारा प्रदान किए जाते हैं।
मुख्य बिंदु
- इलेक्ट्रॉन प्रदान करने वाले परमाणु को दाता कहा जाता है।
- इलेक्ट्रॉन स्वीकार करने वाले परमाणु को ग्राही कहा जाता है।
- NH₄⁺ और BF₃ जैसे संकुलों और अणुओं में सामान्य।
उदाहरण
- NH₃ + H⁺ → NH₄⁺
- BF₃ + NH₃ → F₃B←NH₃
7. सारांश
| अवधारणा | परिभाषा | मुख्य सूत्र/संबंध |
|---|---|---|
| संकरण | नए संकर कक्षक बनाने के लिए परमाणु कक्षकों का मिश्रण | - sp, sp², sp³ संकरण |
| द्विध्रुव आघूर्ण | एक आबंध की ध्रुवता का माप | μ = q ⋅ r |
| फजान का नियम | आयनिक आबंधों में सहसंयोजक लक्षण की भविष्यवाणी करता है | छोटे धनायन, बड़े ऋणायन → अधिक सहसंयोजक |
| जालक एन्थैल्पी | गैसीय आयनों के एक आयनिक ठोस बनने पर मुक्त ऊर्जा | - उच्च जालक एन्थैल्पी → अधिक स्थिर आयनिक यौगिक |
| अनुनाद | अणुओं का दो या दो से अधिक वैध लुईस संरचनाओं द्वारा निरूपण | - इलेक्ट्रॉनों का विस्थानीकरण |
| सहसंयोजक आबंधन | वह आबंध जहाँ दोनों इलेक्ट्रॉन एक ही परमाणु द्वारा प्रदान किए जाते हैं | - दाता और ग्राही की अवधारणा |
निष्कर्ष
- संकरण, द्विध्रुव आघूर्ण, फजान का नियम, जालक एन्थैल्पी, अनुनाद, और सहसंयोजक आबंधन रासायनिक आबंधन और आणविक संरचना की मूलभूत अवधारणाएँ हैं।
- ये अवधारणाएँ आणविक ज्यामिति, ध्रुवता और स्थिरता को समझने में सहायता करती हैं।
- ये रासायनिक अभिक्रियाओं में अणुओं के व्यवहार की भविष्यवाणी और व्याख्या करने के लिए आवश्यक हैं।



