भौतिक एवं रासायनिक साम्यावस्था भाग1
JEE में विषय का महत्व
| मापदंड | मान | टिप्पणियाँ |
|---|---|---|
| कुल प्रश्न (2017-2024) | 10 | JEE में प्रत्येक वर्ष कम से कम एक प्रश्न शामिल किया गया है। |
| भारांक | 4.1% | इस विषय से प्रश्नों के अनुपात को दर्शाता है। |
वार्षिक प्रश्न वितरण
| वर्ष | विषय क्षेत्र | समाविष्ट अवधारणाएँ | प्रश्नों की संख्या | कठिनाई स्तर | प्रमुख फोकस क्षेत्र |
|---|---|---|---|---|---|
| 2024 | अम्ल, क्षार एवं लवण | लवण की अम्लीय / क्षारीय प्रकृति | 1 | सरल | लवणों के अम्ल-क्षार गुण |
| 2023 | K, $Q$ और G के बीच संबंध / अम्ल, क्षार एवं लवण / अल्प विलेय लवण की विलेयता साम्यावस्था। | गिब्स ऊर्जा / लुईस अम्ल और लुईस क्षार / विलेयता गुणनफल। | 1 | औसत | ऊष्मागतिकी, अम्ल-क्षार सिद्धांत, और विलेयता |
| 2022 | द्रव्यमान क्रिया का नियम, साम्यावस्था स्थिरांक और इसका अनुप्रयोग / उभयनिष्ठ आयन प्रभाव, लवण जल-अपघटन, बफर विलयन | साम्यावस्था स्थिरांक / $\mathrm{K} _{\mathrm{p}}$ & $\mathrm{K} _{\mathrm{c}} /$ बफर विलयन | 2 | सरल | साम्यावस्था अवधारणाएँ और बफर विलयन |
| 2021 | दुर्बल अम्लों और क्षारों का आयनन और $\mathrm{K} _{\mathrm{a}}$ और $\mathrm{K} _{\mathrm{b}}$ के बीच संबंध | दुर्बल अम्ल और क्षारों का आयनन। | 1 | औसत | दुर्बल अम्ल-क्षार साम्यावस्था |
| 2020 | अम्ल, क्षार और लवण/ अल्प विलेय लवण की विलेयता/ साम्यावस्था स्थिरांक और गिब्स ऊर्जा के बीच संबंध | विलयन का pH /विलेयता / मुक्त ऊर्जा और साम्यावस्था स्थिरांक के बीच संबंध | 1 | कठिन | pH, विलेयता, और साम्यावस्था की ऊष्मागतिकी |
| 2019 | बफर विलयन, अल्प विलेय लवण की विलेयता/अम्ल, क्षार और लवण | बफर विलयन $/ \mathrm{K}_{\text {sp }} /$ अम्ल और क्षारों का आयनन/अम्ल और क्षार | 2 | औसत | बफर विलयन, विलेयता, और अम्ल-क्षार रसायन |
| 2018 | रासायनिक साम्यावस्था का नियम/अम्ल, क्षार और लवण/ अनुप्रयोग/साम्यावस्था को प्रभावित करने वाले कारक/ बफर विलयन/अल्प विलेय लवण की विलेयता | साम्यावस्था स्थिरांक/विलयन का pH/ले शातेलिए सिद्धांत/ $\mathrm{K} _{\text {sp }}$ | 1 | औसत | साम्यावस्था, ले शातेलिए का सिद्धांत, और विलेयता |
| 2017 | बफर विलयन, अल्प विलेय लवण की विलेयता/रासायनिक साम्यावस्था का नियम/ अम्ल, क्षार और लवण | बफर विलयन/विलेयता गुणनफल/साम्यावस्था स्थिरांक/ अम्ल और क्षारों का आयनन/अम्ल और क्षार | 1 | औसत | बफर, विलेयता, और साम्यावस्था स्थिरांक |
संबंधित वीडियो
अध्ययन नोट्स: रासायनिक साम्यावस्था
विषयसूची
- रासायनिक साम्यावस्था का परिचय
- गतिक साम्यावस्था और साम्यावस्था स्थिरांक
- ले शातेलिए का सिद्धांत
- साम्यावस्था को प्रभावित करने वाले कारक
- साम्यावस्था का गणितीय निरूपण
- वियोजन की मात्रा और घनत्व
- सारांश और प्रमुख अवधारणाएँ
1. रासायनिक साम्यावस्था का परिचय
रासायनिक साम्यावस्था क्या है?
रासायनिक साम्यावस्था एक ऐसी अवस्था है जिसमें अभिकारकों और उत्पादों की सांद्रताएँ समय के साथ स्थिर रहती हैं क्योंकि अग्र अभिक्रिया की दर पश्च अभिक्रिया की दर के बराबर होती है।
परिभाषा: गतिक साम्यावस्था एक ऐसी अवस्था है जहाँ अग्र और पश्च अभिक्रियाएँ समान दर पर होती रहती हैं, जिसके परिणामस्वरूप अभिकारकों और उत्पादों की सांद्रताओं में कोई शुद्ध परिवर्तन नहीं होता।
2. गतिक साम्यावस्था और साम्यावस्था स्थिरांक
गतिक साम्यावस्था
- गतिक का अर्थ है कि अभिक्रियाएँ होती रहती हैं, लेकिन अभिकारकों और उत्पादों की सांद्रताएँ स्थिर रहती हैं।
- निकाय एक स्थायी अवस्था में होता है।
साम्यावस्था स्थिरांक (K)
- साम्यावस्था स्थिरांक एक ऐसा मान है जो साम्यावस्था पर उत्पादों और अभिकारकों की सांद्रताओं के अनुपात का वर्णन करता है।
- इसकी गणना निम्न सूत्र का उपयोग करके की जाती है:
$$ K = \dfrac{[\text{Products}]^{\text{coefficients}}}{[\text{Reactants}]^{\text{coefficients}}} $$
नोट: $ K $ का मान तापमान पर निर्भर करता है।
3. ले शातेलिए का सिद्धांत
ले शातेलिए के सिद्धांत का कथन
- यदि साम्यावस्था में स्थित किसी निकाय को परिस्थितियों (सांद्रता, दाब, तापमान) में परिवर्तन द्वारा विचलित किया जाता है, तो निकाय उस विचलन का प्रतिकार करने के लिए स्थानांतरित होगा और साम्यावस्था को पुनः स्थापित करेगा।
ले शातेलिए के सिद्धांत के उदाहरण
| विचलन | साम्यावस्था पर प्रभाव | उदाहरण |
|---|---|---|
| अभिकारकों की सांद्रता में वृद्धि | दाईं ओर स्थानांतरण (उत्पादों की ओर) | निकाय में अधिक अभिकारक मिलाना |
| दाब में वृद्धि (गैसों के लिए) | कम मोल वाली गैस की ओर स्थानांतरण | $ \text{N}_2 + 3\text{H}_2 \rightleftharpoons 2\text{NH}_3 $ |
| तापमान में वृद्धि | ऊष्माशोषी अभिक्रिया की दिशा में स्थानांतरण | $ \text{N}_2\text{O}_4 \rightleftharpoons 2\text{NO}_2 $ (ऊष्माशोषी) |
| उत्प्रेरक की उपस्थिति | साम्यावस्था में कोई स्थानांतरण नहीं, केवल दर प्रभावित होती है | उत्प्रेरक अग्र और पश्च दोनों अभिक्रियाओं की गति बढ़ाता है |
4. साम्यावस्था को प्रभावित करने वाले कारक
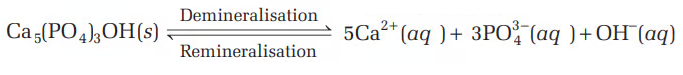
4.1 सांद्रता परिवर्तन का प्रभाव
- अभिकारकों या उत्पादों की सांद्रता बदलने से साम्यावस्था स्थानांतरित होती है।
- ले शातेलिए का सिद्धांत: यदि अधिक अभिकारक मिलाया जाता है, तो निकाय अधिक उत्पाद बनाने के लिए स्थानांतरित होता है।
4.2 दाब का प्रभाव
- गैसों से संबंधित अभिक्रियाओं के लिए, दाब बढ़ाने से साम्यावस्था कम मोल वाली गैस की ओर स्थानांतरित होती है।
- उदाहरण: $ \text{N}_2 + 3\text{H}_2 \rightleftharpoons 2\text{NH}_3 $ – दाब बढ़ाने पर $ \text{NH}_3 $ के निर्माण को प्राथमिकता मिलती है।
4.3 तापमान का प्रभाव
- तापमान बढ़ाने पर अभिक्रिया की ऊष्माशोषी दिशा को प्राथमिकता मिलती है।
- उदाहरण: अभिक्रिया $ \text{N}_2\text{O}_4 \rightleftharpoons 2\text{NO}_2 $, जो ऊष्माशोषी है, के लिए तापमान बढ़ाने पर $ \text{NO}_2 $ के निर्माण को प्राथमिकता मिलती है।
4.4 उत्प्रेरक का प्रभाव
- एक उत्प्रेरक अग्र और पश्च दोनों अभिक्रियाओं की गति बढ़ाता है लेकिन साम्यावस्था को स्थानांतरित नहीं करता।
- महत्वपूर्ण: उत्प्रेरक साम्यावस्था की स्थिति को प्रभावित नहीं करते, केवल साम्यावस्था तक पहुँचने की दर को प्रभावित करते हैं।
4.5 अक्रिय गैस का प्रभाव
- स्थिर आयतन पर एक अक्रिय गैस (एक ऐसी गैस जो निकाय के साथ अभिक्रिया नहीं करती) मिलाने से साम्यावस्था पर कोई प्रभाव नहीं पड़ता।
- यदि आयतन बढ़ाया जाता है, तो दाब कम हो जाता है, और निकाय अधिक मोल वाली गैस की ओर स्थानांतरित होता है।
5. साम्यावस्था का गणितीय निरूपण
एक सामान्य अभिक्रिया के लिए साम्यावस्था व्यंजक
एक सामान्य अभिक्रिया के लिए:
$$ aA + bB \rightleftharpoons cC + dD $$
साम्यावस्था स्थिरांक है:
$$ K_c = \dfrac{[C]^c [D]^d}{[A]^a [B]^b} $$
नोट: $ K_c $ की इकाइयाँ अभिक्रिया पर निर्भर करती हैं, लेकिन कई मामलों में, यदि सांद्रताओं को सक्रियता के रूप में व्यक्त किया जाता है तो $ K $ इकाईहीन होता है।
6. वियोजन की मात्रा और घनत्व
वियोजन की मात्रा और घनत्व के बीच संबंध
- वियोजन की मात्रा ($ \alpha $) निकाय के घनत्व में परिवर्तन से संबंधित है।
- एक अभिक्रिया जैसे:
$$ \text{AB} \rightleftharpoons \text{A} + \text{B} $$
के लिए वियोजन की मात्रा दी जाती है:
$$ \alpha = \dfrac{D - d}{d(y - 1)} $$
जहाँ:
- $ D $ प्रारंभिक घनत्व है
- $ d $ अंतिम घनत्व है
- $ y $ मोलर द्रव्यमान अनुपात (या कुछ अन्य परिभाषित कारक) है
महत्वपूर्ण: प्रायोगिक घनत्व माप से वियोजन की मात्रा निर्धारित करने में यह संबंध उपयोगी है।
7. सारांश और प्रमुख अवधारणाएँ
प्रमुख अवधारणाओं का पुनरावलोकन
| अवधारणा | विवरण |
|---|---|
| रासायनिक साम्यावस्था | एक अवस्था जहाँ अग्र और पश्च अभिक्रियाओं की दरें समान होती हैं। |
| साम्यावस्था स्थिरांक (K) | साम्यावस्था पर उत्पादों और अभिकारकों की सांद्रताओं का अनुपात। |
| ले शातेलिए का सिद्धांत | साम्यावस्था में स्थित निकाय किसी विचलन का प्रतिकार करने के लिए स्थानांतरित होगा। |
| साम्यावस्था को प्रभावित करने वाले कारक | सांद्रता, दाब, तापमान, उत्प्रेरक, और अक्रिय गैसें। |
| वियोजन की मात्रा | एक माप कि किसी अभिक्रिया में कोई पदार्थ कितना वियोजित होता है। |
8. महत्वपूर्ण सूत्र
| सूत्र | विवरण |
|---|---|
| $ K = \dfrac{[\text{Products}]^{\text{coefficients}}}{[\text{Reactants}]^{\text{coefficients}}} $ | साम्यावस्था स्थिरांक व्यंजक |
| $ \alpha = \dfrac{D - d}{d(y - 1)} $ | घनत्व के पदों में वियोजन की मात्रा |
9. उदाहरण
उदाहरण 1: साम्यावस्था स्थिरांक गणना
अभिक्रिया के लिए:
$$ \text{N}_2 + 3\text{H}_2 \rightleftharpoons 2\text{NH}_3 $$
यदि साम्यावस्था सांद्रताएँ हैं:
- $ [\text{N}_2] = 0.1 $ M
- $ [\text{H}_2] = 0.3 $ M
- $ [\text{NH}_3] = 0.2 $ M
तब:
$$ K_c = \dfrac{(0.2)^2}{(0.1)(0.3)^3} = \dfrac{0.04}{0.0027} \approx 14.81 $$
10. निष्कर्ष
- रासायनिक साम्यावस्था एक गतिक अवस्था है जिसमें निकाय संतुलन में रहता है।
- साम्यावस्था स्थिरांक और ले शातेलिए का सिद्धांत साम्यावस्था प्रणालियों के व्यवहार की भविष्यवाणी और समझ के लिए आवश्यक उपकरण हैं।
- तापमान, दाब और सांद्रता जैसे बाह्य कारक साम्यावस्था को स्थानांतरित कर सकते हैं, लेकिन उत्प्रेरक साम्यावस्था की स्थिति को नहीं बदलते।
- वियोजन की मात्रा और घनत्व के बीच संबंध गैसों और विलयनों में वियोजन का विश्लेषण करने के लिए एक उपयोगी विधि है।



