अध्याय 08 रेडॉक्स अभिक्रियाएं
“जहां ऑक्सीकरण होता है, वहां हमेशा अपचयन भी होता है। रसायन विज्ञान मूल रूप से रेडॉक्स प्रणालियों के अध्ययन का अध्ययन है।”
रसायन विज्ञान विभिन्न पदार्थों और एक पदार्थ के दूसरे पदार्थ में परिवर्तन के अध्ययन के बारे में है। एक पदार्थ से दूसरे पदार्थ में पदार्थ के परिवर्तन विभिन्न प्रकार की अभिक्रियाओं के माध्यम से होता है। इस प्रकार की अभिक्रियाओं की एक महत्वपूर्ण श्रेणी रेडॉक्स अभिक्रियाएं हैं। रेडॉक्स अभिक्रियाओं के साथ-साथ भौतिक और जैविक घटनाएं भी संबंधित होती हैं। ये अभिक्रियाएं औषधीय, जैविक, औद्योगिक, खनिज और कृषि क्षेत्रों में व्यापक रूप से उपयोग में लाई जाती हैं। इन अभिक्रियाओं की महत्वता इस तथ्य से स्पष्ट होती है कि घरेलू, परिवहन और अन्य व्यापारिक उद्देश्यों के लिए ऊर्जा प्राप्त करने के लिए विभिन्न प्रकार के ईंधन के जलने, उच्च प्रतिस्पर्धी धातु और अधातुओं के निस्पत्ति के लिए विद्युत रासायनिक प्रक्रम, कास्टिक सोडा जैसे रासायनिक यौगिकों के निर्माण, सूखे और नम बैटरी के संचालन और धातुओं के विरोधाभास के अंतर्गत रेडॉक्स प्रक्रमों के अंतर्गत आते हैं। हाल के वर्षों में, हाइड्रोजन अर्थव्यवस्था (तरल हाइड्रोजन के रूप में ईंधन का उपयोग) और ‘ओजोन छेद’ के विकास जैसे पर्यावरण संबंधी मुद्दे रेडॉक्स घटनाओं के अंतर्गत आने लगे हैं।
8.1 रेडॉक्स अभिक्रियाओं की क्लासिकल धारणा - ऑक्सीकरण और अपचायन अभिक्रियाएं
प्रारंभ में, “ऑक्सीकरण” शब्द का उपयोग एक तत्व या यौगिक में ऑक्सीजन के योग के वर्णन के लिए किया जाता था। वातावरण में डाइऑक्सीजन की उपस्थिति के कारण (20%) कई तत्व इसके साथ संयोजित हो जाते हैं और इसी कारण वे पृथ्वी पर अपने ऑक्साइड के रूप में आमतौर पर पाए जाते हैं। नीचे दिए गए अभिक्रियाएं ऑक्सीकरण की सीमित परिभाषा के अनुसार ऑक्सीकरण प्रक्रियाओं को प्रस्तुत करती हैं:
$$2 \mathrm{Mg}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{MgO}(\mathrm{s}) \tag{8.1}$$
$$\mathrm{S}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow \mathrm{SO_2}(\mathrm{~g}) \tag{8.2}$$
अभिक्रिया (8.1) और (8.2) में, मैग्नीशियम और सल्फर तत्वों में ऑक्सीजन के योग से ऑक्सीकृत होते हैं। इसी तरह, मेथेन ऑक्सीजन के योग के कारण ऑक्सीकृत होता है।
$$\mathrm{CH} _{4}(\mathrm{~g})+2 \mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g})+2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{7.3}$$
अभिक्रिया (8.3) के ध्यानपूर्वक अध्ययन से, जहाँ हाइड्रोजन के स्थान पर ऑक्सीजन है, रसायनशास्त्रियों को ऑक्सीकरण के अर्थ को हाइड्रोजन के अपसारण के रूप में परिभाषित करने के लिए प्रेरित किया गया। इसलिए, ऑक्सीकरण शब्द के विस्तार के लिए एक वस्तु से हाइड्रोजन के अपसारण को शामिल कर लिया गया। नीचे दिया गया उदाहरण एक अभिक्रिया है जहाँ हाइड्रोजन के अपसारण को ऑक्सीकरण अभिक्रिया के रूप में भी देखा जा सकता है।
$$ \begin{equation*} 2 \mathrm{H_2} \mathrm{~S}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{~S}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \tag{8.4} \end{equation*} $$
जैसे-जैसे रसायनज्ञों के ज्ञान में वृद्धि हुई, इसके लिए आसानी से अभिक्रियाओं (7.1 से 7.4) के लिए ऑक्सीकरण शब्द को विस्तारित करना प्राकृतिक था, जो ऑक्सीजन के बिना अन्य विद्युत ऋणात्मक तत्वों के साथ अभिक्रिया करती हैं। मैग्नीशियम के फ्लूओरीन, क्लोरीन और सल्फर आदि के साथ ऑक्सीकरण निम्नलिखित अभिक्रियाओं के अनुसार होता है :
$$\operatorname{Mg}(\mathrm{s})+\mathrm{F_2} (\mathrm{~g}) \rightarrow \operatorname{MgF_2} (s) \tag{8.5}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{Cl_2} (g) \rightarrow \mathrm{MgCl_2} (s) \tag{8.6}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{S} (s) \rightarrow \operatorname{MgS}(\mathrm{s}) \tag{8.7}$$
अभिक्रिया 7.5 से 7.7 के अंतर्गत ऑक्सीकरण अभिक्रियाओं के ढांचे में शामिल करने से रसायन विशेषज्ञों को अब न केवल हाइड्रोजन के अपसारण को ऑक्सीकरण मानने के अलावा, धनात्मक विद्युत धारित तत्वों के अपसारण को भी ऑक्सीकरण मानने के लिए प्रेरित किया गया। इस प्रकार अभिक्रिया :
$$ 2 \mathrm{~K_4} \left[ \mathrm{Fe} ( \mathrm{CN})_{6} \right] ( \mathrm{aq}) + \mathrm{H_2} \mathrm{O_2} ( \mathrm{aq}) \rightarrow 2 \mathrm{~K_3} \left[\mathrm{Fe}( \mathrm{CN})_6 \right] ( \mathrm{aq}) + 2 \mathrm{KOH} ( \mathrm{aq}) $$
$$
कार्बनेट फेरोसाइएनाइड से पोटेशियम फेर्रिसाइएनाइड में बदलने से पहले पोटेशियम के अपसार के कारण यह ऑक्सीकरण के रूप में व्याख्यान किया जाता है। सारांश के रूप में, “ऑक्सीकरण” शब्द को एक पदार्थ में ऑक्सीजन/इलेक्ट्रोनेगेटिव तत्व के जोड़ के रूप में परिभाषित किया जाता है या एक पदार्थ में हाइड्रोजन/इलेक्ट्रोपॉजिटिव तत्व के अपसार के रूप में।
आरंभ में, अपचयन को एक यौगिक से ऑक्सीजन के अपसार के रूप में विचार किया जाता था। हालांकि, आजकल “अपचयन” शब्द को विस्तारित कर दिया गया है ताकि एक पदार्थ में ऑक्सीजन/इलेक्ट्रोनेगेटिव तत्व के अपसार या हाइड्रोजन/इलेक्ट्रोपॉजिटिव तत्व के जोड़ के रूप में शामिल किया जा सके।
ऊपर दिए गए परिभाषा के आधार पर, निम्नलिखित अपचायक प्रक्रियाओं के उदाहरण हैं:
$$2 \mathrm{HgO}(\mathrm{s}) \xrightarrow{\Delta} 2 \mathrm{Hg}(\mathrm{l})+\mathrm{O_2}(\mathrm{~g}) \tag{8.8}$$
(सीसा ऑक्साइड से ऑक्सीजन के अपसारण)
$$2 \mathrm{FeCl_3}(\mathrm{aq})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{FeCl_2}(\mathrm{aq})+2 \mathrm{HCl}(\mathrm{aq}) \tag{8.9}$$
(फेरिक क्लोराइड से विद्युत ऋणात्मक तत्व, क्लोरीन के अपसारण)
$$\mathrm{CH_2}=\mathrm{CH_2}(\mathrm{~g})+\mathrm{H_2}(\mathrm{~g}) \rightarrow \mathrm{H_3} \mathrm{C}-\mathrm{CH_3}(\mathrm{~g})\tag{8.10}$$
(हाइड्रोजन के योग)
$$2 \mathrm{HgCl_2}(\mathrm{aq})+\mathrm{SnCl_2}(\mathrm{aq}) \rightarrow \mathrm{Hg_2} \mathrm{Cl_2}(\mathrm{~s})+\mathrm{SnCl_4}(\mathrm{aq})\tag{8.11}$$
(मर्करी के अतिरिक्त एक मर्करिक क्लोराइड में)
अभिक्रिया (8.11) में साथ ही स्टैनोस क्लोराइड के ऑक्सीकरण करके स्टैनिक क्लोराइड के निर्माण की घटना भी हो रही है क्योंकि इसमें विद्युत ऋणात्मक तत्व क्लोरीन के योग हो रहा है। इसके तुरंत पहले ही यह देखा गया कि ऑक्सीकरण और अपचयन हमेशा एक साथ होते हैं (ऊपर दिए गए सभी समीकरणों को फिर से देखकर यह स्पष्ट हो जाएगा), इसलिए इस प्रकार की रासायनिक अभिक्रियाओं के लिए “रेडॉक्स” शब्द बनाया गया।
समस्या 8.1
नीचे दिए गए अभिक्रियाओं में, ऑक्सीकरण और अपचयन कर रहे अपवर्जी अणुओं की पहचान करें:
(i) $\mathrm{H_2} \mathrm{~S}$ (g) $+\mathrm{Cl_2}$ (g) $\rightarrow 2 \mathrm{HCl}$ (g) $+\mathrm{S}$ (s)
(ii) $3 \mathrm{Fe_3} \mathrm{O_4}$ (s) $+8 \mathrm{Al}$ (s) $\rightarrow 9 \mathrm{Fe}$ (s) $+4 \mathrm{Al_2} \mathrm{O_3}(\mathrm{~s})$
(iii) $2 \mathrm{Na}$ (s) $+\mathrm{H_2}$ (g) $\rightarrow 2 \mathrm{NaH}$ (s)
हल
(i) $\mathrm{H_2} \mathrm{~S}$ ऑक्सीकृत होता है क्योंकि हाइड्रोजन के लिए अधिक विद्युत ऋणात्मक तत्व, क्लोरीन, हाइड्रोजन के साथ जुड़ गया है (या सल्फर के लिए अधिक विद्युत धनात्मक तत्व, हाइड्रोजन, सल्फर से हट गया है)। क्लोरीन अपचयित होता है क्योंकि इसमें हाइड्रोजन के जुड़े होने के कारण।
(ii) एल्यूमीनियम ऑक्सीकृत होता है क्योंकि ऑक्सीजन इसमें मिल जाती है। लौह लौह ऑक्साइड $\left(\mathrm{Fe_3} \mathrm{O_4}\right)$ अपचयित होता है क्योंकि इसमें ऑक्सीजन को निकाल लिया गया है।
(iii) इलेक्ट्रोनगेटिवता के अवधारणा के साथ ध्यानपूर्वक अनुप्रयोग करके ही हम यह निष्कर्ष निकाल सकते हैं कि सोडियम ऑक्सीकृत होता है और हाइड्रोजन अपचयित होता है।
इस अभिक्रिया (iii) के चयन से हमें रेडॉक्स अभिक्रियाओं को एक अन्य तरीके से परिभाषित करने के लिए सोचने के लिए प्रेरित किया जाता है।
8.2 इलेक्ट्रॉन परिवहन अभिक्रियाओं के अनुसार रेडॉक्स अभिक्रियाएँ
हम पहले से ही सीख चुके हैं कि अभिक्रियाएँ रेडॉक्स अभिक्रियाएँ हैं क्योंकि इन अभिक्रियाओं में से प्रत्येक में सोडियम के ऑक्सीकरण के कारण ऑक्सीजन या अधिक इलेक्ट्रोनगेटिव तत्व के जोड़ने से सोडियम ऑक्सीकृत होता है।
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaCl}(\mathrm{s})\tag{8.12}$$
$$4 \mathrm{Na}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na_2} \mathrm{O}(\mathrm{s})\tag{8.13}$$
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{S}(\mathrm{s}) \rightarrow \mathrm{Na_2} \mathrm{~S}(\mathrm{~s}) \tag{8.14}$$
साथ ही, क्लोरीन, ऑक्सीजन और सल्फर कम हो जाते हैं क्योंकि इनमें से प्रत्येक में विद्युत धनात्मक तत्व सोडियम को जोड़ दिया गया है। हमारे रासायनिक बंधन के ज्ञान से हम भी जानते हैं कि सोडियम क्लोराइड, सोडियम ऑक्साइड और सोडियम सल्फाइड आयनिक यौगिक हैं और शायद बेहतर रूप से लिखे जा सकते हैं के रूप में $\mathrm{Na}^{+} \mathrm{Cl}^{-}( \mathrm{s}),\left(\mathrm{Na}^{+} \right)_2 \mathrm{O}^{2-}( \mathrm{s})$, और $ \left(\mathrm{Na}^{+} \right)_2$ $\mathrm{S}^{2-}( \mathrm{s})$. उत्पादित विशिष्टताओं पर आवेश के विकास से हमें अनुमान लगाने के लिए अभिक्रियाओं (8.12 से 8 तक 8.14) को निम्नलिखित रूप में लिखने के लिए प्रेरित करता है:
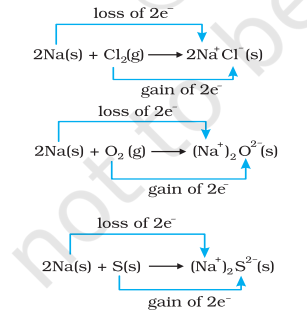
आसानी के लिए, उपरोक्त प्रक्रियाओं में से प्रत्येक को दो अलग-अलग चरणों के रूप में विचार किया जा सकता है, एक में इलेक्ट्रॉनों के नुकसान और दूसरे में इलेक्ट्रॉनों के लाभ। उदाहरण के लिए, हम इनमें से एक को और विस्तार से समझ सकते हैं, जैसे कि सोडियम क्लोराइड के निर्माण।
$2 \mathrm{Na}(\mathrm{s}) \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
$\mathrm{Cl_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{Cl}^{-}(\mathrm{g})$
ऊपर के प्रत्येक कदम को आधा अभिक्रिया कहा जाता है, जो इलेक्ट्रॉन के भाग लेने को विशिष्ट रूप से दर्शाता है। आधा अभिक्रिया के योग से समग्र अभिक्रिया प्राप्त होती है :
$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na}^{+} \mathrm{Cl}^{-}(\mathrm{s})$ या $2 \mathrm{NaCl}(\mathrm{s})$
अभिक्रिया 8.12 से 8.14 तक से स्पष्ट होता है कि इलेक्ट्रॉन के नुकसान वाली आधा अभिक्रियाओं को ऑक्सीकरण अभिक्रिया कहा जाता है। इसी तरह, इलेक्ट्रॉन के लाभ वाली आधा अभिक्रियाओं को अपचयन अभिक्रिया कहा जाता है। यहां यह भी बताना उचित नहीं होगा कि ऑक्सीकरण और अपचयन के नए तरीके की परिभाषा केवल क्लासिक विचार के अनुसार विविध प्रकार के विस्तार के बीच संबंध की स्थापना के बाद ही संभव हुई है। अभिक्रिया (8.12 से 8.14) में, जो ऑक्सीकृत होता है, सोडियम, इलेक्ट्रॉन देकर अपने साथ अंतरक्रिया करने वाले प्रत्येक तत्व को अपचयित करने में सहायता करता है इसलिए एक अपचायक एजेंट के रूप में कार्य करता है। क्लोरीन, ऑक्सीजन और सल्फर अपचयित होते हैं और ऑक्सीकारक एजेंट के रूप में कार्य करते हैं क्योंकि ये सोडियम से इलेक्ट्रॉन ग्रहण करते हैं। संक्षेप में, हम बता सकते हैं कि
उपचयन : किसी भी पदार्थ द्वारा इलेक्ट्रॉन (इलेक्ट्रॉनों) के नुकसान के कारण।
अपचयन : किसी भी पदार्थ द्वारा इलेक्ट्रॉन (इलेक्ट्रॉनों) के लाभ के कारण।
उपचयक : इलेक्ट्रॉन (इलेक्ट्रॉनों) के स्वीकारक।
अपचयक : इलेकट्रॉन (इलेक्ट्रॉनों) के दाता।
समस्या 8.2
समझाइए कि अभिक्रिया: $2 \mathrm{Na}(\mathrm{s})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaH}$ (s) एक रेडॉक्स परिवर्तन है।
हल
ऊपर दी गई अभिक्रिया में बना यौगिक आयनिक यौगिक है, जिसे भी $\mathrm{Na}^{+} \mathrm{H}^{-}$(s) के रूप में दर्शाया जा सकता है, इससे इस प्रक्रिया में एक आधा अभिक्रिया इस प्रकार हो सकती है:
$2 \mathrm{Na}(\mathrm{s}) \quad \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
और दूसरा आधा अभिक्रिया यह है:
$\mathrm{H_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{H}^{-}(\mathrm{g})$
इस अभिक्रिया को दो आधी अभिक्रियाओं में विभाजित करने से स्पष्ट हो जाता है कि यहाँ सोडियम ऑक्सीकृत हो रहा है और हाइड्रोजन अपचयित हो रहा है, इसलिए पूर्ण अभिक्रिया एक रेडॉक्स परिवर्तन है।
8.2.1 प्रतिस्पर्धात्मक इलेक्ट्रॉन स्थानांतरण अभिक्रियाएँ
चित्र 8.1 में दिखाए गए अनुसार एक धातु जिंक की बैंड को कॉपर नाइट्रेट के जलीय घोल में रखें और लगभग एक घंटा तक छोड़ दें। आप ध्यान दें सकते हैं कि बैंड लाल धातु कॉपर के साथ ढक जाता है और घोल के नीले रंग का अपसर चल जाता है। घोल में $\mathrm{Cu}^{2+}$ के कारण नीला रंग चल जाने पर $\mathrm{Zn}^{2+}$ आयनों के निर्माण के बारे में आसानी से निर्णय लिया जा सकता है। यदि हाइड्रोजन सल्फाइड गैस को रंगहीन घोल में $\mathrm{Zn}^{2+}$ आयनों के साथ प्रवाहित किया जाए तो अमोनिया के साथ घोल को क्षारीय बनाने पर श्वेत जिंक सल्फाइड, $\mathrm{ZnS}$ के उत्पादन को देखा जा सकता है।
स्थायी जिंक और कॉपर नाइट्रेट के जलीय घोल के बीच अभिक्रिया निम्नलिखित है :
$$\mathrm{Zn}(\mathrm{s})+\mathrm{Cu}^{2+}(\mathrm{aq}) \rightarrow \mathrm{Zn}^{2+}(\mathrm{aq})+\mathrm{Cu}(\mathrm{s}) \tag{8.15}$$
अभिक्रिया (8.15) में, जिंक इलेक्ट्रॉन खोकर $Zn^{2+}$ के रूप में बन गया है और इसलिए जिंक ऑक्सीकृत हो गया है। स्पष्ट रूप से, अब यदि जिंक ऑक्सीकृत हो रहा है और इलेक्ट्रॉन छोड़ रहा है, तो कुछ चीज इलेक्ट्रॉन ग्रहण करके अपचयित हो रही होनी चाहिए। कॉपर आयन जिंक से इलेक्ट्रॉन प्राप्त करके अपचयित हो जाते हैं।
अभिक्रिया (8.15) को इस प्रकार भी लिखा जा सकता है:
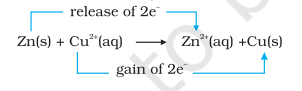
इस स्तर पर हम अभिक्रिया (8.15) के लिए साम्यावस्था की अवस्था की जांच कर सकते हैं। इसके लिए हम एक धातु कॉपर की एक छड़ को जिंक सल्फेट विलयन में रखते हैं। कोई दृश्य अभिक्रिया नहीं दिखाई देती और हम विलयन में $\mathrm{Cu}^{2+}$ आयनों की उपस्थिति को पता लगाने के लिए विलयन में $\mathrm{H_2} \mathrm{~S}$ गैस प्रवाहित करते हैं जिससे कॉपर सल्फाइड, CuS के काले रंग के उत्पाद के निर्माण के लिए प्रयास करते हैं लेकिन यह असफल रहता है। कॉपर सल्फाइड इतना कम विलेय होता है कि यह एक बहुत संवेदनशील परीक्षण होता है; फिर भी $\mathrm{Cu}^{2+}$ के उत्पादित अंश का पता लगाया नहीं जा सकता। इसलिए हम निष्कर्ष निकालते हैं कि अभिक्रिया (8.15) के लिए साम्यावस्था उत्पादों के प्रति अभिकर्मकों की तुलना में बहुत अधिक पक्षपाती होती है।
अब हम इलेक्ट्रॉन परिवहन अभिक्रिया को तांबा धातु और जल में सिल्वर नाइट्रेट विलयन तक विस्तारित करते हैं और चित्र 8.2 में दिखाए गए सेट-अप को व्यवस्थित करते हैं। अभिक्रिया के कारण $\mathrm{Cu}^{2+}$ आयनों के निर्माण के कारण विलयन नीला रंग ले लेता है:
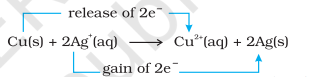
यहाँ, $\mathrm{Cu}(\mathrm{s})$ को $\mathrm{Cu}^{2+}(\mathrm{aq})$ में ऑक्सीकृत किया जाता है और $\mathrm{Ag}^{+}(\mathrm{aq})$ को $\mathrm{Ag}(\mathrm{s})$ में अपचयित किया जाता है। साम्य उत्पाद $\mathrm{Cu}^{2+}(\mathrm{aq})$ और $\mathrm{Ag}(\mathrm{s})$ के अनुकूल है।
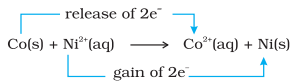
किसी अन्य तुलना के रूप में, चालक एक और तुलना करते हैं जहां धात्विक कोबाल्ट निकल सल्फेट विलयन में रखा जाता है। यहां होने वाली अभिक्रिया निम्नलिखित है :

चित्र 8.1 एक बीकर में जिंक और सिल्वर नाइट्रेट के जलीय घोल के बीच रेडॉक्स अभिक्रिया।
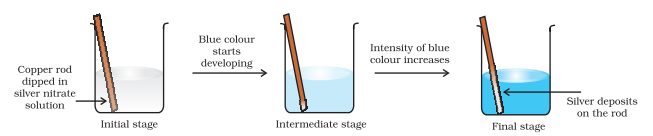
चित्र 8.2 एक बीकर में कॉपर और सिल्वर नाइट्रेट के जलीय घोल के बीच रेडॉक्स अभिक्रिया
संतुलन पर, रासायनिक परीक्षण दर्शाते हैं कि दोनों $\mathrm{Ni}^{2+}(\mathrm{aq})$ और $\mathrm{Co}^{2+}(\mathrm{aq})$ मध्यम सांद्रता में उपस्थित हैं। इस स्थिति में, अभिकर्मक $\left[\mathrm{Co}(\mathrm{s})\right.$ और $\left.\mathrm{Ni}^{2+}(\mathrm{aq})\right]$ या उत्पाद $\left[\mathrm{Co}^{3+}(\mathrm{aq})\right.$ और $\left.\mathrm{Ni}(\mathrm{s})\right]$ दोनों बहुत अधिक प्रभावित नहीं हैं।
इलेक्ट्रॉन विमुक्ति के विस्तार के लिए प्रतियोगिता अम्लों के बीच प्रोटॉन विमुक्ति के लिए प्रतियोगिता के साथ तुलना करती है। इस समानता से हम यह अनुमान लगा सकते हैं कि हम एक ऐसे तालिका के विकास के लिए तैयार हैं जिसमें धातुएँ और उनके आयन अपनी इलेक्ट्रॉन विमुक्ति की प्रवृत्ति के आधार पर सूचीबद्ध होंगे, जैसे कि हम अम्लों के मामले में करते हैं ताकि अम्ल की क्षमता को दर्शाया जा सके। वास्तव में हमने इसकी कुछ तुलना कर चुके हैं। तुलना के माध्यम से हम जान गए हैं कि जिंक कॉपर को इलेक्ट्रॉन देता है और कॉपर सिल्वर को इलेकट्रॉन देता है और इसलिए धातुओं की इलेक्ट्रॉन विमुक्ति की प्रवृत्ति क्रम में होती है: $\mathrm{Zn}>\mathrm{Cu}>\mathrm{Ag}$. हम अपनी सूची को और विस्तारित करना चाहेंगे और धातु गतिशीलता श्रेणी या विद्युतरसायनिक श्रेणी बनाना चाहेंगे। विभिन्न धातुओं के बीच इलेक्ट्रॉन के लिए प्रतियोगिता हमें गैल्वैनिक सेल के एक श्रेणी के डिज़ाइन में सहायता करती है जिसमें रासायनिक अभिक्रियाएँ विद्युत ऊर्जा के स्रोत बन जाती हैं। हम कक्षा XII में इन सेलों के बारे में अधिक अध्ययन करेंगे।
8.3 ऑक्सीकरण संख्या
इलेक्ट्रॉन परिवहन का एक कम ज्ञात उदाहरण जब हाइड्रोजन ऑक्सीजन के साथ संयोजित होकर जल बनाता है, तब होता है:
$$2 \mathrm{H_2}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{H_2} \mathrm{O}(\mathrm{l})\tag{8.18}$$
हालांकि इसकी विधि सरल नहीं है, लेकिन हम $\mathrm{H}$ परमाणु को $\mathrm{H_2}$ में उदासीन (शून्य) अवस्था से $\mathrm{H_2} \mathrm{O}$ में धनात्मक अवस्था में बदले जाने के रूप में कल्पना कर सकते हैं, जबकि $\mathrm{O}$ परमाणु $\mathrm{O_2}$ में शून्य अवस्था से $\mathrm{H_2} \mathrm{O}$ में दुनिया ऋणात्मक अवस्था में बदल जाता है। मान लीजिए कि $\mathrm{H}$ से $\mathrm{O}$ में इलेक्ट्रॉन परिवहन होता है और इसलिए $\mathrm{H_2}$ ऑक्सीकृत हो जाता है और $\mathrm{O_2}$ अपचयित हो जाता है।
हालांकि, बाद में हम देखेंगे कि आवेश परिवहन केवल आंशिक होता है और यह शायद एक इलेक्ट्रॉन विस्थापन के रूप में बेहतर वर्णित किया जा सकता है, जबकि $\mathrm{H}$ द्वारा इलेक्ट्रॉन का पूर्ण खोना और O द्वारा इलेक्ट्रॉन का प्राप्त करना नहीं होता। इस बात के संदर्भ में विवरण (8.18) के संबंध में कहा गया है कि यह एक अच्छी संख्या में अन्य अभिक्रियाओं के लिए भी सत्य हो सकता है, जिनमें सहसंयोजक यौगिकों की शामिल होती है। इस श्रेणी की दो ऐसी उदाहरण हैं:
$$\mathrm{H_2}(\mathrm{~s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{HCl}(\mathrm{g})\tag{8.19}$$
और,
$$\mathrm{CH_4}(\mathrm{~g})+4 \mathrm{Cl_2}(\mathrm{~g}) \rightarrow \mathrm{CCl_4}(\mathrm{l})+4 \mathrm{HCl}(\mathrm{g})\tag{8.20}$$
अतिरिक्त इलेक्ट्रॉन विस्थापन के लेखन के लिए एक अधिक प्रायोगिक विधि विकसित की गई है। इस विधि में, हमेशा यह माना जाता है कि कम विद्युत ऋणात्मक अणु से अधिक विद्युत ऋणात्मक अणु में इलेक्ट्रॉन का पूर्ण अंतरण होता है। उदाहरण के लिए, हम समीकरण (8.18 से 8.20) को लिखते हैं ताकि प्रत्येक अणु के आवेश को दिखाया जा सके :
$$ \begin{array}{cccc} 2 \stackrel{0}{\mathrm{H_2}}(\mathrm{~g}) + \stackrel{0}{\mathrm{O_2}}(\mathrm{~g}) & \rightarrow & 2 \stackrel{+1}{\mathrm{H_2}} \stackrel{-2}{\mathrm{O}}(\mathrm{l}) \tag{8.21}
\end{array} $$
$$ \begin{array}{llll} \stackrel {0}{\mathrm{H_2}}(\mathrm{~s}) + \stackrel{0}{\mathrm{Cl_2}}(\mathrm{~g}) & \rightarrow & 2 \stackrel{+1-1}{\mathrm{HCl}}(\mathrm{g}) \tag{8.22} \end{array} $$
$$ \begin{array}{cccc} \stackrel{-4 +1}{\mathrm{CH_4}}(\mathrm{~g}) + & 4 \stackrel{0}{\mathrm{Cl_2}}(\mathrm{~g}) \rightarrow & \stack \stackrel{+4 -1}{\mathrm{C}\mathrm{Cl_4}} (\mathrm{l})+4 \stackrel{+1 -1 }{\mathrm{H } \mathrm{Cl}} (\mathrm{g})\tag{8.23} \end{array} $$
उल्लेखनीय है कि इलेक्ट्रॉन परिवहन के अनुमान केवल बुक कीपिंग के उद्देश्य के लिए किया जाता है और इकाई के बाद चरण में यह स्पष्ट हो जाएगा कि यह रेडॉक्स अभिक्रियाओं के सरल वर्णन के लिए जाता है।
ऑक्सीकरण संख्या एक यौगिक में एक तत्व के ऑक्सीकरण अवस्था को बताती है, जो एक नियमों के आधार पर निर्धारित की जाती है, जो यह मानते हुए बनाए गए हैं कि सहसंयोजक बंध में इलेक्ट्रॉन युग्म अधिक विद्युत ऋणात्मक तत्व के पूरी तरह से स्वामी होता है।
एक यौगिक/आयन में आसानी से यह याद रखना या निर्धारित करना कि कौन सा तत्व दूसरे तत्व की तुलना में अधिक विद्युत ऋणात्मक है, हमेशा संभव नहीं होता। इसलिए, एक सेट नियमों के निर्माण के लिए एक यौगिक/आयन में एक तत्व की ऑक्सीकरण संख्या निर्धारित करने के लिए नियम बनाए गए हैं। यदि एक यौगिक/आयन में एक तत्व के दो या दो से अधिक परमाणु उपस्थित हों, जैसे $\mathrm{Na_2} \mathrm{~S_2} \mathrm{O_3} / \mathrm{Cr_2} \mathrm{O_7}^{2-}$, तो उस तत्व के परमाणु की ऑक्सीकरण संख्या उस तत्व के सभी परमाणुओं की ऑक्सीकरण संख्या के औसत के बराबर होगी। इस चरण में हम ऑक्सीकरण संख्या की गणना के लिए नियम बता सकते हैं। ये नियम हैं:
1. तत्वों में, मुक्त या संयोजन अवस्था में, प्रत्येक परमाणु के ऑक्सीकरण संख्या शून्य होती है। स्पष्ट रूप से $\mathrm{H_2}, \mathrm{O_2}, \mathrm{Cl_2}, \mathrm{O_3}, \mathrm{P_4}, \mathrm{~S_8}, \mathrm{Na}, \mathrm{Mg}, \mathrm{Al}$ में प्रत्येक परमाणु के ऑक्सीकरण संख्या शून्य होती है।
2. एक एकल परमाणु से बने आयनों के लिए, ऑक्सीकरण संख्या आयन पर आवेश के बराबर होती है। इसलिए $\mathrm{Na}^{+}$ आयन के ऑक्सीकरण संख्या $+1$, $\mathrm{Mg}^{2+}$ आयन के ऑक्सीकरण संख्या $+2$, $\mathrm{Fe}^{3+}$ आयन के ऑक्सीकरण संख्या +3, $\mathrm{Cl}^{-}$ आयन के ऑक्सीकरण संख्या $-1$, $\mathrm{O}^{2-}$ आयन के ऑक्सीकरण संख्या -2 होती है आदि। अपने यौगिकों में सभी क्षार धातुएं +1 के ऑक्सीकरण संख्या के साथ होती हैं, और सभी क्षारीय भूमि धातुएं +2 के ऑक्सीकरण संख्या के साथ होती हैं। एल्यूमिनियम के सभी यौगिकों में इसे +3 के ऑक्सीकरण संख्या के रूप में देखा जाता है।
3. अधिकांश यौगिकों में ऑक्सीजन की ऑक्सीकरण संख्या -2 होती है। हालांकि, यहां दो प्रकार के अपवाद होते हैं। एक विशेषता परॉक्साइड और सुपरऑक्साइड के मामले में होती है, जहां ऑक्सीजन के परमाणु एक दूसरे के सीधे जुड़े होते हैं। परॉक्साइड में (जैसे, $\mathrm{H_2} \mathrm{O_2}$, $\mathrm{Na_2} \mathrm{O_2}$), प्रत्येक ऑक्सीजन परमाणु की ऑक्सीकरण संख्या -1 होती है, जबकि सुपरऑक्साइड में (जैसे, $\mathrm{KO_2}$, $\mathrm{RbO_2}$) प्रत्येक ऑक्सीजन परमाणु की ऑक्सीकरण संख्या $-(1/2)$ होती है। दूसरा अपवाद बहुत घट घट आता है, अर्थात जब ऑक्सीजन फ्लुओरीन के साथ बंधे होते हैं। ऐसे यौगिकों में, जैसे, ऑक्सीजन डाइफ्लुओराइड $\left(\mathrm{OF_2}\right)$ और डाइऑक्सीजन डाइफ्लुओराइड $\left(\mathrm{O_2} \mathrm{~F_2}\right)$, ऑक्सीजन की ऑक्सीकरण संख्या क्रमशः +2 और +1 होती है। ऑक्सीजन की ऑक्सीकरण संख्या ऑक्सीजन के बंधन के अवस्था पर निर्भर करेगी, लेकिन अब यह संख्या धनात्मक होगी।
4. हाइड्रोजन की ऑक्सीकरण संख्या +1 होती है, बिना धातुओं के साथ द्वितीयक यौगिकों में जुड़े होने के अतिरिक्त। उदाहरण के लिए, $\mathrm{LiH}, \mathrm{NaH}$ और $\mathrm{CaH_2}$ में इसकी ऑक्सीकरण संख्या -1 होती है।
5. सभी अपने यौगिकों में फ्लूओरीन की ऑक्सीकरण संख्या -1 होती है। अन्य हैलोजन $(\mathrm{Cl}$, $\mathrm{Br}$ और I) भी अपने यौगिकों में हैलाइड आयन के रूप में उपस्थित होने पर ऑक्सीकरण संख्या -1 होती है। क्लोरीन, ब्रोमीन और आयोडीन जब ऑक्सीजन के साथ संयोजित होते हैं, उदाहरण के लिए ऑक्सोएसिड और ऑक्सोएनियन में, उनकी ऑक्सीकरण संख्या धनात्मक होती है।
6. किसी यौगिक में सभी परमाणुओं के ऑक्सीकरण संख्या का बीजगणितीय योग शून्य होना चाहिए। एक बहुपरमाणुक आयन में सभी परमाणुओं के ऑक्सीकरण संख्या का बीजगणितीय योग आयन के आवेश के बराबर होना चाहिए। इसलिए, कार्बोनेट आयन, $\left(\mathrm{CO_3}\right)^{2-}$ में तीन ऑक्सीजन परमाणु और एक कार्बन परमाणु के ऑक्सीकरण संख्या का योग -2 होना चाहिए।
उपरोक्त नियमों के अनुप्रयोग से हम किसी अणु या आयन में चाहे गए तत्व की ऑक्सीकरण संख्या ज्ञात कर सकते हैं। स्पष्ट है कि धातु तत्वों के ऑक्सीकरण संख्या धनात्मक होती है और अधातु तत्वों के ऑक्सीकरण संख्या धनात्मक या ऋणात्मक हो सकती है। संक्रमण तत्वों के परमाणु आमतौर पर कई धनात्मक ऑक्सीकरण संख्या दर्शाते हैं। प्रतिनिधि तत्व के उच्चतम ऑक्सीकरण संख्या पहले दो समूहों के लिए समूह संख्या होती है और अन्य समूहों के लिए लंबे रूप के आवर्त सारणी के अनुसार समूह संख्या कम 10 होती है। इसलिए, यह बताता है कि आवर्त सारणी में एक तत्व के परमाणु के द्वारा दिखाए गए उच्चतम ऑक्सीकरण संख्या का मान आवर्त में बढ़ते हुए बदलता रहता है। तीसरे आवर्त में, तत्वों के यौगिकों में उच्चतम ऑक्सीकरण संख्या 1 से 7 तक बदलती है, जैसा कि नीचे दिखाया गया है।
एक शब्द जो ऑक्सीकरण संख्या के साथ अक्सर बदल बैठकर प्रयोग किया जाता है, वह ऑक्सीकरण अवस्था है। इसलिए $\mathrm{CO_2}$ में कार्बन की ऑक्सीकरण अवस्था +4 है, जो इसकी ऑक्सीकरण संख्या भी है और इसी तरह ऑक्सीजन की ऑक्सीकरण अवस्था और ऑक्सीकरण संख्या दोनों -2 है। इसका अर्थ है कि ऑक्सीकरण संख्या एक यौगिक में एक तत्व की ऑक्सीकरण अवस्था को दर्शाती है।
| समूह | $\mathbf{1}$ | $\mathbf{2}$ | $\mathbf{1 3}$ | $\mathbf{1 4}$ | $\mathbf{1 5}$ | $\mathbf{1 6}$ | $\mathbf{1 7}$ |
|---|
| तत्व | $\mathrm{Na}$ | $\mathrm{Mg}$ | $\mathrm{Al}$ | $\mathrm{Si}$ | $\mathrm{P}$ | $\mathrm{S}$ | $\mathrm{Cl}$ | | यौगिक | $\mathrm{NaCl}$ | $\mathrm{MgSO_4}$ | $\mathrm{AlF_3}$ | $$\mathrm{SiCl_4}$ | $\mathrm{P_4} \mathrm{O_{10}}$ | $\mathrm{SF_6}$ | $\mathrm{HClO}$ | | समूह तत्व के उच्चतम ऑक्सीकरण संख्या अवस्था | +1 | +2 | +3 | +4 | +5 | +6 | +7 |
एक धातु के यौगिक में ऑक्सीकरण संख्या/अवस्था को कभी-कभी जर्मन रसायनज्ञ अल्फ्रेड स्टॉक द्वारा दी गई नोटेशन के अनुसार प्रस्तुत किया जाता है। इसे लोकप्रिय रूप से स्टॉक नोटेशन के रूप में जाना जाता है। इसके अनुसार, ऑक्सीकरण संख्या को अणुसूत्र में धातु के चिह्न के पीछे ऑक्सीकरण संख्या को प्रकट करने वाला रोमन संख्या के रूप में व्यक्त किया जाता है। इस प्रकार, एवरस ब्रोमाइड और एवरिक ब्रोमाइड को $\mathrm{Au}(\mathrm{I}) \mathrm{Cl}$ और $\mathrm{Au}(\mathrm{III}) \mathrm{Cl_3}$ के रूप में लिखा जाता है। इसी तरह, स्टैनस ब्रोमाइड और स्टैनिक ब्रोमाइड को $\mathrm{Sn}$ (II) $\mathrm{Cl_2}$ और $\mathrm{Sn}(\mathrm{IV}) \mathrm{Cl_4}$ के रूप में लिखा जाता है। ऑक्सीकरण संख्या में परिवर्तन ऑक्सीकरण अवस्था में परिवर्तन को दर्शाता है, जो इसके अवस्था के आधार पर विशेषता के बारे में बताता है कि यह ऑक्सीकृत रूप या अपचयित रूप में है। इसलिए, $\mathrm{Hg_2}(\mathrm{I}) \mathrm{Cl_2}$, $\mathrm{Hg}$ (II) $\mathrm{Cl_2}$ के अपचयित रूप है।
समस्या 8.3
स्टॉक नोटेशन का उपयोग करके निम्नलिखित यौगिकों का प्रतिनिधित्व करें: $\mathrm{HAuCl_4}, \mathrm{Tl_2} \mathrm{O}, \mathrm{FeO}$, $\mathrm{Fe_2} \mathrm{O_3}$, CuI, $\mathrm{CuO}, \mathrm{MnO}$ और $\mathrm{MnO_2}$।
हल
एक यौगिक में चाहे तत्व के ऑक्सीकरण संख्या की गणना करने के विभिन्न नियमों के अनुसार, इस यौगिक में प्रत्येक धातु तत्व के ऑक्सीकरण संख्या निम्नलिखित हैं:
$ \begin{array}{ccc} \mathrm{HAuCl_4} & \rightarrow & \mathrm{Au} \text{ has } 3 \\
इसलिए, ये यौगिक निम्नलिखित रूप में प्रस्तुत किए जा सकते हैं:
$\mathrm{HAu}(\mathrm{III}) \mathrm{Cl_4}, \mathrm{Tl_2}$ (I)O, $\mathrm{Fe}(\mathrm{II}) \mathrm{O}, \mathrm{Fe_2}(\mathrm{III}) \mathrm{O_3}$, $\mathrm{Cu}(\mathrm{I}) \mathrm{I}, \mathrm{Cu}(\mathrm{II}) \mathrm{O}, \mathrm{Mn}(\mathrm{II}) \mathrm{O}, \mathrm{Mn}(\mathrm{IV}) \mathrm{O_2}$। oxidation number के अवधारण का एक अक्षुत रूप से ऑक्सीकरण, अपचयन, ऑक्सीकारक (ऑक्सीडेंट), अपचायक (रेडक्टेंट) और रेडॉक्स अभिक्रिया को परिभाषित करने में उपयोग किया गया है। सारांशित करते हुए, हम कह सकते हैं कि:
-
ऑक्सीकरण: दिए गए पदार्थ में तत्व के ऑक्सीकरण संख्या में वृद्धि।
-
कमी : दिए गए पदार्थ में तत्व के ऑक्सीकरण संख्या में कमी।
-
ऑक्सीकरण एजेंट : एक रासायनिक अभिकर्मक जो किसी दिए गए पदार्थ में तत्व के ऑक्सीकरण संख्या को बढ़ा सकता है। इन अभिकर्मकों को ऑक्सीकारक भी कहा जाता है।
-
अपचायक एजेंट : एक रासायनिक अभिकर्मक जो किसी दिए गए पदार्थ में तत्व के ऑक्सीकरण संख्या को कम कर सकता है। इन अभिकर्मकों को अपचायक भी कहा जाता है।
-
रेडॉक्स अभिक्रियाएं : वे अभिक्रियाएं जिनमें अंतरक्रिया कर रहे अणुओं के ऑक्सीकरण संख्या में परिवर्तन होता है।
समस्या 8.4
उपयोग करके बताइए कि अभिक्रिया: $2 \mathrm{Cu_2} \mathrm{O}(\mathrm{s})+\mathrm{Cu_2} \mathrm{~S}(\mathrm{~s}) \rightarrow 6 \mathrm{Cu}(\mathrm{s})+\mathrm{SO_2}(\mathrm{~g})$ एक अपचायक-उपचायक अभिक्रिया है। अपचायक एवं उपचायक के रूप में कौन कार्य करता है और अपचित एवं उपचित विषम कौन हैं?
हल
हम अभिक्रिया में प्रत्येक अवयव के ऑक्सीकरण संख्या का निर्धारण करते हैं। इसके परिणामस्वरूप हमें निम्नलिखित प्राप्त होता है:
$$ \begin{aligned} & 2 \stackrel{+1}{\mathrm{Cu_2}} \stackrel{-2}{\mathrm{O}}(\mathrm{s})+\stackrel{+1}{\mathrm{Cu_2}} \stack
\end{aligned} $$
हम इसलिए निष्कर्ष निकालते हैं कि इस अभिक्रिया में कॉपर +1 अवस्था से शून्य ऑक्सीकरण अवस्था में अवाप्त हो जाता है और सल्फर -2 अवस्था से +4 अवस्था में ऑक्सीकृत हो जाता है। इसलिए उपरोक्त अभिक्रिया एक रेडॉक्स अभिक्रिया है।
अतः, $\mathrm{Cu_2} \mathrm{O}$, $\mathrm{Cu_2} \mathrm{~S}$ में सल्फर के ऑक्सीकरण संख्या को बढ़ाने में सहायता करता है, इसलिए $\mathrm{Cu}(\mathrm{I})$ एक ऑक्सीकारक है; और $\mathrm{Cu_2} \mathrm{~S}$ के सल्फर, $\mathrm{Cu_2} \mathrm{~S}$ में अपने स्वयं के कॉपर और $\mathrm{Cu_2} \mathrm{O}$ में कॉपर के ऑक्सीकरण संख्या को कम करने में सहायता करता है, इसलिए $\mathrm{Cu_2} \mathrm{~S}$ के सल्फर एक अपचायक है।
8.3.1 रेडॉक्स अभिक्रियाओं के प्रकार
1. संयोजन अभिक्रियाएं
एक संयोजन अभिक्रिया को इस प्रकार दर्शाया जा सकता है:
$$ \mathrm{A}+\mathrm{B} \rightarrow \mathrm{C} $$
ऐसी अभिक्रिया के लिए या तो A और B में से कोई एक तत्वात्मक रूप में होना चाहिए या दोनों A और B तत्वात्मक रूप में होना चाहिए। सभी ज्वलन अभिक्रियाएं, जिनमें तत्वात्मक डाइऑक्सीजन का उपयोग किया जाता है, तथा अन्य अभिक्रियाएं, जिनमें डाइऑक्सीजन के अतिरिक्त अन्य तत्वों का उपयोग किया जाता है, रेडॉक्स अभिक्रियाएं होती हैं। इस श्रेणी के कुछ महत्वपूर्ण उदाहरण हैं:
$$\stackrel{0}{\mathrm{C}}(\mathrm{s}) + \stackrel{0}{\mathrm{O_2}}(\mathrm{~g}) \xrightarrow{\Delta} \stackrel{+4-2}{\mathrm{CO_2}} (\mathrm{~g}) \tag{8.24} $$
$$3 \stackrel{0}{\mathrm{Mg}}(\mathrm{s})+ \stackrel{0}{\mathrm{N_2}}(\mathrm{~g}) \xrightarrow{\Delta} \stackrel{+2}{\mathrm{Mg_3}} \stackrel{-3}{\mathrm{~N_2}}(\mathrm{~s}) \tag{8.25}$$
$$\stackrel{-4+1}{\mathrm{CH_4}}(\mathrm{~g})+2 \stackrel{0}{\mathrm{O_2}}(\mathrm{~g}) \xrightarrow{\Delta} \stackrel{+4-2}{\mathrm{CO_2}}(\mathrm{~g})+2 \stackrel{+1}{\mathrm{H_2}} \stackrel{-2}{\mathrm{O}}(\mathrm{l})$$
2. अपघटन अभिक्रियाएं
अपघटन अभिक्रियाएं संयोजन अभिक्रियाओं के विपरीत होती हैं। ठीक ही, एक अपघटन अभिक्रिया एक यौगिक के दो या अधिक घटकों में विघटन करती है जिसमें कम से कम एक घटक तत्वीय अवस्था में होता है। इस श्रेणी के उदाहरण निम्नलिखित हैं:
$$2 \stackrel{+1}{\mathrm{H_2}} \stackrel{-2}{\mathrm{O}}(\mathrm{l}) \xrightarrow{\Delta} 2 \stackrel{0}{\mathrm{H_2}}(\mathrm{~g}) + \stackrel{0}{\mathrm{O_2}}(\mathrm{~g})\tag{8.26}$$
$$\stackrel{+1-1}{\mathrm{NaH}}(\mathrm{s}) \xrightarrow{\Delta} 2 \stackrel{0}{\mathrm{Na}}(\mathrm{s})+ \stackrel{0}{\mathrm{H_2}} (\mathrm{~g}) \tag{8.27}$$
$$ 2 \stackrel{+1+5}{\mathrm{KCl}}\stackrel{-2}{\mathrm{O_3}}(\mathrm{~s}) \xrightarrow{\Delta} 2 \stackrel{+1-1}{\mathrm{KCl}}(\mathrm{s})+3 \stackrel{0}{\mathrm{O_2}}(\mathrm{~g}) \tag{8.28}$$
ध्यान देने योग्य है कि मिश्रण अभिक्रियाओं में मेथेन में हाइड्रोजन के ऑक्सीकरण संख्या में कोई परिवर्तन नहीं होता और पोटैशियम क्लोरेट में पोटैशियम के ऑक्सीकरण संख्या में अभिक्रिया (7.28) में कोई परिवर्तन नहीं होता। यहाँ ध्यान देने योग्य है कि सभी अपघटन अभिक्रियाएँ रेडॉक्स अभिक्रियाएँ नहीं होती हैं। उदाहरण के लिए, कैल्शियम कार्बोनेट के अपघटन एक रेडॉक्स अभिक्रिया नहीं होता।
$$\stackrel{+2}{\mathrm{Ca}}\stackrel{+4}{\mathrm{C}}\stackrel{-2}{\mathrm{O_3}} \mathrm{(s)} \xrightarrow{\Delta} \stackrel{+2-2}{\mathrm{CaO}} + \stackrel{+4-2}{\mathrm{CO_2}}\mathrm{(g)}$$
3. विस्थापन अभिक्रियाएं
एक विस्थापन अभिक्रिया में, एक यौगिक में एक आयन (या एक परमाणु) दूसरे तत्व के आयन (या परमाणु) द्वारा प्रतिस्थापित हो जाता है। इसे इस प्रकार दर्शाया जा सकता है:
$$ \mathrm{X}+\mathrm{YZ} \rightarrow \mathrm{XZ}+\mathrm{Y} $$
विस्थापन अभिक्रियाएं दो श्रेणियों में वर्गीकृत होती हैं: धातु विस्थापन और अधातु विस्थापन।
(a) धातु विस्थापन: एक यौगिक में धातु अपररूप में दूसरी धातु द्वारा प्रतिस्थापित हो सकती है। हम पहले अनुच्छेद 7.2.1 में इस अभिक्रिया के वर्ग के बारे में चर्चा कर चुके हैं। धातु विस्थापन अभिक्रियाएं धातु के खनिजों से शुद्ध धातुओं के निष्कर्षण में उपयोग होती हैं। कुछ उदाहरण नीचे दिए गए हैं:
$$\stackrel{+2+6-2}{\mathrm{CuSO_4}}(\mathrm{aq})+ \stackrel{0}{\mathrm{Zn}}(\mathrm{s}) \rightarrow \stackrel{0}{\mathrm{Cu}}(\mathrm{s})+\stackrel{+2+6-3}{\mathrm{ZnSO_4}}(\mathrm{aq}) \tag{8.29}$$
$$\stackrel{+5-2}{\mathrm{V_2O_5}}\mathrm{(s)} + 5 \stackrel{0}{\mathrm{Ca}}\mathrm{(s)} \xrightarrow{\Delta} 2 \stackrel{0}{\mathrm{V}} \mathrm{(s)} + 5 \stackrel{+2-2}{\mathrm{CaO}}\mathrm{(s)} \tag{8.30}$$
$$\stackrel{+4-1}{\mathrm{TiCl_4}}\mathrm{(l)} + 2 \stackrel{0}{\mathrm{Mg}}\mathrm{(s)} \xrightarrow{\Delta} \stackrel{0}{\mathrm{Ti}} \mathrm{(s)} + 2\stackrel{+2-1}{\mathrm{MgCl_2}}\mathrm{(s)} \tag{8.31}$$
$$\stackrel{+3-2}{\mathrm{Cr_2O_3}}\mathrm{(l)} + 2 \stackrel{0}{\mathrm{Al}}\mathrm{(s)} \xrightarrow{\Delta} \stackrel{+3-2}{\mathrm{Al_2O_3}} \mathrm{(s)} + 2\stackrel{0}{\mathrm{Cr}}\mathrm{(s)} \tag{8.32}$$
प्रत्येक मामले में, अपचायक धातु उस धातु की तुलना में बेहतर अपचायक होती है जो कि अपचयित हो रही है, जो आसानी से इलेक्ट्रॉन खोने की क्षमता के लिए स्पष्ट रूप से अधिक उपलब्ध होती है जो कि अपचयित हो रही है।
(b) अधातु विस्थापन: अधातु विस्थापन रेडॉक्स अभिक्रियाएं जल विस्थापन और बहुत कम घटनाओं में ऑक्सीजन विस्थापन शामिल होती है।
सभी अल्कली धातुएँ और कुछ अल्कली भूमि धातुएँ $(\mathrm{Ca}, \mathrm{Sr}$, और $\mathrm{Ba})$ जो बहुत अच्छे अपचायक होते हैं, ठंडे पानी से हाइड्रोजन विस्थापित करते हैं।
$$2 \stackrel{0}{\mathrm{Na}}\mathrm{(s)} + 2 \stackrel{+1-2}{\mathrm{H_2O}}\mathrm{(l)} \rightarrow 2 \stackrel{+1-2+1}{\mathrm{NaOH}} \mathrm{(aq)} + \stackrel{0}{\mathrm{Hg}}\mathrm{(g)} \tag{8.33}$$
$$ \stackrel{0}{\mathrm{2Ca}}\mathrm{(s)} + 2 \stackrel{+1-2}{\mathrm{H_2O}}\mathrm{(l)} \rightarrow 2 \stackrel{+2-2+1}{\mathrm{Ca(OH)_2}} \mathrm{(aq)} + \stackrel{0}{\mathrm{Hg}}\mathrm{(g)} \tag{8.34}$$
कम सक्रिय धातुओं जैसे मैग्नीशियम और लोहा, भाप के साथ अभिक्रिया करके डाइहाइड्रोजन गैस उत्पन्न करते हैं:
$$ \stackrel{0}{\mathrm{Mg}}\mathrm{(s)} + \stackrel{+1-2}{2\mathrm{H_2O}}\mathrm{(l)} \xrightarrow{\Delta} \stackrel{+2-2+1}{\mathrm{Mg(OH)_2}} \mathrm{(s)} + \stackrel{0}{\mathrm{Hg}}\mathrm{(g)} \tag{8.35}$$
$$ \stackrel{0}{2\mathrm{Fe}}\mathrm{(s)} + \stackrel{+1-2}{3\mathrm{H_2O}}\mathrm{(l)} \xrightarrow{\Delta} \stackrel{+3-2}{\mathrm{Fe_2O_3}} \mathrm{(s)} + \stackrel{0}{3\mathrm{Hg}}\mathrm{(g)} \tag{8.36}$$
कई धातुएँ, जिनमें से कुछ ठंडे पानी के साथ अभिक्रिया नहीं करती, अम्लों से हाइड्रोजन को विस्थापित करने में सक्षम होती हैं। ऐसी धातुएँ तकनीकी रूप से भी हाइड्रोजन के उत्पादन में भाग ले सकती हैं जो भाप के साथ अभिक्रिया नहीं करती। कadmium और tin ऐसी धातुओं के उदाहरण हैं। अम्लों से हाइड्रोजन के विस्थापन के कुछ उदाहरण नीचे दिए गए हैं:
$$ \stackrel{0}{\mathrm{Zn}}\mathrm{(s)} + \stackrel{+1-1}{2\mathrm{HCl}}\mathrm{(aq)} \rightarrow \stackrel{+2-1}{\mathrm{ZnCl_2}} \mathrm{(aq)} + \stackrel{0}{\mathrm{H_2}}\mathrm{(g)} \tag{8.37}$$
$$ \stackrel{0}{\mathrm{Mg}}\mathrm{(s)} + \stackrel{+1-1}{2\mathrm{HCl}}\mathrm{(aq)} \rightarrow \stackrel{+2-1}{\mathrm{MgCl_2}} \mathrm{(aq)} + {\mathrm{H_2}}\mathrm{(g)} \tag{8.38}$$
$$ \stackrel{0}{\mathrm{Fe}}\mathrm{(s)} + \stackrel{+1-1}{2\mathrm{HCl}}\mathrm{(aq)} \rightarrow \stackrel{+2-1}{\mathrm{FeCl_2}} \mathrm{(aq)} + {\mathrm{H_2}}\mathrm{(g)} \tag{8.39}$$
प्रतिक्रियाएँ (8.37 से 8.39) लैब में डाइहाइड्रोजन गैस के तैयार करने के लिए उपयोग की जाती हैं। यहाँ, धातुओं की प्रतिक्रियाशीलता हाइड्रोजन गैस के उत्पादन की दर में प्रतिबिंबित होती है, जो सबसे कम प्रतिक्रियाशील धातु $\mathrm{Fe}$ के लिए सबसे धीमी होती है, और सबसे अधिक प्रतिक्रियाशील धातु, Mg के लिए सबसे तेज होती है। बहुत कम प्रतिक्रियाशील धातुएँ, जो अपने स्वतंत्र अवस्था में उपस्थित हो सकती हैं, जैसे कि चांदी (Ag), और स्वर्ण (Au), ताकत वाले हाइड्रोक्लोरिक अम्ल के साथ भी प्रतिक्रिया नहीं करती हैं।
अनुच्छेद (8.2.1) में हमने पहले ही चर्चा की है कि धातुएँ - जिंक $(\mathrm{Zn})$, तांबा $(\mathrm{Cu})$ और चांदी (Ag) इलेक्ट्रॉन खोने की प्रवृत्ति के कारण अपनी अपचायक गतिविधि के क्रम में $\mathrm{Zn} >$ $\mathrm{Cu} > \mathrm{Ag}$ के क्रम में होती हैं। धातुओं के समान, हैलोजन के लिए भी गतिविधि श्रेणी का अस्तित्व होता है। आवर्त सारणी के 17वें समूह में फ्लूओरीन से आयोडीन तक नीचे जाने पर इन तत्वों के ऑक्सीकारक क्षमता कम होती जाती है। इसका अर्थ है कि फ्लूओरीन इतना अभिक्रियाशील है कि यह विलयन में क्लोराइड, ब्रोमाइड और आयोडाइड आयनों को बदल सकता है। वास्तव में, फ्लूओरीन इतना अभिक्रियाशील है कि यह पानी के साथ अभिक्रिया करता है और पानी के ऑक्सीजन को विस्थापित कर देता है :
$$ \stackrel{+1-2}{2\mathrm{H_2O}}\mathrm{(l)} + \stackrel{0}{2\mathrm{F_2}}\mathrm{(g)} \rightarrow \stackrel{+1-1}{4\mathrm{HF}} \mathrm{(aq)} + \stackrel{0}{\mathrm{O_2}}\mathrm{(g)} \tag{8.40}$$
इस कारण फ्लूओरीन के प्रयोग से क्लोरीन, ब्रोमीन और आयोडीन के विस्थापन अभिक्रियाएं आमतौर पर जलीय विलयन में नहीं की जाती हैं। दूसरी ओर, क्लोरीन जलीय विलयन में ब्रोमाइड और आयोडाइड आयनों को विस्थापित कर सकती है, जैसा कि नीचे दिखाया गया है:
$$ \stackrel{0}{\mathrm{Cl_2}}\mathrm{(g)} + \stackrel{+1-1}{2\mathrm{KBr}}\mathrm{(aq)} \rightarrow \stackrel{+1-1}{2\mathrm{KCl}} \stackrel{0} {\mathrm{(aq)}} + {\mathrm{Br_2}}\mathrm{(l)} \tag{8.41}$$
$$ \stackrel{0}{\mathrm{Cl_2}}\mathrm{(g)} + \stackrel{+1-1}{2\mathrm{KI}}\mathrm{(aq)} \rightarrow \stackrel{+1-1}{2\mathrm{KCl}} \stackrel{0} {\mathrm{(aq)}} + {\mathrm{I_2}}\mathrm{(s)} \tag{8.42}$$
जैसे $\mathrm{Br_2}$ और $\mathrm{I_2}$ रंग वाले होते हैं और $\mathrm{CCl_4}$ में घुलते हैं, इन्हें विलयन के रंग से आसानी से पहचाना जा सकता है। उपरोक्त अभिक्रियाओं को आयनिक रूप में लिखा जा सकता है जैसे:
$$ \stackrel{0}{\mathrm{Cl_2}}\mathrm{(g)} + \stackrel{-1}{2\mathrm{Br^-}}\mathrm{(aq)} \rightarrow \stackrel{-1}{2\mathrm{Cl^-}} \mathrm{(aq)} + \stackrel{0}{\mathrm{Br_2}}\mathrm{(s)} \tag{8.41a}$$
$$ \stackrel{0}{\mathrm{Cl_2}}\mathrm{(g)} + \stackrel{-1}{2\mathrm{I^-}}\mathrm{(aq)} \rightarrow \stackrel{-1}{2\mathrm{Cl^-}} \mathrm{(aq)} + \stackrel{0}{\mathrm{I_2}}\mathrm{(s)} \tag{8.42a}$$
अभिक्रियाएँ (8.41) और (8.42) प्रयोगशाला में $\mathrm{Br}^{-}$ और $\mathrm{I}^{-}$ की पहचान के लिए प्रसिद्ध ‘स्तर परीक्षण’ नामक परीक्षण के आधार के रूप में हैं। यहाँ यह उल्लेख करना उचित नहीं होगा कि ब्रोमीन भी विलयन में आयोडाइड आयन को विस्थापित कर सकती है:
$$ \stackrel{0}{\mathrm{Br_2}(\mathrm{l})}+\stackrel{-1}{2 \mathrm{I}^{-}}(\mathrm{aq}) \rightarrow \stackrel{-1}{2 \mathrm{Br}^{-}} (\mathrm{aq})+ \stackrel{0}{\mathrm{I_2}} (\mathrm{~s}) \tag{8.43} $$
$$
हैलोजन प्रतिस्थापन अभिक्रियाएं एक सीधे औद्योगिक अनुप्रयोग के रूप में हैं। अपने हैलाइड से हैलोजन के पुनः प्राप्ति के लिए एक ऑक्सीकरण प्रक्रिया की आवश्यकता होती है, जिसे निम्नलिखित द्वारा प्रस्तुत किया गया है:
$$2 \mathrm{X}^{-} \rightarrow \mathrm{X_2}+2 \mathrm{e}^{-} \tag{8.44}$$
यहाँ $\mathrm{X}$ एक हैलोजन तत्व को दर्शाता है। जबकि रासायनिक तरीकों के माध्यम से $\mathrm{Cl}^{-}$, $\mathrm{Br}^{-}$ और $\mathrm{I}^{-}$ के ऑक्सीकरण के लिए साधन उपलब्ध हैं, फ्लूओरीन सबसे मजबूत ऑक्सीकरण एजेंट है; इसलिए रासायनिक तरीकों के माध्यम से $\mathrm{F}^{-}$ आयनों को $\mathrm{F_2}$ में परिवर्तित करना संभव नहीं है। $\mathrm{F}^{-}$ से $\mathrm{F_2}$ प्राप्त करने का एकमात्र तरीका विद्युत अपघटन द्वारा ऑक्सीकरण है, जिसके विस्तारित विवरण आप बाद में अध्ययन करेंगे।
4. असमानुपाती अभिक्रियाएं
असमानुपाती अभिक्रियाएं एक विशेष प्रकार की रूपांतरण अभिक्रियाएं होती हैं। एक असमानुपाती अभिक्रिया में, एक ऑक्सीकरण अवस्था में उपस्थित एक तत्व एक साथ ऑक्सीकृत और अपचयित होता है। एक असमानुपाती अभिक्रिया में एक अभिकर्मक पदार्थ में हमेशा एक तत्व होता है जो कम से कम तीन ऑक्सीकरण अवस्थाओं में विद्यमान हो सकता है। अभिकर्मक पदार्थ के रूप में उपस्थित तत्व की मध्यम ऑक्सीकरण अवस्था होती है; और इस तत्व की उच्च और निम्न ऑक्सीकरण अवस्थाएं अभिक्रिया में बनती हैं। हाइड्रोजन परॉक्साइड के अपघटन असमानुपाती अभिक्रिया का एक परिचित उदाहरण है, जहां ऑक्सीजन असमानुपाती अभिक्रिया का अनुभव करता है।
$$\stackrel{+1-1}{2\mathrm{H_2O_2}}\mathrm{(aq)} \rightarrow \stackrel{+1-2}{2\mathrm{H_2O}} \mathrm{(l)} + \stackrel{0}{\mathrm{O_2}}\mathrm{(g)} \tag{8.45}$$
यहाँ परऑक्साइड में उपस्थित ऑक्सीजन, जो -1 ऑक्सीकरण अवस्था में होती है, $\mathrm{O_2}$ में शून्य ऑक्सीकरण अवस्था में और $\mathrm{H_2O}$ में -2 ऑक्सीकरण अवस्था में परिवर्तित हो जाती है।
फॉस्फोरस, सल्फर और क्लोरीन के अल्कली माध्यम में अपनी ऑक्सीकरण अवस्था में विभेदन (disproportionation) होता है, जैसा कि नीचे दिखाया गया है :
$$\stackrel{0}{\mathrm{P_4}}\mathrm{(s)}+ \stackrel{}{3\mathrm{OH^-}}\mathrm{(aq)} + \stackrel{}{3\mathrm{H_2O}}\mathrm{(l)} \rightarrow \stackrel{-3}{2\mathrm{P}} \mathrm{H_3} \mathrm{(g)} + 3\mathrm{H_2P}\stackrel{+1}{\mathrm{O_2^-}}\mathrm{(aq)} \tag{8.46}$$
$$\stackrel{0}{\mathrm{S_8}}\mathrm{(s)}+ \stackrel{}{12\mathrm{OH^-}}\mathrm{(aq)} \rightarrow \stackrel{-2}{4\mathrm{S}^{2-}}\mathrm{(aq)} + \stackrel{+2}{2\mathrm{S_2O_3}^{2-}} \mathrm{(aq)} + 6\mathrm{H_2O}\mathrm{(l)} \tag{8.47}$$
$$\stackrel{0}{\mathrm{Cl_2}}\mathrm{(g)}+ \stackrel{}{2\mathrm{OH^-}}\mathrm{(aq)} \rightarrow \stackrel{+1}{4\mathrm{ClO^-}}\mathrm{(aq)} + \stackrel{-1}{2\mathrm{Cl^-}} \mathrm{(aq)} + \mathrm{H_2O}\mathrm{(l)} \tag{8.48}$$
अभिक्रिया (8.48) घरेलू ब्लीचिंग एजेंट के निर्माण का वर्णन करती है। अभिक्रिया में उत्पन्न होने वाले हाइपोक्लोराइट आयन $\left(\mathrm{ClO}^{-}\right)$ वस्तुओं के रंग वाले धब्बों को रंगहीन यौगिकों में ऑक्सीकृत करता है।
यहाँ उल्लेख करना रोचक होगा कि ब्रोमीन और आयोडीन, अभिक्रिया (8.48) में क्लोरीन के द्वारा दिखाए गए प्रवृत्ति के समान प्रवृत्ति का पालन करते हैं, लेकिन फ्लूओरीन जब एल्कली के साथ अभिक्रिया करता है तो इस व्यवहार से विचलन दिखाता है। फ्लूओरीन के मामले में होने वाली अभिक्रिया निम्नलिखित है:
$$2 \mathrm{~F_2}(\mathrm{~g})+2 \mathrm{OH}^{-}(\mathrm{aq}) \rightarrow 2 \mathrm{~F}^{-}(\mathrm{aq})+\mathrm{OF_2}(\mathrm{~g})+\mathrm{H_2} \mathrm{O}(\mathrm{l}) \tag{8.49}$$
(ध्यान देने योग्य है कि अभिक्रिया (8.49) में फ्लूओरीन पानी के साथ निश्चित रूप से अभिक्रिया करेगा और थोड़ा ऑक्सीजन भी उत्पन्न करेगा।) फ्लूओरीन द्वारा दिखाए गए विचलन के लिए हमें आश्चर्य नहीं होना चाहिए क्योंकि हम जानते हैं कि फ्लूओरीन की सीमा यह है कि यह सबसे इलेक्ट्रोनेगेटिव तत्व होने के कारण कोई धनात्मक ऑक्सीकरण अवस्था नहीं दिखा सकता। इसका अर्थ है कि हैलोजन में, फ्लूओरीन अपचयन और ऑक्सीकरण दोनों के लिए असमान व्यवहार नहीं दिखाता।
समस्या 8.5
निम्नलिखित अनुपातिक अनियमित अभिक्रिया दिखाते नहीं हैं और कारण बताइए?
$\mathrm{ClO}^{-}, \mathrm{ClO_2}^{-}, \mathrm{ClO_3}^{-}$ और $\mathrm{ClO_4}^{-}$
साथ ही, विघटन अभिक्रिया के लिए प्रत्येक अनुपातिक अनियमित अभिक्रिया के लिए अभिक्रिया लिखिए।
हल
ऊपर सूचित क्लोरीन के ऑक्सोआयन में, $\mathrm{ClO_4}^{-}$ अनुपातिक अनियमित अभिक्रिया नहीं दिखाता क्योंकि इस ऑक्सोआयन में क्लोरीन के उच्चतम ऑक्सीकरण अवस्था में उपस्थित होता है, अर्थात +7। अन्य तीन ऑक्सोआयन के लिए विघटन अभिक्रिया निम्नलिखित हैं:
$\stackrel{+1}{2\mathrm{ClO^-}} \longrightarrow \stackrel{-1}{2\mathrm{Cl^-}}+ \stackrel{+5}{\mathrm{ClO_3^-}}$
$\stackrel{+}{6\mathrm{Cl}} \mathrm{O_2}^- \xrightarrow{hv} \stackrel{+5}{4\mathrm{Cl}} \mathrm{C_3}^- + \stackrel{-1}{2\mathrm{Cl^-}}$
$\stackrel{+5}{4\mathrm{Cl}} \mathrm{O_3}^- \longrightarrow \stackrel{-1}{\mathrm{Cl^-}} + 3\stackrel{+7}{\mathrm{Cl}}\mathrm{O_4}^-$
समस्या 8.6
निम्नलिखित अपचयन-उपचय अभिक्रियाओं के वर्गीकरण के एक योजना सुझाएं
(a) $\mathrm{N_2}$ (g) $+\mathrm{O_2}$ (g) $\rightarrow 2 \mathrm{NO}$ (g)
(b) $2 \mathrm{~Pb}\left(\mathrm{NO_3}\right)_{2}$ (s) $\rightarrow 2 \mathrm{PbO}$ (s) $+4 \mathrm{NO_2}$ (g) + $\mathrm{O_2}(\mathrm{~g})$
(c) $\mathrm{NaH}$ (s) $+\mathrm{H_2} \mathrm{O}$ (l) $\rightarrow \mathrm{NaOH}\left(\right.$ aq) $+\mathrm{H_2}$ (g)
(d) $2 \mathrm{NO_2}$ (g) $+2 \mathrm{OH}^{-}$(aq) $\rightarrow \mathrm{NO_2}^{-}(\mathrm{aq})+$ $\mathrm{NO_3}^{-}(\mathrm{aq})+\mathrm{H_2} \mathrm{O}(\mathrm{l})$
हल
अभिक्रिया (a) में, तत्वों नाइट्रोजन और ऑक्सीजन के संयोजन से नाइट्रिक ऑक्साइड बनता है; इसलिए, यह संयोजन रेडॉक्स अभिक्रिया का उदाहरण है। अभिक्रिया (b) में, सीसा नाइट्रेट तीन घटकों में विघटित हो जाता है; इसलिए, यह विघटन रेडॉक्स अभिक्रिया के अंतर्गत आती है। अभिक्रिया (c) में, जल के हाइड्रोजन को हाइड्राइड आयन द्वारा डाइहाइड्रोजन गैस में विस्थापित कर दिया गया है। इसलिए, इसे विस्थापन रेडॉक्स अभिक्रिया कहा जा सकता है। अभिक्रिया (d) में, $\mathrm{NO_2}$ (+4 अवस्था) के $\mathrm{NO_2}^{-}$ (+3 अवस्था) और $\mathrm{NO_3}^{-}$ (+5 अवस्था) में अपचयन एवं ऑक्सीकरण के माध्यम से अपने आप बदल देता है। इसलिए, अभिक्रिया (d) अपने आप बदलने वाली रेडॉक्स अभिक्रिया का उदाहरण है।
अंशात्मक ऑक्सीकरण संख्या का विरोधाभास
कभी-कभी हम ऐसे यौगिकों के साथ सामना करते हैं जिनमें यौगिक में एक विशिष्ट तत्व की ऑक्सीकरण संख्या अंशात्मक होती है। उदाहरण के लिए:
$\mathrm{C_3} \mathrm{O_2}$ [जहाँ कार्बन की ऑक्सीकरण संख्या (4/3) होती है],
$\mathrm{Br_3} \mathrm{O_8}$ [जहाँ ब्रोमीन की ऑक्सीकरण संख्या (16/3) होती है]
और $\mathrm{Na_2} \mathrm{~S_4} \mathrm{O_6}$ (जहाँ सल्फर की ऑक्सीकरण संख्या 2.5 होती है)।
हम जानते हैं कि अंशात्मक ऑक्सीकरण संख्या के विचार के लिए हमें अस्पष्टता महसूस होती है, क्योंकि इलेक्ट्रॉन कभी भी अंशात्मक रूप से साझा या परिवहन नहीं किए जाते। वास्तव में, यह अंशात्मक ऑक्सीकरण अवस्था विचार के तत्व की औसत ऑक्सीकरण अवस्था होती है और संरचनात्मक पैरामीटर बताते हैं कि जिस तत्व के लिए अंशात्मक ऑक्सीकरण अवस्था विचार किया जाता है, वह विभिन्न ऑक्सीकरण अवस्थाओं में उपस्थित होता है। $\mathrm{C_3} \mathrm{O_2}, \mathrm{Br_3} \mathrm{O_8}$ और $\mathrm{S_4} \mathrm{O_6}^{2-}$ के अणु की संरचना निम्नलिखित बंधन स्थितियों को दर्शाती है:

प्रत्येक अणु में तारांकित तत्व अपने समान तत्व के अन्य परमाणुओं से भिन्न ऑक्सीकरण अवस्था (ऑक्सीकरण संख्या) दिखाई दे रहा है। इससे पता चलता है कि $\mathrm{C_3} \mathrm{O_2}$ में दो कार्बन परमाणु +2 ऑक्सीकरण अवस्था में हैं, जबकि तीसरा कार्बन शून्य ऑक्सीकरण अवस्था में है और औसत ऑक्सीकरण संख्या $4 / 3$ है। हालांकि, वास्तविक चित्र यह है कि दो सिरे वाले कार्बन परमाणु +2 ऑक्सीकरण अवस्था में हैं और मध्य कार्बन शून्य ऑक्सीकरण अवस्था में है। इसी तरह $\mathrm{Br_3} \mathrm{O_8}$ में दो सिरे वाले ब्रोमीन परमाणु +6 ऑक्सीकरण अवस्था में हैं और मध्य ब्रोमीन परमाणु +4 ऑक्सीकरण अवस्था में है। फिर से औसत, जो वास्तविकता से भिन्न है, $16 / 3$ है। इसी तरह, $\mathrm{S_4} \mathrm{O_6}^{2-}$ विशिष्टता में, दो अत्यधिक सल्फर परमाणु +5 ऑक्सीकरण अवस्था में हैं और दो मध्य सल्फर परमाणु शून्य ऑक्सीकरण अवस्था में हैं। $\mathrm{S_4} \mathrm{O_6}^{2-}$ के सल्फर के चार ऑक्सीकरण संख्या का औसत 2.5 है, जबकि वास्तविक ऑक्सीकरण संख्या क्रमशः प्रत्येक सल्फर के लिए +5, 0, 0 और +5 है।
हम इस प्रकार, सामान्य रूप से निष्कर्ष ले सकते हैं कि भिन्न ऑक्सीकरण अवस्था के विचार के साथ सावधानी से ले जाया जाना चाहिए और वास्तविकता केवल संरचनाओं द्वारा खोली जाती है। इसके अतिरिक्त, जब भी हम किसी विशिष्ट तत्व के किसी भी अपवाहक में भिन्न ऑक्सीकरण अवस्था के साथ मिलते हैं, तो हमें समझना चाहिए कि यह केवल औसत ऑक्सीकरण संख्या है। वास्तविकता (केवल संरचनाओं द्वारा खोली जाती है), उस विशिष्ट अपवाहक में तत्व केवल एक से अधिक पूर्ण संख्या ऑक्सीकरण अवस्था में उपस्थित होता है। $\mathrm{Fe_3} \mathrm{O_4}, \mathrm{Mn_3} \mathrm{O_4}$, $\mathrm{Pb_3} \mathrm{O_4}$ जैसे कुछ अन्य यौगिकों के उदाहरण हैं, जो मिश्रित ऑक्साइड होते हैं, जहां हम धातु परमाणु के भिन्न ऑक्सीकरण अवस्था के साथ मिलते हैं। हालांकि, ऑक्सीकरण अवस्था भिन्न रूप में हो सकती है, जैसे $\mathrm{O_2}^{+}$ और $\mathrm{O_2}^{-}$ में यह क्रमशः $+1 / 2$ और $-1 / 2$ होती है।
समस्या 8.7
निम्नलिखित अभिक्रियाएँ अलग-अलग क्यों चलती हैं?
$$ \begin{array}{r} \mathrm{Pb_3} \mathrm{O_4}+8 \mathrm{HCl} \rightarrow 3 \mathrm{PbCl_2}+\mathrm{Cl_2}+4 \mathrm{H_2} \mathrm{O} \text { और } \\ \mathrm{Pb_3} \mathrm{O_4}+4 \mathrm{HNO_3} \rightarrow 2 \mathrm{~Pb}\left(\mathrm{NO_3}\right)_{2}+\mathrm{PbO_2}+ 2 \mathrm{H_2} \mathrm{O}\\ \end{array} $$
हल
$\mathrm{Pb_3} \mathrm{O_4}$ वास्तव में $2 \mathrm{~mol}$ के $\mathrm{PbO}$ और $1 \mathrm{~mol}$ के $\mathrm{PbO_2}$ के स्थैतिक मिश्रण होता है। $\mathrm{PbO_2}$ में लेड की ऑक्सीकरण अवस्था +4 होती है, जबकि $\mathrm{PbO}$ में लेड की स्थायी ऑक्सीकरण अवस्था +2 होती है। अतः $\mathrm{PbO_2}$ एक ऑक्सीकारक (ऑक्सीकरण एजेंट) के रूप में कार्य कर सकता है और इसलिए इसके माध्यम से $\mathrm{HCl}$ के $\mathrm{Cl}^{-}$ आयन को क्लोरीन में ऑक्सीकृत किया जा सकता है। हम यह भी ध्यान रख सकते हैं कि $\mathrm{PbO}$ एक क्षारीय ऑक्साइड होता है। अतः अभिक्रिया
$\mathrm{Pb_3} \mathrm{O_4}+8 \mathrm{HCl} \rightarrow 3 \mathrm{PbCl_2}+\mathrm{Cl_2}+4 \mathrm{H_2} \mathrm{O}$ को दो अभिक्रियाओं में विभाजित किया जा सकता है:
$$ \begin{aligned} & 2 \mathrm{PbO}+4 \mathrm{HCl} \rightarrow 2 \mathrm{PbCl_2}+2 \mathrm{H_2} \mathrm{O} \\ & \text { (अम्ल-क्षार अभिक्रिया) } \\ \end{aligned} $$
$$ \begin{aligned} & & \stackrel{+4}{\mathrm{Pb}} \mathrm{O_2} +4 \stackrel{-1}{\mathrm{HCl}} \rightarrow \stackrel{+2}{\mathrm{PbCl_2}} + \stackrel{0}{\mathrm{Cl_2}}+2 \mathrm{H_2} \mathrm{O} \\
$$ & &\text { (अपचायक-उपचायक अभिक्रिया) } \end{aligned} $$
क्योंकि $\mathrm{HNO_3}$ स्वयं एक उपचायक एजेंट है, इसलिए $\mathrm{PbO_2}$ और $\mathrm{HNO_3}$ के बीच अभिक्रिया होने की संभावना कम है। हालांकि, $\mathrm{PbO}$ और $\mathrm{HNO_3}$ के बीच अम्ल-क्षार अभिक्रिया होती है जैसे:
$$ 2 \mathrm{PbO}+4 \mathrm{HNO_3} \rightarrow 2 \mathrm{~Pb}\left(\mathrm{NO_3}\right)_{2}+2 \mathrm{H_2} \mathrm{O} $$
$\mathrm{PbO_2}$ के $\mathrm{HNO_3}$ के विरुद्ध पासिव गुण ही उस अभिक्रिया को $\mathrm{HCl}$ के साथ अलग बनाए रखते हैं।
8.3.2 रेडॉक्स अभिक्रियाओं के संतुलन
रेडॉक्स प्रक्रियाओं के रासायनिक समीकरणों के संतुलन के लिए दो विधियों का उपयोग किया जाता है। इन विधियों में से एक विधि अपचायक एजेंट और ऑक्सीकारक एजेंट के ऑक्सीकरण संख्या में परिवर्तन पर आधारित होती है, जबकि दूसरी विधि रेडॉक्स अभिक्रिया को दो आधा अभिक्रियाओं में विभाजित करके आधारित होती है - एक ऑक्सीकरण और दूसरी अपचायन के आधार पर। ये दोनों विधियाँ उपयोग में हैं और इनके उपयोग के चयन उपयोगकर्ता के अनुसार होता है।
(a) ऑक्सीकरण संख्या विधि: ऑक्सीकरण-अपचायन अभिक्रियाओं के लिखने में, अन्य अभिक्रियाओं के लिए जैसे, अभिकर्मक और उत्पाद के अणु संरचना और सूत्र जानना आवश्यक होता है। ऑक्सीकरण संख्या विधि निम्नलिखित चरणों के माध्यम से अब सबसे बेहतर रूप से दिखाई देती है:
चरण 1: प्रत्येक अभिकर्मक और उत्पाद के लिए सही सूत्र लिखें।
चरण 2: अभिक्रिया में ऑक्सीकरण संख्या में परिवर्तन करने वाले परमाणुओं की पहचान करें। इसके लिए अभिक्रिया में सभी तत्वों की ऑक्सीकरण संख्या निर्धारित करें।
चर नंबर 3: प्रति परमाणु और उस परमाणु के अणु/आयन में ऑक्सीकरण संख्या में वृद्धि या कमी की गणना करें। यदि ये समान नहीं हैं, तो उपयुक्त संख्या से गुणा करें ताकि ये समान हो जाएं। (अगर आप देखते हैं कि दो पदार्थ अपचयित हो रहे हैं और कुछ ऑक्सीकृत नहीं हो रहा है या विपरीत, तो कुछ गलत है। या तो अभिकर्मक या उत्पाद के सूत्र गलत हैं या ऑक्सीकरण संख्या का सही तरीके से निर्धारण नहीं किया गया है।)
चरण 4: यदि अभिक्रिया पानी में हो रही है, तो आयनों की भाग लेने की पुष्टि करें, तथा उचित ओर अभिक्रिया के समीकरण में $\mathrm{H}^{+}$ या $\mathrm{OH}^{-}$ आयनों को जोड़ें ताकि अभिकर्मक और उत्पाद के कुल आयनिक आवेश समान हों। यदि अभिक्रिया अम्लीय विलयन में की जा रही है, तो समीकरण में $\mathrm{H}^{+}$ आयनों का उपयोग करें; यदि क्षारीय विलयन में, तो $\mathrm{OH}^{-}$ आयनों का उपयोग करें।
चरण 5: अभिक्रिया के दोनों ओर हाइड्रोजन अणुओं की संख्या समान बनाने के लिए पानी $\left(\mathrm{H_2} \mathrm{O}\right)$ अणुओं को अभिकर्मक या उत्पाद में जोड़ें। अब, ऑक्सीजन अणुओं की संख्या की भी जांच करें। यदि अभिकर्मक और उत्पाद में ऑक्सीजन अणुओं की संख्या समान है, तो तब समीकरण संतुलित रेडॉक्स अभिक्रिया को प्रस्तुत करता है।
अब हम नीचे दिए गए कुछ समस्याओं की सहायता से विधि में शामिल कदमों की व्याख्या करेंगे:
समस्या 8.8
पोटेशियम डाइक्रोमेट(VI), $\mathrm{K_2} \mathrm{Cr_2} \mathrm{O_7}$ के सोडियम सल्फाइट, $\mathrm{Na_2} \mathrm{SO_3}$ के साथ अम्लीय विलयन में अभिक्रिया के लिए आयनिक समीकरण लिखें, जो क्रोमियम(III) आयन और सल्फेट आयन देती है।
हल
कदम 1: असंगठित आयनिक समीकरण है:
$$ \mathrm{Cr_2} \mathrm{O_7}^{2-}(\mathrm{aq})+\mathrm{SO_3}^{2-}(\mathrm{aq}) \rightarrow \mathrm{Cr}^{3+}(\mathrm{aq}) +\mathrm{SO_4}^{2-}(\mathrm{aq}) $$
$$
चरण 2: $\mathrm{Cr}$ और $\mathrm{S}$ के ऑक्सीकरण संख्या निर्धारित करें
$\stackrel{+6}{\mathrm{Cr_2}} \stackrel{-2}{\mathrm{O_7}^{2-}}(\mathrm{aq})+\stackrel{+4-2}{\mathrm{SO_3}^{2-}}(\mathrm{aq}) \rightarrow \stackrel{+3}{\mathrm{Cr}}(\mathrm{aq})+ \stackrel{+6-2}{\mathrm{SO_4}{ }^{2-}}(\mathrm{aq})$
इससे ज्ञात होता है कि डाइक्रोमेट आयन ऑक्सीकारक है और सल्फाइट आयन अपचायक है।
चरण 3: ऑक्सीकरण संख्या में वृद्धि और कमी की गणना करें और उन्हें समान करें: चरण-2 से हम देख सकते हैं कि क्रोमियम और सल्फर के ऑक्सीकरण संख्या में परिवर्तन हो रहा है। क्रोमियम के ऑक्सीकरण संख्या +6 से +3 में घट जाती है। समीकरण के दाहिने तरफ क्रोमियम के ऑक्सीकरण संख्या में +3 की कमी होती है। सल्फर के ऑक्सीकरण संख्या +4 से +6 में बढ़ जाती है। समीकरण के दाहिने तरफ सल्फर के ऑक्सीकरण संख्या में +2 की वृद्धि होती है। ऑक्सीकरण संख्या में वृद्धि और कमी को समान बनाने के लिए, समीकरण के दाहिने तरफ क्रोमियम आयन के सामने संख्या 2 लगाएं और सल्फेट आयन के सामने संख्या 3 लगाएं और समीकरण के दोनों तरफ क्रोमियम और सल्फर के परमाणुओं को संतुलित करें। इस प्रकार हमें प्राप्त होता है
$\stackrel{+6}{\mathrm{Cr_2}} \stackrel{-2}{\mathrm{O_7}^{2-}}(\mathrm{aq})+3\stackrel{+4-2}{\mathrm{SO_3}^{2-}}(\mathrm{aq}) \rightarrow \stackrel{+3}{\mathrm{Cr^{3+}}}(\mathrm{aq})+ 3\stackrel{+6-2}{\mathrm{SO_4}{ }^{2-}}(\mathrm{aq})$
चरण 4: चूंकि अभिक्रिया अम्लीय माध्यम में हो रही है, और इसके अतिरिक्त दोनों ओर आयनिक आवेश बराबर नहीं है, तो बाईं ओर $8 \mathrm{H}^{+}$ जोड़ें ताकि आयनिक आवेश बराबर हो जाए
$$ \mathrm{Cr_2} \mathrm{O_7}^{2-}(\mathrm{aq})+3\mathrm{SO_3}^{2-}(\mathrm{aq}) + 8\mathrm{H^+} \rightarrow 2\mathrm{Cr}^{3+}(\mathrm{aq}) + 3\mathrm{SO_4}^{2-}(\mathrm{aq})
$$
स्टेप 5: अंत में, हाइड्रोजन परमाणुओं की संख्या गिनें, और बाईं ओर उचित संख्या में जल अणु (अर्थात, $4 \mathrm{H_2} \mathrm{O}$ ) जोड़ें ताकि ऑक्सीकरण अपचयन परिवर्तन संतुलित हो जाए।
$$ \begin{aligned} & \mathrm{Cr_2} \mathrm{O_7}^{2-}(\mathrm{aq})+3 \mathrm{SO_3}{ }^{2-}(\mathrm{aq})+8 \mathrm{H}^{+}(\mathrm{aq}) \rightarrow 2 \mathrm{Cr}^{3+}(\mathrm{aq})+3 \mathrm{SO_4}{ }^{2-}(\mathrm{aq})+4 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \end{aligned} $$
समस्या 8.9
परमैंगनेट आयन, क्षारीय माध्यम में ब्रोमाइड आयन के साथ अभिक्रिया करके मैंगनीज डाइऑक्साइड और ब्रोमेट आयन देता है। अभिक्रिया के संतुलित आयनिक समीकरण को लिखिए।
हल
कदम 1: नाभिकीय आयनिक समीकरण है:
$\mathrm{MnO_4}^{-}(\mathrm{aq})+\mathrm{Br}^{-}(\mathrm{aq}) \rightarrow \mathrm{MnO_2}(\mathrm{~s})+\mathrm{BrO_3}^{-}(\mathrm{aq})$
कदम 2: $\mathrm{Mn}$ और $\mathrm{Br}$ के ऑक्सीकरण संख्या का निर्धारण करें
$\stackrel{+7}{\mathrm{Mn}} \mathrm{O_4}^{-} (\mathrm{aq})+\stackrel{-1}{\mathrm{Br^-}}(\mathrm{aq}) \longrightarrow \stackrel{+4}{\mathrm{Mn}} \mathrm{O_2}(\mathrm{s})+\stackrel{+5}{\mathrm{BrO_3}^{-}}(\mathrm{aq})$
इससे पता चलता है कि परमैंगनेट आयन ऑक्सीकारक है और ब्रोमाइड आयन अपचायक है।
चरण 3: ऑक्सीकरण संख्या में वृद्धि और कमी की गणना करें और वृद्धि को कमी के बराबर कर दें।
$\stackrel{+7}{2 \mathrm{Mn}} \mathrm{O_4}^{-} (\mathrm{aq})+\stackrel{-1}{\mathrm{Br}}(\mathrm{aq}) \rightarrow 2 \stackrel{+4}{\mathrm{Mn}} \mathrm{O_2}(\mathrm{~s})+ \stackrel{+5}{\mathrm{Br}} \mathrm{O_3}^{-}(\mathrm{aq})$
चरण 4: चूंकि अभिक्रिया कार्बोहाइड्रेट माध्यम में हो रही है और दोनों तरफ आयनिक आवेश बराबर नहीं है, तो दाहिने तरफ $2 \mathrm{OH}^{-}$ आयन जोड़ें ताकि आयनिक आवेश बराबर हो जाए।
$2 \mathrm{MnO_4}^{-}(\mathrm{aq})+\mathrm{Br}^{-}(\mathrm{aq}) \rightarrow 2 \mathrm{MnO_2}(\mathrm{~s})+ \mathrm{BrO_3}^{-}(\mathrm{aq})+2 \mathrm{OH}^{-}(\mathrm{aq})$
स्टेप 5: अंत में, हाइड्रोजन परमाणुओं की संख्या गिनें और उचित संख्या में जल अणु (अर्थात एक $\mathrm{H_2} \mathrm{O}$ अणु) को बाईं ओर जोड़ें ताकि ऑक्सीकरण अपचयन परिवर्तन संतुलित हो जाए।
$$ 2 \mathrm{MnO_4}^{-}(\mathrm{aq})+\mathrm{Br}^{-}(\mathrm{aq})+\mathrm{H_2} \mathrm{O}(\mathrm{l}) \rightarrow 2 \mathrm{MnO_2}(\mathrm{~s}) +\mathrm{BrO_3}^{-}(\mathrm{aq})+2 \mathrm{OH}^{-}(\mathrm{aq})
$$
(ब) आधा अभिक्रिया विधि: इस विधि में, दो आधा अभिक्रिया अलग-अलग संतुलित किए जाते हैं और फिर एक संतुलित अभिक्रिया के रूप में एक साथ जोड़ दिए जाते हैं।
मान लीजिए हम एक अभिक्रिया के समीकरण को संतुलित कर रहे हैं जो $\mathrm{Fe}^{2+}$ आयनों के $\mathrm{Fe}^{3+}$ आयनों में ऑक्सीकरण को दिखाती है, जो एसिडिक माध्यम में डाइक्रोमेट आयन $\left(\mathrm{Cr_2} \mathrm{O_7}\right)^{2-}$ द्वारा होता है, जहां $\mathrm{Cr_2} \mathrm{O_7}^{2-}$ आयन $\mathrm{Cr}^{3+}$ आयन में अवांछित हो जाते हैं। इस कार्य में शामिल निम्नलिखित कदम हैं।
कदम 1: अभिक्रिया के लिए असंतुलित समीकरण को आयनिक रूप में बनाएँ :
Step 2: Balance the atoms other than oxygen and hydrogen in each half-reaction. For the oxidation half-reaction, the iron atoms are already balanced. For the reduction half-reaction, balance the chromium atoms :
$$\mathrm{Fe}^{2+}(\mathrm{aq})+\mathrm{Cr_2} \mathrm{O_7}^{2-}(\mathrm{aq}) \rightarrow \mathrm{Fe}^{3+}(\mathrm{aq})+\mathrm{Cr}^{3+}(\mathrm{aq}) \tag{8.50}$$
चरण 2: समीकरण को आधा अभिक्रिया में विभाजित करें:
ऑक्सीकरण आधा अभिक्रिया :
$$\mathrm{Fe}^{2+}(\mathrm{aq}) \rightarrow \mathrm{Fe}^{3+}(\mathrm{aq})$$
अपचयन आधा अभिक्रिया :
$$\mathrm{Cr}^{+6}{ } _{2} \mathrm{O} _{7}^{2-}(\mathrm{aq}) \rightarrow \mathrm{Cr}^{+3}(\mathrm{aq})$$
चरण 3: प्रत्येक आधा अभिक्रिया में $O$ और $\mathrm{H}$ के अलावा अन्य परमाणुओं को संतुलित करें। यहाँ ऑक्सीकरण आधा अभिक्रिया $\mathrm{Fe}$ परमाणुओं के संतुलन के लिहाज से पहले से ही संतुलित है। अपचयन आधा अभिक्रिया में, $\mathrm{Cr}^{3+}$ को 2 से गुणा करके $\mathrm{Cr}$ परमाणुओं को संतुलित कर लिया जाता है।
$$\mathrm{Cr_2} \mathrm{O_7}^{2-}(\mathrm{aq}) \rightarrow 2 \mathrm{Cr}^{3+}(\mathrm{aq}) \tag{8.53}$$
चरण 4: अम्लीय माध्यम में होने वाली अभिक्रियाओं के लिए, $\mathrm{O}$ परमाणुओं के संतुलन के लिए $\mathrm{H_2} \mathrm{O}$ और $\mathrm{H}^{+}$ के उपयोग करें।
इस प्रकार हमें प्राप्त होता है :
$$\mathrm{Cr_2} \mathrm{O_7}^{2-}(\mathrm{aq})+14 \mathrm{H}^{+}(\mathrm{aq}) \rightarrow 2 \mathrm{Cr}^{3+}(\mathrm{aq})+7 \mathrm{H_2} \mathrm{O}(\mathrm{l})\tag{8.54}$$
चरण 5: आधा अभिक्रिया के एक तरफ इलेक्ट्रॉन जोड़ें ताकि आवेश का संतुलन हो जाए। आवश्यकता पड़े तो दोनों आधा अभिक्रियाओं में इलेक्ट्रॉन की संख्या बराबर करें, इसके लिए एक या दोनों आधा अभिक्रियाओं को उपयुक्त संख्या से गुणा करें।
ऑक्सीकरण अर्ध-अभिक्रिया को आवेश के संतुलन के लिए इस प्रकार लिखा जाता है:
$$\mathrm{Fe}^{2+}(\mathrm{aq}) \rightarrow \mathrm{Fe}^{3+}(\mathrm{aq})+\mathrm{e}^{-} \tag{8.55}$$
अब अपचयन अर्ध-अभिक्रिया में बाईं ओर आठ से अधिक सकारात्मक आवेश हैं और दाईं ओर केवल छह सकारात्मक आवेश हैं। इसलिए, हम बाईं ओर छह इलेक्ट्रॉन जोड़ते हैं।
$$ \begin{equation*} \mathrm{Cr_2} \mathrm{O_7}^{2-}(\mathrm{aq})+14 \mathrm{H}^{+}(\mathrm{aq})+6 \mathrm{e}^{-} \rightarrow 2 \mathrm{Cr}^{3+}(\mathrm{aq})+ 7\mathrm{H_2O} \tag{8.56}
\end{equation*} $$
दोनों हाफ अभिक्रियाओं में इलेक्ट्रॉन की संख्या को समान बनाने के लिए, हम ऑक्सीकरण हाफ अभिक्रिया को 6 से गुणा करते हैं और इस प्रकार लिखते हैं :
$$6 \mathrm{Fe}^{2+}(\mathrm{aq}) \rightarrow 6 \mathrm{Fe}^{3+}(\mathrm{aq})+6 \mathrm{e}^{-} \tag{8.57}$$
चरण 6: हम दोनों हाफ अभिक्रियाओं को जोड़ते हैं ताकि समग्र अभिक्रिया प्राप्त की जा सके और प्रत्येक तरफ इलेक्ट्रॉन को खत्म कर दें। इससे नेट आयनिक समीकरण निम्नलिखित हो जाता है :
$$6 \mathrm{Fe}^{2+}(\mathrm{aq})+\mathrm{Cr_2} \mathrm{O_7}^{2-}(\mathrm{aq})+14 \mathrm{H}^{+}(\mathrm{aq}) \rightarrow 6 \mathrm{Fe}^{3+}(\mathrm{aq})+ 2 \mathrm{Cr}^{3+}(\mathrm{aq})+7 \mathrm{H_2} \mathrm{O}(\mathrm{l})$$
चरण 7: जांच करें कि समीकरण में दोनों तरफ समान प्रकार और संख्या में परमाणु तथा आवेश हों। इस अंतिम जांच से पता चलता है कि समीकरण परमाणुओं की संख्या और आवेशों के संदर्भ में पूर्ण रूप से संतुलित है।
किसी क्षारीय माध्यम में अभिक्रिया के लिए, सबसे पहले अम्लीय माध्यम में जैसे तरीके से परमाणुओं को संतुलित करें। फिर प्रत्येक $\mathrm{H}^{+}$ आयन के लिए समीकरण के दोनों तरफ समान संख्या में $\mathrm{OH}^{-}$ आयन जोड़ें। जहाँ $\mathrm{H}^{+}$ और $\mathrm{OH}^{-}$ समीकरण के एक ही तरफ उपस्थित हों, उन्हें $\mathrm{H_2} \mathrm{O}$ में संयोजित कर दें।
समस्या 8.10
बेसिक विलयन में परमैंगनेट(VII) आयन, $\mathrm{MnO_4}^{-}$ आयोडाइड आयन, $\mathrm{I}^{-}$ को अणुकृत आयोडीन $\left(\mathrm{I_2}\right)$ और मैंगनेज (IV) ऑक्साइड $\left(\mathrm{MnO_2}\right)$ बनाने में ऑक्सीकृत करता है। इस रेडॉक्स अभिक्रिया को प्रकट करने वाला संतुलित आयनिक समीकरण लिखिए।
हल
चरण 1: सबसे पहले हम आंतरिक आयनिक समीकरण लिखते हैं, जो इस प्रकार है:
$\mathrm{MnO_4}^{-}(\mathrm{aq})+\mathrm{I}^{-}(\mathrm{aq}) \rightarrow \mathrm{MnO_2}(\mathrm{~s})+\mathrm{I_2}(\mathrm{~s})$
स्टेप 2: दो आधी अभिक्रियाएं हैं:
$$ \begin{aligned} & \text { ऑक्सीकरण आधी अभिक्रिया : } \stackrel{-1}{\mathrm{I^-}} \mathrm{(aq)} \rightarrow \stackrel{0}{\mathrm{I_3}}(\mathrm{s}) \end{aligned} $$
$$ \begin{aligned} & \text { अपचयन आधी अभिक्रिया : } \stackrel{+7}{\mathrm{Mn}} \mathrm{O_4}^{-}\mathrm{(aq)} \rightarrow \stackrel{+4}{\mathrm{Mn}} \mathrm{O_2}(\mathrm{s}) \end{aligned} $$
स्टेप 3: ऑक्सीकरण आधी अभिक्रिया में I परमाणुओं के संतुलन के लिए, हम इसे इस तरह लिखते हैं:
$$ 2 \mathrm{I}^{-}(\mathrm{aq}) \rightarrow \mathrm{I_2}(\mathrm{~s})
$$
चरण 4: अपचयन अर्ध-अभिक्रिया में $O$ परमाणुओं के संतुलन के लिए, हम दाएं ओर दो जल अणु जोड़ते हैं:
$\mathrm{MnO_4}^{-}(\mathrm{aq}) \rightarrow \mathrm{MnO_2}$ (s) $+2 \mathrm{H_2} \mathrm{O}$ (l)
$\mathrm{H}$ परमाणुओं के संतुलन के लिए, हम बाएं ओर चार $\mathrm{H}^{+}$ आयन जोड़ते हैं:
$\mathrm{MnO_4}^{-}(\mathrm{aq})+4 \mathrm{H}^{+}(\mathrm{aq}) \rightarrow \mathrm{MnO_2}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O} \mathrm{(l)}$
क्योंकि अभिक्रिया एक क्षारीय विलयन में होती है, इसलिए चार $\mathrm{H}^{+}$ आयन के लिए, हम समीकरण के दोनों ओर चार $\mathrm{OH}^{-}$ आयन जोड़ते हैं:
$\mathrm{MnO_4}^{-}(\mathrm{aq})+4 \mathrm{H}^{+}(\mathrm{aq})+4 \mathrm{OH}^{-}(\mathrm{aq}) \rightarrow\mathrm{MnO_2}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l})+4 \mathrm{OH}^{-}(\mathrm{aq})$
$\mathrm{H}^{+}$ और $\mathrm{OH}^{-}$ आयनों को पानी के साथ बदलने पर, परिणामी समीकरण निम्नलिखित होता है:
$\mathrm{MnO_4}^{-}(\mathrm{aq})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \rightarrow \mathrm{MnO_2}(\mathrm{~s})+4 \mathrm{OH}^{-}(\mathrm{aq})$
स्टेप 5 : इस स्टेप में हम दोनों अर्ध-समीकरणों के आवेश को उस प्रकार संतुलित करते हैं जैसा कि नीचे दिखाया गया है:
$$ \begin{gathered} 2 \mathrm{I}^{-}(\mathrm{aq}) \rightarrow \mathrm{I_2}(\mathrm{~s})+2 \mathrm{e}^{-} \\ \mathrm{MnO_4}^{-}(\mathrm{aq})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l})+3 \mathrm{e}^{-} \rightarrow \mathrm{MnO_2}(\mathrm{~s}) +4 \mathrm{OH}^{-}(\mathrm{aq}) \end{gathered} $$
अब इलेक्ट्रॉन की संख्या को समान करने के लिए, हम ऑक्सीकरण अर्ध-अभिक्रिया को 3 से और अपचयन अर्ध-अभिक्रिया को 2 से गुणा करते हैं।
$6 \mathrm{I}^{-}(\mathrm{aq}) \rightarrow 3 \mathrm{I_2}$ (s) $+6 \mathrm{e}^{-}$
$2 \mathrm{MnO_4}^{-}(\mathrm{aq})+4 \mathrm{H_2} \mathrm{O}$ (l) $+6 \mathrm{e}^{-} \rightarrow 2 \mathrm{MnO_2}(\mathrm{~s})+8 \mathrm{OH}^{-}(\mathrm{aq})$
स्टेप 6: दो आधे अभिक्रियाएं जोड़ें ताकि इलेक्ट्रॉनों को दोनों ओर से खत्म करके शुद्ध अभिक्रिया प्राप्त की जा सके।
$6 \mathrm{I}^{-}(\mathrm{aq})+2 \mathrm{MnO_4}^{-}(\mathrm{aq})+4 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \rightarrow 3 \mathrm{I_2}(\mathrm{~s})+ 2 \mathrm{MnO_2}(\mathrm{~s})+8 \mathrm{OH}^{-}(\mathrm{aq})$
स्टेप 7: अंतिम जांच दिखाती है कि समीकरण दोनों ओर परमाणुओं और आवेशों की संख्या के संदर्भ में संतुलित है।
8.3.3 रेडॉक्स अभिक्रियाएं टिट्रेशन के आधार के रूप में
अम्ल-क्षार प्रणालियों में हम एक विधि के साथ सामना करते हैं जिसे टिट्रेशन कहते हैं, जिसके माध्यम से एक विलयन की शक्ति दूसरे विलयन के विस्थापन के आधार पर निर्धारित की जाती है। इसी तरह, रेडॉक्स प्रणालियों में टिट्रेशन विधि का उपयोग किया जा सकता है ताकि एक अपचायक/ऑक्सीकारक की शक्ति का निर्धारण किया जा सके, जिसके लिए एक रेडॉक्स संवेदी सूचक का उपयोग किया जाता है। रेडॉक्स टिट्रेशन में सूचक के उपयोग को नीचे दिखाया गया है:
(i) एक स्थिति में, अपचायक या ऑक्सीकारक खुद गहरा रंग रखता है, जैसे कि परमैंगनेट आयन, $\mathrm{MnO_4}^{-}$. यहाँ $\mathrm{MnO_4}^{-}$ स्वयं एक सूचक के रूप में कार्य करता है। इस स्थिति में दृश्य अंत बिंदु तब प्राप्त होता है जब अपचायक $\left(\mathrm{Fe}^{2+}\right.$ या $\left.\mathrm{C_2} \mathrm{O_4}{ }^{2-}\right)$ के अंतिम अंश का ऑक्सीकरण हो जाता है और $\mathrm{MnO_4}^{-}$ के सांद्रण के नीचे $10^{-6} \mathrm{~mol} \quad \mathrm{dm}^{-3}$ $\left(10^{-6} \mathrm{~mol} \mathrm{~L}^{-1}\right)$ के बराबर एक पहली बार लंबे समय तक लाल रंग के झांकी के रूप में दिखाई देता है। यह तुलना बिंदु के बाद रंग के अतिरिक्त अंश को न्यूनतम बनाता है, जहाँ अपचायक और ऑक्सीकारक के मोल अनुपात में समानता होती है।
(ii) यदि कोई ड्रामैटिक स्वतः रंग परिवर्तन नहीं होता (जैसे कि $\mathrm{MnO_4}^{-}$ के तिर्यकन के साथ), तो इंडिकेटर उसके अंतिम बिट के उपयोग के बाद तुरंत ऑक्सीकृत हो जाते हैं, जिससे ड्रामैटिक रंग परिवर्तन होता है। सर्वोत्तम उदाहरण $\mathrm{Cr_2} \mathrm{O_7}^{2-}$ द्वारा दिया जाता है, जो स्वयं इंडिकेटर नहीं होता, लेकिन तुल्यांक बिंदु के ठीक बाद इंडिकेटर पदार्थ डाइफेनिलएमीन को ऑक्सीकृत करता है और एक तीव्र नीला रंग उत्पन्न करता है, जिससे अंतिम बिंदु के अंत को संकेत देता है।
(iii) अब एक और विधि है जो दिलचस्प और बहुत सामान्य है। इसका उपयोग केवल उन रासायनिक पदार्थों के लिए सीमित है जो $\mathrm{I}^{-}$ आयनों को ऑक्सीकृत कर सकते हैं, जैसे कि, उदाहरण के लिए,
$$\mathrm{Cu}(\mathrm{II}) : 2 \mathrm{Cu}^{2+}(\mathrm{aq})+4 \mathrm{I}^{-}(\mathrm{aq}) \rightarrow \mathrm{Cu_2} \mathrm{I_2}(\mathrm{~s})+\mathrm{I_2}(\mathrm{aq}) \tag{8.59}$$
इस विधि के आधार इस तथ्य पर है कि आयोडीन आयोडीन एवं स्टार्च के साथ गहरा नीला रंग देती है तथा इसके थायोसल्फेट आयन $\left(\mathrm{S_2} \mathrm{O_3}{ }^{2-}\right)$ के साथ बहुत विशिष्ट प्रतिक्रिया होती है, जो भी एक रेडॉक्स प्रतिक्रिया है:
$$\mathrm{I_2}(\mathrm{aq})+2 \mathrm{~S_2} \mathrm{O_3}^{2-}(\mathrm{aq}) \rightarrow 2 \mathrm{I}^{-}(\mathrm{aq})+\mathrm{S_4} \mathrm{O_6}{ }^{2-}(\mathrm{aq}) \tag{8.60}$$
$\mathrm{I_2}$, हालांकि पानी में अघुलनशील है, लेकिन $\mathrm{KI}$ वाले विलयन में $\mathrm{KI_3}$ के रूप में उपस्थित रहता है।
$\mathrm{Cu}^{2+}$ आयनों के आयोडाइड आयनों पर क्रिया के दौरान आयोडीन के विमुक्त होने के बाद स्टार्च के योग करने पर एक तीव्र नीला रंग दिखाई देता है। जैसे ही आयोडीन थायोसल्फेट आयनों द्वारा उपयोग कर लिया जाता है, यह रंग चले जाते हैं। इस प्रकार, समापन बिंदु को आसानी से ट्रैक किया जा सकता है और शेष भाग केवल आस्टोइकियोमेट्रिक गणना ही है।
8.3.4 ऑक्सीकरण संख्या के अवधारणा की सीमाएं
जैसा कि आप उपरोक्त चर्चा में देख चुके हैं, रेडॉक्स प्रक्रियाओं के अवधारणा के साथ समय के साथ विकास हो रहा है। यह विकास प्रक्रिया जारी रहती है। वास्तव में, हाल के दिनों में, ऑक्सीकरण प्रक्रिया को परमाणुओं के आसपास इलेक्ट्रॉन घनत्व में कमी के रूप में और अपचयन प्रक्रिया को इलेक्ट्रॉन घनत्व में वृद्धि के रूप में देखा जाता है।
8.4 रेडॉक्स अभिक्रियाएँ एवं इलेक्ट्रोड प्रक्रियाएँ
अभिक्रिया (8.15) के संगत प्रयोग को यदि जिंक छड़ को कॉपर सल्फेट विलयन में डुबोया जाए तो इसे भी देखा जा सकता है। रेडॉक्स अभिक्रिया होती है और अभिक्रिया के दौरान जिंक जिंक आयन में ऑक्सीकृत हो जाता है और कॉपर आयन कॉपर के धातु के रूप में अपचयित हो जाते हैं क्योंकि इलेक्ट्रॉन जिंक से कॉपर आयन में सीधे स्थानांतरित होते हैं। इस अभिक्रिया के दौरान ऊष्मा भी उत्सर्जित होती है। अब हम इस प्रयोग को इस प्रकार बदल देते हैं कि एक ही रेडॉक्स अभिक्रिया के लिए इलेक्ट्रॉन के स्थानांतरण के लिए अप्रत्यक्ष रूप से आवश्यकता होती है। इसके लिए जिंक धातु को कॉपर सल्फेट विलयन से अलग कर देना आवश्यक होता है। हम एक बीकर में कॉपर सल्फेट विलयन लेते हैं और इसमें एक कॉपर छड़ या छटी रखते हैं। हम दूसरे बीकर में जिंक सल्फेट विलयन लेते हैं और इसमें एक जिंक छड़ या छटी रखते हैं। अब दोनों बीकरों में अभिक्रिया होती है और प्रत्येक बीकर में धातु और उसके लवण विलयन के संपर्क बिंदु पर एक ही वस्तु के अपचयित एवं ऑक्सीकृत रूप उपस्थित होते हैं। ये वस्तुएँ अपचयन एवं ऑक्सीकरण अर्ध-अभिक्रियाओं में वस्तु के रूप को प्रतिनिधित्व करती हैं। रेडॉक्स युग्म को एक वस्तु के ऑक्सीकृत एवं अपचयित रूप के साथ एक साथ विद्यमान होने के रूप में परिभाषित किया जाता है जो एक ऑक्सीकरण या अपचयन अर्ध-अभिक्रिया में भाग ले रही हो।
यह एक लंबवत रेखा या एक विभाजक चिह्न (जैसे स्थैतिक/समाधान) द्वारा ऑक्सीकृत रूप और अपचयित रूप के बीच अलग करके दर्शाया जाता है। उदाहरण के लिए, इस प्रयोग में दो रेडॉक्स युग्म $\mathrm{Zn}^{2+} / \mathrm{Zn}$ और $\mathrm{Cu}^{2+} / \mathrm{Cu}$ के रूप में दर्शाए गए हैं। दोनों मामलों में, ऑक्सीकृत रूप को अपचयित रूप के पहले लिखा जाता है।

चित्र 8.3 डानियल सेल के सेट-अप। जिंक के ऑक्सीकरण के कारण एनोड पर उत्पन्न इलेक्ट्रॉन बाहरी परिपथ के माध्यम से कैथोड तक जाते हैं, जहां ये कॉपर आयनों को अपचयित करते हैं। सेल के भीतर परिपथ को लवण पुली के माध्यम से आयनों के प्रवाह द्वारा पूरा किया जाता है। ध्यान देने योग्य है कि विद्युत धारा की दिशा इलेक्ट्रॉन प्रवाह की दिशा के विपरीत होती है।
अब हम तांबा सल्फेट विलयन वाले बीकर और जिंक सल्फेट विलयन वाले बीकर को एक दूसरे के ओर रखते हैं (चित्र 7.3)। हम दोनों बीकरों के विलयन को एक लवण पुली (एक U-नली जिसमें पोटेशियम क्लोराइड या एमोनियम नाइट्रेट के घोल आमतौर पर आग लगाकर ठोस हो जाते हैं और बाद में ठंडा होकर जेल जैसे पदार्थ बन जाते हैं) के माध्यम से जोड़ते हैं। यह दोनों विलयनों के बीच विद्युत संपर्क प्रदान करता है लेकिन उनके बीच मिश्रण करने की अनुमति नहीं देता। जिंक और कॉपर के छड़ों को एक धातु तार के माध्यम से जोड़ा जाता है जिसमें एमीटर और स्विच के लिए सुविधा होती है। चित्र 7.3 में दिखाए गए सेट-अप को डानियल सेल कहा जाता है। जब स्विच बंद नहीं होता है, तो दोनों बीकरों में कोई अभिक्रिया नहीं होती और धातु तार में कोई विद्युत धारा प्रवाह नहीं होती। जैसे ही स्वि चालू हो जाता है, हम निम्नलिखित अवलोकन करते हैं:
1. इलेक्ट्रॉनों के स्थानांतरण अब $\mathrm{Zn}$ से $\mathrm{Cu}^{2+}$ के सीधे नहीं हो रहा है बल्कि दो छड़ों को जोड़ने वाले धातु के तार के माध्यम से हो रहा है, जैसा कि तीर से स्पष्ट है जो धारा के प्रवाह को दर्शाता है।
2. एक बीकर में घोल से दूसरे बीकर में घोल तक बिजली के प्रवाह के लिए आयनों के अपवाह द्वारा नमक के पुल के माध्यम से होता है। हम जानते हैं कि धारा के प्रवाह के लिए केवल ताम्बा और जस्ता छड़ों के बीच विभवांतर की आवश्यकता होती है, जिसे यहाँ इलेक्ट्रोड के रूप में जाना जाता है।
प्रत्येक इलेक्ट्रोड के साथ संबंधित संभावना को इलेक्ट्रोड विभव के रूप में जाना जाता है। यदि इलेक्ट्रोड अभिक्रिया में भाग लेने वाले प्रत्येक अणु की सांद्रता एक (यदि इलेक्ट्रोड अभिक्रिया में कोई गैस उपस्थित हो, तो इसे 1 वायुमंडलीय दबाव पर सीमित कर दिया जाता है) और इसके अलावा अभिक्रिया $298 \mathrm{~K}$ पर की जाती है, तो प्रत्येक इलेक्ट्रोड के विभव को मानक इलेक्ट्रोड विभव कहा जाता है। परंपरा के अनुसार, हाइड्रोजन इलेक्ट्रोड का मानक इलेक्ट्रोड विभव $\left(\mathrm{E}^{\ominus}\right)$ 0.00 वोल्ट होता है। प्रत्येक इलेक्ट्रोड प्रक्रिया के इलेक्ट्रोड विभव मान उस प्रक्रिया में सक्रिय अणु के ऑक्सीकृत/अपचयित रूप में रहने की संभावना के संबंध में मापदंड होता है। एक नकारात्मक $\mathrm{E}^{\ominus}$ यह दर्शाता है कि रेडॉक्स युग्म $\mathrm{H}^{+} / \mathrm{H_2}$ युग्म की तुलना में एक शक्तिशाली अपचायक एजेंट है। एक धनात्मक $\mathrm{E}^{\ominus}$ यह दर्शाता है कि रेडॉक्स युग्म $\mathrm{H}^{+} / \mathrm{H_2}$ युग्म की तुलना में एक कम शक्तिशाली अपचायक एजेंट है। मानक इलेक्ट्रोड विभव बहुत महत्वपूर्ण होते हैं और हम उनसे बहुत सारी उपयोगी जानकारी प्राप्त कर सकते हैं। कुछ चयनित इलेक्ट्रोड प्रक्रियाओं (अपचयन अभिक्रियाओं) के मानक इलेक्ट्रोड विभव के मान तालिका 8.1 में दिए गए हैं। आप कक्षा XII में इलेक्ट्रोड अभिक्रियाओं और सेलों के बारे में अधिक जानेंगे।
सारणी 7.1 298 K पर मानक इलेक्ट्रोड विभव
आयन जलीय विषम रूप में उपस्थित होते हैं और $H_2O$ तरल रूप में होता है; गैस और ठोस क्रमशः g और s द्वारा दर्शाए जाते हैं।

-
एक नकारात्मक E यह दर्शाता है कि रेडॉक्स युग्म $ H^{+} / H_2 $ युग्म की तुलना में एक शक्तिशाली अपचायक एजेंट है।
-
एक धनात्मक E यह दर्शाता है कि रेडॉक्स युग्म $ H^{+} / H_2 $ युग्म की तुलना में एक कम शक्तिशाली अपचायक एजेंट है।
सारांश
रेडॉक्स अभिक्रियाएं एक महत्वपूर्ण श्रेणी की अभिक्रियाएं होती हैं जहां ऑक्सीकरण और अपचयन एक साथ होते हैं। तीन स्तरीय अवधारणाएं, जैसे कि क्लासिकल, इलेक्ट्रॉनिक और ऑक्सीकरण संख्या, जो कि पाठ्यपुस्तकों में आमतौर पर उपलब्ध होती हैं, विस्तार से प्रस्तुत की गई हैं। ऑक्सीकरण, अपचयन, ऑक्सीकरण एजेंट (ऑक्सीडेंट) और अपचयन एजेंट (रेडक्टेंट) को प्रत्येक अवधारणा के अनुसार देखा गया है। ऑक्सीकरण संख्या को एक सांतर नियमों के अनुसार निर्धारित किया जाता है। ऑक्सीकरण संख्या और आयन-इलेक्ट्रॉन विधि दोनों ही रेडॉक्स अभिक्रियाओं के समीकरण लिखने में उपयोगी तरीके हैं। रेडॉक्स अभिक्रियाएं चार श्रेणियों में वर्गीकृत होती हैं: संयोजन, विघटन, विस्थापन और अपचयन अभिक्रियाएं। यहां रेडॉक्स जोड़े और इलेक्ट्रोड प्रक्रियाओं की अवधारणा को परिचय दिया गया है। रेडॉक्स अभिक्रियाएं इलेक्ट्रोड प्रक्रियाओं और सेलों के अध्ययन में व्यापक रूप से उपयोग की जाती हैं।



