अध्याय 09 जैव अणु
हमारे जैवमंडल में जीवित जीवों की एक विस्तृत विविधता है। अब हमारे मन में एक प्रश्न उठता है: क्या सभी जीवित जीव एक ही रसायनों, अर्थात् तत्वों और यौगिकों से बने हैं? आपने रसायन विज्ञान में सीखा है कि तत्व विश्लेषण कैसे किया जाता है। यदि हम पादप ऊतक, पशु ऊतक या सूक्ष्मजीव पेस्ट पर ऐसा विश्लेषण करें, तो हमें कार्बन, हाइड्रोजन, ऑक्सीजन और कई अन्य तत्वों की एक सूची और जीवित ऊतक की प्रति इकाई द्रव्यमान में उनकी संबंधित सामग्री प्राप्त होती है। यदि वही विश्लेषण पृथ्वी की पपड़ी के एक टुकड़े पर — अजीव पदार्थ के उदाहरण के रूप में — किया जाता है, तो हमें एक समान सूची प्राप्त होती है। इन दोनों सूचियों के बीच क्या अंतर हैं? निरपेक्ष पदों में, कोई ऐसा अंतर स्पष्ट नहीं होता। पृथ्वी की पपड़ी के नमूने में मौजूद सभी तत्व जीवित ऊतक के नमूने में भी मौजूद होते हैं। हालांकि, एक निकट परीक्षण से पता चलता है कि अन्य तत्वों के सापेक्ष कार्बन और हाइड्रोजन की सापेक्ष प्रचुरता किसी भी जीवित जीव में पृथ्वी की पपड़ी की तुलना में अधिक होती है (तालिका 9.1)।
9.1 रासायनिक संघटन का विश्लेषण कैसे करें?
हम इसी तरह पूछते रह सकते हैं, जीवित जीवों में किस प्रकार के कार्बनिक यौगिक पाए जाते हैं? इस प्रश्न का उत्तर कैसे प्राप्त किया जाए? उत्तर पाने के लिए रासायनिक विश्लेषण करना होता है। हम कोई भी जीवित ऊतक (एक सब्जी या लीवर का टुकड़ा आदि) ले सकते हैं और इसे मोर्टार और पेस्टल की सहायता से ट्राइक्लोरोएसिटिक अम्ल (Cl3CCOOH) में पीस सकते हैं। हमें एक गाढ़ा गाढ़ा लेई मिलता है। यदि हम इसे चीज़क्लोथ या सूती कपड़े से छानें तो हमें दो भाग प्राप्त होते हैं। एक को फिल्ट्रेट या तकनीकी रूप से अम्ल-विलेय पूल कहा जाता है, और दूसरे को रिटेनेट या अम्ल-अविलेय भाग। वैज्ञानिकों ने अम्ल-विलेय पूल में हजारों कार्बनिक यौगिक पाए हैं।
उच्च कक्षाओं में आप सीखेंगे कि किसी जीवित ऊतक के नमूने का विश्लेषण कैसे किया जाता है और किसी विशिष्ट कार्बनिक यौगिक की पहचान कैसे की जाती है। यहाँ इतना कहना पर्याप्त होगा कि यौगिकों को निकाला जाता है, फिर उस निकाले गए भाग को विभिन्न पृथक्करण तकनीकों के अधीन किया जाता है जब तक कि कोई यौगिक अन्य सभी यौगिकों से अलग न हो जाए। दूसरे शब्दों में, कोई यौगिक को पृथक करता है और शुद्ध करता है। विश्लेषणात्मक तकनीकों को जब उस यौगिक पर लागू किया जाता है तो हमें अणुसूत्र और यौगिक की संभावित संरचना का एक अनुमान मिलता है। सभी कार्बन यौगिक जो हम जीवित ऊतकों से प्राप्त करते हैं, उन्हें ‘जैव अणु’ कहा जा सकता है। हालाँकि, जीवित जीवों में अकार्बनिक तत्व और यौगिक भी होते हैं। हमें यह कैसे पता है? एक थोड़ा अलग लेकिन विनाशकारी प्रयोग करना होता है। कोई जीवित ऊतक की थोड़ी मात्रा (मान लीजिए एक पत्ती या यकृत और इसे तर वजन कहा जाता है) को तौलता है और उसे सुखाता है। सारा पानी वाष्पित हो जाता है। शेष बची सामग्री शुष्क वजन देती है। अब यदि ऊतक को पूरी तरह से जला दिया जाए, तो सभी कार्बन यौगिक गैसीय रूप में ऑक्सीकृत हो जाते हैं (CO₂, जल वाष्प) और निकल जाते हैं। जो बचता है उसे ‘राख’ कहा जाता है। इस राख में अकार्बनिक तत्व (जैसे कैल्शियम, मैग्नीशियम आदि) होते हैं। सल्फेट, फॉस्फेट आदि जैसे अकार्बनिक यौगिक अम्ल-घुलनशील अंश में भी देखे जाते हैं। इसलिए तत्वीय विश्लेषण जीवित ऊतकों में तत्वीय संघटन को हाइड्रोजन, ऑक्सीजन, क्लोरीन, कार्बन आदि के रूप में देता है।
TABLE 9.1 A Comparison of Elements Present in Non-living and Living Matter
| तत्व | % भार पृथ्वी की भूपटल मानव शरीर |
|
|---|---|---|
| हाइड्रोजन (H) | 0.14 | 0.5 |
| कार्बन (C) | 0.03 | 18.5 |
| ऑक्सीजन (O) | 46.6 | 65.0 |
| नाइट्रोजन (N) | बहुत कम | 3.3 |
| सल्फर (S) | 0.03 | 0.3 |
| सोडियम (Na) | 2.8 | 0.2 |
| कैल्शियम (Ca) | 3.6 | 1.5 |
| मैग्नीशियम (Mg) | 2.1 | 0.1 |
| सिलिकॉन (Si) | 27.7 | नगण्य |
| * सी.एन.आर. राव, अंडरस्टैंडिंग केमिस्ट्री से अनुकूलित। | ||
| यूनिवर्सिटीज प्रेस, हैदराबाद। |
तालिका 9.2 जीवित ऊतकों के प्रतिनिधि अकार्बनिक घटकों की सूची
| घटक | सूत्र |
|---|---|
| सोडियम | $\mathrm{Na}^{+}$ |
| पोटैशियम | $\mathrm{K}^{+}$ |
| कैल्शियम | $\mathrm{Ca}^{++}$ |
| मैग्नीशियम | $\mathrm{Mg}^{++}$ |
| जल | $\mathrm{H}_2 \mathrm{O}$ |
| यौगिक | $\mathrm{NaCl}^{+}, \mathrm{CaCO}_3$, |
| $\mathrm{PO}_4^{3-}, \mathrm{SO}_4^{2-}$ |
जबकि यौगिकों के विश्लेषण से जीवित ऊतकों में उपस्थित कार्बनिक (चित्र 9.1) और अकार्बनिक घटकों (तालिका 9.2) के प्रकार का अनुमान लगाया जा सकता है। रसायन विज्ञान के दृष्टिकोण से कोई एल्डिहाइड, कीटोन, एरोमैटिक यौगिक आदि जैसे कार्यात्मक समूहों की पहचान कर सकता है। परंतु जीव विज्ञान के दृष्टिकोण से हम उन्हें अमीनो अम्ल, न्यूक्लियोटाइड क्षारक, फैटी अम्ल आदि में वर्गीकृत करेंगे। जीवित और अजीवित पदार्थों में उपस्थित तत्वों की तुलना*
अमीनो अम्ल ऐसे कार्बनिक यौगिक होते हैं जिनमें एक ही कार्बन, अर्थात् α-कार्बन पर एक अमीनो समूह और एक अम्लीय समूह उपस्थित होते हैं। इसलिए इन्हें α-अमीनो अम्ल कहा जाता है। ये प्रतिस्थापित मीथेन होते हैं। चार वैलेन्सी स्थानों पर चार प्रतिस्थापक समूह कब्जा करते हैं। ये हैं—हाइड्रोजन, कार्बोक्सिल समूह, अमीनो समूह और एक चर समूह जिसे R समूह कहा जाता है। R समूह की प्रकृति के आधार पर कई प्रकार के अमीनो अम्ल होते हैं, पर प्रोटीनों में पाए जाने वाले केवल बीस प्रकार के होते हैं। इन प्रोटीनयुक्त अमीनो अम्लों में R समूह हाइड्रोजन (तब अमीनो अम्ल को ग्लाइसिन कहते हैं), मेथिल समूह (एलानिन), हाइड्रॉक्सी मेथिल (सेरिन) आदि हो सकता है। इन बीस में से तीन को चित्र 9.1 में दिखाया गया है।
अमीनो अम्लों के रासायनिक और भौतिक गुण मुख्यतः अमीनो, कार्बोक्सिल और R कार्यात्मक समूहों के होते हैं। अमीनो और कार्बोक्सिल समूहों की संख्या के आधार पर ये अम्लीय (जैसे ग्लूटामिक अम्ल), क्षारीय (लाइसिन) और उदासीन (वैलिन) अमीनो अम्लों में वर्गीकृत होते हैं। इसी प्रकार, एरोमैटिक अमीनो अम्ल (टायरोसिन, फ़ेनिलएलानिन, ट्रिप्टोफ़ैन) भी होते हैं। अमीनो अम्लों का एक विशिष्ट गुण –NH2 और –COOH समूहों की आयनयोग्य प्रकृति है; इसलिए विभिन्न pH के विलयनों में अमीनो अम्लों की संरचना बदल जाती है।

लिपिड्स आमतौर पर पानी में अघुलनशील होते हैं। ये सरल फैटी एसिड हो सकते हैं। एक फैटी एसिड में कार्बोक्सिल समूह एक R समूह से जुड़ा होता है। R समूह एक मेथिल (–CH3), या एथिल (–C2H5) या अधिक संख्या में –CH2 समूह (1 कार्बन से 19 कार्बन तक) हो सकता है। उदाहरण के लिए, पामिटिक एसिड में 16 कार्बन होते हैं जिनमें कार्बोक्सिल कार्बन भी शामिल है। अरैकिडोनिक एसिड में 20 कार्बन परमाणु होते हैं जिनमें कार्बोक्सिल कार्बन भी शामिल है। फैटी एसिड संतृप्त (बिना डबल बॉन्ड) या असंतृप्त (एक या अधिक C=C डबल बॉन्ड के साथ) हो सकते हैं। एक अन्य सरल लिपिड ग्लिसरॉल है जो ट्राइहाइड्रॉक्सी प्रोपेन है। कई लिपिड्स में ग्लिसरॉल और फैटी एसिड दोनों होते हैं। यहाँ फैटी एसिड ग्लिसरॉल के साथ एस्टरिफाइड पाए जाते हैं। ये मोनोग्लिसराइड्स, डाइग्लिसराइड्स और ट्राइग्लिसराइड्स हो सकते हैं। इन्हें गलनांक के आधार पर वसा और तेल भी कहा जाता है। तेलों का गलनांक कम होता है (जैसे तिल का तेल) और इसलिए ये सर्दियों में तेल के रूप में रहते हैं। क्या आप बाजार से वसा की पहचान कर सकते हैं? कुछ लिपिड्स में फॉस्फोरस और एक फॉस्फोरिलेटेड कार्बनिक यौगिक होता है। ये फॉस्फोलिपिड्स होते हैं। ये कोशिका झिल्ली में पाए जाते हैं। लेसिथिन एक उदाहरण है। कुछ ऊतक विशेष रूप से तंत्रिका ऊतक अधिक जटिल संरचना वाले लिपिड्स रखते हैं।
जीवित जीवों में कार्बन के कई यौगिक होते हैं जिनमें हेट्रोसाइक्लिक वलय पाए जाते हैं। इनमें से कुछ नाइट्रोजन आधार हैं - एडेनिन, ग्वानिन, साइटोसिन, यूरेसिल और थाइमिन। जब ये किसी शर्करा से जुड़े होते हैं, तो इन्हें न्यूक्लियोसाइड कहा जाता है। यदि शर्करा से फॉस्फेट समूह भी एस्टरिफाइड हो तो इन्हें न्यूक्लियोटाइड कहा जाता है। एडेनोसिन, ग्वानोसिन, थाइमिडिन, यूरिडिन और साइटिडिन न्यूक्लियोसाइड हैं। एडेनिलिक अम्ल, थाइमिडिलिक अम्ल, ग्वानिलिक अम्ल, यूरिडिलिक अम्ल और साइटिडिलिक अम्ल न्यूक्लियोटाइड हैं। डीएनए और आरएनए जैसी न्यूक्लिक अम्ल केवल न्यूक्लियोटाइड से बनी होती हैं। डीएनए और आरएनए जीनेटिक पदार्थ के रूप में कार्य करते हैं।

आकृति 9.1 जीवित ऊतकों में छोटे अणुभार कार्बनिक यौगिकों का आरेखीय प्रतिनिधित्व
9.2 प्राथमिक और द्वितीयक उपापचयिक
रसायन विज्ञान का सबसे रोमांचक पहलू जीवित जीवों से हजारों छोटे-बड़े यौगिकों को पृथक करना, उनकी संरचना निर्धारित करना और यदि संभव हो तो उनका संश्लेषण करना है।
यदि कोई जैव-अणुओं की सूची बनाए, तो ऐसी सूची में अमीनो अम्ल, शर्कराएँ आदि सहित हजारों कार्बनिक यौगिक होंगे। जिन कारणों की व्याख्या अनुभाग 9.10 में दी गई है, हम इन जैव-अणुओं को ‘उपापचयज’ कह सकते हैं। पशु ऊतकों में चित्र 9.1 में दिखाए गए सभी वर्गों के यौगिक उपस्थित पाए जाते हैं। इन्हें प्राथमिक उपापचयज कहा जाता है। तथापि, जब कोई पादप, कवक और सूक्ष्मजीव कोशिकाओं का विश्लेषण करता है, तो इन प्राथमिक उपापचयजों के अतिरिक्त हजारों अन्य यौगिक देखे जाते हैं, जैसे क्षारीय यौगिक, फ़्लेवोनॉयड, रबर, आवश्यक तेल, प्रतिजैविक, रंगीन वर्णक, सुगंध, गोंद, मसाले। इन्हें द्वितीयक उपापचयज कहा जाता है (तालिका 9.3)। जबकि प्राथमिक उपापचयजों की पहचान योग्य कार्य होते हैं और वे सामान्य शारीरिक प्रक्रियाओं में ज्ञात भूमिकाएँ निभाते हैं, हम इस समय मेज़बान जीवों में सभी ‘द्वितीयक उपापचयजों’ की भूमिका या कार्यों को नहीं समझते हैं। तथापि, इनमें से कई ‘मानव कल्याण’ के लिए उपयोगी हैं (जैसे रबर, औषधियाँ, मसाले, सुगंध और लेक्टिन्स कॉन्केनवेलिन ए वर्णक)। कुछ द्वितीयक उपापचयजों का पारिस्थितिक महत्व है। आगामी अध्यायों और वर्षों में आप इसके बारे में और अधिक जानेंगे।
तालिका 9.3 कुछ द्वितीयक उपापचयज
| वर्णक | कैरोटीनॉयड, एंथोसायनिन, आदि |
|---|---|
| क्षारीय यौगिक | मॉर्फिन, कोडीन, आदि |
| टरपेनॉयड | मोनोटरपीन, डाइटरपीन आदि |
| आवश्यक तेल | लेमनग्रास ऑयल, आदि |
| विषाक्त पदार्थ | एब्रिन, रिसिन |
| लेक्टिन | कॉन्केनावेलिन A |
| औषधियाँ | विनब्लास्टिन, करक्यूमिन, आदि |
| बहुलकीय पदार्थ |
रबर, गम, सेल्युलोज |
9.3 जैव-बृहदाणु
इन सभी यौगिकों में जो अम्ल-घुलनशील पूल में पाए जाते हैं, एक सामान्य विशेषता होती है। इनका आण्विक भार लगभग 18 से 800 डाल्टन (Da) तक होता है।
अम्ल-अघुलनशील भाग में केवल चार प्रकार के कार्बनिक यौगिक होते हैं—प्रोटीन, न्यूक्लिक अम्ल, पॉलीसैकेराइड और लिपिड। इनमें से लिपिड को छोड़कर शेष सभी यौगिकों का आण्विक भार दस हजार डाल्टन या उससे अधिक होता है। इसी कारण जीवों में पाए जाने वाले रासायनिक यौगिकों, अर्थात् जैव-अणुओं को दो प्रकारों में बाँटा गया है। पहले वे जिनका आण्विक भार एक हजार डाल्टन से कम होता है, उन्हें सामान्यतः सूक्ष्म-अणु या केवल जैव-अणु कहा जाता है, जबकि जो यौगिक अम्ल-अघुलनशील भाग में पाए जाते हैं उन्हें बृहदाणु या जैव-बृहदाणु कहा जाता है।
अघुलनशील अंश में उपस्थित अणुओं को छोड़कर लिपिड, बहुलकीय पदार्थ होते हैं। फिर लिपिड, जिनका आण्विक भार 800 Da से अधिक नहीं होता, अम्ल-अघुलनशील अंश, अर्थात् बृहत्-आण्विक अंश में क्यों आते हैं? लिपिड वास्तव में छोटे आण्विक भार के यौगिक हैं और केवल स्वतंत्र रूप से ही नहीं, बल्कि कोशिका झिल्ली तथा अन्य झिल्लियों जैसी संरचनाओं में भी व्यवस्थित रहते हैं। जब हम ऊतक को पीसते हैं, तो कोशिका संरचना भंग हो जाती है। कोशिका झिल्ली तथा अन्य झिल्लियाँ टुकड़ों में टूट जाती हैं और वेसिकल्स बनाती हैं जो जल में विलेय नहीं होतीं। इसलिए ये झिल्ली अंश वेसिकल्स के रूप में अम्ल-अघुलनशील पूल के साथ अलग हो जाते हैं और इस प्रकार बृहत्-आण्विक अंश में चले जाते हैं। लिपिड कड़ाई से बृहत्-आण्विक अणु नहीं हैं।
अम्ल-विलेय पूल लगभग कोशिकाद्रव्यीय संघटन को दर्शाता है। कोशिकाद्रव्य तथा कोशिकांगों से आने वाले बृहत्-आण्विक पदार्थ अम्ल-अघुलनशील अंश बन जाते हैं। दोनों मिलकर किसी जीवित ऊतक या जीव के संपूर्ण रासायनिक संघटन को प्रस्तुत करते हैं।
संक्षेप में, यदि हम जीवित ऊतक के रासायनिक संघटन को बहुलता के दृष्टिकोण से प्रस्तुत करें और वर्गवार व्यवस्थित करें, तो हम देखते हैं कि जल जीवित जीवों में सबसे अधिक मात्रा वाला रसायन है (Table 9.4)।
TABLE 9.4 कोशिकाओं की औसत संरचना
| घटक | $%$ of the total cellular mass |
|---|---|
| Water | $70-90$ |
| Proteins | $10-15$ |
| Carbohydrates | 3 |
| Lipids | 2 |
| Nucleic acids | $5-7$ |
| Ions | 1 |
9.4 PROTEINS
प्रोटीन पॉलीपेप्टाइड होते हैं। ये अमीनो अम्लों की रेखीय श्रृंखलाएँ होती हैं जो पेप्टाइड बॉन्ड द्वारा जुड़ी होती हैं जैसा कि चित्र 9.3 में दिखाया गया है।
प्रत्येक प्रोटीन अमीनो अम्लों का एक बहुलक होता है। चूँकि 20 प्रकार के अमीनो अम्ल होते हैं (जैसे एलानिन, सिस्टीन, प्रोलिन, ट्रिप्टोफेन, लाइसिन आदि), एक प्रोटीन हेटेरोपॉलिमर होता है न कि होमोपॉलिमर। एक होमोपॉलिमर में केवल एक ही प्रकार का मोनोमर ‘n’ बार दोहराया जाता है। अमीनो अम्लों की सामग्री के बारे में यह जानकारी महत्वपूर्ण है क्योंकि आगे चलकर आपके पोषण पाठों में आप सीखेंगे कि कुछ अमीनो अम्ल हमारे स्वास्थ्य के लिए आवश्यक होते हैं और इन्हें हमारे आहार के माध्यम से देना पड़ता है। इसलिए, आहारीय प्रोटीन आवश्यक अमीनो अम्लों का स्रोत होते हैं। इस प्रकार, अमीनो अम्ल आवश्यक या अनावश्यक हो सकते हैं। अनावश्यक वे होते हैं जो हमारा शरीर बना सकता है, जबकि आवश्यक अमीनो अम्ल हमें अपने आहार/भोजन के माध्यम से मिलते हैं। प्रोटीन जीवित जीवों में कई कार्य करते हैं, कुछ पोषक तत्वों को कोशिका झिल्ली के पार पहुँचाते हैं, कुछ संक्रामक जीवों से लड़ते हैं, कुछ हार्मोन होते हैं, कुछ एंजाइम होते हैं आदि (तालिका 9.5)। कोलाजन पशु जगत में सबसे प्रचुर प्रोटीन है और रिब्युलोस बिस्फॉस्फेट कार्बोक्सिलेस-ऑक्सीजनेस (RuBisCO) पूरे जैवमंडल में सबसे प्रचुर प्रोटीन है।
तालिका 9.5 कुछ प्रोटीन और उनके कार्य
| प्रोटीन | कार्य |
|---|---|
| कोलाजन | अंतःकोशिकीय आधार पदार्थ |
| ट्रिप्सिन | एंजाइम |
| इंसुलिन | हार्मोन |
| एंटीबॉडी | संक्रामक एजेंटों से लड़ता है |
| रिसेप्टर | संवेदी ग्रहण (गंध, स्वाद, हार्मोन, आदि) |
| GLUT-4 | कोशिकाओं में ग्लूकोज परिवहन को सक्षम बनाता है |
9.5 पॉलीसैकेराइड्स
अम्ल अघुलनशील गोली में पॉलीसैकेराइड्स (कार्बोहाइड्रेट्स) भी एक अन्य वर्ग के बड़े अणुओं के रूप में होते हैं। पॉलीसैकेराइड्स चीनी की लंबी श्रृंखलाएं होती हैं। ये धागे (शाब्दिक रूप से एक सूती धागा) होते हैं जिनमें विभिन्न मोनोसैकेराइड्स बिल्डिंग ब्लॉक्स के रूप में होते हैं। उदाहरण के लिए, सेल्युलोज एक बहुलक पॉलीसैकेराइड है जिसमें केवल एक प्रकार का मोनोसैकेराइड होता है, अर्थात् ग्लूकोज। सेल्युलोज एक समबहुलक है। स्टार्च इसका एक रूपांतर है लेकिन यह पादप ऊतकों में ऊर्जा के भंडार के रूप में उपस्थित होता है। जानवरों में इसका एक अन्य रूपांतर ग्लाइकोजन कहलाता है। इनुलिन फ्रुक्टोज का एक बहुलक है। एक पॉलीसैकेराइड श्रृंखला में (मान लीजिए ग्लाइकोजन), दायां सिरा अपचयी सिरा कहलाता है और बायां सिरा अनपचयी सिरा कहलाता है। इसमें शाखाएं होती हैं जैसा कि एक कार्टून के रूप में दिखाया गया है (चित्र 9.2)। स्टार्च हेलिकल द्वितीयक संरचनाएं बनाता है। वास्तव में, स्टार्च हेलिकल भाग में I2 अणुओं को धारण कर सकता है। स्टार्च-I2 नीले रंग का होता है। सेल्युलोज में जटिल हेलिक्स नहीं होते हैं और इसलिए यह I2 को धारण नहीं कर सकता।

आकृति 9.2 ग्लाइकोजन के एक भाग का आरेखीय प्रतिनिधित्व
पादप कोशिका भित्तियाँ सेल्यूलोज़ से बनी होती हैं। पादप गुद्दे और कपास के रेशे से बना काग़ज़ सेल्यूलोसिक होता है। प्रकृति में अधिक जटिल पॉलिसैकेराइड होते हैं। इनके संरचनात्मक इकाइयाँ अमीनो-शर्कराएँ और रासायनिक रूप से संशोधित शर्कराएँ होती हैं (जैसे ग्लूकोसैमीन, N-एसिटिल गैलेक्टोसैमीन आदि)। उदाहरण के लिए, आर्थ्रोपोड्स के बाह्यकंकाल में एक जटिल पॉलिसैकेराइड काइटिन होता है। ये जटिल पॉलिसैकेराइड अधिकांशतः समबहुलक होते हैं।
9.6 न्यूक्लिक अम्ल
कोई अन्य प्रकार का बृहत् अणु जो किसी भी जीवित ऊतक के अम्ल अविलेय भाग में पाया जाता है, वह न्यूक्लिक अम्ल है। ये पॉलिन्यूक्लियोटाइड होते हैं। पॉलिसैकेराइड और पॉलिपेप्टाइड के साथ मिलकर ये किसी भी जीवित ऊतक या कोशिका के वास्तविक बृहत् अणु भाग का निर्माण करते हैं। न्यूक्लिक अम्लों के लिए संरचनात्मक इकाई न्यूक्लियोटाइड होती है। एक न्यूक्लियोटाइड में तीन रासायनिक रूप से भिन्न घटक होते हैं। एक विषुवतीय चक्रीय यौगिक, दूसरा एक मोनोसैकेराइड और तीसरा फॉस्फोरिक अम्ल या फॉस्फेट।
जैसा कि आप चित्र 9.1 में देखते हैं, न्यूक्लिक अम्लों में उपस्थित विषमचक्रिक यौगिक नाइट्रोजनीय क्षार हैं जिनके नाम एडेनिन, ग्वानिन, यूरेसिल, साइटोसिन और थाइमिन हैं। एडेनिन और ग्वानिन प्रतिस्थापित प्यूरीन हैं जबकि शेष प्रतिस्थापित पिरिमिडिन हैं। अस्थायी विषमचक्रिक वलय को क्रमशः प्यूरीन और पिरिमिडिन कहा जाता है। पॉलिन्यूक्लिओटाइड में पाया जाने वाला शर्करा या तो राइबोज (एक मोनोसैकेराइड पेन्टोज) या 2’-डिऑक्सीराइबोज होता है। एक न्यूक्लिक अम्ल जिसमें डिऑक्सीराइबोज होता है उसे डिऑक्सीराइबोन्यूक्लिक अम्ल (DNA) कहा जाता है जबकि जिसमें राइबोज होता है उसे राइबोन्यूक्लिक अम्ल (RNA) कहा जाता है।
9.7 प्रोटीनों की संरचना
प्रोटीन, जैसा कि पहले उल्लेख किया गया है, अमीनो अम्लों की श्रृंखला वाले विषमबहुलक होते हैं। अणुओं की संरचना से विभिन्न संदर्भों में भिन्न-भिन्न बातें तात्पर्यित होती हैं। अकार्बनिक रसायन में संरचना सदैव आण्विक सूत्रों (जैसे NaCl, MgCl₂ आदि) को संदर्भित करती है। कार्बनिक रसायनज्ञ अणुओं की संरचना का प्रतिनिधित्व करते समय सदैव द्वि-आयामी दृश्य लिखते हैं (जैसे बेंजीन, नैफ्थलीन आदि)। भौतिकविद् अणु संरचनाओं की त्रि-आयामी दृश्य कल्पना करते हैं जबकि जीवविज्ञानी प्रोटीन संरचना को चार स्तरों पर वर्णित करते हैं। अमीनो अम्लों का क्रम, अर्थात् एक प्रोटीन में स्थितिगत सूचना—कौन-सा पहला अमीनो अम्ल है, दूसरा कौन-सा है, और इसी तरह—प्रोटीन की प्राथमिक संरचना (चित्र 9.3a) कहलाती है।
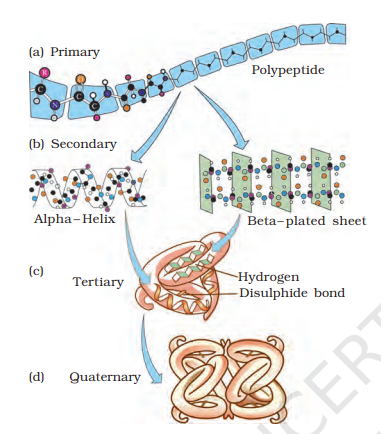
चित्र 9.3 प्रोटीन संरचना के विभिन्न स्तर
एक प्रोटीन को एक रेखा के रूप में कल्पित किया जाता है, बायाँ छोर पहले अमीनो अम्ल से और दायाँ छोर अंतिम अमीनो अम्ल से प्रदर्शित होता है। पहले अमीनो अम्ल को N-टर्मिनल अमीनो अम्ल भी कहा जाता है। अंतिम अमीनो अम्ल को C-टर्मिनल अमीनो अम्ल कहा जाता है। प्रोटीन की यह धागी पूरी लंबाई में एक फैली हुई कठोर छड़ के रूप में नहीं होती। यह धागी एक हेलिक्स के रूप में मुड़ी होती है (एक घूमती हुई सीढ़ी के समान)। निश्चय ही, प्रोटीन धागी के केवल कुछ भाग ही हेलिक्स के रूप में व्यवस्थित होते हैं। प्रोटीनों में केवल दक्षिणावर्त हेलिक्स ही देखे जाते हैं। प्रोटीन धागी के अन्य क्षेत्र अन्य रूपों में मुड़े होते हैं जिन्हें द्वितीयक संरचना कहा जाता है (चित्र 9.4 b)। इसके अतिरिक्त, लंबी प्रोटीन श्रृंखला स्वयं पर ही इस प्रकार मुड़ी होती है जैसे खोखली ऊनी गेंद, जिससे तृतीयक संरचना उत्पन्न होती है (चित्र 9.4 c)। यह हमें प्रोटीन का त्रि-आयामी दृश्य देता है। तृतीयक संरचना प्रोटीन की अनेक जैविक क्रियाओं के लिए पूर्णतः आवश्यक है।
कुछ प्रोटीन एक से अधिक पॉलीपेप्टाइड या उप-इकाइयों के समूह होते हैं। इन व्यक्तिगत मुड़े हुए पॉलीपेप्टाइड या उप-इकाइयों को आपस में जिस प्रकार व्यवस्थित किया जाता है (जैसे गोलों की रैखिक श्रृंखला, एक-दूसरे के ऊपर घन या प्लेट के रूप में व्यवस्थित गोले आदि), वह प्रोटीन की संरचना है जिसे अन्यथा प्रोटीन की चतुष्कीय संरचना कहा जाता है (चित्र 9.4 d)। वयस्क मानव हीमोग्लोबिन में 4 उप-इकाइयाँ होती हैं। इनमें से दो एक-दूसरी के समान होती हैं। इस प्रकार, दो α प्रकार की उप-इकाइयाँ और दो β प्रकार की उप-इकाइयाँ मिलकर मानव हीमोग्लोबिन (Hb) बनाती हैं।
9.8 एंजाइम
लगभग सभी एंजाइम प्रोटीन होते हैं। कुछ न्यूक्लिक अम्ल ऐसे भी होते हैं जो एंजाइमों की तरह व्यवहार करते हैं। इन्हें राइबोज़ाइम्स कहा जाता है। किसी एंजाइम को रेखा-चित्र द्वारा दर्शाया जा सकता है। कोई भी एंजाइम, किसी भी प्रोटीन की तरह, एक प्राथमिक संरचना रखता है, अर्थात् प्रोटीन का अमीनो अम्ल क्रम। कोई भी एंजाइम, किसी भी प्रोटीन की तरह, द्वितीयक और तृतीयक संरचना रखता है। जब आप तृतीयक संरचना (चित्र 9.4 b) देखते हैं तो आप देखेंगे कि प्रोटीन श्रृंखला की रीढ़ स्वयं पर मुड़ जाती है, श्रृंखला स्वयं को काट-काट कर पार करती है और इससे कई दरारें या जेबें बन जाती हैं। ऐसी ही एक जेब ‘सक्रिय स्थल’ है। किसी एंजाइम का सक्रिय स्थल एक दरार या जेब होती है जिसमें सब्सट्रेट फिट बैठता है। इस प्रकार एंजाइम अपने सक्रिय स्थल के माध्यम से अत्यधिक दर से अभिक्रियाओं को उत्प्रेरित करते हैं। एंजाइम उत्प्रेरक अकार्बनिक उत्प्रेरकों से कई मायनों में भिन्न होते हैं, पर एक प्रमुख अंतर का उल्लेख आवश्यक है। अकार्बनिक उत्प्रेरक उच्च तापमान और उच्च दाब पर कुशलता से कार्य करते हैं, जबकि एंजाइम उच्च तापमान (कहिए 40°C से ऊपर) पर क्षतिग्रस्त हो जाते हैं। फिर भी, जीवों से पृथक किए गए एंजाइम जो सामान्यतः अत्यधिक उच्च तापमान (जैसे गर्म वेंट और गंधक स्प्रिंग्स) में जीते हैं, स्थिर रहते हैं और उच्च तापमान (80°-90°C तक) पर भी अपनी उत्प्रेरक क्षमता बनाए रखते हैं। तापीय स्थिरता इस प्रकार ऐसे एंजाइमों का एक महत्वपूर्ण गुण है जो थर्मोफिलिक जीवों से पृथक किए जाते हैं।
9.8.1 रासायनिक अभिक्रियाएँ
हम इन एंजाइमों को कैसे समझते हैं? आइए पहले एक रासायनिक अभिक्रिया को समझें। रासायनिक यौगिक दो प्रकार के परिवर्तनों से गुजरते हैं। एक भौतिक परिवर्तन सिर्फ आकार में बदलाव को दर्शाता है बिना बंधनों के टूटने के। यह एक भौतिक प्रक्रिया है। एक अन्य भौतिक प्रक्रिया पदार्थ की अवस्था में बदलाव है: जब बर्फ पानी में पिघलती है, या जब पानी वाष्प बन जाता है। ये भी भौतिक प्रक्रियाएं हैं। हालांकि, जब रूपांतरण के दौरान बंधन टूटते हैं और नए बंधन बनते हैं, तो इसे रासायनिक अभिक्रिया कहा जाएगा। उदाहरण के लिए:
$$ \mathrm{Ba}(\mathrm{OH}) _{2}+\mathrm{H} _{2} \mathrm{SO} _{4} \rightarrow \mathrm{BaSO} _{4}+2 \mathrm{H} _{2} \mathrm{O} $$
एक अकार्बनिक रासायनिक अभिक्रिया है। इसी तरह, स्टार्च का ग्लूकोज में जल-विघटन एक कार्बनिक रासायनिक अभिक्रिया है। किसी भौतिक या रासायनिक प्रक्रिया की दर का अर्थ है प्रति इकाई समय बना उत्पाद की मात्रा। इसे इस प्रकार व्यक्त किया जा सकता है:
$$ \text { rate }=\frac{\delta P}{\delta t} $$
यदि दिशा निर्दिष्ट हो तो दर को वेग भी कहा जा सकता है। भौतिक और रासायनिक प्रक्रियाओं की दरें तापमान सहित अन्य कारकों से प्रभावित होती हैं। एक सामान्य नियम यह है कि हर 10°C बदलाव पर दर दोगुनी हो जाती है या आधी हो जाती है। उत्प्रेरित अभिक्रियाएं बिना उत्प्रेरक वाली अभिक्रियाओं की तुलना में बहुत अधिक दर से चलती हैं। जब एंजाइम-उत्प्रेरित अभिक्रियाओं का अवलोकन किया जाता है, तो दर उसी अभिक्रिया की तुलना में बहुत अधिक होगी जो बिना उत्प्रेरक के हो। उदाहरण के लिए

किसी एंजाइम की अनुपस्थिति में यह अभिक्रिया बहुत धीमी होती है, जिसमें लगभग 200 अणु H₂CO₃ प्रति घंटा बनते हैं। हालाँकि, कोशिकाद्रव्य में उपस्थित कार्बोनिक एनहाइड्रेज़ नामक एंजाइम का उपयोग करके, अभिक्रिया नाटकीय रूप से तेज हो जाती है और प्रति सेकंड लगभग 600,000 अणु बनते हैं। एंजाइम ने अभिक्रिया की दर को लगभग 10 लाख गुना तक तेज कर दिया है। एंजाइमों की शक्ति वास्तव में अविश्वसनीय है!
हजारों प्रकार के एंजाइम होते हैं, जिनमें से प्रत्येक एक अद्वितीय रासायनिक या उपापचयी अभिक्रिया को उत्प्रेरित करता है। एक बहु-चरणीय रासायनिक अभिक्रिया, जब प्रत्येक चरण को एक ही एंजाइम समूह या विभिन्न एंजाइमों द्वारा उत्प्रेरित किया जाता है, को उपापचयी पथ कहा जाता है। उदाहरण के लिए,
$$ \begin{gathered} \text { ग्लूकोज } \rightarrow 2 \text { पाइरूविक अम्ल } \ \mathrm{C}{6} \mathrm{H}{12} \mathrm{O}{6}+\mathrm{O}{2} \rightarrow 2 \mathrm{C}{3} \mathrm{H}{4} \mathrm{O}{3}+2 \mathrm{H}{2} \mathrm{O} \end{gathered} $$
यह वास्तव में एक चयापचयी पथ है जिसमें ग्लूकोस दस विभिन्न एंजाइम-उत्प्रेरित चयापचयी अभिक्रियाओं के माध्यम से पाइरूविक अम्ल बन जाता है। जब आप अध्याय 14 में श्वसन का अध्ययन करेंगे तो आप इन अभिक्रियाओं का अध्ययन करेंगे। इस चरण पर आपको यह जानना चाहिए कि यही चयापचयी पथ एक या दो अतिरिक्त अभिक्रियाओं के साथ विभिन्न चयापचयी अंतिम उत्पादों को जन्म देता है। हमारी अस्थि-पेशियों में, अवायवीय परिस्थितियों में, लैक्टिक अम्ल बनता है। सामान्य वायवीय परिस्थितियों में, पाइरूविक अम्ल बनता है। यीस्ट में, किण्वन के दौरान, वही पथ एथेनॉल (अल्कोहल) के उत्पादन की ओर ले जाता है। इस प्रकार, विभिन्न परिस्थितियों में विभिन्न उत्पाद संभव हैं।
9.8.2 एंजाइम इतनी उच्च दर से रासायनिक रूपांतरण कैसे करते हैं?
इसे समझने के लिए हमें एंजाइमों का थोड़ा और अध्ययन करना चाहिए। हम पहले ही ‘सक्रिय स्थल’ की अवधारणा को समझ चुके हैं। रासायनिक या चयापचयी रूपांतरण एक अभिक्रिया को संदर्भित करता है। वह रासायनिक पदार्थ जिसे उत्पाद में बदला जाता है, उसे ‘आधार’ कहा जाता है। इसलिए एंजाइम, अर्थात् त्रि-आयामी संरचना वाले प्रोटीन जिनमें एक ‘सक्रिय स्थल’ होता है, एक आधार (S) को उत्पाद (P) में बदलते हैं। प्रतीकात्मक रूप से इसे इस प्रकार दर्शाया जा सकता है:
S $\rightarrow$ P
अब यह समझा गया है कि सब्सट्रेट ‘S’ को एंज़ाइम के ‘ऐक्टिव साइट’ से, जो एक दी गई खाँच या जेब में होता है, बाँधना पड़ता है। सब्सट्रेट को ‘ऐक्टिव साइट’ की ओर विसरित होना पड़ता है। इस प्रकार, एक ‘ES’ कॉम्प्लेक्स का बनना अनिवार्य है। E सक्रियण ऊर्जा एंज़ाइम के लिए खड़ा है। यह कॉम्प्लेक्स बनना एंज़ाइम के बिना एक क्षणिक घटना है। उस अवस्था के दौरान जब सब्सट्रेट एंज़ाइम के ऐक्टिव साइट से बँधा होता है, सब्सट्रेट की एक नई संरचना, जिसे सक्रियण संक्रमण-अवस्था संरचना कहा जाता है, बनती है। बहुत जल्द ही, एंज़ाइम के साथ ऊर्जा के बाद अपेक्षित बंध टूटने/बनने की प्रक्रिया पूरी होती है, उत्पाद ऐक्टिव साइट से मुक्त हो जाता है। दूसरे शब्दों में, सब्सट्रेट की संरचना उत्पाद(ओं) की संरचना में रूपांतरित हो जाती है। इस रूपांतरण का मार्ग तथाकथित उत्पाद (P) संक्रमण-अवस्था संरचना से होकर गुज़रना चाहिए। स्थिर सब्सट्रेट और उत्पाद के बीच कई और ‘परिवर्तित संरचनात्मक अवस्थाएँ’ हो सकती हैं। प्रतिक्रिया की प्रगति इस कथन में निहित है कि सभी अन्य मध्यवर्ती संरचनात्मक अवस्थाएँ अस्थिर होती हैं। स्थिरता किसी अणु या संरचना की ऊर्जा स्थिति से संबंधित होती है। इसलिए, जब हम इसे ग्राफ के माध्यम से चित्रात्मक रूप से देखते हैं, तो यह कुछ ऐसा दिखता है जैसा कि चित्र 9.6 में है।

आकृति 9.4 सक्रियण ऊर्जा की अवधारणा
y-अक्ष विभव ऊर्जा सामग्री को दर्शाती है। x-अक्ष संरचनात्मक रूपांतरण या अवस्थाओं की प्रगति को ‘संक्रमण अवस्था’ के माध्यम से दर्शाती है। आप दो बातें देखेंगे। S और P के बीच ऊर्जा स्तर का अंतर। यदि ‘P’ ‘S’ से निचले स्तर पर है, तो अभिक्रिया एक ऊष्माक्षेपी अभिक्रिया है। उत्पाद बनाने के लिए ऊर्जा (गर्म करके) आपूर्ति करने की आवश्यकता नहीं है। हालाँकि, चाहे वह ऊष्माक्षेपी या स्वतः होने वाली अभिक्रिया हो या ऊष्माशोषी या ऊर्जा-आवश्यक अभिक्रिया, ‘S’ को एक बहुत अधिक ऊर्जा अवस्था या संक्रमण अवस्था से गुजरना पड़ता है। ‘S’ की औसत ऊर्जा सामग्री और इस संक्रमण अवस्था की ऊर्जा सामग्री के बीच का अंतर ‘सक्रियण ऊर्जा’ कहलाता है। एंजाइम अंततः इस ऊर्जा बाधा को कम कर देते हैं जिससे ‘S’ से ‘P’ में संक्रमण अधिक आसान हो जाता है।
9.8.3 एंजाइम क्रिया की प्रकृति
प्रत्येक एंजाइम (E) के अणु में एक क्षेत्र होता है जहाँ यह अपने क्रियाधार (S) से बंधता है ताकि एक अत्यंत क्रियाशील एंजाइम-क्रियाधार संकुल (ES) बने। यह संकुल अल्पकालिक होता है और एंजाइम-उत्पाद संकुल (EP) के मध्यवर्ती निर्माण के साथ यह अपने उत्पाद(ों) P और अपरिवर्तित एंजाइम में विघटित हो जाता है।
कैटालिसिस के लिए ES संकुल का बनना अनिवार्य है।
E + S $\quad \quad$ ES $\rightarrow$ EP $\rightarrow$ E + P
एंजाइम क्रिया का उत्प्रेरक चक्र निम्नलिखित चरणों में वर्णित किया जा सकता है:
- सबसे पहले, सब्सट्रेट एंजाइम की सक्रिय साइट से बंधता है, सक्रिय साइट में फिट बैठता है।
- सब्सट्रेट के बंधन से एंजाइम अपना आकार बदलता है, सब्सट्रेट के चारों ओर और भी कसकर फिट हो जाता है।
- एंजाइम की सक्रिय साइट, अब सब्सट्रेट के निकट आ जाने पर, सब्सट्रेट के रासायनिक बंधों को तोड़ती है और नया एंजाइम-उत्पाद संकुल बनता है।
- एंजाइम अभिक्रिया के उत्पादों को मुक्त करता है और मुक्त एंजाइम फिर से किसी अन्य सब्सट्रेट अणु से बंधने और उत्प्रेरक चक्र को पुनः चलाने के लिए तैयार हो जाता है।
9.8.4 एंजाइम गतिविधि को प्रभावित करने वाले कारक
किसी एंजाइम की गतिविधि परिस्थितियों में आए बदलाव से प्रभावित हो सकती है जो प्रोटीन की तृतीयक संरचना को बदल देते हैं। इनमें तापमान, pH, सब्सट्रेट सांद्रता में परिवर्तन या विशिष्ट रसायनों का बंधन शामिल है जो इसकी गतिविधि को नियंत्रित करते हैं।
तापमान और pH
एंजाइम सामान्यतः तापमान और pH के एक संकीर्ण परिसर में कार्य करते हैं (चित्र 9.7)। प्रत्येक एंजाइम एक विशिष्ट तापमान और pH पर अपनी उच्चतम गतिविधि दिखाता है, जिसे इष्टतम तापमान और इष्टतम pH कहा जाता है। इष्टतम मान से नीचे और ऊपर दोनों दिशाओं में गतिविधि घट जाती है। निम्न तापमान एंजाइम को अस्थायी रूप से निष्क्रिय अवस्था में संरक्षित करता है जबकि उच्च तापमान एंजाइम की गतिविधि को नष्ट कर देता है क्योंकि प्रोटीन उष्मा द्वारा विकृत हो जाते हैं।
सब्सट्रेट की सांद्रता
सब्सट्रेट की सांद्रता में वृद्धि के साथ, एंजाइमेटिक अभिक्रिया की वेग प्रारंभ में बढ़ता है। अभिक्रिया अंततः एक अधिकतम वेग (Vmax) तक पहुँचती है जिसे सब्सट्रेट की सांद्रता में और वृद्धि से पार नहीं किया जा सकता। ऐसा इसलिए है क्योंकि एंजाइम अणु सब्सट्रेट अणुओं से कम होते हैं और इन अणुओं के संतृप्त होने के बाद, अतिरिक्त सब्सट्रेट अणुओं से बंधने के लिए कोई मुक्त एंजाइम अणु नहीं होते (चित्र 9.7)।
एंजाइम की सक्रियता एंजाइम से बंधने वाले विशिष्ट रसायनों की उपस्थिति के प्रति भी संवेदनशील होती है। जब रसायन के बंधन से एंजाइम की सक्रियता बंद हो जाती है, तो इस प्रक्रिया को निरोधन कहा जाता है और रसायन को निरोधक कहा जाता है।

चित्र 9.5 परिवर्तन के प्रभाव: (a) pH (b) तापमान और (c) सब्सट्रेट की सांद्रता पर एंजाइम की सक्रियता
जब अवरोधक अपनी आण्विक संरचना में आधार से बहुत मिलता-जुलता हो और एंजाइम की क्रियाशीलता को अवरुद्ध करे, तो इसे प्रतिस्पर्धी अवरोधक कहा जाता है। आधार से संरचनात्मक समानता के कारण, अवरोधक एंजाइम के आधार-बंधन स्थल के लिए आधार से प्रतिस्पर्धा करता है। परिणामस्वरूप, आधार नहीं बंध पाता और एंजाइम की क्रिया घट जाती है, उदाहरणार्थ, सक्सिनेट डिहाइड्रोजनेज का मैलोनेट द्वारा अवरोधन, जो आधार सक्सिनेट से संरचना में बहुत मिलता-जुलता है। ऐसे प्रतिस्पर्धी अवरोधक प्रायः जीवाणु रोगजनकों के नियंत्रण में प्रयुक्त होते हैं।
9.8.5 एंजाइमों का वर्गीकरण और नामकरण
हजारों एंजाइमों की खोज, पृथक्करण और अध्ययन किया गया है। इनमें से अधिकांश एंजाइमों को उनके द्वारा उत्प्रेरित अभिक्रियाओं के प्रकार के आधार पर विभिन्न समूहों में वर्गीकृत किया गया है। एंजाइमों को 6 वर्गों में बाँटा गया है, प्रत्येक में 4-13 उपवर्ग होते हैं और इन्हें चार-अंकीय संख्या द्वारा नामित किया जाता है।
ऑक्सिडोरिडक्टेस/डिहाइड्रोजनेज: वे एंजाइम जो दो आधारों S और S’ के बीच ऑक्सिडो-अपचयन उत्प्रेरित करते हैं, उदाहरणार्थ,
S अपचयित + S’ ऑक्सीकृत $\rightarrow$ S ऑक्सीकृत + S’ अपचयित।
ट्रांसफेरेस: वे एंजाइम जो किसी समूह G (हाइड्रोजन के अतिरिक्त) के स्थानांतरण को उत्प्रेरित करते हैं, एक आधार युग्म S और S’ के बीच, उदाहरणार्थ,
$$ \mathrm{S}-\mathrm{G}+\mathrm{S}^{1} \rightarrow \mathrm{S}+\mathrm{S}^{1} \mathrm{G} $$
हाइड्रोलेज: वे एंजाइम जो एस्टर, ईथर, पेप्टाइड, ग्लाइकोसिडिक, C-C, C-हैलाइड या P-N बंधों के जलअपघटन को उत्प्रेरित करते हैं।
लाइएसेज़: ऐसे एंजाइम जो सब्सट्रेट्स से समूहों को हाइड्रोलिसिस के अलावा अन्य तंत्रों द्वारा हटाकर डबल बॉन्ड छोड़ते हैं।
$$ \begin{array}{ll} \mathrm{X} & \mathrm{Y} \ \mathrm{C}-\mathrm{C} \rightarrow \mathrm{X}-\mathrm{Y}+\mathrm{C}=\mathrm{C} \end{array} $$
आइसोमरेज़ेज़: वे सभी एंजाइम शामिल हैं जो ऑप्टिकल, ज्योमेट्रिक या पोज़िशनल आइसोमरों के आपसी रूपांतरण को उत्प्रेरित करते हैं।
लाइगेज़: ऐसे एंजाइम जो 2 यौगिकों को एक साथ जोड़ने की क्रिया को उत्प्रेरित करते हैं, उदाहरण के लिए, वे एंजाइम जो C-O, C-S, C-N, P-O आदि बॉन्डों के जुड़ाव को उत्प्रेरित करते हैं।
9.8.6 सह-कारक
एंजाइम एक या अनेक पॉलीपेप्टाइड श्रृंखलाओं से बने होते हैं। हालांकि, कई ऐसे मामले हैं जिनमें गैर-प्रोटीन घटक, जिन्हें सह-कारक कहा जाता है, एंजाइम से जुड़े होते हैं ताकि एंजाइम उत्प्रेरक रूप से सक्रिय हो सके। इन स्थितियों में, एंजाइम का प्रोटीन भाग एपोएंजाइम कहलाता है। तीन प्रकार के सह-कारक पहचाने जा सकते हैं: प्रोस्थेटिक समूह, सह-एंजाइम और धातु आयन।
प्रोस्थेटिक समूह कार्बनिक यौगिक होते हैं और इन्हें अन्य सह-कारकों से इस आधार पर अलग किया जाता है कि ये एपोएंजाइम से दृढ़ता से जुड़े होते हैं। उदाहरण के लिए, पेरोक्सिडेज़ और कैटलेज़ में, जो हाइड्रोजन पेरोक्साइड को पानी और ऑक्सीजन में विघटित करने की क्रिया को उत्प्रेरित करते हैं, हीम प्रोस्थेटिक समूह है और यह एंजाइम की सक्रिय साइट का एक भाग है।
सह-एंजाइम भी कार्बनिक यौगिक होते हैं, परंतु उनका अपोएंजाइम से संबंध केवल अस्थायी होता है, आमतौर पर उत्प्रेरण की प्रक्रिया के दौरान। इसके अतिरिक्त, सह-एंजाइम अनेक भिन्न एंजाइम-उत्प्रेरित अभिक्रियाओं में सह-कारक के रूप में कार्य करते हैं। अनेक सह-एंजाइमों के आवश्यक रासायनिक घटक विटामिन होते हैं, उदाहरणार्थ, सह-एंजाइम निकोटिनामाइड एडेनिन डाइन्यूक्लियोटाइड (NAD) और NADP में नियासिन विटामिन होता है।
कई एंजाइमों को अपनी सक्रियता के लिए धातु आयनों की आवश्यकता होती है, जो सक्रिय स्थल पर साइड श्रृंखलाओं के साथ समन्वय बंध बनाते हैं और साथ ही एक या अधिक समन्वय बंध अधिश्रय के साथ भी बनाते हैं, उदाहरणार्थ, जिंक प्रोटियोलिटिक एंजाइम कार्बोक्सीपेप्टिडेज़ का सह-कारक है।
जब एंजाइम से सह-कारक को हटा दिया जाता है तो उत्प्रेरक सक्रियता समाप्त हो जाती है, जो इस बात की गवाही देता है कि वे एंजाइम की उत्प्रेरक सक्रियता में महत्वपूर्ण भूमिका निभाते हैं।
सारांश
यद्यपि जीवित जीवों में भ्रमित कर देने वाली विविधता है, उनका रासायनिक संघटन और उपापचयी अभिक्रियाएं उल्लेखनीय रूप से समान प्रतीत होती हैं। जीवित ऊतकों और अजीव पदार्थों की तत्वीय संरचना गुणात्मक विश्लेषण पर समान प्रतीत होती है। परंतु, निकटवर्ती परीक्षण से पता चलता है कि कार्बन, हाइड्रोजन और ऑक्सीजन की सापेक्ष प्रचुरता जीवित प्रणालियों में अजीव पदार्थों की तुलना में अधिक है। जीवित जीवों में सबसे प्रचुर रसायन जल है। हजारों छोटे आणविक भार (<1000 Da) के जैवअणु मौजूद हैं।
अमीनो अम्ल, मोनोसैकेराइड और डाइसैकेराइड शर्कराएँ, फैटी अम्ल, ग्लिसरॉल, न्यूक्लियोटाइड, न्यूक्लियोसाइड और नाइट्रोजन बेस जीवित जीवों में पाए जाने वाले कुछ कार्बनिक यौगिक हैं। 20 प्रकार के अमीनो अम्ल और 5 प्रकार के न्यूक्लियोटाइड होते हैं। वसाएँ और तेल ग्लिसराइड होते हैं जिनमें फैटी अम्ल ग्लिसरॉल से एस्टरिफाइड होते हैं। फॉस्फोलिपिड्स में इसके अतिरिक्त एक फॉस्फोरिलेटेड नाइट्रोजनयुक्त यौगिक होता है।
केवल तीन प्रकार के बड़े अणु, अर्थात् प्रोटीन, न्यूक्लिक अम्ल और पॉलीसैकेराइड जीवित प्रणालियों में पाए जाते हैं। लिपिड्स, झिल्लियों के साथ अपने संबंध के कारण, बड़े अणु के अंश में अलग हो जाते हैं। जैव-बड़े अणु बहुलक होते हैं। ये भिन्न प्रकार की इकाइयों से बने होते हैं। प्रोटीन अमीनो अम्लों से बने विभिन्न प्रकार के बहुलक होते हैं। न्यूक्लिक अम्ल (RNA और DNA) न्यूक्लियोटाइडों से बने होते हैं। जैव-बड़े अणुओं में संरचनाओं की पदानुक्रमिता होती है - प्राथमिक, द्वितीयक, तृतीयक और चतुर्धातुक। न्यूक्लिक अम्ल आनुवंशिक पदार्थ के रूप में कार्य करते हैं। पॉलीसैकेराइड पौधों, कवक की कोशिका भित्ति के घटक होते हैं और आर्थ्रोपोड्स के बाहरी कंकाल के भी होते हैं। ये ऊर्जा के संचय रूप भी होते हैं (जैसे स्टार्च और ग्लाइकोजन)। प्रोटीन विभिन्न प्रकार के कोशिकीय कार्य करते हैं। इनमें से कई एंजाइम होते हैं, कुछ प्रतिरक्षी होते हैं, कुछ ग्राही होते हैं, कुछ हार्मोन होते हैं और कुछ संरचनात्मक प्रोटीन होते हैं। कोलाजन पशु जगत में सबसे प्रचुर प्रोटीन है और राइब्युलोस बिस्फॉस्फेट कार्बोक्सिलेज-ऑक्सीजनेज (RuBisCO) सम्पूर्ण जैवमंडल में सबसे प्रचुर प्रोटीन है।
एंजाइम प्रोटीन होते हैं जो कोशिकाओं में जैव रासायनिक अभिक्रियाओं को उत्प्रेरित करते हैं। राइबोजाइम उत्प्रेरक क्षमता वाले न्यूक्लिक अम्ल होते हैं। प्रोटीनयुक्त एंजाइम सब्सट्रेट विशिष्टता प्रदर्शित करते हैं, अधिकतम सक्रियता के लिए इष्टतम तापमान और pH की आवश्यकता होती है। वे उच्च तापमान पर विकृत हो जाते हैं। एंजाइम अभिक्रियाओं की सक्रियण ऊर्जा को कम करते हैं और अभिक्रियाओं की दर को बहुत बढ़ा देते हैं। न्यूक्लिक अम्ल वंशानुगत सूचना वहन करते हैं और माता-पिता की पीढ़ी से संतानों तक प्रेषित होते हैं।












