ಅಧ್ಯಾಯ 04 ರಾಸಾಯನಿಕ ಬಂಧ ಮತ್ತು ಆಣ್ವಿಕ ರಚನೆ
=== ಮುಂಭಾಗದ ವಿಷಯ ಕ್ಷೇತ್ರಗಳು === ಶೀರ್ಷಿಕೆ: ಅಧ್ಯಾಯ 04 ರಾಸಾಯನಿಕ ಬಂಧನ ಮತ್ತು ಆಣ್ವಿಕ ರಚನೆ
=== ಮುಖ್ಯ ವಿಷಯ ===
“ವಿಜ್ಞಾನಿಗಳು ನಿರಂತರವಾಗಿ ಹೊಸ ಸಂಯುಕ್ತಗಳನ್ನು ಕಂಡುಹಿಡಿಯುತ್ತಿದ್ದಾರೆ, ಅವುಗಳ ಬಗ್ಗೆ ವಾಸ್ತವಾಂಶಗಳನ್ನು ಕ್ರಮಬದ್ಧವಾಗಿ ಜೋಡಿಸುತ್ತಿದ್ದಾರೆ, ಅಸ್ತಿತ್ವದಲ್ಲಿರುವ ಜ್ಞಾನದೊಂದಿಗೆ ವಿವರಿಸಲು ಪ್ರಯತ್ನಿಸುತ್ತಿದ್ದಾರೆ, ಹಿಂದಿನ ದೃಷ್ಟಿಕೋನಗಳನ್ನು ಮಾರ್ಪಡಿಸಲು ಅಥವಾ ಹೊಸದಾಗಿ ಗಮನಿಸಿದ ವಾಸ್ತವಾಂಶಗಳನ್ನು ವಿವರಿಸಲು ಸಿದ್ಧಾಂತಗಳನ್ನು ರೂಪಿಸಲು ಸಂಘಟಿಸುತ್ತಿದ್ದಾರೆ.”
ದ್ರವ್ಯವು ಒಂದು ಅಥವಾ ವಿಭಿನ್ನ ಪ್ರಕಾರದ ಅಂಶಗಳಿಂದ ಮಾಡಲ್ಪಟ್ಟಿದೆ. ಸಾಮಾನ್ಯ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ, ಉದಾತ್ತ ಅನಿಲಗಳನ್ನು ಹೊರತುಪಡಿಸಿ, ಬೇರೆ ಯಾವುದೇ ಅಂಶವು ಪ್ರಕೃತಿಯಲ್ಲಿ ಸ್ವತಂತ್ರ ಪರಮಾಣುವಾಗಿ ಅಸ್ತಿತ್ವದಲ್ಲಿಲ್ಲ. ಆದರೆ, ಪರಮಾಣುಗಳ ಗುಂಪು ಒಂದೇ ಪ್ರಭೇದವಾಗಿ ಒಟ್ಟಿಗೆ ಅಸ್ತಿತ್ವದಲ್ಲಿದೆ ಎಂದು ಕಂಡುಬರುತ್ತದೆ, ಇದು ವಿಶಿಷ್ಟ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಅಂತಹ ಪರಮಾಣುಗಳ ಗುಂಪನ್ನು ಅಣು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಸ್ಪಷ್ಟವಾಗಿ, ಈ ಘಟಕ ಪರಮಾಣುಗಳನ್ನು ಅಣುಗಳಲ್ಲಿ ಒಟ್ಟಿಗೆ ಹಿಡಿದಿಡುವ ಕೆಲವು ಬಲವಿರಬೇಕು. ವಿವಿಧ ರಾಸಾಯನಿಕ ಪ್ರಭೇದಗಳಲ್ಲಿ ವಿವಿಧ ಘಟಕಗಳನ್ನು (ಪರಮಾಣುಗಳು, ಅಯಾನುಗಳು, ಇತ್ಯಾದಿ) ಒಟ್ಟಿಗೆ ಹಿಡಿದಿಡುವ ಆಕರ್ಷಕ ಬಲವನ್ನು ರಾಸಾಯನಿಕ ಬಂಧ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ರಾಸಾಯನಿಕ ಸಂಯುಕ್ತಗಳ ರಚನೆಯು ವಿವಿಧ ಅಂಶಗಳ ಪರಮಾಣುಗಳ ವಿವಿಧ ರೀತಿಯ ಸಂಯೋಜನೆಯ ಪರಿಣಾಮವಾಗಿ ನಡೆಯುವುದರಿಂದ, ಇದು ಅನೇಕ ಪ್ರಶ್ನೆಗಳನ್ನು ಎಬ್ಬಿಸುತ್ತದೆ. ಪರಮಾಣುಗಳು ಏಕೆ ಸಂಯೋಗಗೊಳ್ಳುತ್ತವೆ? ಕೆಲವು ನಿರ್ದಿಷ್ಟ ಸಂಯೋಜನೆಗಳು ಮಾತ್ರ ಏಕೆ ಸಾಧ್ಯ? ಕೆಲವು ಪರಮಾಣುಗಳು ಸಂಯೋಗಗೊಳ್ಳುವಾಗ, ಇತರ ಕೆಲವು ಏಕೆ ಸಂಯೋಗಗೊಳ್ಳುವುದಿಲ್ಲ? ಅಣುಗಳು ನಿರ್ದಿಷ್ಟ ಆಕಾರಗಳನ್ನು ಏಕೆ ಹೊಂದಿರುತ್ತವೆ? ಅಂತಹ ಪ್ರಶ್ನೆಗಳಿಗೆ ಉತ್ತರಿಸಲು ವಿವಿಧ ಸಿದ್ಧಾಂತಗಳು ಮತ್ತು ಪರಿಕಲ್ಪನೆಗಳನ್ನು ಕಾಲಕಾಲಕ್ಕೆ ಮುಂದಿಡಲಾಗಿದೆ. ಇವುಗಳೆಂದರೆ ಕೊಸೆಲ್-ಲೂಯಿಸ್ ವಿಧಾನ, ವೇಲೆನ್ಸ್ ಶೆಲ್ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿ ವಿಕರ್ಷಣೆ (VSEPR) ಸಿದ್ಧಾಂತ, ವೇಲೆನ್ಸ್ ಬಾಂಡ್ (VB) ಸಿದ್ಧಾಂತ ಮತ್ತು ಮಾಲಿಕ್ಯುಲರ್ ಆರ್ಬಿಟಲ್ (MO) ಸಿದ್ಧಾಂತ. ವೇಲೆನ್ಸ್ನ ವಿವಿಧ ಸಿದ್ಧಾಂತಗಳ ವಿಕಾಸ ಮತ್ತು ರಾಸಾಯನಿಕ ಬಂಧಗಳ ಸ್ವರೂಪದ ವ್ಯಾಖ್ಯಾನವು ಪರಮಾಣುವಿನ ರಚನೆ, ಅಂಶಗಳ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ವಿನ್ಯಾಸ ಮತ್ತು ಆವರ್ತಕ ಕೋಷ್ಟಕದ ತಿಳುವಳಿಕೆಯ ಅಭಿವೃದ್ಧಿಗಳೊಂದಿಗೆ ನಿಕಟ ಸಂಬಂಧ ಹೊಂದಿದೆ. ಪ್ರತಿಯೊಂದು ವ್ಯವಸ್ಥೆಯು ಹೆಚ್ಚು ಸ್ಥಿರವಾಗಿರುವ ಪ್ರವೃತ್ತಿ ಹೊಂದಿದೆ ಮತ್ತು ಬಂಧನವು ಸ್ಥಿರತೆಯನ್ನು ಪಡೆಯಲು ವ್ಯವಸ್ಥೆಯ ಶಕ್ತಿಯನ್ನು ಕಡಿಮೆ ಮಾಡುವ ಪ್ರಕೃತಿಯ ಮಾರ್ಗವಾಗಿದೆ.
4.1 ರಾಸಾಯನಿಕ ಬಂಧನಕ್ಕೆ ಕೊಸೆಲ್-ಲೂಯಿಸ್ ವಿಧಾನ
ರಾಸಾಯನಿಕ ಬಂಧದ ರಚನೆಯನ್ನು ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಪರಿಭಾಷೆಯಲ್ಲಿ ವಿವರಿಸಲು ಅನೇಕ ಪ್ರಯತ್ನಗಳು ನಡೆದವು, ಆದರೆ 1916 ರಲ್ಲಿ ಮಾತ್ರ ಕೊಸೆಲ್ ಮತ್ತು ಲೂಯಿಸ್ ಸ್ವತಂತ್ರವಾಗಿ ತೃಪ್ತಿಕರ ವಿವರಣೆ ನೀಡುವಲ್ಲಿ ಯಶಸ್ವಿಯಾದರು. ಉದಾತ್ತ ಅನಿಲಗಳ ನಿಷ್ಕ್ರಿಯತೆಯನ್ನು ಆಧರಿಸಿದ ವೇಲೆನ್ಸ್ಗೆ ಕೆಲವು ತಾರ್ಕಿಕ ವಿವರಣೆಯನ್ನು ಒದಗಿಸಿದವರು ಅವರೇ ಮೊದಲಿಗರು.
ಲೂಯಿಸ್ ಪರಮಾಣುವನ್ನು ಧನಾತ್ಮಕವಾಗಿ ಆವೇಶಿತ ‘ಕರ್ನೆಲ್’ (ನ್ಯೂಕ್ಲಿಯಸ್ ಮತ್ತು ಒಳ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು) ಮತ್ತು ಗರಿಷ್ಠ ಎಂಟು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿಕೊಳ್ಳಬಹುದಾದ ಹೊರ ಶೆಲ್ನ ಪರಿಭಾಷೆಯಲ್ಲಿ ಚಿತ್ರಿಸಿದರು. ಮತ್ತಷ್ಟು, ಈ ಎಂಟು ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ‘ಕರ್ನೆಲ್’ ಅನ್ನು ಸುತ್ತುವರೆದಿರುವ ಘನದ ಮೂಲೆಗಳನ್ನು ಆಕ್ರಮಿಸುತ್ತವೆ ಎಂದು ಅವರು ಭಾವಿಸಿದರು. ಹೀಗಾಗಿ ಸೋಡಿಯಂನ ಏಕೈಕ ಹೊರ ಶೆಲ್ ಎಲೆಕ್ಟ್ರಾನ್ ಘನದ ಒಂದು ಮೂಲೆಯನ್ನು ಆಕ್ರಮಿಸುತ್ತದೆ, ಆದರೆ ಉದಾತ್ತ ಅನಿಲದ ಸಂದರ್ಭದಲ್ಲಿ ಎಲ್ಲಾ ಎಂಟು ಮೂಲೆಗಳೂ ಆಕ್ರಮಿಸಲ್ಪಡುತ್ತವೆ. ಈ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಅಷ್ಟಕವು ವಿಶೇಷವಾಗಿ ಸ್ಥಿರ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ವ್ಯವಸ್ಥೆಯನ್ನು ಪ್ರತಿನಿಧಿಸುತ್ತದೆ. ಪರಮಾಣುಗಳು ರಾಸಾಯನಿಕ ಬಂಧಗಳಿಂದ ಜೋಡಿಸಲ್ಪಟ್ಟಾಗ ಸ್ಥಿರ ಅಷ್ಟಕವನ್ನು ಸಾಧಿಸುತ್ತವೆ ಎಂದು ಲೂಯಿಸ್ ಪ್ರತಿಪಾದಿಸಿದರು. ಸೋಡಿಯಂ ಮತ್ತು ಕ್ಲೋರಿನ್ನ ಸಂದರ್ಭದಲ್ಲಿ, ಇದು ಸೋಡಿಯಂನಿಂದ ಕ್ಲೋರಿನ್ಗೆ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ವರ್ಗಾವಣೆಯಿಂದ ನಡೆಯಬಹುದು, ಇದರಿಂದಾಗಿ $\mathrm{Na}^+$ ಮತ್ತು $\mathrm{Cl}^{-}$ ಅಯಾನುಗಳು ಉಂಟಾಗುತ್ತವೆ. $ \mathrm{Cl}_2, \mathrm{H}_2, \mathrm{~F}_2 $, ಇತ್ಯಾದಿ ಅಣುಗಳ ಸಂದರ್ಭದಲ್ಲಿ, ಬಂಧವು ಪರಮಾಣುಗಳ ನಡುವೆ ಒಂದು ಜೋಡಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಹಂಚಿಕೆಯಿಂದ ರೂಪುಗೊಳ್ಳುತ್ತದೆ. ಈ ಪ್ರಕ್ರಿಯೆಯಲ್ಲಿ ಪ್ರತಿ ಪರಮಾಣುವು ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸ್ಥಿರ ಹೊರ ಅಷ್ಟಕವನ್ನು ಪಡೆಯುತ್ತದೆ.
ಲೂಯಿಸ್ ಚಿಹ್ನೆಗಳು: ಒಂದು ಅಣುವಿನ ರಚನೆಯಲ್ಲಿ, ಹೊರ ಶೆಲ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಮಾತ್ರ ರಾಸಾಯನಿಕ ಸಂಯೋಜನೆಯಲ್ಲಿ ಭಾಗವಹಿಸುತ್ತವೆ ಮತ್ತು ಅವು ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಎಂದು ಕರೆಯಲ್ಪಡುತ್ತವೆ. ಒಳ ಶೆಲ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಚೆನ್ನಾಗಿ ರಕ್ಷಿಸಲ್ಪಟ್ಟಿರುತ್ತವೆ ಮತ್ತು ಸಾಮಾನ್ಯವಾಗಿ ಸಂಯೋಜನೆ ಪ್ರಕ್ರಿಯೆಯಲ್ಲಿ ಒಳಗೊಳ್ಳುವುದಿಲ್ಲ. ಅಮೆರಿಕನ್ ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞ ಜಿ.ಎನ್. ಲೂಯಿಸ್ ಪರಮಾಣುವಿನಲ್ಲಿ ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಪ್ರತಿನಿಧಿಸಲು ಸರಳ ಸಂಕೇತಗಳನ್ನು ಪರಿಚಯಿಸಿದರು. ಈ ಸಂಕೇತಗಳನ್ನು ಲೂಯಿಸ್ ಚಿಹ್ನೆಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, ಎರಡನೇ ಆವರ್ತದ ಅಂಶಗಳ ಲೂಯಿಸ್ ಚಿಹ್ನೆಗಳು ಈ ಕೆಳಗಿನಂತಿವೆ:

ಲೂಯಿಸ್ ಚಿಹ್ನೆಗಳ ಪ್ರಾಮುಖ್ಯತೆ : ಚಿಹ್ನೆಯ ಸುತ್ತಲಿನ ಚುಕ್ಕೆಗಳ ಸಂಖ್ಯೆಯು ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯನ್ನು ಪ್ರತಿನಿಧಿಸುತ್ತದೆ. ಈ ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯು ಅಂಶದ ಸಾಮಾನ್ಯ ಅಥವಾ ಗುಂಪು ವೇಲೆನ್ಸ್ ಅನ್ನು ಲೆಕ್ಕಾಚಾರ ಮಾಡಲು ಸಹಾಯ ಮಾಡುತ್ತದೆ. ಅಂಶಗಳ ಗುಂಪು ವೇಲೆನ್ಸ್ ಸಾಮಾನ್ಯವಾಗಿ ಲೂಯಿಸ್ ಚಿಹ್ನೆಗಳಲ್ಲಿನ ಚುಕ್ಕೆಗಳ ಸಂಖ್ಯೆಗೆ ಸಮನಾಗಿರುತ್ತದೆ ಅಥವಾ 8 ಮೈನಸ್ ಚುಕ್ಕೆಗಳ ಸಂಖ್ಯೆ ಅಥವಾ ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು.
ರಾಸಾಯನಿಕ ಬಂಧನಕ್ಕೆ ಸಂಬಂಧಿಸಿದಂತೆ, ಕೊಸೆಲ್ ಈ ಕೆಳಗಿನ ವಾಸ್ತವಾಂಶಗಳತ್ತ ಗಮನ ಸೆಳೆದರು:
- ಆವರ್ತಕ ಕೋಷ್ಟಕದಲ್ಲಿ, ಅತ್ಯಂತ ವಿದ್ಯುದೃಣಾತ್ಮಕ ಹ್ಯಾಲೊಜನ್ಗಳು ಮತ್ತು ಅತ್ಯಂತ ವಿದ್ಯುದ್ಧನಾತ್ಮಕ ಕ್ಷಾರ ಲೋಹಗಳು ಉದಾತ್ತ ಅನಿಲಗಳಿಂದ ಬೇರ್ಪಡಿಸಲ್ಪಟ್ಟಿವೆ;
- ಹ್ಯಾಲೊಜನ್ ಪರಮಾಣುವಿನಿಂದ ಋಣಾತ್ಮಕ ಅಯಾನು ಮತ್ತು ಕ್ಷಾರ ಲೋಹದ ಪರಮಾಣುವಿನಿಂದ ಧನಾತ್ಮಕ ಅಯಾನು ರಚನೆಯು ಅನುಕ್ರಮವಾಗಿ ಪರಮಾಣುಗಳಿಂದ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ಗಳಿಕೆ ಮತ್ತು ನಷ್ಟದೊಂದಿಗೆ ಸಂಬಂಧ ಹೊಂದಿದೆ;
- ಹೀಗೆ ರೂಪುಗೊಂಡ ಋಣಾತ್ಮಕ ಮತ್ತು ಧನಾತ್ಮಕ ಅಯಾನುಗಳು ಸ್ಥಿರ ಉದಾತ್ತ ಅನಿಲ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ವಿನ್ಯಾಸಗಳನ್ನು ಪಡೆಯುತ್ತವೆ. ಉದಾತ್ತ ಅನಿಲಗಳು (ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ದ್ವಯತೆಯನ್ನು ಹೊಂದಿರುವ ಹೀಲಿಯಂ ಅನ್ನು ಹೊರತುಪಡಿಸಿ) ಎಂಟು (ಅಷ್ಟಕ) ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವಿಶೇಷವಾಗಿ ಸ್ಥಿರ ಹೊರ ಶೆಲ್ ವಿನ್ಯಾಸವನ್ನು ಹೊಂದಿರುತ್ತವೆ, $n s^{2} n p^{6}$.
- ಋಣಾತ್ಮಕ ಮತ್ತು ಧನಾತ್ಮಕ ಅಯಾನುಗಳು ಸ್ಥಾಯೀವಿದ್ಯುತ್ ಆಕರ್ಷಣೆಯಿಂದ ಸ್ಥಿರಗೊಳ್ಳುತ್ತವೆ.
ಉದಾಹರಣೆಗೆ, ಮೇಲಿನ ಯೋಜನೆಯ ಪ್ರಕಾರ ಸೋಡಿಯಂ ಮತ್ತು ಕ್ಲೋರಿನ್ನಿಂದ $\mathrm{NaCl}$ ರಚನೆಯನ್ನು ಈ ಕೆಳಗಿನಂತೆ ವಿವರಿಸಬಹುದು:
| $\mathrm{Na}$ | $\rightarrow$ | $\mathrm{Na}^{+}+\mathrm{e}^{-}$ |
| $[\mathrm{Ne}] 3 \mathrm{~s}^{1}$ | $[\mathrm{Ne}]$ | |
| $\mathrm{Cl}+\mathrm{e}^{-}$ | $\rightarrow$ | $\mathrm{Cl}^{-}$ |
| $[\mathrm{Ne}] 3 s^{2} 3 p^{5}$ | $[\mathrm{Ne}] 3 s^{2} 3 p^{6}$ ಅಥವಾ $[\mathrm{Ar}]$ | |
| $\mathrm{Na}^{+}+\mathrm{Cl}^{-}$ | $\rightarrow$ | $\mathrm{NaCl}$ ಅಥವಾ $\mathrm{Na}^{+} \mathrm{Cl}^{-}$ |
ಅಂತೆಯೇ $\mathrm{CaF}_{2}$ ರಚನೆಯನ್ನು ಈ ಕೆಳಗಿನಂತೆ ತೋರಿಸಬಹುದು:
| $\mathrm{Ca}$ | $\rightarrow$ | $\mathrm{Ca}^{2+}+2 \mathrm{e}^{-}$ |
| $[\mathrm{Ar}] 4 s^{2}$ | $[\mathrm{Ar}]$ | |
| $\mathrm{F}+\mathrm{e}^{-}$ | $\rightarrow$ | $\mathrm{F}^{-}$ |
| $[\mathrm{He}] 2 s^{2} 2 p^{5}$ | $[\mathrm{He}] 2 s^{2} 2 p^{6}$ ಅಥವಾ $[\mathrm{Ne}]$ | |
| $\mathrm{Ca}^{2+}+2 \mathrm{~F}^{-}$ | $\rightarrow$ | $\mathrm{CaF}_2$ ಅಥವಾ $\mathrm{Ca}^{2+}\left(\mathrm{F}^{-}\right)_2$ |
ಧನಾತ್ಮಕ ಮತ್ತು ಋಣಾತ್ಮಕ ಅಯಾನುಗಳ ನಡುವಿನ ಸ್ಥಾಯೀವಿದ್ಯುತ್ ಆಕರ್ಷಣೆಯ ಪರಿಣಾಮವಾಗಿ ರೂಪುಗೊಂಡ ಬಂಧವನ್ನು ವಿದ್ಯುದ್ವೇಲೆನ್ಸ್ ಬಂಧ ಎಂದು ಕರೆಯಲಾಯಿತು. ಹೀಗಾಗಿ ವಿದ್ಯುದ್ವೇಲೆನ್ಸ್ ಅಯಾನಿನ ಮೇಲಿನ ಏಕಮಾನ ಆವೇಶ(ಗಳ) ಸಂಖ್ಯೆಗೆ ಸಮನಾಗಿರುತ್ತದೆ. ಹೀಗೆ, ಕ್ಯಾಲ್ಸಿಯಂಗೆ ಎರಡರ ಧನಾತ್ಮಕ ವಿದ್ಯುದ್ವೇಲೆನ್ಸ್ ನಿಗದಿಪಡಿಸಲಾಗಿದೆ, ಆದರೆ ಕ್ಲೋರಿನ್ಗೆ ಒಂದರ ಋಣಾತ್ಮಕ ವಿದ್ಯುದ್ವೇಲೆನ್ಸ್ ನಿಗದಿಪಡಿಸಲಾಗಿದೆ.
ಎಲೆಕ್ಟ್ರಾನ್ ವರ್ಗಾವಣೆಯಿಂದ ಅಯಾನು-ರಚನೆ ಮತ್ತು ಅಯಾನಿಕ್ ಸ್ಫಟಿಕೀಯ ಸಂಯುಕ್ತಗಳ ರಚನೆಗೆ ಸಂಬಂಧಿಸಿದ ಆಧುನಿಕ ಪರಿಕಲ್ಪನೆಗಳಿಗೆ ಕೊಸೆಲ್ನ ಪ್ರತಿಪಾದನೆಗಳು ಆಧಾರವನ್ನು ಒದಗಿಸುತ್ತವೆ. ಅಯಾನಿಕ್ ಸಂಯುಕ್ತಗಳ ತಿಳುವಳಿಕೆ ಮತ್ತು ವ್ಯವಸ್ಥೀಕರಣದಲ್ಲಿ ಅವರ ದೃಷ್ಟಿಕೋನಗಳು ಮಹತ್ವದ ಮೌಲ್ಯವನ್ನು ಹೊಂದಿವೆ ಎಂದು ಸಾಬೀತಾಗಿದೆ. ಅದೇ ಸಮಯದಲ್ಲಿ, ಬಹಳಷ್ಟು ಸಂಯುಕ್ತಗಳು ಈ ಪರಿಕಲ್ಪನೆಗಳಿಗೆ ಹೊಂದಿಕೊಳ್ಳುವುದಿಲ್ಲ ಎಂಬ ಅಂಶವನ್ನು ಅವರು ಗುರುತಿಸಿದ್ದರು.
4.1.1 ಅಷ್ಟಕ ನಿಯಮ
1916 ರಲ್ಲಿ ಕೊಸೆಲ್ ಮತ್ತು ಲೂಯಿಸ್ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ರಾಸಾಯನಿಕ ಬಂಧನ ಸಿದ್ಧಾಂತ ಎಂದು ಕರೆಯಲ್ಪಡುವ ಪರಮಾಣುಗಳ ನಡುವಿನ ರಾಸಾಯನಿಕ ಸಂಯೋಜನೆಯ ಪ್ರಮುಖ ಸಿದ್ಧಾಂತವನ್ನು ಅಭಿವೃದ್ಧಿಪಡಿಸಿದರು. ಇದರ ಪ್ರಕಾರ, ಪರಮಾಣುಗಳು ಒಂದು ಪರಮಾಣುವಿನಿಂದ ಇನ್ನೊಂದು ಪರಮಾಣುವಿಗೆ ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ವರ್ಗಾವಣೆಯಿಂದ (ಪಡೆಯುವುದು ಅಥವಾ ಕಳೆದುಕೊಳ್ಳುವುದು) ಅಥವಾ ಅವುಗಳ ವೇಲೆನ್ಸ್ ಶೆಲ್ಗಳಲ್ಲಿ ಅಷ್ಟಕವನ್ನು ಹೊಂದಲು ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಹಂಚಿಕೆಯಿಂದ ಸಂಯೋಗಗೊಳ್ಳಬಹುದು. ಇದನ್ನು ಅಷ್ಟಕ ನಿಯಮ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
4.1.2 ಸಹಸಂಯೋಜಕ ಬಂಧ
ಲ್ಯಾಂಗ್ಮುಯಿರ್ (1919) ಅಷ್ಟಕದ ಸ್ಥಿರ ಘನಾಕೃತಿ ವ್ಯವಸ್ಥೆಯ ಕಲ್ಪನೆಯನ್ನು ತ್ಯಜಿಸಿ ಮತ್ತು ಸಹಸಂಯೋಜಕ ಬಂಧ ಎಂಬ ಪದವನ್ನು ಪರಿಚಯಿಸುವ ಮೂಲಕ ಲೂಯಿಸ್ ಪ್ರತಿಪಾದನೆಗಳನ್ನು ಸಂಸ್ಕರಿಸಿದರು. ಕ್ಲೋರಿನ್ ಅಣುವಿನ ರಚನೆಯನ್ನು ಪರಿಗಣಿಸುವ ಮೂಲಕ ಲೂಯಿಸ್-ಲ್ಯಾಂಗ್ಮುಯಿರ್ ಸಿದ್ಧಾಂತವನ್ನು ಅರ್ಥಮಾಡಿಕೊಳ್ಳಬಹುದು, $\mathrm{Cl}_2$. $\mathrm{Cl}$ ಪರಮಾಣುವು ಎಲೆಕ್ಟ್ರಾನಿಕ್ ವಿನ್ಯಾಸ $[\mathrm{Ne}] 3 s^2 3 p^5$ ಹೊಂದಿದೆ, ಇದು ಆರ್ಗಾನ್ ವಿನ್ಯಾಸಕ್ಕಿಂತ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ಕಡಿಮೆ ಇದೆ. $\mathrm{Cl}_2$ ಅಣುವಿನ ರಚನೆಯನ್ನು ಎರಡು ಕ್ಲೋರಿನ್ ಪರಮಾಣುಗಳ ನಡುವೆ ಒಂದು ಜೋಡಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಹಂಚಿಕೆಯ ಪರಿಭಾಷೆಯಲ್ಲಿ ಅರ್ಥಮಾಡಿಕೊಳ್ಳಬಹುದು, ಪ್ರತಿ ಕ್ಲೋರಿನ್ ಪರಮಾಣುವು ಹಂಚಿದ ಜೋಡಿಗೆ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ಕೊಡುಗೆ ನೀಡುತ್ತದೆ. ಈ ಪ್ರಕ್ರಿಯೆಯಲ್ಲಿ ಎರಡೂ ಕ್ಲೋರಿನ್ ಪರಮಾಣುಗಳು ಹತ್ತಿರದ ಉದಾತ್ತ ಅನಿಲದ (ಅಂದರೆ, ಆರ್ಗಾನ್) ಹೊರ ಶೆಲ್ ಅಷ್ಟಕವನ್ನು ಪಡೆಯುತ್ತವೆ.

ಎರಡು Cl ಪರಮಾಣುಗಳ ನಡುವಿನ ಸಹಸಂಯೋಜಕ ಬಂಧ
ಚುಕ್ಕೆಗಳು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಪ್ರತಿನಿಧಿಸುತ್ತವೆ. ಅಂತಹ ರಚನೆಗಳನ್ನು ಲೂಯಿಸ್ ಚುಕ್ಕೆ ರಚನೆಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ಲೂಯಿಸ್ ಚುಕ್ಕೆ ರಚನೆಗಳನ್ನು ಇತರ ಅಣುಗಳಿಗೂ ಬರೆಯಬಹುದು, ಇದರಲ್ಲಿ ಸಂಯೋಜಿಸುವ ಪರಮಾಣುಗಳು ಒಂದೇ ರೀತಿಯ ಅಥವಾ ವಿಭಿನ್ನವಾಗಿರಬಹುದು. ಪ್ರಮುಖ ಷರತ್ತುಗಳೆಂದರೆ:
- ಪ್ರತಿ ಬಂಧವು ಪರಮಾಣುಗಳ ನಡುವೆ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಯ ಹಂಚಿಕೆಯ ಪರಿಣಾಮವಾಗಿ ರೂಪುಗೊಳ್ಳುತ್ತದೆ.
- ಪ್ರತಿ ಸಂಯೋಜಿಸುವ ಪರಮಾಣುವು ಹಂಚಿದ ಜೋಡಿಗೆ ಕನಿಷ್ಠ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ಕೊಡುಗೆ ನೀಡುತ್ತದೆ.
- ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಹಂಚಿಕೆಯ ಪರಿಣಾಮವಾಗಿ ಸಂಯೋಜಿಸುವ ಪರಮಾಣುಗಳು ಹೊರ ಶೆಲ್ ಉದಾತ್ತ ಅನಿಲ ವಿನ್ಯಾಸಗಳನ್ನು ಪಡೆಯುತ್ತವೆ.
- ಹೀಗೆ ನೀರು ಮತ್ತು ಕಾರ್ಬನ್ ಟೆಟ್ರಾಕ್ಲೋರೈಡ್ ಅಣುಗಳಲ್ಲಿ, ಸಹಸಂಯೋಜಕ ಬಂಧಗಳ ರಚನೆಯನ್ನು ಈ ಕೆಳಗಿನಂತೆ ಪ್ರತಿನಿಧಿಸಬಹುದು:

ಹೀಗೆ, ಎರಡು ಪರಮಾಣುಗಳು ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಯನ್ನು ಹಂಚಿಕೊಂಡಾಗ ಅವು ಒಂದೇ ಸಹಸಂಯೋಜಕ ಬಂಧದಿಂದ ಜೋಡಿಸಲ್ಪಟ್ಟಿವೆ ಎಂದು ಹೇಳಲಾಗುತ್ತದೆ. ಅನೇಕ ಸಂಯುಕ್ತಗಳಲ್ಲಿ ನಾವು ಪರಮಾಣುಗಳ ನಡುವೆ ಬಹು ಬಂಧಗಳನ್ನು ಹೊಂದಿದ್ದೇವೆ. ಬಹು ಬಂಧಗಳ ರಚನೆಯು ಎರಡು ಪರಮಾಣುಗಳ ನಡುವೆ ಒಂದಕ್ಕಿಂತ ಹೆಚ್ಚು ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳ ಹಂಚಿಕೆಯನ್ನು ಊಹಿಸುತ್ತದೆ. ಎರಡು ಪರಮಾಣುಗಳು ಎರಡು ಜೋಡಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹಂಚಿಕೊಂಡರೆ, ಅವುಗಳ ನಡುವಿನ ಸಹಸಂಯೋಜಕ ಬಂಧವನ್ನು ದ್ವಿ ಬಂಧ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, ಕಾರ್ಬನ್ ಡೈಆಕ್ಸೈಡ್ ಅಣುವಿನಲ್ಲಿ, ನಾವು ಕಾರ್ಬನ್ ಮತ್ತು ಆಮ್ಲಜನಕ ಪರಮಾಣುಗಳ ನಡುವೆ ಎರಡು ದ್ವಿ ಬಂಧಗಳನ್ನು ಹೊಂದಿದ್ದೇವೆ. ಅಂತೆಯೇ ಈಥೇನ್ ಅಣುವಿನಲ್ಲಿ ಎರಡು ಕಾರ್ಬನ್ ಪರಮಾಣುಗಳು ದ್ವಿ ಬಂಧದಿಂದ ಜೋಡಿಸಲ್ಪಟ್ಟಿವೆ..

$\mathrm{C} _{2} \mathrm{H} _{4}$ ಅಣು
ಸಂಯೋಜಿಸುವ ಪರಮಾಣುಗಳು ಮೂರು ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳನ್ನು ಹಂಚಿಕೊಂಡಾಗ, $N_{2}$ ಅಣುವಿನಲ್ಲಿ ಎರಡು ನೈಟ್ರೋಜನ್ ಪರಮಾಣುಗಳ ಸಂದರ್ಭದಲ್ಲಿ ಮತ್ತು ಈಥೈನ್ ಅಣುವಿನಲ್ಲಿ ಎರಡು ಕಾರ್ಬನ್ ಪರಮಾಣುಗಳ ಸಂದರ್ಭದಲ್ಲಿ, ತ್ರಿ ಬಂಧ ರೂಪುಗೊಳ್ಳುತ್ತದೆ.
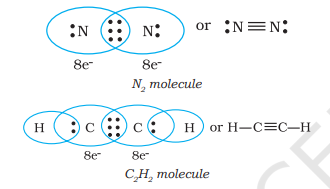
4.1.3 ಸರಳ ಅಣುಗಳ ಲೂಯಿಸ್ ಪ್ರತಿನಿಧಾನ (ಲೂಯಿಸ್ ರಚನೆಗಳು)
ಲೂಯಿಸ್ ಚುಕ್ಕೆ ರಚನೆಗಳು ಹಂಚಿದ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳು ಮತ್ತು ಅಷ್ಟಕ ನಿಯಮದ ಪರಿಭಾಷೆಯಲ್ಲಿ ಅಣುಗಳು ಮತ್ತು ಅಯಾನುಗಳಲ್ಲಿನ ಬಂಧನದ ಚಿತ್ರಣವನ್ನು ಒದಗಿಸುತ್ತವೆ. ಅಂತಹ ಚಿತ್ರಣವು ಅಣುವಿನ ಬಂಧನ ಮತ್ತು ನಡವಳಿಕೆಯನ್ನು ಸಂಪೂರ್ಣವಾಗಿ ವಿವರಿಸದಿದ್ದರೂ, ಇದು ಅಣುವಿನ ರಚನೆ ಮತ್ತು ಗುಣಲಕ್ಷಣಗಳನ್ನು ಹೆಚ್ಚಿನ ಮಟ್ಟಿಗೆ ಅರ್ಥಮಾಡಿಕೊಳ್ಳಲು ಸಹಾಯ ಮಾಡುತ್ತದೆ. ಆದ್ದರಿಂದ, ಅಣುಗಳ ಲೂಯಿಸ್ ಚುಕ್ಕೆ ರಚನೆಗಳನ್ನು ಬರೆಯುವುದು ಬಹಳ ಉಪಯುಕ್ತವಾಗಿದೆ. ಲೂಯಿಸ್ ಚುಕ್ಕೆ ರಚನೆಗಳನ್ನು ಈ ಕೆಳಗಿನ ಹಂತಗಳನ್ನು ಅಳವಡಿಸಿಕೊಂಡು ಬರೆಯಬಹುದು:
- ರಚನೆಗಳನ್ನು ಬರೆಯಲು ಅಗತ್ಯವಾದ ಒಟ್ಟು ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯನ್ನು ಸಂಯೋಜಿಸುವ ಪರಮಾಣುಗಳ ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಸೇರಿಸುವ ಮೂಲಕ ಪಡೆಯಲಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, $\mathrm{CH}_{4}$ ಅಣುವಿನಲ್ಲಿ ಬಂಧನಕ್ಕಾಗಿ ಎಂಟು ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಲಭ್ಯವಿವೆ (ಕಾರ್ಬನ್ನಿಂದ 4 ಮತ್ತು ನಾಲ್ಕು ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳಿಂದ 4).
- ಋಣಾತ್ಮಕ ಅಯಾನುಗಳಿಗೆ, ಪ್ರತಿ ಋಣಾತ್ಮಕ ಆವೇಶವು ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ನ ಸೇರ್ಪಡೆಯನ್ನು ಅರ್ಥೈಸುತ್ತದೆ. ಧನಾತ್ಮಕ ಅಯಾನುಗಳಿಗೆ, ಪ್ರತಿ ಧನಾತ್ಮಕ ಆವೇಶವು ಒಟ್ಟು ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯಿಂದ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ನ ವ್ಯವಕಲನಕ್ಕೆ ಕಾರಣವಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, $CO_3^{2-}$ ಅಯಾನಿಗೆ, ಎರಡು ಋಣಾತ್ಮಕ ಆವೇಶಗಳು ತಟಸ್ಥ ಪರಮಾಣುಗಳು ಒದಗಿಸಿದ್ದಕ್ಕಿಂತ ಎರಡು ಹೆಚ್ಚುವರಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿವೆ ಎಂದು ಸೂಚಿಸುತ್ತದೆ. $\mathrm{NH}_{4}^{+}$ ಅಯಾನಿಗೆ, ಒಂದು ಧನಾತ್ಮಕ ಆವೇಶವು ತಟಸ್ಥ ಪರಮಾಣುಗಳ ಗುಂಪಿನಿಂದ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ನಷ್ಟವನ್ನು ಸೂಚಿಸುತ್ತದೆ.
- ಸಂಯೋಜಿಸುವ ಪರಮಾಣುಗಳ ರಾಸಾಯನಿಕ ಚಿಹ್ನೆಗಳನ್ನು ತಿಳಿದುಕೊಳ್ಳುವುದು ಮತ್ತು ಸಂಯುಕ್ತದ ಅಸ್ಥಿರಚನೆಯ ರಚನೆಯ ಜ್ಞಾನವನ್ನು ಹೊಂದಿರುವುದು (ತಿಳಿದಿರುವ ಅಥವಾ ಬುದ್ಧಿವಂತಿಕೆಯಿಂದ ಊಹಿಸಲಾದ), ಒಟ್ಟು ಬಂಧಗಳಿಗೆ ಅನುಪಾತದಲ್ಲಿ ಪರಮಾಣುಗಳ ನಡುವೆ ಬಂಧನ ಹಂಚಿದ ಜೋಡಿಗಳಾಗಿ ಒಟ್ಟು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ವಿತರಿಸುವುದು ಸುಲಭ.
- ಸಾಮಾನ್ಯವಾಗಿ ಕನಿಷ್ಠ ವಿದ್ಯುದೃಣಾತ್ಮಕ ಪರಮಾಣುವು ಅಣು/ಅಯಾನಿನ ಕೇಂದ್ರ ಸ್ಥಾನವನ್ನು ಆಕ್ರಮಿಸುತ್ತದೆ. ಉದಾಹರಣೆಗೆ $\mathrm{NF}_3$ ಮತ್ತು $CO_3^{2-}$ ನಲ್ಲಿ, ನೈಟ್ರೋಜನ್ ಮತ್ತು ಕಾರ್ಬನ್ ಕೇಂದ್ರ ಪರಮಾಣುಗಳಾಗಿದ್ದರೆ ಫ್ಲೋರಿನ್ ಮತ್ತು ಆಮ್ಲಜನಕ ತುದಿ ಸ್ಥಾನಗಳನ್ನು ಆಕ್ರಮಿಸುತ್ತವೆ.
- ಏಕ ಬಂಧಗಳಿಗೆ ಹಂಚಿದ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳ ಲೆಕ್ಕಾಚಾರದ ನಂತರ, ಉಳಿದ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳನ್ನು ಬಹು ಬಂಧನಕ್ಕಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ ಅಥವಾ ಏಕಾಂಗಿ ಜೋಡಿಗಳಾಗಿ ಉಳಿಯುತ್ತವೆ. ಪ್ರತಿ ಬಂಧಿತ ಪರಮಾಣುವು ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಅಷ್ಟಕವನ್ನು ಪಡೆಯುತ್ತದೆ ಎಂಬುದು ಮೂಲ ಅವಶ್ಯಕತೆಯಾಗಿದೆ.
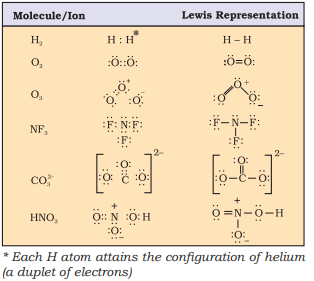
ಕೆಲವು ಅಣುಗಳ/ಅಯಾನುಗಳ ಲೂಯಿಸ್ ಪ್ರತಿನಿಧಾನಗಳನ್ನು ಕೋಷ್ಟಕ 4.1 ರಲ್ಲಿ ನೀಡಲಾಗಿದೆ.
ಕೋಷ್ಟಕ 4.1 ಕೆಲವು ಅಣುಗಳ ಲೂಯಿಸ್ ಪ್ರತಿನಿಧಾನ
ಸಮಸ್ಯೆ 4.1
$\mathrm{CO}$ ಅಣುವಿನ ಲೂಯಿಸ್ ಚುಕ್ಕೆ ರಚನೆಯನ್ನು ಬರೆಯಿರಿ.
ಪರಿಹಾರ
ಹಂತ 1. ಕಾರ್ಬನ್ ಮತ್ತು ಆಮ್ಲಜನಕ ಪರಮಾಣುಗಳ ಒಟ್ಟು ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯನ್ನು ಎಣಿಸಿ. ಕಾರ್ಬನ್ ಮತ್ತು ಆಮ್ಲಜನಕ ಪರಮಾಣುಗಳ ಹೊರ (ವೇಲೆನ್ಸ್) ಶೆಲ್ ವಿನ್ಯಾಸಗಳು: $2 s^{2} 2 p^{2}$ ಮತ್ತು $2 s^{2} 2 p^{4}$, ಅನುಕ್ರಮವಾಗಿ. ಲಭ್ಯವಿರುವ ವೇಲೆನ್ಸ್ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು $4+6=10$.
ಹಂತ 2. $\mathrm{CO}$ ನ ಅಸ್ಥಿರಚನೆಯ ರಚನೆಯನ್ನು ಈ ರೀತಿ ಬರೆಯಲಾಗಿದೆ: C O
ಹಂತ 3. $\mathrm{C}$ ಮತ್ತು $\mathrm{O}$ ನಡುವೆ ಒಂದೇ ಬಂಧವನ್ನು (ಒಂದು ಹಂಚಿದ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿ) ಎಳೆಯಿರಿ ಮತ್ತು $\mathrm{O}$ ನಲ್ಲಿ ಅಷ್ಟಕವನ್ನು ಪೂರ್ಣಗೊಳಿಸಿ, ಉಳಿದ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳು $\mathrm{C}$ ನ ಮೇಲಿನ ಏಕಾಂಗಿ ಜೋಡಿಯಾಗಿವೆ.
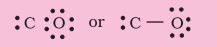
ಇದು ಕಾರ್ಬನ್ನಲ್ಲಿ ಅಷ್ಟಕವನ್ನು ಪೂರ್ಣಗೊಳಿಸುವುದಿಲ್ಲ ಮತ್ತು ಆದ್ದರಿಂದ ನಾವು $\mathrm{C}$ ಮತ್ತು $\mathrm{O}$ ಪರಮಾಣುಗಳ ನಡುವೆ ಬಹು ಬಂಧನಕ್ಕೆ (ಈ ಸಂದರ್ಭದಲ್ಲಿ ತ್ರಿ ಬಂಧ) ಆಶ








