ಅಧ್ಯಾಯ 08 ರೆಡಾಕ್ಸ್ ಪ್ರತಿಕ್ರಿಯೆಗಳು
“ಆಕ್ಸಿಡೀಕರಣ ಇರುವಲ್ಲಿ, ಯಾವಾಗಲೂ ರಿಡಕ್ಷನ್ ಇರುತ್ತದೆ ರಸಾಯನಶಾಸ್ತ್ರವು ಮೂಲಭೂತವಾಗಿ ರೆಡಾಕ್ಸ್ ವ್ಯವಸ್ಥೆಗಳ ಅಧ್ಯಯನವಾಗಿದೆ.”
ರಸಾಯನಶಾಸ್ತ್ರವು ವಿವಿಧ ರೀತಿಯ ದ್ರವ್ಯ ಮತ್ತು ಒಂದು ರೀತಿಯ ದ್ರವ್ಯವು ಇನ್ನೊಂದರಲ್ಲಿ ಬದಲಾವಣೆಯನ್ನು ಕುರಿತು ವ್ಯವಹರಿಸುತ್ತದೆ. ದ್ರವ್ಯದ ರೂಪಾಂತರವು ಒಂದು ರೀತಿಯಿಂದ ಇನ್ನೊಂದಕ್ಕೆ ವಿವಿಧ ರೀತಿಯ ಕ್ರಿಯೆಗಳ ಮೂಲಕ ಸಂಭವಿಸುತ್ತದೆ. ಅಂತಹ ಕ್ರಿಯೆಗಳ ಒಂದು ಪ್ರಮುಖ ವರ್ಗವೆಂದರೆ ರೆಡಾಕ್ಸ್ ಕ್ರಿಯೆಗಳು. ಅನೇಕ ವಿದ್ಯಮಾನಗಳು, ಭೌತಿಕ ಹಾಗೂ ಜೈವಿಕ ಎರಡೂ, ರೆಡಾಕ್ಸ್ ಕ್ರಿಯೆಗಳೊಂದಿಗೆ ಸಂಬಂಧಿಸಿವೆ. ಈ ಕ್ರಿಯೆಗಳು ಔಷಧೀಯ, ಜೈವಿಕ, ಕೈಗಾರಿಕಾ, ಲೋಹವಿಜ್ಞಾನ ಮತ್ತು ಕೃಷಿ ಕ್ಷೇತ್ರಗಳಲ್ಲಿ ವ್ಯಾಪಕವಾಗಿ ಬಳಕೆಯಾಗುತ್ತವೆ. ಈ ಕ್ರಿಯೆಗಳ ಪ್ರಾಮುಖ್ಯತೆಯು ವಿವಿಧ ರೀತಿಯ ಇಂಧನಗಳ ದಹನ, ಗೃಹ, ಸಾರಿಗೆ ಮತ್ತು ಇತರ ವಾಣಿಜ್ಯ ಉದ್ದೇಶಗಳಿಗಾಗಿ ಶಕ್ತಿ ಪಡೆಯುವುದು, ಅತ್ಯಂತ ಕ್ರಿಯಾಶೀಲ ಲೋಹಗಳು ಮತ್ತು ಅಲೋಹಗಳ ಹೊರತೆಗೆಯುವಿಕೆಗಾಗಿ ವಿದ್ಯುತ್ ರಾಸಾಯನಿಕ ಪ್ರಕ್ರಿಯೆಗಳು, ಕಾಸ್ಟಿಕ್ ಸೋಡಾ ನಂತಹ ರಾಸಾಯನಿಕ ಸಂಯುಕ್ತಗಳ ತಯಾರಿಕೆ, ಶುಷ್ಕ ಮತ್ತು ಆರ್ದ್ರ ಬ್ಯಾಟರಿಗಳ ಕಾರ್ಯಾಚರಣೆ ಮತ್ತು ಲೋಹಗಳ ತುಕ್ಕು ಹಿಡಿಯುವಿಕೆ ರೆಡಾಕ್ಸ್ ಪ್ರಕ್ರಿಯೆಗಳ ವ್ಯಾಪ್ತಿಗೆ ಬರುತ್ತವೆ ಎಂಬ ಅಂಶದಿಂದ ಸ್ಪಷ್ಟವಾಗಿದೆ. ಇತ್ತೀಚೆಗೆ, ಹೈಡ್ರೋಜನ್ ಇಕಾನಮಿ (ದ್ರವ ಹೈಡ್ರೋಜನ್ ಅನ್ನು ಇಂಧನವಾಗಿ ಬಳಸುವುದು) ಮತ್ತು ‘ಓಝೋನ್ ಹೋಲ್’ ಅಭಿವೃದ್ಧಿಯಂತಹ ಪರಿಸರ ಸಮಸ್ಯೆಗಳು ರೆಡಾಕ್ಸ್ ವಿದ್ಯಮಾನದ ಅಡಿಯಲ್ಲಿ ಕಾಣಿಸಿಕೊಳ್ಳಲು ಪ್ರಾರಂಭಿಸಿವೆ.
8.1 ರೆಡಾಕ್ಸ್ ಕ್ರಿಯೆಗಳ ಶಾಸ್ತ್ರೀಯ ಕಲ್ಪನೆ - ಆಕ್ಸಿಡೀಕರಣ ಮತ್ತು ರಿಡಕ್ಷನ್ ಕ್ರಿಯೆಗಳು
ಮೂಲತಃ, ಆಕ್ಸಿಡೀಕರಣ ಎಂಬ ಪದವನ್ನು ಒಂದು ಮೂಲಧಾತು ಅಥವಾ ಸಂಯುಕ್ತಕ್ಕೆ ಆಮ್ಲಜನಕದ ಸೇರ್ಪಡೆಯನ್ನು ವಿವರಿಸಲು ಬಳಸಲಾಗುತ್ತಿತ್ತು. ವಾತಾವರಣದಲ್ಲಿ ಡೈಆಕ್ಸಿಜನ್ ಇರುವುದರಿಂದ (20%), ಅನೇಕ ಮೂಲಧಾತುಗಳು ಅದರೊಂದಿಗೆ ಸಂಯೋಜಿಸುತ್ತವೆ ಮತ್ತು ಅವು ಸಾಮಾನ್ಯವಾಗಿ ಭೂಮಿಯ ಮೇಲೆ ಅವುಗಳ ಆಕ್ಸೈಡ್ ರೂಪದಲ್ಲಿ ಕಂಡುಬರುವುದಕ್ಕೆ ಇದು ಪ್ರಮುಖ ಕಾರಣವಾಗಿದೆ. ಕೆಳಗಿನ ಕ್ರಿಯೆಗಳು ಆಕ್ಸಿಡೀಕರಣದ ಸೀಮಿತ ವ್ಯಾಖ್ಯಾನದ ಪ್ರಕಾರ ಆಕ್ಸಿಡೀಕರಣ ಪ್ರಕ್ರಿಯೆಗಳನ್ನು ಪ್ರತಿನಿಧಿಸುತ್ತವೆ:
$$2 \mathrm{Mg}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{MgO}(\mathrm{s}) \tag{8.1}$$
$$\mathrm{S}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow \mathrm{SO_2}(\mathrm{~g}) \tag{8.2}$$
ಕ್ರಿಯೆಗಳು (8.1) ಮತ್ತು (8.2) ರಲ್ಲಿ, ಮೆಗ್ನೀಶಿಯಮ್ ಮತ್ತು ಸಲ್ಫರ್ ಮೂಲಧಾತುಗಳು ಅವುಗಳಿಗೆ ಆಮ್ಲಜನಕ ಸೇರಿದ್ದರಿಂದ ಆಕ್ಸಿಡೀಕರಣಗೊಳ್ಳುತ್ತವೆ. ಅಂತೆಯೇ, ಮೀಥೇನ್ ಅದಕ್ಕೆ ಆಮ್ಲಜನಕ ಸೇರಿದ್ದರಿಂದ ಆಕ್ಸಿಡೀಕರಣಗೊಳ್ಳುತ್ತದೆ.
$$\mathrm{CH} _{4}(\mathrm{~g})+2 \mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g})+2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{7.3}$$
ಕ್ರಿಯೆ (8.3) ನ ಸೂಕ್ಷ್ಮ ಪರೀಕ್ಷೆಯು, ಅದರಿಂದ ಹೈಡ್ರೋಜನ್ ಆಮ್ಲಜನಕದಿಂದ ಬದಲಾಯಿಸಲ್ಪಟ್ಟಿದೆ, ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞರನ್ನು ಹೈಡ್ರೋಜನ್ ತೆಗೆದುಹಾಕುವಿಕೆಯ ಪರಿಭಾಷೆಯಲ್ಲಿ ಆಕ್ಸಿಡೀಕರಣವನ್ನು ಪುನರ್ವ್ಯಾಖ್ಯಾನಿಸಲು ಪ್ರೇರೇಪಿಸಿತು ಮತ್ತು ಆದ್ದರಿಂದ, ಆಕ್ಸಿಡೀಕರಣ ಪದದ ವ್ಯಾಪ್ತಿಯು ಒಂದು ವಸ್ತುವಿನಿಂದ ಹೈಡ್ರೋಜನ್ ತೆಗೆದುಹಾಕುವಿಕೆಯನ್ನು ಒಳಗೊಳ್ಳುವಂತೆ ವಿಸ್ತರಿಸಲ್ಪಟ್ಟಿತು. ಕೆಳಗಿನ ವಿವರಣೆಯು ಹೈಡ್ರೋಜನ್ ತೆಗೆದುಹಾಕುವಿಕೆಯನ್ನು ಆಕ್ಸಿಡೀಕರಣ ಕ್ರಿಯೆಯಾಗಿ ಉಲ್ಲೇಖಿಸಬಹುದಾದ ಇನ್ನೊಂದು ಕ್ರಿಯೆಯಾಗಿದೆ.
$$ \begin{equation*} 2 \mathrm{H_2} \mathrm{~S}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{~S}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \tag{8.4} \end{equation*} $$
ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞರ ಜ್ಞಾನ ಬೆಳೆದಂತೆ, ಆಕ್ಸಿಡೀಕರಣ ಪದವನ್ನು (7.1 ರಿಂದ 7.4) ನಂತಹ, ಆಮ್ಲಜನಕವನ್ನು ಒಳಗೊಳ್ಳದ ಆದರೆ ಇತರ ವಿದ್ಯುದೃಣಾತ್ಮಕ ಮೂಲಧಾತುಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ಕ್ರಿಯೆಗಳಿಗೆ ವಿಸ್ತರಿಸುವುದು ಸ್ವಾಭಾವಿಕವಾಗಿತ್ತು. ಮೆಗ್ನೀಶಿಯಮ್ನ ಆಕ್ಸಿಡೀಕರಣವು ಫ್ಲೋರಿನ್, ಕ್ಲೋರಿನ್ ಮತ್ತು ಸಲ್ಫರ್ ಇತ್ಯಾದಿಗಳೊಂದಿಗೆ ಕೆಳಗಿನ ಕ್ರಿಯೆಗಳ ಪ್ರಕಾರ ಸಂಭವಿಸುತ್ತದೆ:
$$\operatorname{Mg}(\mathrm{s})+\mathrm{F_2} (\mathrm{~g}) \rightarrow \operatorname{MgF_2} (s) \tag{8.5}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{Cl_2} (g) \rightarrow \mathrm{MgCl_2} (s) \tag{8.6}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{S} (s) \rightarrow \operatorname{MgS}(\mathrm{s}) \tag{8.7}$$
ಕ್ರಿಯೆಗಳು (7.5 ರಿಂದ 7.7) ಅನ್ನು ಆಕ್ಸಿಡೀಕರಣ ಕ್ರಿಯೆಗಳ ವ್ಯಾಪ್ತಿಯೊಳಗೆ ಸೇರಿಸಿಕೊಳ್ಳುವುದು ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞರನ್ನು ಹೈಡ್ರೋಜನ್ ತೆಗೆದುಹಾಕುವಿಕೆಯನ್ನು ಮಾತ್ರವಲ್ಲದೆ ವಿದ್ಯುದ್ಧನಾತ್ಮಕ ಮೂಲಧಾತುಗಳ ತೆಗೆದುಹಾಕುವಿಕೆಯನ್ನು ಸಹ ಆಕ್ಸಿಡೀಕರಣವೆಂದು ಪರಿಗಣಿಸಲು ಪ್ರೋತ್ಸಾಹಿಸಿತು. ಹೀಗೆ ಕ್ರಿಯೆ:
$$ 2 \mathrm{~K_4} \left[ \mathrm{Fe} ( \mathrm{CN})_{6} \right] ( \mathrm{aq}) + \mathrm{H_2} \mathrm{O_2} ( \mathrm{aq}) \rightarrow 2 \mathrm{~K_3} \left[\mathrm{Fe}( \mathrm{CN})_6 \right] ( \mathrm{aq}) + 2 \mathrm{KOH} ( \mathrm{aq}) $$
ಅದು ಪೊಟ್ಯಾಸಿಯಮ್ ಫೆರ್ರಿಕ್ಯಾನೈಡ್ ಆಗಿ ಬದಲಾಗುವ ಮೊದಲು ಪೊಟ್ಯಾಸಿಯಮ್ ಫೆರ್ರೋಸಯನೈಡ್ನಿಂದ ವಿದ್ಯುದ್ಧನಾತ್ಮಕ ಮೂಲಧಾತು ಪೊಟ್ಯಾಸಿಯಮ್ ತೆಗೆದುಹಾಕಿದ್ದರಿಂದ ಆಕ್ಸಿಡೀಕರಣವೆಂದು ವ್ಯಾಖ್ಯಾನಿಸಲಾಗಿದೆ. ಸಂಕ್ಷಿಪ್ತವಾಗಿ ಹೇಳುವುದಾದರೆ, “ಆಕ್ಸಿಡೀಕರಣ” ಪದವನ್ನು ಒಂದು ವಸ್ತುವಿಗೆ ಆಮ್ಲಜನಕ/ವಿದ್ಯುದೃಣಾತ್ಮಕ ಮೂಲಧಾತುವಿನ ಸೇರ್ಪಡೆ ಅಥವಾ ಒಂದು ವಸ್ತುವಿನಿಂದ ಹೈಡ್ರೋಜನ್/ವಿದ್ಯುದ್ಧನಾತ್ಮಕ ಮೂಲಧಾತುವಿನ ತೆಗೆದುಹಾಕುವಿಕೆ ಎಂದು ವ್ಯಾಖ್ಯಾನಿಸಲಾಗಿದೆ.
ಆರಂಭದಲ್ಲಿ, ರಿಡಕ್ಷನ್ ಅನ್ನು ಒಂದು ಸಂಯುಕ್ತದಿಂದ ಆಮ್ಲಜನಕ ತೆಗೆದುಹಾಕುವಿಕೆಯೆಂದು ಪರಿಗಣಿಸಲಾಗಿತ್ತು. ಆದರೆ, ರಿಡಕ್ಷನ್ ಪದವನ್ನು ಈ ದಿನಗಳಲ್ಲಿ ಒಂದು ವಸ್ತುವಿನಿಂದ ಆಮ್ಲಜನಕ/ವಿದ್ಯುದೃಣಾತ್ಮಕ ಮೂಲಧಾತುವಿನ ತೆಗೆದುಹಾಕುವಿಕೆ ಅಥವಾ ಒಂದು ವಸ್ತುವಿಗೆ ಹೈಡ್ರೋಜನ್/ವಿದ್ಯುದ್ಧನಾತ್ಮಕ ಮೂಲಧಾತುವಿನ ಸೇರ್ಪಡೆಯನ್ನು ಒಳಗೊಳ್ಳುವಂತೆ ವಿಸ್ತರಿಸಲಾಗಿದೆ.
ಮೇಲೆ ನೀಡಲಾದ ವ್ಯಾಖ್ಯಾನದ ಪ್ರಕಾರ, ಕೆಳಗಿನವು ರಿಡಕ್ಷನ್ ಪ್ರಕ್ರಿಯೆಗಳ ಉದಾಹರಣೆಗಳಾಗಿವೆ:
$$2 \mathrm{HgO}(\mathrm{s}) \xrightarrow{\Delta} 2 \mathrm{Hg}(\mathrm{l})+\mathrm{O_2}(\mathrm{~g}) \tag{8.8}$$
(ಮರ್ಕ್ಯುರಿಕ್ ಆಕ್ಸೈಡ್ನಿಂದ ಆಮ್ಲಜನಕ ತೆಗೆದುಹಾಕುವಿಕೆ)
$$2 \mathrm{FeCl_3}(\mathrm{aq})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{FeCl_2}(\mathrm{aq})+2 \mathrm{HCl}(\mathrm{aq}) \tag{8.9}$$
(ವಿದ್ಯುದೃಣಾತ್ಮಕ ಮೂಲಧಾತು, ಕ್ಲೋರಿನ್ ಅನ್ನು ಫೆರಿಕ್ ಕ್ಲೋರೈಡ್ನಿಂದ ತೆಗೆದುಹಾಕುವಿಕೆ)
$$\mathrm{CH_2}=\mathrm{CH_2}(\mathrm{~g})+\mathrm{H_2}(\mathrm{~g}) \rightarrow \mathrm{H_3} \mathrm{C}-\mathrm{CH_3}(\mathrm{~g})\tag{8.10}$$
(ಹೈಡ್ರೋಜನ್ ಸೇರ್ಪಡೆ)
$$2 \mathrm{HgCl_2}(\mathrm{aq})+\mathrm{SnCl_2}(\mathrm{aq}) \rightarrow \mathrm{Hg_2} \mathrm{Cl_2}(\mathrm{~s})+\mathrm{SnCl_4}(\mathrm{aq})\tag{8.11}$$
(ಮರ್ಕ್ಯುರಿಕ್ ಕ್ಲೋರೈಡ್ಗೆ ಪಾದರಸದ ಸೇರ್ಪಡೆ)
ಕ್ರಿಯೆ (8.11) ರಲ್ಲಿ, ಸ್ಟ್ಯಾನಸ್ ಕ್ಲೋರೈಡ್ನಿಂದ ಸ್ಟ್ಯಾನಿಕ್ ಕ್ಲೋರೈಡ್ಗೆ ಏಕಕಾಲಿಕ ಆಕ್ಸಿಡೀಕರಣವೂ ಸಂಭವಿಸುತ್ತಿದೆ ಏಕೆಂದರೆ ಅದಕ್ಕೆ ವಿದ್ಯುದೃಣಾತ್ಮಕ ಮೂಲಧಾತು ಕ್ಲೋರಿನ್ ಸೇರಿದೆ. ಆಕ್ಸಿಡೀಕರಣ ಮತ್ತು ರಿಡಕ್ಷನ್ ಯಾವಾಗಲೂ ಏಕಕಾಲದಲ್ಲಿ ಸಂಭವಿಸುತ್ತವೆ ಎಂದು ಶೀಘ್ರದಲ್ಲೇ ಅರಿವಾಯಿತು (ಮೇಲೆ ನೀಡಲಾದ ಎಲ್ಲಾ ಸಮೀಕರಣಗಳನ್ನು ಪುನಃ ಪರೀಕ್ಷಿಸುವ ಮೂಲಕ ಸ್ಪಷ್ಟವಾಗುತ್ತದೆ), ಆದ್ದರಿಂದ, ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗಳ ಈ ವರ್ಗಕ್ಕೆ “ರೆಡಾಕ್ಸ್” ಎಂಬ ಪದವನ್ನು ರಚಿಸಲಾಯಿತು.
ಸಮಸ್ಯೆ 8.1
ಕೆಳಗೆ ನೀಡಲಾದ ಕ್ರಿಯೆಗಳಲ್ಲಿ, ಆಕ್ಸಿಡೀಕರಣ ಮತ್ತು ರಿಡಕ್ಷನ್ ಅನುಭವಿಸುವ ಪ್ರಜಾತಿಗಳನ್ನು ಗುರುತಿಸಿ:
(i) $\mathrm{H_2} \mathrm{~S}$ (g) $+\mathrm{Cl_2}$ (g) $\rightarrow 2 \mathrm{HCl}$ (g) $+\mathrm{S}$ (s)
(ii) $3 \mathrm{Fe_3} \mathrm{O_4}$ (s) $+8 \mathrm{Al}$ (s) $\rightarrow 9 \mathrm{Fe}$ (s) $+4 \mathrm{Al_2} \mathrm{O_3}(\mathrm{~s})$
(iii) $2 \mathrm{Na}$ (s) $+\mathrm{H_2}$ (g) $\rightarrow 2 \mathrm{NaH}$ (s)
ಪರಿಹಾರ
(i) $\mathrm{H_2} \mathrm{~S}$ ಆಕ್ಸಿಡೀಕರಣಗೊಳ್ಳುತ್ತದೆ ಏಕೆಂದರೆ ಹೆಚ್ಚು ವಿದ್ಯುದೃಣಾತ್ಮಕ ಮೂಲಧಾತು, ಕ್ಲೋರಿನ್ ಅನ್ನು ಹೈಡ್ರೋಜನ್ಗೆ ಸೇರಿಸಲಾಗಿದೆ (ಅಥವಾ ಹೆಚ್ಚು ವಿದ್ಯುದ್ಧನಾತ್ಮಕ ಮೂಲಧಾತು, ಹೈಡ್ರೋಜನ್ ಅನ್ನು S ನಿಂದ ತೆಗೆದುಹಾಕಲಾಗಿದೆ). ಕ್ಲೋರಿನ್ ಅದಕ್ಕೆ ಹೈಡ್ರೋಜನ್ ಸೇರಿದ್ದರಿಂದ ರಿಡಕ್ಷನ್ ಆಗುತ್ತದೆ.
(ii) ಅಲ್ಯೂಮಿನಿಯಮ್ ಆಕ್ಸಿಡೀಕರಣಗೊಳ್ಳುತ್ತದೆ ಏಕೆಂದರೆ ಅದಕ್ಕೆ ಆಮ್ಲಜನಕ ಸೇರಿದೆ. ಫೆರಸ್ ಫೆರಿಕ್ ಆಕ್ಸೈಡ್ $\left(\mathrm{Fe_3} \mathrm{O_4}\right)$ ರಿಡಕ್ಷನ್ ಆಗುತ್ತದೆ ಏಕೆಂದರೆ ಅದರಿಂದ ಆಮ್ಲಜನಕ ತೆಗೆದುಹಾಕಲಾಗಿದೆ.
(iii) ವಿದ್ಯುದೃಣಾತ್ಮಕತೆಯ ಪರಿಕಲ್ಪನೆಯನ್ನು ಎಚ್ಚರಿಕೆಯಿಂದ ಅನ್ವಯಿಸುವ ಮೂಲಕ ಮಾತ್ರ ನಾವು ಸೋಡಿಯಮ್ ಆಕ್ಸಿಡೀಕರಣಗೊಂಡಿದೆ ಮತ್ತು ಹೈಡ್ರೋಜನ್ ರಿಡಕ್ಷನ್ ಆಗಿದೆ ಎಂದು ನಿರ್ಣಯಿಸಬಹುದು.
ಇಲ್ಲಿ ಆಯ್ಕೆ ಮಾಡಲಾದ ಕ್ರಿಯೆ (iii) ನಮ್ಮನ್ನು ರೆಡಾಕ್ಸ್ ಕ್ರಿಯೆಗಳನ್ನು ವ್ಯಾಖ್ಯಾನಿಸಲು ಇನ್ನೊಂದು ಮಾರ್ಗದ ಬಗ್ಗೆ ಯೋಚಿಸಲು ಪ್ರೇರೇಪಿಸುತ್ತದೆ.
8.2 ಎಲೆಕ್ಟ್ರಾನ್ ವರ್ಗಾವಣೆ ಕ್ರಿಯೆಗಳ ಪರಿಭಾಷೆಯಲ್ಲಿ ರೆಡಾಕ್ಸ್ ಕ್ರಿಯೆಗಳು
ಈಗಾಗಲೇ ನಾವು ಕಲಿತಿದ್ದೇವೆ, ಈ ಕ್ರಿಯೆಗಳು ರೆಡಾಕ್ಸ್ ಕ್ರಿಯೆಗಳಾಗಿವೆ ಏಕೆಂದರೆ ಈ ಪ್ರತಿಯೊಂದು ಕ್ರಿಯೆಗಳಲ್ಲಿಯೂ ಸೋಡಿಯಮ್ಗೆ ಆಮ್ಲಜನಕ ಅಥವಾ ಹೆಚ್ಚು ವಿದ್ಯುದೃಣಾತ್ಮಕ ಮೂಲಧಾತು ಸೇರಿದ್ದರಿಂದ ಸೋಡಿಯಮ್ ಆಕ್ಸಿಡೀಕರಣಗೊಳ್ಳುತ್ತದೆ.
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaCl}(\mathrm{s})\tag{8.12}$$
$$4 \mathrm{Na}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na_2} \mathrm{O}(\mathrm{s})\tag{8.13}$$
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{S}(\mathrm{s}) \rightarrow \mathrm{Na_2} \mathrm{~S}(\mathrm{~s}) \tag{8.14}$$
ಏಕಕಾಲದಲ್ಲಿ, ಕ್ಲೋರಿನ್, ಆಮ್ಲಜನಕ ಮತ್ತು ಸಲ್ಫರ್ ರಿಡಕ್ಷನ್ ಆಗುತ್ತವೆ ಏಕೆಂದರೆ ಇವುಗಳಲ್ಲಿ ಪ್ರತಿಯೊಂದಕ್ಕೂ ವಿದ್ಯುದ್ಧನಾತ್ಮಕ ಮೂಲಧಾತು ಸೋಡಿಯಮ್ ಸೇರಿದೆ. ರಾಸಾಯನಿಕ ಬಂಧದ ಬಗ್ಗೆ ನಮ್ಮ ಜ್ಞಾನದಿಂದ ನಾವು ಸೋಡಿಯಮ್ ಕ್ಲೋರೈಡ್, ಸೋಡಿಯಮ್ ಆಕ್ಸೈಡ್ ಮತ್ತು ಸೋಡಿಯಮ್ ಸಲ್ಫೈಡ್ ಅಯಾನಿಕ್ ಸಂಯುಕ್ತಗಳು ಮತ್ತು ಬಹುಶಃ ಉತ್ತಮವಾಗಿ $\mathrm{Na}^{+} \mathrm{Cl}^{-}( \mathrm{s}),\left(\mathrm{Na}^{+} \right)_2 \mathrm{O}^{2-}( \mathrm{s})$, ಮತ್ತು $ \left(\mathrm{Na}^{+} \right)_2$ $\mathrm{S}^{2-}( \mathrm{s})$ ಎಂದು ಬರೆಯಬಹುದು ಎಂದು ತಿಳಿದಿದ್ದೇವೆ. ಉತ್ಪತ್ತಿಯಾದ ಪ್ರಜಾತಿಗಳ ಮೇಲೆ ಆವೇಶಗಳ ಅಭಿವೃದ್ಧಿಯು ನಮಗೆ ಕ್ರಿಯೆಗಳನ್ನು (8.12 ರಿಂದ 8.14) ಕೆಳಗಿನ ರೀತಿಯಲ್ಲಿ ಪುನಃ ಬರೆಯಲು ಸೂಚಿಸುತ್ತದೆ:
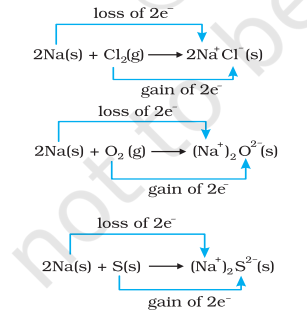
ಅನುಕೂಲಕ್ಕಾಗಿ, ಮೇಲಿನ ಪ್ರತಿಯೊಂದು ಪ್ರಕ್ರಿಯೆಗಳನ್ನು ಎರಡು ಪ್ರತ್ಯೇಕ ಹಂತಗಳಾಗಿ ಪರಿಗಣಿಸಬಹುದು, ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ನಷ್ಟವನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ ಮತ್ತು ಇನ್ನೊಂದು ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಲಾಭವನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ. ವಿವರಣೆಯಾಗಿ, ನಾವು ಇವುಗಳಲ್ಲಿ ಒಂದನ್ನು, ಅಂದರೆ, ಸೋಡಿಯಮ್ ಕ್ಲೋರೈಡ್ ರಚನೆಯನ್ನು ಮತ್ತಷ್ಟು ವಿವರಿಸಬಹುದು.
$2 \mathrm{Na}(\mathrm{s}) \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
$\mathrm{Cl_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{Cl}^{-}(\mathrm{g})$
ಮೇಲಿನ ಪ್ರತಿಯೊಂದು ಹಂತವನ್ನು ಅರ್ಧ ಕ್ರಿಯೆ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ, ಇದು ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಒಳಗೊಳ್ಳುವಿಕೆಯನ್ನು ಸ್ಪಷ್ಟವಾಗಿ ತೋರಿಸುತ್ತದೆ. ಅರ್ಧ ಕ್ರಿಯೆಗಳ ಮೊತ್ತವು ಒಟ್ಟಾರೆ ಕ್ರಿಯೆಯನ್ನು ನೀಡುತ್ತದೆ:
$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na}^{+} \mathrm{Cl}^{-}(\mathrm{s})$ ಅಥವಾ $2 \mathrm{NaCl}(\mathrm{s})$
ಕ್ರಿಯೆಗಳು 8.12 ರಿಂದ 8.14 ಸೂಚಿಸುವಂತೆ, ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ನಷ್ಟವನ್ನು ಒಳಗೊಂಡಿರುವ ಅರ್ಧ ಕ್ರಿಯೆಗಳನ್ನು ಆಕ್ಸಿಡೀಕರಣ ಕ್ರಿಯೆಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಅಂತೆಯೇ, ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಲಾಭವನ್ನು ಒಳಗೊಂಡಿರುವ ಅರ್ಧ ಕ್ರಿಯೆಗಳನ್ನು ರಿಡಕ್ಷನ್ ಕ್ರಿಯೆಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಶಾಸ್ತ್ರೀಯ ಕಲ್ಪನೆಯ ಪ್ರಕಾರ ಪ್ರಜಾತಿಗಳ ವರ್ತನೆ ಮತ್ತು ಎಲೆಕ್ಟ್ರಾನ್-ವರ್ಗಾವಣೆ ಬದಲಾವಣೆಯಲ್ಲಿ ಅವುಗಳ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ನಡುವೆ ಸಂಬಂಧವನ್ನು ಸ್ಥಾಪಿಸುವ ಮೂಲಕ ಮಾತ್ರ ಆಕ್ಸಿಡೀಕರಣ ಮತ್ತು ರಿಡಕ್ಷನ್ ಅನ್ನು ವ್ಯಾಖ್ಯಾನಿಸುವ ಹೊಸ ಮಾರ್ಗವನ್ನು ಸಾಧಿಸಲಾಗಿದೆ ಎಂದು ಇಲ್ಲಿ ಪ್ರಸ್ತಾಪಿಸುವುದು ಸಂದರ್ಭೋಚಿತವಾಗಿರಬಹುದು. ಕ್ರಿಯೆಗಳಲ್ಲಿ (8.12 ರಿಂದ 8.14) ಸೋಡಿಯಮ್, ಇದು ಆಕ್ಸಿಡೀಕರಣಗೊಂಡಿದೆ, ಅದು ಕಡಿಮೆ ಮಾಡುವ ಕಾರಕವಾಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸುತ್ತದೆ ಏಕೆಂದರೆ ಅದು ಅದರೊಂದಿಗೆ ಸಂವಹನ ನಡೆಸುವ ಪ್ರತಿಯೊಂದು ಮೂಲಧಾತುಗಳಿಗೆ ಎಲೆಕ್ಟ್ರಾನ್ ದಾನ ಮಾಡುತ್ತದೆ ಮತ್ತು ಆ ಮೂಲಕ ಅವುಗಳನ್ನು ಕಡಿಮೆ ಮಾಡಲು ಸಹಾಯ ಮಾಡುತ್ತದೆ. ಕ್ಲೋರಿನ್, ಆಮ್ಲಜನಕ ಮತ್ತು ಸಲ್ಫರ್ ರಿಡಕ್ಷನ್ ಆಗುತ್ತವೆ ಮತ್ತು ಆಕ್ಸಿಡೀಕಾರಕಗಳಾಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸುತ್ತವೆ ಏಕೆಂದರೆ ಇವು ಸೋಡಿಯಮ್ನಿಂದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಸ್ವೀಕರಿಸುತ್ತವೆ. ಸಂಕ್ಷಿಪ್ತವಾಗಿ ಹೇಳುವುದಾದರೆ, ನಾವು ಇದನ್ನು ಪ್ರಸ್ತಾಪಿಸಬಹುದು
ಆಕ್ಸಿಡೀಕರಣ: ಯಾವುದೇ ಪ್ರಜಾತಿಯಿಂದ ಎಲೆಕ್ಟ್ರಾನ್(ಗಳ) ನಷ್ಟ.
ರಿಡಕ್ಷನ್: ಯಾವುದೇ ಪ್ರಜಾತಿಯಿಂದ ಎಲೆಕ್ಟ್ರಾನ್(ಗಳ) ಲಾಭ.
ಆಕ್ಸಿಡೀಕಾರಕ: ಎಲೆಕ್ಟ್ರಾನ್(ಗಳ) ಸ್ವೀಕರ್ತ.
ಕಡಿಮೆ ಮಾಡುವ ಕಾರಕ: ಎಲೆಕ್ಟ್ರಾನ್(ಗಳ) ದಾತ.
ಸಮಸ್ಯೆ 8.2
ಕ್ರಿಯೆ: $2 \mathrm{Na}(\mathrm{s})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaH}$ (s) ಒಂದು ರೆಡಾಕ್ಸ್ ಬದಲಾವಣೆ ಎಂದು ಸಮರ್ಥಿಸಿ.
ಪರಿಹಾರ
ಮೇಲಿನ ಕ್ರಿಯೆಯಲ್ಲಿ ರೂಪುಗೊಂಡ ಸಂಯುಕ್ತವು ಅಯಾನಿಕ್ ಸಂಯುಕ್ತವಾಗಿರುವುದರಿಂದ, ಅದನ್ನು $\mathrm{Na}^{+} \mathrm{H}^{-}$(s) ಎಂದು ಸಹ ಪ್ರತಿನಿಧಿಸಬಹುದು, ಇದು ಈ ಪ್ರಕ್ರಿಯೆಯಲ್ಲಿ ಒಂದು ಅರ್ಧ ಕ್ರಿಯೆ ಎಂದು ಸೂಚಿಸುತ್ತದೆ:
$2 \mathrm{Na}(\mathrm{s}) \quad \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
ಮತ್ತು ಇನ್ನೊಂದು ಅರ್ಧ ಕ್ರಿಯೆ:
$\mathrm{H_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{H}^{-}(\mathrm{g})$
ಪರೀಕ್ಷೆಯಲ್ಲಿರುವ ಕ್ರಿಯೆಯನ್ನು ಎರಡು ಅರ್ಧ ಕ್ರಿಯೆಗಳಾಗಿ ವಿಭಜಿಸುವುದು ಸ್ವಯಂಚಾಲಿತವಾಗಿ ಇಲ್ಲಿ ಸೋಡಿಯಮ್ ಆಕ್ಸಿಡೀಕರಣಗೊಂಡಿದೆ ಮತ್ತು ಹೈಡ್ರೋಜನ್ ರಿಡಕ್ಷನ್ ಆಗಿದೆ ಎಂದು ಬಹಿರಂಗಪಡಿಸುತ್ತದೆ, ಆದ್ದರಿಂದ, ಸಂಪೂರ್ಣ ಕ್ರಿಯೆಯು ರೆಡಾಕ್ಸ್ ಬದಲಾವಣೆಯಾಗಿದೆ.
8.2.1 ಸ್ಪರ್ಧಾತ್ಮಕ ಎಲೆಕ್ಟ್ರಾನ್ ವರ್ಗಾವಣೆ ಕ್ರಿಯೆಗಳು
ತಾಮ್ರ ನೈಟ್ರೇಟ್ನ ಜಲೀಯ ದ್ರಾವಣದಲ್ಲಿ ಲೋಹೀಯ ಜಿಂಕ್ನ ಒಂದು ಪಟ್ಟಿಯನ್ನು ಚಿತ್ರ 8.1 ರಲ್ಲಿ ತೋರಿಸಿರುವಂತೆ ಸುಮಾರು ಒಂದು ಗಂಟೆ ಇರಿಸಿ. ಪಟ್ಟಿಯು ಕೆಂಪು ಬಣ್ಣದ ಲೋಹೀಯ ತಾಮ್ರದಿಂದ ಲೇಪಿತವಾಗಿದೆ ಮತ್ತು ದ್ರಾವಣದ ನೀಲಿ ಬಣ್ಣವು ಕಣ್ಮರೆಯಾಗುತ್ತದೆ ಎಂದು ನೀವು ಗಮನಿಸಬಹುದು. $\mathrm{Zn}^{2+}$ ಅಯಾನುಗಳ ರಚನೆಯನ್ನು ಉತ್ಪನ್ನಗಳಲ್ಲಿ ಸುಲಭವಾಗಿ ನಿರ್ಣಯಿಸಬಹುದು, ಏಕೆಂದರೆ $\mathrm{Cu}^{2+}$ ಕಾರಣದಿಂದಾಗಿ ದ್ರಾವಣದ ನೀಲಿ ಬಣ್ಣ ಕಣ್ಮರೆಯಾಗಿದೆ. ಹೈಡ್ರೋಜನ್ ಸಲ್ಫೈಡ್ ಅನಿಲವನ್ನು $\mathrm{Zn}^{2+}$ ಅಯಾನುಗಳನ್ನು ಹೊಂದಿರುವ ಬಣ್ಣರಹಿತ ದ್ರಾವಣದ ಮೂಲಕ ಹಾಯಿಸಿದರೆ, ದ್ರಾವಣವನ್ನು ಅಮೋನಿಯಾದಿಂದ ಕ್ಷಾರೀಯಗೊಳಿಸಿದಾಗ ಬಿಳಿ ಜಿಂಕ್ ಸಲ್ಫೈಡ್, $\mathrm{ZnS}$ ಕಾಣಿಸಿಕೊಳ್ಳುವುದನ್ನು ನೋಡಬಹುದು.
ಲೋಹೀಯ ಜಿಂಕ್ ಮತ್ತು ತಾಮ್ರ ನೈಟ್ರೇಟ್ನ ಜಲೀಯ ದ್ರಾವಣದ ನಡುವಿನ ಕ್ರಿಯೆ:
$$\mathrm{Zn}(\mathrm{s})+\mathrm{Cu}^{2+}(\mathrm{aq}) \rightarrow \mathrm{Zn}^{2+}(\mathrm{aq})+\mathrm{Cu}(\mathrm{s}) \tag{8.15}$$
ಕ್ರಿಯೆ (8.15) ರಲ್ಲಿ, ಜಿಂಕ್ $Zn^{2+}$ ರಚಿಸಲು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಕಳೆದುಕೊಂಡಿದೆ ಮತ್ತು ಆದ್ದರಿಂದ, ಜಿಂಕ್ ಆಕ್ಸಿಡೀಕರಣಗೊಂಡಿದೆ. ಸ್ಪಷ್ಟವಾಗಿ, ಈಗ ಜಿಂಕ್ ಆಕ್ಸಿಡೀಕರಣಗೊಂಡರೆ, ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಬಿಡುಗಡೆ ಮಾಡುತ್ತದೆ, ಏನಾದರೂ ಕಡಿಮೆಯಾಗಬೇಕು, ಜಿಂಕ್ ಕಳೆದುಕೊಂಡ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಸ್ವೀಕರಿಸಬೇಕು. ತಾಮ್ರ ಅಯಾನು ಜಿಂಕ್ನಿಂದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಪಡೆದು ರಿಡಕ್ಷನ್ ಆಗುತ್ತದೆ.
ಕ್ರಿಯೆ (8.15) ಅನ್ನು ಈ ರೀತಿ ಪುನಃ ಬರೆಯಬಹುದು:
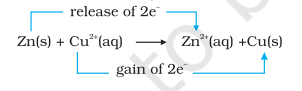
ಈ ಹಂತದಲ್ಲಿ ನಾವು ಸಮೀಕರಣ (8.15) ರಿಂದ ಪ್ರತಿನಿಧಿಸಲ್ಪಟ್ಟ ಕ್ರಿಯೆಗಾಗಿ ಸಮತೋಲನ ಸ್ಥಿತಿಯನ್ನು ತನಿಖೆ ಮಾಡಬಹುದು. ಈ ಉದ್ದೇಶಕ್ಕಾಗಿ, ಜಿಂಕ್ ಸಲ್ಫೇಟ್ ದ್ರಾವಣದಲ್ಲಿ ಲೋಹೀಯ ತಾಮ್ರದ ಒಂದು ಪಟ್ಟಿಯನ್ನು ಇರಿಸೋಣ. ಯಾವುದೇ ಗೋಚರ ಕ್ರಿಯೆ ಗಮನಿಸಲಾಗುವುದಿಲ್ಲ ಮತ್ತು $\mathrm{Cu}^{2+}$ ಅಯಾನುಗಳ ಉಪಸ್ಥಿತಿಯನ್ನು ಪತ್ತೆಹಚ್ಚಲು ಪ್ರಯತ್ನಿಸಿ $\mathrm{H_2} \mathrm{~S}$ ಅನಿಲವನ್ನು ದ್ರಾವಣದ ಮೂಲಕ ಹಾಯಿಸಿ ಕಪ್ರಿಕ್ ಸಲ್ಫೈಡ್, CuS ನ ಕಪ್ಪು ಬಣ್ಣವನ್ನು ಉತ್ಪತ್ತಿ ಮಾಡಲು ಯಶಸ್ವಿಯಾಗುವುದಿಲ್ಲ. ಕಪ್ರಿಕ್ ಸಲ್ಫೈಡ್ ಅಂತಹ ಕಡಿಮೆ ದ್ರಾವ್ಯತೆಯನ್ನು ಹೊಂದಿದೆ, ಇದು ಅತ್ಯಂತ ಸೂಕ್ಷ್ಮ ಪರೀಕ್ಷೆಯಾಗಿದೆ; ಆದರೂ ರೂಪುಗೊಂಡ $\mathrm{Cu}^{2+}$ ನ ಪ್ರಮಾಣವನ್ನು ಪತ್ತೆಹಚ್ಚಲಾಗುವುದಿಲ್ಲ. ಹೀಗಾಗಿ ನಾವು ಕ್ರಿಯೆ (8.15) ಗಾಗಿ ಸಮತೋಲನ ಸ್ಥಿತಿಯು ಕಾರಕಗಳಿಗಿಂತ ಉತ್ಪನ್ನಗಳನ್ನು ಹೆಚ್ಚು ಆದ್ಯತೆ ನೀಡುತ್ತದೆ ಎಂದು ತೀರ್ಮಾನಿಸುತ್ತೇವೆ.
ಈಗ ಎಲೆಕ್ಟ್ರಾನ್ ವರ್ಗಾವಣೆ ಕ್ರಿಯೆಯನ್ನು ತಾಮ್ರ ಲೋಹ ಮತ್ತು ನೀರಿನಲ್ಲಿ ಸಿಲ್ವರ್ ನೈಟ್ರೇಟ್ ದ್ರಾವಣಕ್ಕೆ ವಿಸ್ತರಿಸೋಣ ಮತ್ತು ಚಿತ್ರ 8.2 ರಲ್ಲಿ ತೋರಿಸಿರುವಂತೆ ಒಂದು ಸೆಟ್-ಅಪ್ ಅನ್ನು ಏರ್ಪಡಿಸೋಣ. ಕ್ರಿಯೆಯ ಕಾರಣದಿಂದಾಗಿ ದ್ರಾವಣವು $\mathrm{Cu}^{2+}$ ಅಯಾನುಗಳ ರಚನೆಯಿಂದಾಗಿ ನೀಲಿ ಬಣ್ಣವನ್ನು ಅಭಿವೃದ್ಧಿಪಡಿಸುತ್ತದೆ:
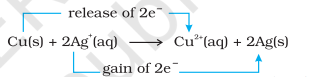
ಇಲ್ಲಿ, $\mathrm{Cu}(\mathrm{s})$ $\mathrm{Cu}^{2+}(\mathrm{aq})$ ಗೆ ಆಕ್ಸಿಡೀಕರಣಗೊಳ್ಳುತ್ತದೆ ಮತ್ತು $\mathrm{Ag}^{+}(\mathrm{aq})$ $\mathrm{Ag}(\mathrm{s})$ ಗೆ ರಿಡಕ್ಷನ್ ಆಗುತ್ತದೆ. ಸಮತೋಲನವು ಉತ್ಪನ್ನಗಳಾದ $\mathrm{Cu}^{2+}(\mathrm{aq})$ ಮತ್ತು $\mathrm{Ag}(\mathrm{s})$ ಗಳನ್ನು ಹೆಚ್ಚು ಆದ್ಯತೆ ನೀಡುತ್ತದೆ.
ವ್ಯತ್ಯಾಸದ ಮೂಲಕ, ನಿಕೆಲ್ ಸಲ್ಫೇಟ್ ದ್ರಾವಣದಲ್ಲಿ ಇರಿಸಲಾದ ಲೋಹೀಯ ಕೋಬಾಲ್ಟ್ನ ಕ್ರಿಯೆಯನ್ನು ಸಹ ಹೋಲಿಕೆ ಮಾಡೋಣ. ಇಲ್ಲಿ ಸಂಭವಿಸುವ ಕ್ರಿಯೆ:
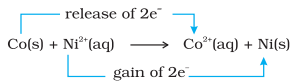
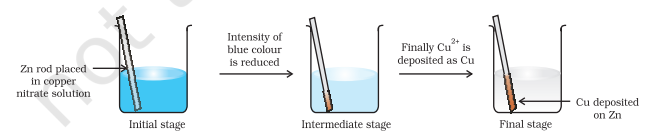
ಚಿತ್ರ 8.1 ಜಿಂಕ್ ಮತ್ತು ತಾಮ್ರ ನೈಟ್ರೇಟ್ನ ಜಲೀಯ ದ್ರಾವಣದ ನಡುವಿನ ರೆಡಾಕ್ಸ್ ಕ್ರಿಯೆಯು ಬೀಕರ್ನಲ್ಲಿ ಸಂಭವಿಸುತ್ತದೆ.
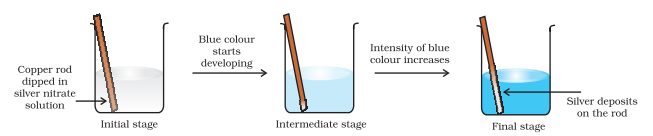
ಚಿತ್ರ 8.2 ತಾಮ್ರ ಮತ್ತು ಸಿಲ್ವರ್ ನೈಟ್ರೇಟ್ನ ಜಲೀಯ ದ್ರಾವಣದ ನಡುವಿನ ರೆಡಾಕ್ಸ್ ಕ್ರಿಯೆಯು ಬೀಕರ್ನಲ್ಲಿ ಸಂಭವಿಸುತ್ತದೆ
ಸಮತೋಲನದಲ್ಲಿ, ರಾಸಾಯನಿಕ ಪರೀಕ್ಷೆಗಳು $\mathrm{Ni}^{2+}(\mathrm{aq})$ ಮತ್ತು $\mathrm{Co}^{2+}(\mathrm{aq})$ ಎರಡೂ ಮಧ್ಯಮ ಸಾಂದ್ರತೆಯಲ್ಲಿ ಇರುತ್ತವೆ ಎಂದು ಬಹಿರಂಗಪಡಿಸುತ್ತವೆ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ಕಾರಕಗಳಾದ $\left[\mathrm{Co}(\mathrm{s})\right.$ ಮತ್ತು $\left.\mathrm{Ni}^{2+}(\mathrm{aq})\right]$ ಅಥವಾ ಉತ್ಪನ್ನಗಳಾದ $\left[\mathrm{Co}^{2+}(\mathrm{aq})\right.$ ಮತ್ತು $\left.\mathrm{Ni}(\mathrm{s})\right]$ ಗಳಲ್ಲಿ ಯಾವುದೂ ಹೆಚ್ಚು ಆದ್ಯತೆ ಪಡೆಯುವುದಿಲ್ಲ.
ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಬಿಡುಗಡೆಗಾಗಿ ಈ ಸ್ಪರ್ಧೆಯು ಆಕಸ್ಮಿಕವಾಗಿ ಆಮ್ಲಗಳ ನಡುವೆ ಪ್ರೋಟಾನ್ಗಳ ಬಿಡುಗಡೆಗಾಗಿ ಸ್ಪರ್ಧೆಯನ್ನು ನೆನಪಿಸುತ್ತದೆ. ಈ ಹೋಲಿಕೆಯು ನಾವು ಲೋಹಗಳು ಮತ್ತು ಅವುಗಳ ಅಯಾನುಗಳನ್ನು ಆಮ್ಲಗಳ ಬಲವನ್ನು ಸೂಚಿಸುವ ಸಂದರ್ಭದಲ್ಲಿ ನಾವು ಮಾಡುವಂತೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಬಿಡುಗಡೆ ಮಾಡುವ ಪ್ರವೃತ್ತಿಯ ಆಧಾರದ ಮೇಲೆ ಪಟ್ಟಿ ಮಾಡಲಾದ ಕೋಷ್ಟಕವನ್ನು ಅಭಿವೃದ್ಧಿಪಡಿಸಬಹುದು ಎಂದು ಸೂಚಿಸುತ್ತದೆ. ವಾಸ್ತವವಾಗಿ ನಾವು ಈಗಾಗಲೇ ಕೆಲವು ಹೋಲಿಕೆಗಳನ್ನು ಮಾಡಿದ್ದೇವೆ. ಹೋಲಿಕೆಯ ಮೂಲಕ ಜಿಂಕ್ ತಾಮ್ರಕ್ಕೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಬಿಡುಗಡೆ ಮಾಡುತ್ತದೆ ಮತ್ತು ತಾಮ್ರ ಬೆಳ್ಳಿಗೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಬಿಡುಗಡೆ ಮಾಡುತ್ತದೆ ಎಂದು ನಮಗೆ ತಿಳಿದಿದೆ ಮತ್ತು ಆದ್ದರಿಂದ, ಲೋಹಗಳ ಎಲೆಕ್ಟ್ರಾನ್ ಬಿಡುಗಡೆ ಪ್ರವೃತ್ತಿಯು ಕ್ರಮದಲ್ಲಿದೆ: $\mathrm{Zn}>\mathrm{Cu}>\mathrm{Ag}$. ನಮ್ಮ ಪಟ್ಟಿಯನ್ನು ಹೆಚ್ಚು ವಿಶಾಲಗೊಳಿಸಲು ಮತ್ತು ಲೋಹ ಚಟುವಟಿಕೆ ಶ್ರೇಣಿ ಅಥವಾ ವಿದ್ಯುತ್ ರಾಸಾಯನಿಕ ಶ್ರೇಣಿಯನ್ನು ವಿನ್ಯಾಸಗೊಳಿಸಲು ನಾವು ಇಷ್ಟಪಡುತ್ತೇವೆ. ವಿವಿಧ ಲೋಹಗಳ ನಡುವಿನ ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಗಾಗಿ ಸ್ಪರ್ಧೆಯು ಗ್ಯಾಲ್ವಾನಿಕ್ ಕೋಶಗಳು ಎಂಬ ಹೆಸರಿನ ಕೋಶಗಳ








