അദ്ധ്യായം 04 രാസബന്ധനവും തന്മാത്രാ ഘടനയും
“ശാസ്ത്രജ്ഞർ നിരന്തരം പുതിയ സംയുക്തങ്ങൾ കണ്ടെത്തുകയും, അവയെക്കുറിച്ചുള്ള വസ്തുതകൾ ക്രമപ്പെടുത്തി ക്രമീകരിക്കുകയും, നിലവിലുള്ള അറിവുകളുപയോഗിച്ച് വിശദീകരിക്കാൻ ശ്രമിക്കുകയും, മുമ്പത്തെ വീക്ഷണങ്ങൾ പരിഷ്കരിക്കുന്നതിനോ പുതുതായി നിരീക്ഷിക്കപ്പെട്ട വസ്തുതകൾ വിശദീകരിക്കുന്നതിനുള്ള സിദ്ധാന്തങ്ങൾ വികസിപ്പിക്കുന്നതിനോ ചട്ടക്കൂട് നൽകുകയും ചെയ്യുന്നു.”
ദ്രവ്യം ഒന്നോ വ്യത്യസ്ത തരം മൂലകങ്ങളോ കൊണ്ടാണ് നിർമ്മിച്ചിരിക്കുന്നത്. സാധാരണ സാഹചര്യങ്ങളിൽ, ഉദാത്ത വാതകങ്ങൾ ഒഴികെ മറ്റൊരു മൂലകവും പ്രകൃതിയിൽ സ്വതന്ത്ര ആറ്റമായി നിലനിൽക്കുന്നില്ല. എന്നിരുന്നാലും, ഒരു കൂട്ടം ആറ്റങ്ങൾ ഒരു സ്പീഷീസായി ഒന്നിച്ച് നിലനിൽക്കുന്നതായി കണ്ടെത്തിയിട്ടുണ്ട്, അവയ്ക്ക് സവിശേഷ ഗുണങ്ങളുണ്ട്. ഇത്തരം ആറ്റങ്ങളുടെ ഒരു കൂട്ടത്തെ തന്മാത്ര എന്ന് വിളിക്കുന്നു. തന്മാത്രകളിലെ ഈ ഘടക ആറ്റങ്ങളെ ഒരുമിച്ച് പിടിച്ചിരിക്കുന്ന ചില ശക്തികൾ ഉണ്ടായിരിക്കണം എന്നത് വ്യക്തമാണ്. വിവിധ രാസ സ്പീഷീസുകളിൽ വിവിധ ഘടകങ്ങളെ (ആറ്റങ്ങൾ, അയോണുകൾ മുതലായവ) ഒരുമിച്ച് പിടിക്കുന്ന ആകർഷക ശക്തിയെ രാസബന്ധനം എന്ന് വിളിക്കുന്നു. വിവിധ മൂലകങ്ങളുടെ ആറ്റങ്ങൾ വിവിധ രീതികളിൽ സംയോജിപ്പിക്കുന്നതിന്റെ ഫലമായി രാസ സംയുക്തങ്ങളുടെ രൂപീകരണം നടക്കുന്നതിനാൽ, ഇത് പല ചോദ്യങ്ങളും ഉയർത്തുന്നു. ആറ്റങ്ങൾ എന്തുകൊണ്ട് സംയോജിക്കുന്നു? ചില സംയോജനങ്ങൾ മാത്രമേ സാധ്യമാകൂ എന്തുകൊണ്ട്? ചില ആറ്റങ്ങൾ സംയോജിക്കുമ്പോൾ മറ്റുചിലത് എന്തുകൊണ്ട് സംയോജിക്കുന്നില്ല? തന്മാത്രകൾക്ക് നിശ്ചിത ആകൃതികൾ ഉണ്ടാകുന്നത് എന്തുകൊണ്ട്? അത്തരം ചോദ്യങ്ങൾക്ക് ഉത്തരം നൽകുന്നതിന് കാലാകാലങ്ങളിൽ വിവിധ സിദ്ധാന്തങ്ങളും ആശയങ്ങളും മുന്നോട്ട് വെച്ചിട്ടുണ്ട്. ഇവ കോസൽ-ലൂയിസ് സമീപനം, വാലൻസ് ഷെൽ ഇലക്ട്രോൺ പെയർ റിപ്പൽഷൻ (VSEPR) സിദ്ധാന്തം, വാലൻസ് ബോണ്ട് (VB) സിദ്ധാന്തം, മോളിക്യുലാർ ഓർബിറ്റൽ (MO) സിദ്ധാന്തം എന്നിവയാണ്. വാലൻസിന്റെ വിവിധ സിദ്ധാന്തങ്ങളുടെ പരിണാമവും രാസബന്ധനങ്ങളുടെ സ്വഭാവത്തിന്റെ വ്യാഖ്യാനവും ആറ്റത്തിന്റെ ഘടന, മൂലകങ്ങളുടെ ഇലക്ട്രോണിക് കോൺഫിഗറേഷൻ, പീരിയോഡിക് ടേബിൾ എന്നിവയെക്കുറിച്ചുള്ള ധാരണയിലെ വികസനങ്ങളുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു. ഓരോ സിസ്റ്റവും കൂടുതൽ സ്ഥിരതയുള്ളതായിരിക്കാൻ ശ്രമിക്കുന്നു, സ്ഥിരത നേടുന്നതിന് സിസ്റ്റത്തിന്റെ ഊർജ്ജം കുറയ്ക്കുന്നതിനുള്ള പ്രകൃതിയുടെ മാർഗമാണ് ബന്ധനം.
4.1 രാസബന്ധനത്തിലേക്കുള്ള കോസൽ-ലൂയിസ് സമീപനം
ഇലക്ട്രോണുകളുടെ അടിസ്ഥാനത്തിൽ രാസബന്ധനത്തിന്റെ രൂപീകരണം വിശദീകരിക്കുന്നതിന് നിരവധി ശ്രമങ്ങൾ നടത്തിയെങ്കിലും, 1916-ൽ മാത്രമാണ് കോസലും ലൂയിസും സ്വതന്ത്രമായി തൃപ്തികരമായ വിശദീകരണം നൽകുന്നതിൽ വിജയിച്ചത്. ഉദാത്ത വാതകങ്ങളുടെ നിഷ്ക്രിയത്വത്തെ അടിസ്ഥാനമാക്കിയുള്ള വാലൻസിനെക്കുറിച്ച് ആദ്യമായി ചില യുക്തിസഹമായ വിശദീകരണം നൽകിയത് അവരാണ്.
ലൂയിസ് ആറ്റത്തെ പോസിറ്റീവ് ചാർജ്ജ് ചെയ്ത ‘കെർണൽ’ (ന്യൂക്ലിയസും ആന്തരിക ഇലക്ട്രോണുകളും) ഉം പരമാവധി എട്ട് ഇലക്ട്രോണുകൾക്ക് സ്ഥാനം നൽകാൻ കഴിയുന്ന ബാഹ്യ ഷെല്ലും ഉള്ളതായി ചിത്രീകരിച്ചു. കൂടാതെ, ഈ എട്ട് ഇലക്ട്രോണുകൾ ‘കെർണൽ’ ചുറ്റുമുള്ള ഒരു ക്യൂബിന്റെ കോണുകൾ കൈവശപ്പെടുത്തുന്നുവെന്ന് അദ്ദേഹം അനുമാനിച്ചു. അങ്ങനെ സോഡിയത്തിന്റെ ഒറ്റ ബാഹ്യ ഷെൽ ഇലക്ട്രോൺ ക്യൂബിന്റെ ഒരു കോണിൽ കൈവശപ്പെടുത്തും, ഒരു ഉദാത്ത വാതകത്തിന്റെ കാര്യത്തിൽ എല്ലാ എട്ട് കോണുകളും കൈവശപ്പെടുത്തപ്പെടും. ഇലക്ട്രോണുകളുടെ ഈ ഒക്റ്ററ്റ്, പ്രത്യേകിച്ചും സ്ഥിരമായ ഇലക്ട്രോണിക് ക്രമീകരണത്തെ പ്രതിനിധീകരിക്കുന്നു. രാസബന്ധനങ്ങളാൽ ബന്ധിപ്പിക്കപ്പെടുമ്പോൾ ആറ്റങ്ങൾ സ്ഥിരമായ ഒക്റ്ററ്റ് നേടുന്നുവെന്ന് ലൂയിസ് അനുമാനിച്ചു. സോഡിയവും ക്ലോറിനും തമ്മിലുള്ള കാര്യത്തിൽ, സോഡിയത്തിൽ നിന്ന് ക്ലോറിനിലേക്ക് ഒരു ഇലക്ട്രോൺ കൈമാറ്റം ചെയ്യുന്നതിലൂടെ ഇത് സംഭവിക്കാം, അത് $\mathrm{Na}^+$, $\mathrm{Cl}^{-}$ അയോണുകൾ നൽകുന്നു. $ \mathrm{Cl}_2, \mathrm{H}_2, \mathrm{~F}_2 $ മുതലായവ പോലുള്ള മറ്റ് തന്മാത്രകളുടെ കാര്യത്തിൽ, ആറ്റങ്ങൾ തമ്മിലുള്ള ഒരു ജോടി ഇലക്ട്രോണുകൾ പങ്കിടുന്നതിലൂടെ ബന്ധനം രൂപം കൊള്ളുന്നു. ഈ പ്രക്രിയയിൽ ഓരോ ആറ്റവും ഇലക്ട്രോണുകളുടെ സ്ഥിരമായ ബാഹ്യ ഒക്റ്ററ്റ് നേടുന്നു.
ലൂയിസ് ചിഹ്നങ്ങൾ: ഒരു തന്മാത്രയുടെ രൂപീകരണത്തിൽ, ബാഹ്യ ഷെൽ ഇലക്ട്രോണുകൾ മാത്രമേ രാസ സംയോജനത്തിൽ പങ്കെടുക്കൂ, അവ വാലൻസ് ഇലക്ട്രോണുകൾ എന്നറിയപ്പെടുന്നു. ആന്തരിക ഷെൽ ഇലക്ട്രോണുകൾ നന്നായി സംരക്ഷിക്കപ്പെട്ടിരിക്കുന്നു, സാധാരണയായി സംയോജന പ്രക്രിയയിൽ ഉൾപ്പെടുന്നില്ല. ഒരു അമേരിക്കൻ രസതന്ത്രജ്ഞനായ ജി.എൻ. ലൂയിസ് ഒരു ആറ്റത്തിലെ വാലൻസ് ഇലക്ട്രോണുകളെ പ്രതിനിധീകരിക്കുന്നതിന് ലളിതമായ നൊട്ടേഷനുകൾ അവതരിപ്പിച്ചു. ഈ നൊട്ടേഷനുകളെ ലൂയിസ് ചിഹ്നങ്ങൾ എന്ന് വിളിക്കുന്നു. ഉദാഹരണത്തിന്, രണ്ടാം കാലയളവിലെ മൂലകങ്ങളുടെ ലൂയിസ് ചിഹ്നങ്ങൾ ഇനിപ്പറയുന്നവയാണ്:

ലൂയിസ് ചിഹ്നങ്ങളുടെ പ്രാധാന്യം: ചിഹ്നത്തിന് ചുറ്റുമുള്ള ഡോട്ടുകളുടെ എണ്ണം വാലൻസ് ഇലക്ട്രോണുകളുടെ എണ്ണത്തെ പ്രതിനിധീകരിക്കുന്നു. വാലൻസ് ഇലക്ട്രോണുകളുടെ ഈ എണ്ണം മൂലകത്തിന്റെ പൊതുവായ അല്ലെങ്കിൽ ഗ്രൂപ്പ് വാലൻസ് കണക്കാക്കാൻ സഹായിക്കുന്നു. മൂലകങ്ങളുടെ ഗ്രൂപ്പ് വാലൻസ് സാധാരണയായി ലൂയിസ് ചിഹ്നങ്ങളിലെ ഡോട്ടുകളുടെ എണ്ണത്തിന് തുല്യമാണ് അല്ലെങ്കിൽ 8 മൈനസ് ഡോട്ടുകളുടെ അല്ലെങ്കിൽ വാലൻസ് ഇലക്ട്രോണുകളുടെ എണ്ണം.
രാസബന്ധനവുമായി ബന്ധപ്പെട്ട് കോസൽ ഇനിപ്പറയുന്ന വസ്തുതകളിലേക്ക് ശ്രദ്ധ ആകർഷിച്ചു:
- പീരിയോഡിക് ടേബിളിൽ, അത്യധികം ഇലക്ട്രോനെഗറ്റീവ് ഹാലൊജനുകളും അത്യധികം ഇലക്ട്രോപോസിറ്റീവ് ആൽക്കലി ലോഹങ്ങളും ഉദാത്ത വാതകങ്ങളാൽ വേർതിരിക്കപ്പെട്ടിരിക്കുന്നു;
- ഒരു ഹാലൊജൻ ആറ്റത്തിൽ നിന്ന് ഒരു നെഗറ്റീവ് അയോണും ഒരു ആൽക്കലി ലോഹ ആറ്റത്തിൽ നിന്ന് ഒരു പോസിറ്റീവ് അയോണും രൂപീകരിക്കുന്നത് യഥാക്രമം ആറ്റങ്ങൾ ഒരു ഇലക്ട്രോൺ നേടുന്നതും നഷ്ടപ്പെടുന്നതുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു;
- ഇങ്ങനെ രൂപം കൊള്ളുന്ന നെഗറ്റീവ്, പോസിറ്റീവ് അയോണുകൾ സ്ഥിരമായ ഉദാത്ത വാതക ഇലക്ട്രോണിക് കോൺഫിഗറേഷനുകൾ നേടുന്നു. ഉദാത്ത വാതകങ്ങൾക്ക് (ഹീലിയം ഒഴികെ, അതിന് ഇലക്ട്രോണുകളുടെ ഒരു ഡ്യുപ്ലറ്റ് ഉണ്ട്) പ്രത്യേകിച്ചും സ്ഥിരമായ എട്ട് (ഒക്റ്ററ്റ്) ഇലക്ട്രോണുകളുടെ ബാഹ്യ ഷെൽ കോൺഫിഗറേഷൻ ഉണ്ട്, $n s^{2} n p^{6}$.
- നെഗറ്റീവ്, പോസിറ്റീവ് അയോണുകൾ ഇലക്ട്രോസ്റ്റാറ്റിക് ആകർഷണത്താൽ സ്ഥിരതയുള്ളവയാണ്.
ഉദാഹരണത്തിന്, മുകളിലെ സ്കീമിന് അനുസൃതമായി സോഡിയവും ക്ലോറിനും തമ്മിൽ $\mathrm{NaCl}$ രൂപീകരണം ഇനിപ്പറയുന്ന രീതിയിൽ വിശദീകരിക്കാം:
| $\mathrm{Na}$ | $\rightarrow$ | $\mathrm{Na}^{+}+\mathrm{e}^{-}$ |
| $[\mathrm{Ne}] 3 \mathrm{~s}^{1}$ | $[\mathrm{Ne}]$ | |
| $\mathrm{Cl}+\mathrm{e}^{-}$ | $\rightarrow$ | $\mathrm{Cl}^{-}$ |
| $[\mathrm{Ne}] 3 s^{2} 3 p^{5}$ | $[\mathrm{Ne}] 3 s^{2} 3 p^{6}$ or $[\mathrm{Ar}]$ | |
| $\mathrm{Na}^{+}+\mathrm{Cl}^{-}$ | $\rightarrow$ | $\mathrm{NaCl}$ or $\mathrm{Na}^{+} \mathrm{Cl}^{-}$ |
അതുപോലെ $\mathrm{CaF}_{2}$ രൂപീകരണം ഇനിപ്പറയുന്ന രീതിയിൽ കാണിക്കാം:
| $\mathrm{Ca}$ | $\rightarrow$ | $\mathrm{Ca}^{2+}+2 \mathrm{e}^{-}$ |
| $[\mathrm{Ar}] 4 s^{2}$ | $[\mathrm{Ar}]$ | |
| $\mathrm{F}+\mathrm{e}^{-}$ | $\rightarrow$ | $\mathrm{F}^{-}$ |
| $[\mathrm{He}] 2 s^{2} 2 p^{5}$ | $[\mathrm{He}] 2 s^{2} 2 p^{6}$ or $[\mathrm{Ne}]$ | |
| $\mathrm{Ca}^{2+}+2 \mathrm{~F}^{-}$ | $\rightarrow$ | $\mathrm{CaF}_2$ or $\mathrm{Ca}^{2+}\left(\mathrm{F}^{-}\right)_2$ |
പോസിറ്റീവ്, നെഗറ്റീവ് അയോണുകൾ തമ്മിലുള്ള ഇലക്ട്രോസ്റ്റാറ്റിക് ആകർഷണത്തിന്റെ ഫലമായി രൂപം കൊള്ളുന്ന ബന്ധനം ഇലക്ട്രോവാലന്റ് ബോണ്ട് എന്ന് വിളിക്കപ്പെട്ടു. അങ്ങനെ ഇലക്ട്രോവാലൻസ് അയോണിലെ യൂണിറ്റ് ചാർജ്(കൾ)യുടെ എണ്ണത്തിന് തുല്യമാണ്. അങ്ങനെ, കാൽസ്യത്തിന് രണ്ട് പോസിറ്റീവ് ഇലക്ട്രോവാലൻസ് നൽകിയിരിക്കുന്നു, അതേസമയം ക്ലോറിന് ഒരു നെഗറ്റീവ് ഇലക്ട്രോവാലൻസ് നൽകിയിരിക്കുന്നു.
ഇലക്ട്രോൺ കൈമാറ്റത്തിലൂടെ അയോൺ-രൂപീകരണത്തെക്കുറിച്ചുള്ള ആധുനിക ആശയങ്ങൾക്കും അയോണിക് സ്ഫടിക സംയുക്തങ്ങളുടെ രൂപീകരണത്തിനും കോസലിന്റെ അനുമാനങ്ങൾ അടിസ്ഥാനം നൽകുന്നു. അയോണിക് സംയുക്തങ്ങളെ മനസ്സിലാക്കുന്നതിലും വ്യവസ്ഥാപിതമാക്കുന്നതിലും അദ്ദേഹത്തിന്റെ വീക്ഷണങ്ങൾ വലിയ മൂല്യമുള്ളതായി തെളിയിക്കപ്പെട്ടിട്ടുണ്ട്. അതേ സമയം ഈ ആശയങ്ങളിൽ ഒരു വലിയ എണ്ണം സംയുക്തങ്ങൾ യോജിക്കുന്നില്ല എന്ന വസ്തുതയെ അദ്ദേഹം തിരിച്ചറിഞ്ഞു.
4.1.1 ഒക്റ്ററ്റ് നിയമം
1916-ൽ കോസലും ലൂയിസും ഇലക്ട്രോണിക് രാസബന്ധന സിദ്ധാന്തം എന്നറിയപ്പെടുന്ന ആറ്റങ്ങൾ തമ്മിലുള്ള രാസ സംയോജനത്തിന്റെ ഒരു പ്രധാന സിദ്ധാന്തം വികസിപ്പിച്ചു. ഇതിനനുസരിച്ച്, ആറ്റങ്ങൾക്ക് ഒരു ആറ്റത്തിൽ നിന്ന് മറ്റൊന്നിലേക്ക് വാലൻസ് ഇലക്ട്രോണുകൾ കൈമാറ്റം ചെയ്യുന്നതിലൂടെ (നേടുകയോ നഷ്ടപ്പെടുകയോ ചെയ്യുന്നതിലൂടെ) അല്ലെങ്കിൽ അവയുടെ വാലൻസ് ഷെല്ലുകളിൽ ഒരു ഒക്റ്ററ്റ് ലഭിക്കുന്നതിന് വാലൻസ് ഇലക്ട്രോണുകൾ പങ്കിടുന്നതിലൂടെ സംയോജിക്കാൻ കഴിയും. ഇതിനെ ഒക്റ്ററ്റ് നിയമം എന്ന് വിളിക്കുന്നു.
4.1.2 കോവാലന്റ് ബോണ്ട്
ലാങ്മുയർ (1919) ഒക്റ്ററ്റിന്റെ സ്ഥിരമായ ക്യൂബിക്കൽ ക്രമീകരണത്തിന്റെ ആശയം ഉപേക്ഷിച്ച് കോവാലന്റ് ബോണ്ട് എന്ന പദം അവതരിപ്പിച്ചുകൊണ്ട് ലൂയിസിന്റെ അനുമാനങ്ങൾ ശുദ്ധീകരിച്ചു. ക്ലോറിൻ തന്മാത്രയുടെ രൂപീകരണം, $\mathrm{Cl}_2$ പരിഗണിച്ചുകൊണ്ട് ലൂയിസ്-ലാങ്മുയർ സിദ്ധാന്തം മനസ്സിലാക്കാം. ഇലക്ട്രോണിക് കോൺഫിഗറേഷൻ $[\mathrm{Ne}] 3 s^2 3 p^5$ ഉള്ള $\mathrm{Cl}$ ആറ്റം, ആർഗോൺ കോൺഫിഗറേഷനിൽ നിന്ന് ഒരു ഇലക്ട്രോൺ കുറവാണ്. $\mathrm{Cl}_2$ തന്മാത്രയുടെ രൂപീകരണം രണ്ട് ക്ലോറിൻ ആറ്റങ്ങൾ തമ്മിലുള്ള ഒരു ജോടി ഇലക്ട്രോണുകൾ പങ്കിടുന്നതിന്റെ അടിസ്ഥാനത്തിൽ മനസ്സിലാക്കാം, ഓരോ ക്ലോറിൻ ആറ്റവും പങ്കിട്ട ജോടിയിലേക്ക് ഒരു ഇലക്ട്രോൺ സംഭാവന ചെയ്യുന്നു. ഈ പ്രക്രിയയിൽ രണ്ട് ക്ലോറിൻ ആറ്റങ്ങളും ഏറ്റവും അടുത്തുള്ള ഉദാത്ത വാതകത്തിന്റെ (അതായത്, ആർഗോൺ) ബാഹ്യ ഷെൽ ഒക്റ്ററ്റ് നേടുന്നു.

രണ്ട് Cl ആറ്റങ്ങൾ തമ്മിലുള്ള കോവാലന്റ് ബോണ്ട്
ഡോട്ടുകൾ ഇലക്ട്രോണുകളെ പ്രതിനിധീകരിക്കുന്നു. അത്തരം ഘടനകളെ ലൂയിസ് ഡോട്ട് ഘടനകൾ എന്ന് വിളിക്കുന്നു.
മറ്റ് തന്മാത്രകൾക്കും ലൂയിസ് ഡോട്ട് ഘടനകൾ എഴുതാം, അതിൽ സംയോജിക്കുന്ന ആറ്റങ്ങൾ സമാനമോ വ്യത്യസ്തമോ ആകാം. പ്രധാന വ്യവസ്ഥകൾ ഇവയാണ്:
- ഓരോ ബന്ധനവും ആറ്റങ്ങൾ തമ്മിൽ ഒരു ഇലക്ട്രോൺ ജോടി പങ്കിടുന്നതിന്റെ ഫലമായി രൂപം കൊള്ളുന്നു.
- സംയോജിക്കുന്ന ഓരോ ആറ്റവും പങ്കിട്ട ജോടിയിലേക്ക് കുറഞ്ഞത് ഒരു ഇലക്ട്രോൺ സംഭാവന ചെയ്യുന്നു.
- ഇലക്ട്രോണുകൾ പങ്കിടുന്നതിന്റെ ഫലമായി സംയോജിക്കുന്ന ആറ്റങ്ങൾ ബാഹ്യഷെൽ ഉദാത്ത വാതക കോൺഫിഗറേഷനുകൾ നേടുന്നു.
- അങ്ങനെ ജലത്തിലും കാർബൺ ടെട്രാക്ലോറൈഡ് തന്മാത്രകളിലും, കോവാലന്റ് ബോണ്ടുകളുടെ രൂപീകരണം ഇനിപ്പറയുന്ന രീതിയിൽ പ്രതിനിധീകരിക്കാം:

അങ്ങനെ, രണ്ട് ആറ്റങ്ങൾ ഒരു ഇലക്ട്രോൺ ജോടി പങ്കിടുമ്പോൾ അവ ഒരു ഒറ്റ കോവാലന്റ് ബോണ്ട് വഴി ചേർന്നിരിക്കുന്നു എന്ന് പറയപ്പെടുന്നു. നിരവധി സംയുക്തങ്ങളിൽ ആറ്റങ്ങൾ തമ്മിൽ ഒന്നിലധികം ബന്ധനങ്ങൾ ഉണ്ട്. ഒന്നിലധികം ബന്ധനങ്ങളുടെ രൂപീകരണം രണ്ട് ആറ്റങ്ങൾ തമ്മിൽ ഒന്നിൽ കൂടുതൽ ഇലക്ട്രോൺ ജോടികൾ പങ്കിടുന്നതിനെ സൂചിപ്പിക്കുന്നു. രണ്ട് ആറ്റങ്ങൾ രണ്ട് ജോടി ഇലക്ട്രോണുകൾ പങ്കിടുകയാണെങ്കിൽ, അവ തമ്മിലുള്ള കോവാലന്റ് ബോണ്ടിനെ ഡബിൾ ബോണ്ട് എന്ന് വിളിക്കുന്നു. ഉദാഹരണത്തിന്, കാർബൺ ഡൈ ഓക്സൈഡ് തന്മാത്രയിൽ, കാർബണും ഓക്സിജൻ ആറ്റങ്ങളും തമ്മിൽ രണ്ട് ഡബിൾ ബോണ്ടുകൾ ഉണ്ട്. അതുപോലെ ഈഥീൻ തന്മാത്രയിൽ രണ്ട് കാർബൺ ആറ്റങ്ങൾ ഒരു ഡബിൾ ബോണ്ട് വഴി ചേർന്നിരിക്കുന്നു..

$\mathrm{C} _{2} \mathrm{H} _{4}$ തന്മാത്ര
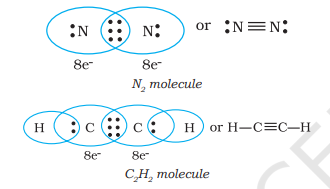
സംയോജിക്കുന്ന ആറ്റങ്ങൾ $N_{2}$ തന്മാത്രയിലെ രണ്ട് നൈട്രജൻ ആറ്റങ്ങളുടെ കാര്യത്തിലും ഈഥൈൻ തന്മാത്രയിലെ രണ്ട് കാർബൺ ആറ്റങ്ങളുടെ കാര്യത്തിലും മൂന്ന് ഇലക്ട്രോൺ ജോടികൾ പങ്കിടുമ്പോൾ, ഒരു ട്രിപ്പിൾ ബോണ്ട് രൂപം കൊള്ളുന്നു.
4.1.3 ലളിതമായ തന്മാത്രകളുടെ ലൂയിസ് പ്രതിനിധാനം (ലൂയിസ് ഘടനകൾ)
ലൂയിസ് ഡോട്ട് ഘടനകൾ പങ്കിട്ട ഇലക്ട്രോൺ ജോടികളുടെയും ഒക്റ്ററ്റ് നിയമത്തിന്റെയും അടിസ്ഥാനത്തിൽ തന്മാത്രകളിലെയും അയോണുകളിലെയും ബന്ധനത്തിന്റെ ഒരു ചിത്രം നൽകുന്നു. അത്തരമൊരു ചിത്രം ഒരു തന്മാത്രയുടെ ബന്ധനവും സ്വഭാവവും പൂർണ്ണമായി വിശദീകരിക്കില്ലെങ്കിലും, ഒരു തന്മാത്രയുടെ രൂപീകരണവും ഗുണങ്ങളും വലിയ അളവിൽ മനസ്സിലാക്കാൻ ഇത് സഹായിക്കുന്നു. അതിനാൽ, തന്മാത്രകളുടെ ലൂയിസ് ഡോട്ട് ഘടനകൾ എഴുതുന്നത് വളരെ ഉപയോഗപ്രദമാണ്. ഇനിപ്പറയുന്ന ഘട്ടങ്ങൾ സ്വീകരിച്ചുകൊണ്ട് ലൂയിസ് ഡോട്ട് ഘടനകൾ എഴുതാം:
- സംയോജിക്കുന്ന ആറ്റങ്ങളുടെ വാലൻസ് ഇലക്ട്രോണുകൾ ചേർത്തുകൊണ്ട് ഘടനകൾ എഴുതുന്നതിന് ആവശ്യമായ ആകെ ഇലക്ട്രോണുകൾ ലഭിക്കും. ഉദാഹരണത്തിന്, $\mathrm{CH}_{4}$ തന്മാത്രയിൽ ബന്ധനത്തിനായി എട്ട് വാലൻസ് ഇലക്ട്രോണുകൾ ലഭ്യമാണ് (കാർബണിൽ നിന്ന് 4, നാല് ഹൈഡ്രജൻ ആറ്റങ്ങളിൽ നിന്ന് 4).
- നെഗറ്റീവ് അയോണുകൾക്ക്, ഓരോ നെഗറ്റീവ് ചാർജും ഒരു ഇലക്ട്രോൺ ചേർക്കുന്നതിനെ അർത്ഥമാക്കുന്നു. പോസിറ്റീവ് അയോണുകൾക്ക്, ഓ








