അദ്ധ്യായം 08 റെഡോക്സ് പ്രവർത്തനങ്ങൾ
“ഓക്സീകരണം ഉള്ളിടത്ത്, എല്ലായിടത്തും റിഡക്ഷൻ ഉണ്ട്. രസതന്ത്രം അടിസ്ഥാനപരമായി റെഡോക്സ് സംവിധാനങ്ങളുടെ ഒരു പഠനമാണ്.”
രസതന്ത്രം വിവിധതരം ദ്രവ്യങ്ങളെയും ഒരു തരം ദ്രവ്യം മറ്റൊന്നായി മാറുന്ന പ്രക്രിയയെയും കൈകാര്യം ചെയ്യുന്നു. ഒരു തരം ദ്രവ്യം മറ്റൊന്നായി മാറുന്നത് വിവിധതരം പ്രവർത്തനങ്ങളിലൂടെയാണ്. അത്തരം പ്രവർത്തനങ്ങളിലെ ഒരു പ്രധാന വിഭാഗമാണ് റെഡോക്സ് പ്രവർത്തനങ്ങൾ. ഭൗതികവും ജൈവികവുമായ നിരവധി പ്രതിഭാസങ്ങൾ റെഡോക്സ് പ്രവർത്തനങ്ങളുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു. ഫാർമസ്യൂട്ടിക്കൽ, ജൈവിക, വ്യാവസായിക, ലോഹവിജ്ഞാനീയ, കാർഷിക മേഖലകളിൽ ഈ പ്രവർത്തനങ്ങൾ വ്യാപകമായി ഉപയോഗിക്കപ്പെടുന്നു. ഗാർഹിക, ഗതാഗത, മറ്റ് വാണിജ്യ ആവശ്യങ്ങൾക്കായി ഊർജ്ജം ലഭിക്കുന്നതിന് വിവിധതരം ഇന്ധനങ്ങളുടെ ജ്വലനം, ഉയർന്ന പ്രതിപ്രവർത്തനക്ഷമതയുള്ള ലോഹങ്ങളും അലോഹങ്ങളും വേർതിരിച്ചെടുക്കുന്നതിനുള്ള വൈദ്യുതരാസ പ്രക്രിയകൾ, കോസ്റ്റിക് സോഡ പോലുള്ള രാസസംയുക്തങ്ങളുടെ നിർമ്മാണം, ഉണങ്ങിയതും നനഞ്ഞതുമായ ബാറ്ററികളുടെ പ്രവർത്തനം, ലോഹങ്ങളുടെ തുരുമ്പെടുക്കൽ എന്നിവ റെഡോക്സ് പ്രക്രിയകളുടെ പരിധിയിൽ വരുന്നു എന്ന വസ്തുതയിൽ നിന്ന് ഈ പ്രവർത്തനങ്ങളുടെ പ്രാധാന്യം വ്യക്തമാണ്. ഈയിടെ, ഹൈഡ്രജൻ ഇക്കോണമി (ദ്രവ ഹൈഡ്രജൻ ഇന്ധനമായി ഉപയോഗിക്കൽ), ‘ഓസോൺ ദ്വാരം’ എന്നിവയുടെ വികസനം പോലുള്ള പാരിസ്ഥിതിക പ്രശ്നങ്ങൾ റെഡോക്സ് പ്രതിഭാസത്തിന് കീഴിൽ ഉൾപ്പെടാൻ തുടങ്ങിയിട്ടുണ്ട്.
8.1 റെഡോക്സ് പ്രവർത്തനങ്ങളുടെ ശാസ്ത്രീയ ആശയം - ഓക്സീകരണവും റിഡക്ഷൻ പ്രവർത്തനങ്ങളും
തുടക്കത്തിൽ, ഒരു മൂലകത്തിലോ സംയുക്തത്തിലോ ഓക്സിജൻ ചേർക്കുന്നതിനെ വിവരിക്കാൻ ഓക്സീകരണം എന്ന പദം ഉപയോഗിച്ചിരുന്നു. അന്തരീക്ഷത്തിൽ ഡൈഓക്സിജന്റെ സാന്നിധ്യം (20%) കാരണം, പല മൂലകങ്ങളും അതുമായി ചേരുന്നു, അവ സാധാരണയായി ഭൂമിയിൽ അവയുടെ ഓക്സൈഡുകളുടെ രൂപത്തിൽ കാണപ്പെടുന്നതിന് ഇതാണ് പ്രധാന കാരണം. ഓക്സീകരണത്തിന്റെ പരിമിതമായ നിർവചനം അനുസരിച്ച് ഇനിപ്പറയുന്ന പ്രവർത്തനങ്ങൾ ഓക്സീകരണ പ്രക്രിയകളെ പ്രതിനിധീകരിക്കുന്നു:
$$2 \mathrm{Mg}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{MgO}(\mathrm{s}) \tag{8.1}$$
$$\mathrm{S}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow \mathrm{SO_2}(\mathrm{~g}) \tag{8.2}$$
(8.1), (8.2) എന്നീ പ്രവർത്തനങ്ങളിൽ, മഗ്നീഷ്യം, സൾഫർ എന്നീ മൂലകങ്ങൾക്ക് ഓക്സിജൻ ചേർക്കപ്പെടുന്നതിനാൽ ഓക്സീകരിക്കപ്പെടുന്നു. അതുപോലെ, മീഥേനിലേക്ക് ഓക്സിജൻ ചേർക്കപ്പെടുന്നതിനാൽ അത് ഓക്സീകരിക്കപ്പെടുന്നു.
$$\mathrm{CH} _{4}(\mathrm{~g})+2 \mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g})+2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{7.3}$$
ഹൈഡ്രജനെ ഓക്സിജൻ ഉപയോഗിച്ച് മാറ്റിസ്ഥാപിച്ച (8.3) എന്ന പ്രവർത്തനം ശ്രദ്ധാപൂർവ്വം പരിശോധിച്ചതിന് ശേഷം, രസതന്ത്രജ്ഞർ അതിൽ നിന്ന് ഹൈഡ്രജൻ നീക്കം ചെയ്യുന്നതിന്റെ അടിസ്ഥാനത്തിൽ ഓക്സീകരണത്തെ വീണ്ടും വ്യാഖ്യാനിക്കാൻ പ്രേരിപ്പിച്ചു, അതിനാൽ, ഓക്സീകരണം എന്ന പദത്തിന്റെ വ്യാപ്തി ഒരു പദാർത്ഥത്തിൽ നിന്ന് ഹൈഡ്രജൻ നീക്കം ചെയ്യുന്നത് ഉൾപ്പെടുത്താൻ വികസിപ്പിച്ചെടുത്തു. ഹൈഡ്രജൻ നീക്കം ചെയ്യുന്നതിനെ ഒരു ഓക്സീകരണ പ്രവർത്തനമായി ഉദ്ധരിക്കാവുന്ന മറ്റൊരു പ്രവർത്തനമാണ് ഇനിപ്പറയുന്ന ഉദാഹരണം.
$$ \begin{equation*} 2 \mathrm{H_2} \mathrm{~S}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{~S}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \tag{8.4} \end{equation*} $$
രസതന്ത്രജ്ഞരുടെ അറിവ് വർദ്ധിച്ചതിനാൽ, ഓക്സിജൻ ഉൾപ്പെടാത്തതും മറ്റ് വിദ്യുത്ഋണ മൂലകങ്ങൾ ഉൾപ്പെടുന്നതുമായ (7.1 മുതൽ 7.4 വരെ) പോലുള്ള പ്രവർത്തനങ്ങൾക്കായി ഓക്സീകരണം എന്ന പദം വിപുലീകരിക്കുന്നത് സ്വാഭാവികമായിരുന്നു. ഫ്ലൂറിൻ, ക്ലോറിൻ, സൾഫർ എന്നിവയുമായി മഗ്നീഷ്യത്തിന്റെ ഓക്സീകരണം ഇനിപ്പറയുന്ന പ്രവർത്തനങ്ങൾക്ക് അനുസൃതമായി സംഭവിക്കുന്നു:
$$\operatorname{Mg}(\mathrm{s})+\mathrm{F_2} (\mathrm{~g}) \rightarrow \operatorname{MgF_2} (s) \tag{8.5}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{Cl_2} (g) \rightarrow \mathrm{MgCl_2} (s) \tag{8.6}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{S} (s) \rightarrow \operatorname{MgS}(\mathrm{s}) \tag{8.7}$$
(7.5 മുതൽ 7.7 വരെ) എന്നീ പ്രവർത്തനങ്ങൾ ഓക്സീകരണ പ്രവർത്തനങ്ങളുടെ വലയത്തിൽ ഉൾപ്പെടുത്തിയത്, ഹൈഡ്രജൻ നീക്കം ചെയ്യുന്നത് മാത്രമല്ല, വിദ്യുത്ധന മൂലകങ്ങൾ നീക്കം ചെയ്യുന്നതും ഓക്സീകരണമായി കണക്കാക്കാൻ രസതന്ത്രജ്ഞരെ പ്രോത്സാഹിപ്പിച്ചു. അങ്ങനെ പ്രവർത്തനം:
$$ 2 \mathrm{~K_4} \left[ \mathrm{Fe} ( \mathrm{CN})_{6} \right] ( \mathrm{aq}) + \mathrm{H_2} \mathrm{O_2} ( \mathrm{aq}) \rightarrow 2 \mathrm{~K_3} \left[\mathrm{Fe}( \mathrm{CN})_6 \right] ( \mathrm{aq}) + 2 \mathrm{KOH} ( \mathrm{aq}) $$
പൊട്ടാസ്യം ഫെറോസയനൈഡ് പൊട്ടാസ്യം ഫെറിസയനൈഡായി മാറുന്നതിന് മുമ്പ്, വിദ്യുത്ധന മൂലകമായ പൊട്ടാസ്യം നീക്കം ചെയ്യുന്നതിനാലുള്ള ഓക്സീകരണമായി വ്യാഖ്യാനിക്കപ്പെടുന്നു. സംഗ്രഹിക്കാം, ഒരു പദാർത്ഥത്തിലേക്ക് ഓക്സിജൻ/വിദ്യുത്ഋണ മൂലകം ചേർക്കുന്നതോ ഒരു പദാർത്ഥത്തിൽ നിന്ന് ഹൈഡ്രജൻ/വിദ്യുത്ധന മൂലകം നീക്കം ചെയ്യുന്നതോ ആണ് “ഓക്സീകരണം” എന്ന് നിർവചിക്കപ്പെടുന്നത്.
തുടക്കത്തിൽ, ഒരു സംയുക്തത്തിൽ നിന്ന് ഓക്സിജൻ നീക്കം ചെയ്യുന്നതായാണ് റിഡക്ഷൻ കണക്കാക്കപ്പെട്ടിരുന്നത്. എന്നിരുന്നാലും, ഈ ദിവസങ്ങളിൽ ഒരു പദാർത്ഥത്തിൽ നിന്ന് ഓക്സിജൻ/വിദ്യുത്ഋണ മൂലകം നീക്കം ചെയ്യുന്നതോ ഒരു പദാർത്ഥത്തിലേക്ക് ഹൈഡ്രജൻ/വിദ്യുത്ധന മൂലകം ചേർക്കുന്നതോ ഉൾപ്പെടുത്താൻ റിഡക്ഷൻ എന്ന പദം വികസിപ്പിച്ചെടുത്തിട്ടുണ്ട്.
മുകളിൽ നൽകിയ നിർവചനം അനുസരിച്ച്, റിഡക്ഷൻ പ്രക്രിയകളുടെ ഉദാഹരണങ്ങൾ ഇനിപ്പറയുന്നവയാണ്:
$$2 \mathrm{HgO}(\mathrm{s}) \xrightarrow{\Delta} 2 \mathrm{Hg}(\mathrm{l})+\mathrm{O_2}(\mathrm{~g}) \tag{8.8}$$
(മെർക്കുറിക് ഓക്സൈഡിൽ നിന്ന് ഓക്സിജൻ നീക്കം ചെയ്യൽ)
$$2 \mathrm{FeCl_3}(\mathrm{aq})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{FeCl_2}(\mathrm{aq})+2 \mathrm{HCl}(\mathrm{aq}) \tag{8.9}$$
(വിദ്യുത്ഋണ മൂലകമായ ക്ലോറിൻ ഫെറിക് ക്ലോറൈഡിൽ നിന്ന് നീക്കം ചെയ്യൽ)
$$\mathrm{CH_2}=\mathrm{CH_2}(\mathrm{~g})+\mathrm{H_2}(\mathrm{~g}) \rightarrow \mathrm{H_3} \mathrm{C}-\mathrm{CH_3}(\mathrm{~g})\tag{8.10}$$
(ഹൈഡ്രജൻ ചേർക്കൽ)
$$2 \mathrm{HgCl_2}(\mathrm{aq})+\mathrm{SnCl_2}(\mathrm{aq}) \rightarrow \mathrm{Hg_2} \mathrm{Cl_2}(\mathrm{~s})+\mathrm{SnCl_4}(\mathrm{aq})\tag{8.11}$$
(മെർക്കുറിക് ക്ലോറൈഡിലേക്ക് മെർക്കുറി ചേർക്കൽ)
(8.11) എന്ന പ്രവർത്തനത്തിൽ, സ്റ്റാനസ് ക്ലോറൈഡിന്റെ ഒരേസമയം ഓക്സീകരണം സ്റ്റാനിക് ക്ലോറൈഡായി മാറുന്നതും സംഭവിക്കുന്നു, കാരണം അതിലേക്ക് വിദ്യുത്ഋണ മൂലകമായ ക്ലോറിൻ ചേർക്കപ്പെടുന്നു. ഓക്സീകരണവും റിഡക്ഷനും എല്ലായ്പ്പോഴും ഒരേസമയം സംഭവിക്കുന്നുവെന്ന് (മുകളിൽ നൽകിയിരിക്കുന്ന എല്ലാ സമവാക്യങ്ങളും വീണ്ടും പരിശോധിച്ചാൽ വ്യക്തമാകും) ഉടൻ തന്നെ മനസ്സിലായി, അതിനാൽ, ഈ രാസപ്രവർത്തന വിഭാഗത്തിനായി “റെഡോക്സ്” എന്ന വാക്ക് നാണയമാക്കി.
പ്രശ്നം 8.1
ചുവടെ നൽകിയിരിക്കുന്ന പ്രവർത്തനങ്ങളിൽ, ഓക്സീകരണവും റിഡക്ഷനും അനുഭവിക്കുന്ന സ്പീഷീസ് തിരിച്ചറിയുക:
(i) $\mathrm{H_2} \mathrm{~S}$ (g) $+\mathrm{Cl_2}$ (g) $\rightarrow 2 \mathrm{HCl}$ (g) $+\mathrm{S}$ (s)
(ii) $3 \mathrm{Fe_3} \mathrm{O_4}$ (s) $+8 \mathrm{Al}$ (s) $\rightarrow 9 \mathrm{Fe}$ (s) $+4 \mathrm{Al_2} \mathrm{O_3}(\mathrm{~s})$
(iii) $2 \mathrm{Na}$ (s) $+\mathrm{H_2}$ (g) $\rightarrow 2 \mathrm{NaH}$ (s)
പരിഹാരം
(i) $\mathrm{H_2} \mathrm{~S}$ ഓക്സീകരിക്കപ്പെടുന്നു, കാരണം കൂടുതൽ വിദ്യുത്ഋണ മൂലകമായ ക്ലോറിൻ ഹൈഡ്രജനിലേക്ക് ചേർക്കപ്പെടുന്നു (അല്ലെങ്കിൽ കൂടുതൽ വിദ്യുത്ധന മൂലകമായ ഹൈഡ്രജൻ S-ൽ നിന്ന് നീക്കം ചെയ്യപ്പെട്ടിരിക്കുന്നു). അതിലേക്ക് ഹൈഡ്രജൻ ചേർക്കപ്പെടുന്നതിനാൽ ക്ലോറിൻ റിഡ്യൂസ് ചെയ്യപ്പെടുന്നു.
(ii) അലുമിനിയം ഓക്സീകരിക്കപ്പെടുന്നു, കാരണം അതിലേക്ക് ഓക്സിജൻ ചേർക്കപ്പെടുന്നു. ഫെറസ് ഫെറിക് ഓക്സൈഡ് ⟦91⟎ റിഡ്യൂസ് ചെയ്യപ്പെടുന്നു, കാരണം അതിൽ നിന്ന് ഓക്സിജൻ നീക്കം ചെയ്യപ്പെട്ടിരിക്കുന്നു.
(iii) വിദ്യുത്ഋണതയുടെ ആശയം ശ്രദ്ധാപൂർവ്വം പ്രയോഗിച്ചുകൊണ്ട് മാത്രം സോഡിയം ഓക്സീകരിക്കപ്പെടുകയും ഹൈഡ്രജൻ റിഡ്യൂസ് ചെയ്യപ്പെടുകയും ചെയ്യുന്നുവെന്ന് നമുക്ക് അനുമാനിക്കാം.
ഇവിടെ തിരഞ്ഞെടുത്ത പ്രവർത്തനം (iii) റെഡോക്സ് പ്രവർത്തനങ്ങളെ നിർവചിക്കാനുള്ള മറ്റൊരു വഴിയെക്കുറിച്ച് ചിന്തിക്കാൻ നമ്മെ പ്രേരിപ്പിക്കുന്നു.
8.2 ഇലക്ട്രോൺ കൈമാറ്റ പ്രവർത്തനങ്ങളുടെ അടിസ്ഥാനത്തിൽ റെഡോക്സ് പ്രവർത്തനങ്ങൾ
ഈ പ്രവർത്തനങ്ങളിൽ ഓരോന്നിലും സോഡിയത്തിലേക്ക് ഓക്സിജൻ അല്ലെങ്കിൽ കൂടുതൽ വിദ്യുത്ഋണ മൂലകം ചേർക്കപ്പെടുന്നതിനാൽ സോഡിയം ഓക്സീകരിക്കപ്പെടുന്നു എന്നതിനാൽ ഈ പ്രവർത്തനങ്ങൾ റെഡോക്സ് പ്രവർത്തനങ്ങളാണെന്ന് നമ്മൾ ഇതിനകം പഠിച്ചിട്ടുണ്ട്.
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaCl}(\mathrm{s})\tag{8.12}$$
$$4 \mathrm{Na}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na_2} \mathrm{O}(\mathrm{s})\tag{8.13}$$
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{S}(\mathrm{s}) \rightarrow \mathrm{Na_2} \mathrm{~S}(\mathrm{~s}) \tag{8.14}$$
ഒരേസമയം, ക്ലോറിൻ, ഓക്സിജൻ, സൾഫർ എന്നിവ റിഡ്യൂസ് ചെയ്യപ്പെടുന്നു, കാരണം ഇവയിൽ ഓരോന്നിനും വിദ്യുത്ധന മൂലകമായ സോഡിയം ചേർക്കപ്പെട്ടിരിക്കുന്നു. രാസബന്ധനത്തെക്കുറിച്ചുള്ള നമ്മുടെ അറിവിൽ നിന്ന് സോഡിയം ക്ലോറൈഡ്, സോഡിയം ഓക്സൈഡ്, സോഡിയം സൾഫൈഡ് എന്നിവ അയോണിക സംയുക്തങ്ങളാണെന്നും ഒരുപക്ഷേ $\mathrm{Na}^{+} \mathrm{Cl}^{-}( \mathrm{s}),\left(\mathrm{Na}^{+} \right)_2 \mathrm{O}^{2-}( \mathrm{s})$, $ \left(\mathrm{Na}^{+} \right)_2$ $\mathrm{S}^{2-}( \mathrm{s})$ എന്നിങ്ങനെ എഴുതുന്നതാണ് നല്ലതെന്നും നമുക്കറിയാം. ഉൽപാദിപ്പിക്കപ്പെടുന്ന സ്പീഷീസുകളിൽ ചാർജുകളുടെ വികസനം ഇനിപ്പറയുന്ന രീതിയിൽ പ്രവർത്തനങ്ങൾ (8.12 മുതൽ 8.14 വരെ) വീണ്ടും എഴുതാൻ നമ്മെ പ്രേരിപ്പിക്കുന്നു:
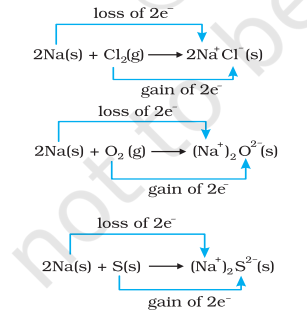
സൗകര്യത്തിനായി, മുകളിലെ ഓരോ പ്രക്രിയയെയും രണ്ട് പ്രത്യേക ഘട്ടങ്ങളായി കണക്കാക്കാം, ഒന്ന് ഇലക്ട്രോണുകളുടെ നഷ്ടം ഉൾപ്പെടുന്നതും മറ്റൊന്ന് ഇലക്ട്രോണുകളുടെ ലാഭം ഉൾപ്പെടുന്നതും. ഒരു ഉദാഹരണമായി, ഇവയിലൊന്ന്, അതായത് സോഡിയം ക്ലോറൈഡിന്റെ രൂപീകരണം, നമുക്ക് കൂടുതൽ വിശദീകരിക്കാം.
$2 \mathrm{Na}(\mathrm{s}) \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
$\mathrm{Cl_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{Cl}^{-}(\mathrm{g})$
മുകളിലെ ഓരോ ഘട്ടത്തെയും ഒരു ഹാഫ് റിയാക്ഷൻ എന്ന് വിളിക്കുന്നു, ഇത് ഇലക്ട്രോണുകളുടെ പങ്കാളിത്തം വ്യക്തമായി കാണിക്കുന്നു. ഹാഫ് റിയാക്ഷനുകളുടെ ആകെത്തുക മൊത്തം പ്രവർത്തനം നൽകുന്നു:
$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na}^{+} \mathrm{Cl}^{-}(\mathrm{s})$ അല്ലെങ്കിൽ $2 \mathrm{NaCl}(\mathrm{s})$
പ്രവർത്തനങ്ങൾ 8.12 മുതൽ 8.14 വരെ, ഇലക്ട്രോണുകളുടെ നഷ്ടം ഉൾപ്പെടുന്ന ഹാഫ് റിയാക്ഷനുകളെ ഓക്സീകരണ പ്രവർത്തനങ്ങൾ എന്ന് വിളിക്കുന്നുവെന്ന് സൂചിപ്പിക്കുന്നു. അതുപോലെ, ഇലക്ട്രോണുകളുടെ ലാഭം ഉൾപ്പെടുന്ന ഹാഫ് റിയാക്ഷനുകളെ റിഡക്ഷൻ പ്രവർത്തനങ്ങൾ എന്ന് വിളിക്കുന്നു. ശാസ്ത്രീയ ആശയം അനുസരിച്ച് സ്പീഷീസുകളുടെ സ്വഭാവവും ഇലക്ട്രോൺ കൈമാറ്റ മാറ്റത്തിലെ അവയുടെ പരസ്പരപ്രവർത്തനവും തമ്മിലുള്ള ബന്ധം സ്ഥാപിച്ചുകൊണ്ട് മാത്രമാണ് ഓക്സീകരണത്തെയും റിഡക്ഷനെയും നിർവചിക്കാനുള്ള പുതിയ മാർഗ്ഗം കൈവരിച്ചതെന്ന് ഇവിടെ പരാമർശിക്കുന്നത് സന്ദർഭോചിതമായിരിക്കില്ല. (8.12 മുതൽ 8.14 വരെ) പ്രവർത്തനങ്ങളിൽ, ഓക്സീകരിക്കപ്പെടുന്ന സോഡിയം, ഒരു റിഡ്യൂസിംഗ് ഏജന്റായി പ്രവർത്തിക്കുന്നു, കാരണം അത് അതുമായി പ്രതിപ്രവർത്തിക്കുന്ന ഓരോ മൂലകത്തിനും ഇലക്ട്രോൺ നൽകുന്നു, അതുവഴി അവയെ റിഡ്യൂസ് ചെയ്യാൻ സഹായിക്കുന്നു. ക്ലോറിൻ, ഓക്സിജൻ, സൾഫർ എന്നിവ റിഡ്യൂസ് ചെയ്യപ്പെടുകയും ഓക്സിഡൈസിംഗ് ഏജന്റുകളായി പ്രവർത്തിക്കുകയും ചെയ്യുന്നു, കാരണം ഇവ സോഡിയത്തിൽ നിന്ന് ഇലക്ട്രോണുകൾ സ്വീകരിക്കുന്നു. സംഗ്രഹിക്കാം, നമുക്ക് പരാമർശിക്കാം:
ഓക്സീകരണം: ഏതെങ്കിലും സ്പീഷീസ് ഇലക്ട്രോൺ(കൾ) നഷ്ടപ്പെടുത്തുന്നു.
റിഡക്ഷൻ: ഏതെങ്കിലും സ്പീഷീസ് ഇലക്ട്രോൺ(കൾ) നേടുന്നു.
ഓക്സിഡൈസിംഗ് ഏജന്റ്: ഇലക്ട്രോൺ(കൾ) സ്വീകരിക്കുന്നവൻ.
റിഡ്യൂസിംഗ് ഏജന്റ്: ഇലക്ട്രോൺ(കൾ) നൽകുന്നവൻ.
പ്രശ്നം 8.2
പ്രവർത്തനം: $2 \mathrm{Na}(\mathrm{s})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaH}$ (s) ഒരു റെഡോക്സ് മാറ്റമാണെന്ന് ന്യായീകരിക്കുക.
പരിഹാരം
മുകളിലെ പ്രവർത്തനത്തിൽ രൂപംകൊണ്ട സംയുക്തം ഒരു അയോണിക സംയുക്തമായതിനാൽ, അത് $\mathrm{Na}^{+} \mathrm{H}^{-}$(s) എന്നും പ്രതിനിധീകരിക്കാം, ഇത് ഈ പ്രക്രിയയിലെ ഒരു ഹാഫ് റിയാക്ഷൻ ഇതാണെന്ന് സൂചിപ്പിക്കുന്നു:
$2 \mathrm{Na}(\mathrm{s}) \quad \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
മറ്റേ ഹാഫ് റിയാക്ഷൻ ഇതാണ്:
$\mathrm{H_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{H}^{-}(\mathrm{g})$
പരിശോധനയിലുള്ള പ്രവർത്തനത്തെ രണ്ട് ഹാഫ് റിയാക്ഷനുകളായി വിഭജിക്കുന്നത് ഇവിടെ സോഡിയം ഓക്സീകരിക്കപ്പെടുകയും ഹൈഡ്രജൻ റിഡ്യൂസ് ചെയ്യപ്പെടുകയും ചെയ്യുന്നുവെന്ന് സ്വയമേവ വെളിപ്പെടുത്തുന്നു, അതിനാൽ, പൂർണ്ണമായ പ്രവർത്തനം ഒരു റെഡോക്സ് മാറ്റമാണ്.
8.2.1 മത്സരാധിഷ്ഠിത ഇലക്ട്രോൺ കൈമാറ്റ പ്രവർത്തനങ്ങൾ
ചിത്രം 8.1-ൽ കാണിച്ചിരിക്കുന്നതുപോലെ, ഒരു മണിക്കൂറോളം ചെമ്പ് നൈട്രേറ്റിന്റെ ജലീയ ലായനിയിൽ ലോഹ സിങ്കിന്റെ ഒരു സ്ട്രിപ്പ് വയ്ക്കുക. സ്ട്രിപ്പ് ചുവപ്പുനിറമുള്ള ലോഹ ചെമ്പ് കൊണ്ട് പൂശപ്പെടുകയും ലായനിയുടെ നീല നിറം അപ്രത്യക്ഷമാവുകയും ചെയ്യുന്നതായി നിങ്ങൾക്ക് ശ്രദ്ധിക്കാം. $\mathrm{Zn}^{2+}$ അയോണുകളുടെ രൂപീകരണം ഉൽപ്പന്നങ്ങളിൽ എളുപ്പത്തിൽ വിധിക്കാനാകും, കാരണം $\mathrm{Cu}^{2+}$ കാരണം ലായനിയുടെ നീല നിറം അപ്രത്യക്ഷമാകുമ്പോൾ. $\mathrm{Zn}^{2+}$ അയോണുകൾ അടങ്ങിയ നിറമില്ലാത്ത ലായനിയിലൂടെ ഹൈഡ്രജൻ സൾഫൈഡ് വാതകം കടത്തിവിട്ടാൽ, വെളുത്ത സിങ്ക് സൾഫൈഡ്, $\mathrm{ZnS}$ ലായനിയെ അമോണിയ ഉപയോഗിച്ച് ആൽക്കലൈൻ ആക്കുമ്പോൾ കാണാം.
ലോഹ സിങ്കും ചെമ്പ് നൈട്രേറ്റിന്റെ ജലീയ ലായനിയും തമ്മിലുള്ള പ്രവർത്തനം ഇതാണ്:
$$\mathrm{Zn}(\mathrm{s})+\mathrm{Cu}^{2+}(\mathrm{aq}) \rightarrow \mathrm{Zn}^{2+}(\mathrm{aq})+\mathrm{Cu}(\mathrm{s}) \tag{8.15}$$
(8.15) എന്ന പ്രവർത്തനത്തിൽ, സിങ്ക് $Zn^{2+}$ രൂപീകരിക്കാൻ ഇലക്ട്രോണുകൾ നഷ്ടപ്പെടുത്തിയിട്ടുണ്ട്, അതിനാൽ, സിങ്ക് ഓക്സീകരിക്കപ്പെടുന്നു. വ്യക്തമായും, ഇപ്പോൾ സിങ്ക് ഓക്സീകരിക്കപ്പെട്ടാൽ, ഇലക്ട്രോണുകൾ പുറത്തുവിടുന്നു, എന്തെങ്കിലും റിഡ്യൂസ് ചെയ്യപ്പെടണം, സിങ്ക് നഷ്ടപ്പെടുത്തിയ ഇലക്ട്രോണുകൾ സ്വീകരിക്കുന്നു. സിങ്കിൽ നിന്ന് ഇലക്ട്രോണുകൾ നേടിക്കൊണ്ട് ചെമ്പ് അയോൺ റിഡ്യൂസ് ചെയ്യപ്പെടുന്നു.
പ്രവർത്തനം (8.15) ഇങ്ങനെ വീണ്ടും എഴുതാം:
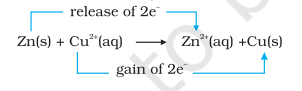
ഈ ഘട്ടത്തിൽ സമവാക്യം (8.15) പ്രതിനിധീകരിക്കുന്ന പ്രവർത്തനത്തിനായി സന്തുലിതാവസ്ഥ നമുക്ക് അന്വേഷിക്കാം. ഈ ആവശ്യത്തിനായി, സിങ്ക് സൾഫേറ്റ് ലായനിയിൽ ലോഹ ചെമ്പിന്റെ ഒരു സ്ട്രിപ്പ് വയ്ക്കാം. ദൃശ്യമായ ഒരു പ്രവർത്തനവും ശ്രദ്ധിക്കപ്പെടുന്നില്ല, കൂടാതെ $\mathrm{Cu}^{2+}$ അയോണുകളുടെ സാന്നിധ്യം കണ്ടെത്താൻ ശ്രമിക്കുന്നത് $\mathrm{H_2} \mathrm{~S}$ വാതകം ലായനിയിലൂടെ കടത്തിവിട്ട് കുപ്രിക് സൾഫൈഡ്, CuS ന്റെ കറുത്ത നിറം ഉത്പാദിപ്പിക്കുന്നതിലൂടെയാണ്, അത് വിജയിക്കുന്നില്ല. കുപ്രിക് സൾഫൈഡിന് വളരെ കുറഞ്ഞ ദ്രാവകതയുണ്ട്, ഇത് ഒരു അത്യന്തം സെൻസിറ്റീവ് ടെസ്റ്റാണ്; എന്നിട്ടും $\mathrm{Cu}^{2+}$ രൂപംകൊണ്ട തുക കണ്ടെത്താൻ കഴിയില്ല. അതിനാൽ, പ്രവർത്തനത്തിനായുള്ള സന്തുലിതാവസ്ഥ (8.15) ഉൽപ്പന്നങ്ങളെ പ്രതിപ്രവർത്തകങ്ങളേക്കാൾ വളരെയധികം പ്രാധാന്യമർഹിക്കുന്നുവെന്ന് നമ്മൾ നിഗമനം ചെയ്യുന്നു.
ഇപ്പോൾ ഇലക്ട്രോൺ കൈമാറ്റ പ്രവർത്തനം ജലത്തിലെ ചെമ്പ് ലോഹവും സിൽവർ നൈട്രേറ്റ് ലായനിയും വരെ വിപുലീകരിക്കുകയും ചിത്രം 8.2-ൽ കാണിച്ചിരിക്കുന്ന








