प्रकरण 03 घटकांचे वर्गीकरण आणि गुणधर्मांमधील कालावधी
“आवर्त सारणी ही तत्त्व आणि व्यवहार या दोन्ही दृष्टीने रसायनशास्त्रातील सर्वात महत्त्वाची संकल्पना आहे असे म्हटले तर ते अतिशयोक्त ठरणार नाही. विद्यार्थ्यांसाठी ती दैनंदिन आधार आहे, व्यावसायिकांसाठी नवीन संशोधनाचे मार्ग सुचवते आणि संपूर्ण रसायनशास्त्राचे सारगर्भित संघटन प्रदान करते. रासायनिक घटक हे घटकांचा यादृच्छिक समूह नसून ते कल दर्शवतात आणि कुटुंबांमध्ये एकत्र असतात या तथ्याचे हे एक उल्लेखनीय प्रात्यक्षिक आहे. आवर्त सारणीची जाणीव असणे हे जगाचा कोडे उलगडून पाहणार्या आणि रसायनशास्त्राच्या मूलभूत बिल्डिंग ब्लॉक्स, म्हणजेच रासायनिक घटकांपासून ते कसे बनलेले आहे हे पाहणाऱ्या प्रत्येकासाठी आवश्यक आहे.”
ग्लेन टी. सीबॉर्ग
या युनिटमध्ये, आजच्या स्वरूपातील आवर्त सारणीचा ऐतिहासिक विकास आणि आधुनिक आवर्त नियम आपण अभ्यासणार आहोत. अणूंच्या इलेक्ट्रॉनिक संरूपणाचे तार्किक परिणाम म्हणून आवर्त वर्गीकरण कसे होते हे देखील आपण शिकू. शेवटी, आपण घटकांच्या भौतिक आणि रासायनिक गुणधर्मांमधील काही आवर्त कलांचे परीक्षण करू.
३.१ घटकांचे वर्गीकरण का आवश्यक आहे?
आतापर्यंत आपल्याला माहित आहे की घटक हे सर्व प्रकारच्या द्रव्याचे मूलभूत एकक आहेत. १८०० मध्ये, फक्त ३१ घटक ज्ञात होते. १८६५ पर्यंत, ओळखलेल्या घटकांची संख्या दुप्पट होऊन ६३ झाली होती. सध्या ११४ घटक ज्ञात आहेत. त्यापैकी, अलीकडे शोधलेले घटक मानवनिर्मित आहेत. नवीन घटक संश्लेषित करण्याचे प्रयत्न सुरू आहेत. इतक्या मोठ्या संख्येने घटक असल्याने, या सर्व घटकांचे आणि त्यांच्या असंख्य संयुगे यांचे स्वतंत्रपणे रसायनशास्त्र वैयक्तिकरित्या अभ्यासणे खूप कठीण आहे. ही समस्या सोडवण्यासाठी, वैज्ञानिकांनी घटकांचे वर्गीकरण करून त्यांच्या ज्ञानाचे पद्धतशीरीकरण करण्याचा मार्ग शोधला. यामुळे केवळ घटकांबद्दलची ज्ञात रासायनिक तथ्ये तर्कसंगत होतील असे नाही, तर पुढील अभ्यासासाठी नवीन तथ्यांचाही अंदाज लावता येईल.
३.२ आवर्त वर्गीकरणाची उत्पत्ती
घटकांचे गटांमध्ये वर्गीकरण आणि आवर्त नियम आणि आवर्त सारणीचा विकास हे अनेक वैज्ञानिकांच्या निरीक्षणे आणि प्रयोगांद्वारे मिळालेल्या ज्ञानाचे पद्धतशीरीकरण करण्याचे परिणाम आहेत. जर्मन रसायनशास्त्रज्ञ जोहान डोबेरायनर यांनी १८०० च्या सुरुवातीला घटकांच्या गुणधर्मांमधील कलांची कल्पना विचारात घेण्यास सुरुवात केली. १८२९ पर्यंत त्यांनी अनेक त्रिक (ट्रायड) घटकांच्या भौतिक आणि रासायनिक गुणधर्मांमध्ये साम्य लक्षात घेतले. प्रत्येक बाबतीत, त्यांनी पाहिले की प्रत्येक त्रिकातील मधल्या घटकाचे अणुवजन इतर दोन घटकांच्या अणुवजनाच्या अंदाजे मध्यभागी असते (सारणी ३.१). तसेच मधल्या घटकाचे गुणधर्म इतर दोन सदस्यांच्या गुणधर्मांच्या दरम्यान असतात.
सारणी ३.१ डोबेरायनरचे त्रिक
| घटक | अणु वजन | घटक | अणु वजन | घटक | अणु वजन |
|---|---|---|---|---|---|
| $\mathbf{L i}$ | 7 | $\mathbf{C a}$ | 40 | $\mathbf{C l}$ | 35.5 |
| $\mathbf{N a}$ | 23 | $\mathbf{S r}$ | 88 | $\mathbf{B r}$ | 80 |
| $\mathbf{K}$ | 39 | $\mathbf{B a}$ | 137 | $\mathbf{I}$ | 127 |
डोबेरायनरचा संबंध, ज्याला त्रिकांचा नियम म्हणून संबोधले जाते, तो फक्त काही घटकांसाठीच कार्य करत असल्याचे दिसून आल्यामुळे, त्याला योगायोग म्हणून दुर्लक्षित करण्यात आले. घटकांचे वर्गीकरण करण्याचा पुढील प्रयत्न १८६२ मध्ये फ्रेंच भूवैज्ञानिक ए.ई.बी. डी शँकूर्त्वा यांनी केला. त्यांनी त्या वेळी ज्ञात असलेल्या घटकांची अणुवजनाच्या चढत्या क्रमाने मांडणी केली आणि गुणधर्मांची आवर्ती पुनरावृत्ती दर्शवण्यासाठी घटकांची एक दंडगोलाकार सारणी बनवली. यालाही फारसे लक्ष मिळाले नाही. इंग्रज रसायनशास्त्रज्ञ जॉन अलेक्झांडर न्यूलँड्स यांनी १८६५ मध्ये अष्टकांचा नियम मांडला. त्यांनी घटकांची अणुवजनाच्या चढत्या क्रमाने मांडणी केली आणि लक्षात घेतले की प्रत्येक आठव्या घटकाचे गुणधर्म पहिल्या घटकासारखेच असतात (सारणी ३.२). हा संबंध संगीतातील अष्टकांमधील प्रत्येक आठव्या स्वरासारखा होता जो पहिल्या स्वरासारखा असतो. न्यूलँड्सचा अष्टकांचा नियम केवळ कॅल्शियमपर्यंतच्या घटकांसाठी खरा वाटत होता. त्यावेळी त्यांची कल्पना व्यापकपणे स्वीकारली गेली नसली तरी, त्यांच्या कार्याबद्दल त्यांना नंतर १८८७ मध्ये रॉयल सोसायटी, लंडन यांनी डेव्ही पदक देऊन सन्मानित केले.
आज आपल्याला माहित असलेला आवर्त नियम त्याच्या विकासासाठी रशियन रसायनशास्त्रज्ञ दिमित्री मेंडेलीव्ह (१८३४-१९०७) आणि जर्मन रसायनशास्त्रज्ञ लोथार मेयर (१८३०-१९९५) यांचे ऋणी आहे.
स्वतंत्रपणे कार्य करत, दोन्ही रसायनशास्त्रज्ञांनी १८६९ मध्ये असे प्रस्तावित केले की घटकांची अणुवजनाच्या चढत्या क्रमाने मांडणी केल्यास, नियमित अंतराने भौतिक आणि रासायनिक गुणधर्मांमध्ये साम्य दिसून येते. लोथार मेयर यांनी अणु आकारमान, द्रवणांक आणि उत्कलनांक यांसारखे भौतिक गुणधर्म अणुवजनाच्या विरुद्ध आलेखित केले आणि आवर्ती पुनरावृत्ती होणारा नमुना मिळवला. न्यूलँड्सच्या विपरीत, लोथार मेयर यांनी त्या पुनरावृत्ती होणाऱ्या नमुन्याच्या लांबीत बदल पाहिला. १८६८ पर्यंत, लोथार मेयर यांनी घटकांची एक सारणी विकसित केली होती जी आधुनिक आवर्त सारणीशी जवळून साधर्म्य दर्शवते. तथापि, दिमित्री मेंडेलीव्ह यांचे कार्य प्रकाशित झाल्यानंतरच त्यांचे कार्य प्रकाशित झाले, ज्यांना सामान्यतः आधुनिक आवर्त सारणीच्या विकासाचे श्रेय दिले जाते.
सारणी ३.२ न्यूलँड्सचे अष्टक
| घटक | $\mathbf{L i}$ | $\mathbf{B e}$ | $\mathbf{B}$ | $\mathbf{C}$ | $\mathbf{N}$ | $\mathbf{O}$ | $\mathbf{F}$ |
|---|---|---|---|---|---|---|---|
| अणु. वज. | 7 | 9 | 11 | 12 | 14 | 16 | 19 |
| घटक | $\mathbf{N a}$ | $\mathbf{M g}$ | $\mathbf{A l}$ | $\mathbf{S i}$ | $\mathbf{P}$ | $\mathbf{S}$ | $\mathbf{C l}$ |
| अणु. वज. | 23 | 24 | 27 | 29 | 31 | 32 | 35.5 |
| घटक | $\mathbf{K}$ | $\mathbf{C a}$ | |||||
| अणु. वज. | 39 | 40 |
डोबेरायनर यांनी आवर्त संबंधांच्या अभ्यासाला सुरुवात केली तर मेंडेलीव्ह हेच प्रथमच आवर्त नियम प्रकाशित करण्यासाठी जबाबदार होते. तो खालीलप्रमाणे सांगतो:
घटकांचे गुणधर्म हे त्यांच्या अणुवजनाचे आवर्ती फलन आहेत.
मेंडेलीव्ह यांनी घटकांची अणुवजनाच्या चढत्या क्रमाने सारणीच्या आडव्या ओळी आणि उभ्या स्तंभांमध्ये अशा प्रकारे मांडणी केली की समान गुणधर्म असलेले घटक समान उभ्या स्तंभात किंवा गटात असतात. मेंडेलीव्हची घटकांचे वर्गीकरण करण्याची पद्धत लोथार मेयरच्या पद्धतीपेक्षा अधिक सविस्तर होती. त्यांनी आवर्ततेचे महत्त्व पूर्णपणे ओळखले आणि घटकांचे वर्गीकरण करण्यासाठी भौतिक आणि रासायनिक गुणधर्मांची विस्तृत श्रेणी वापरली. विशेषतः, मेंडेलीव्ह यांनी घटकांद्वारे तयार होणाऱ्या संयुगांच्या अनुभवजन्य सूत्रे आणि गुणधर्मांमधील साम्यांवर अवलंबून राहिले. अणुवजनाचा क्रम काटेकोरपणे पाळला गेला तर काही घटक त्यांच्या वर्गीकरणाच्या योजनेत बसत नाहीत हे त्यांना समजले. अणु मोजमाप चुकीचे असू शकतात असे मानून त्यांनी अणुवजनाचा क्रम दुर्लक्षित केला आणि समान गुणधर्म असलेले घटक एकत्र ठेवले. उदाहरणार्थ, टेल्युरियम (गट VI) पेक्षा कमी अणुवजन असलेले आयोडीन गुणधर्मांमधील साम्यामुळे (आकृती ३.१) फ्लोरिन, क्लोरिन, ब्रोमिन यांच्यासोबत गट VII मध्ये ठेवले गेले. त्याच वेळी, समान गुणधर्म असलेले घटक एकाच गटात ठेवणे हे त्यांचे प्राथमिक उद्दिष्ट राखून, त्यांनी असे प्रस्तावित केले की काही घटक अजूनहि शोधले गेले नाहीत आणि म्हणून सारणीत अनेक अंतर ठेवली. उदाहरणार्थ, मेंडेलीव्ह यांनी त्यांची आवर्त सारणी प्रकाशित केली तेव्हा गॅलियम आणि जर्मेनियम हे दोन्ही अज्ञात होते. त्यांनी ॲल्युमिनियमच्या खाली आणि सिलिकॉनच्या खाली अंतर ठेवले आणि या घटकांना एका-ॲल्युमिनियम आणि एका-सिलिकॉन असे नाव दिले. मेंडेलीव्ह यांनी केवळ गॅलियम आणि जर्मेनियमचे अस्तित्वच अंदाजले नाही तर त्यांचे काही सामान्य भौतिक गुणधर्मही वर्णन केले. हे घटक नंतर शोधले गेले. मेंडेलीव्ह यांनी या घटकांसाठी अंदाजलेले काही गुणधर्म आणि प्रायोगिकरित्या आढळलेले गुणधर्म सारणी ३.३ मध्ये सूचीबद्ध केले आहेत.
मेंडेलीव्हच्या परिमाणवाचक अंदाजांची धाडसीपणा आणि त्यांचे अंतिम यश यामुळे त्यांना आणि त्यांच्या आवर्त सारणीला प्रसिद्धी मिळाली. १९०५ मध्ये प्रकाशित झालेली मेंडेलीव्हची आवर्त सारणी आकृती ३.१ मध्ये दर्शविली आहे.
सारणी ३.३ एका-ॲल्युमिनियम (गॅलियम) आणि एका-सिलिकॉन (जर्मेनियम) या घटकांसाठी मेंडेलीव्हचे अंदाज
| गुणधर्म | एका-ॲल्युमिनियम (अंदाजित) | गॅलियम (आढळले) | एका-सिलिकॉन (अंदाजित) | जर्मेनियम (आढळले) |
|---|---|---|---|---|
| अणुवजन | 68 | 70 | 72 | 72.6 |
| घनता/(ग्रॅ/सेमी $\mathbf{)}$ | 5.9 | 5.94 | 5.5 | 5.36 |
| द्रवणांक/के | $\mathrm{Low}$ | 302.93 | $\mathrm{High}$ | 1231 |
| ऑक्साईडचे सूत्र | $\mathrm{E}_2 \mathrm{O}_3$ | $\mathrm{Ga}_2 \mathrm{O}_3$ | $\mathrm{EO}_{2}$ | $\mathrm{GeO}_{2}$ |
| क्लोराईडचे सूत्र | $\mathrm{E} \mathrm{Cl}_{3}$ | $\mathrm{GaCl}_{3}$ | $\mathrm{ECl}_{4}$ | $\mathrm{GeCl}_{4}$ |
गट आणि मालिकांमधील घटकांची आवर्ती प्रणाली

आकृती ३.१ पूर्वी प्रकाशित झालेली मेंडेलीव्हची आवर्त सारणी
३.३ आधुनिक आवर्त नियम आणि आवर्त सारणीचे सध्याचे स्वरूप
हे लक्षात ठेवले पाहिजे की जेव्हा मेंडेलीव्ह यांनी त्यांची आवर्त सारणी विकसित केली तेव्हा रसायनशास्त्रज्ञांना अणूच्या अंतर्गत रचनेबद्दल काहीही माहिती नव्हती. तथापि, $20^{\text {th }}$ शतकाच्या सुरुवातीला उप-अणु कणांबद्दलच्या सिद्धांतांमध्ये खोल विकास झाला. १९१३ मध्ये, इंग्रज भौतिकशास्त्रज्ञ हेन्री मोस्ले यांनी घटकांच्या वैशिष्ट्यपूर्ण $X$-किरण वर्णपटांमध्ये नियमितता पाहिली. $\sqrt{v}$ (जेथे $V$ ही $X$-किरणांची उत्सर्जित वारंवारता आहे) विरुद्ध अणुक्रमांक $(Z)$ चा आलेख सरळ रेषा देतो आणि $\sqrt{v}$ विरुद्ध अणुवस्तुमानाचा आलेख देत नाही. यामुळे त्यांनी दर्शविले की अणुक्रमांक हा अणुवस्तुमानापेक्षा घटकाचा अधिक मूलभूत गुणधर्म आहे. त्यामुळे मेंडेलीव्हचा आवर्त नियम त्यानुसार सुधारित करण्यात आला. याला आधुनिक आवर्त नियम म्हणून ओळखले जाते आणि तो खालीलप्रमाणे सांगता येतो:
घटकांचे भौतिक आणि रासायनिक गुणधर्म हे त्यांच्या अणुक्रमांकांची आवर्ती फलने आहेत.
आवर्त नियमाने ९४ नैसर्गिकरित्या आढळणाऱ्या घटकांमध्ये (नेप्ट्युनियम आणि प्लुटोनियम हे ॲक्टिनियम आणि प्रोटोॲक्टिनियम प्रमाणे युरेनियमच्या खनिज पिचब्लेंडमध्ये देखील आढळतात) महत्त्वाचे साधर्म्य प्रकट केले. यामुळे अजैविक रसायनशास्त्रात नवीन स्वारस्य निर्माण झाले आणि कृत्रिमरित्या तयार केलेल्या अल्पायुषी घटकांच्या निर्मितीद्वारे ते सध्याच्या काळातही चालू आहे.
तुम्हाला आठवत असेल की अणुक्रमांक हा केंद्रकीय प्रभार (म्हणजेच प्रोटॉनची संख्या) किंवा तटस्थ अणूमधील इलेक्ट्रॉनच्या संख्येइतका असतो. त्यानंतर घटकांच्या आवर्ततेमध्ये क्वांटम संख्या आणि इलेक्ट्रॉनिक संरूपणांचे महत्त्व दृश्यमान करणे सोपे जाते. खरं तर, आता हे मान्य केले गेले आहे की आवर्त नियम हा मूलतः इलेक्ट्रॉनिक संरूपणांमधील आवर्ती बदलाचा परिणाम आहे, जो खरोखर घटक आणि त्यांच्या संयुगांचे भौतिक आणि रासायनिक गुणधर्म निश्चित करतो.
वेळोवेळी आवर्त सारणीचे अनेक प्रकार तयार करण्यात आले आहेत. काही प्रकार रासायनिक अभिक्रिया आणि संयुजा यावर भर देतात, तर इतर घटकांच्या इलेक्ट्रॉनिक संरूपणावर भर देतात. एक आधुनिक आवृत्ती, म्हणजेच घटकांच्या आवर्त सारणीचे तथाकथित “लांब रूप” (आकृती ३.२), हे सर्वात सोयीचे आणि व्यापकपणे वापरले जाणारे आहे. आडव्या ओळी (ज्याला मेंडेलीव्ह यांनी मालिका म्हटले आहे) यांना आवर्त म्हणतात आणि उभ्या स्तंभांना गट म्हणतात. त्यांच्या अणूंमध्ये समान बाह्य इलेक्ट्रॉनिक संरूपण असलेले घटक उभ्या स्तंभांमध्ये मांडलेले असतात, ज्यांना गट किंवा कुटुंबे म्हणून संबोधले जाते. इंटरनॅशनल युनियन ऑफ प्युअर अँड अॅप्लाइड केमिस्ट्री (आययूपीएसी) च्या शिफारशीनुसार, गट IA … VIIA, VIII, IB … VIIB आणि 0 या जुन्या संकेतांच्या जागी गट १ ते १८ पर्यंत क्रमांकित केले जातात.
एकूण सात आवर्त आहेत. आवर्त क्रमांक त्या आवर्तातील घटकांच्या सर्वोच्च मुख्य क्वांटम संख्या $(n)$ शी संबंधित असतो. पहिल्या आवर्तात २ घटक असतात. त्यानंतरच्या आवर्तांमध्ये अनुक्रमे $8,8,18,18$ आणि ३२ घटक असतात. सातवा आवर्त अपूर्ण आहे आणि सहाव्या आवर्ताप्रमाणेच (क्वांटम संख्यांच्या आधारावर) कमाल ३२ घटक असू शकतात. आवर्त सारणीच्या या स्वरूपात, सहाव्या आणि सातव्या आवर्तातील १४ घटक (अनुक्रमे लॅन्थनॉइड्स आणि ॲक्टिनॉइड्स) तळाशी वेगळ्या पॅनेलमध्ये ठेवले आहेत[^0].
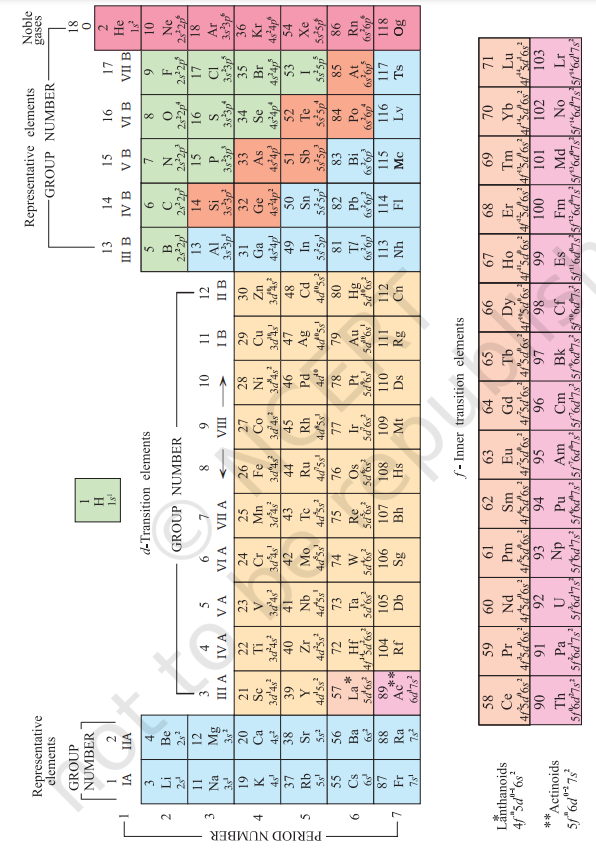
आकृती ३.२ घटकांची आवर्त सारणीची लांब रूप, त्यांचे अणुक्रमांक आणि मूल अवस्थेतील बाह्य इलेक्ट्रॉनिक संरूपणासह. गट १९८४ च्या आययूपीएसी शिफारशीनुसार १-१८ पर्यंत क्रमांकित केले आहेत. हे संकेत घटकांसाठी IA–VIIA, VIII, IB–VIIB आणि 0 या जुन्या क्रमांकन योजनेची जागा घेतात.
३.४ अणुक्रमांक > १०० असलेल्या घटकांची नामकरण पद्धत
नवीन घटकांचे नामकरण पारंपारिकपणे शोधकाचा (किंवा शोधकांचा) विशेषाधिकार होता आणि सुचवलेले नाव आययूपीएसीद्वारे मान्य केले जात असे. अलीकडच्या वर्षांत यामुळे काही वाद निर्माण झाले आहेत. खूप जास्त अणुक्रमांक असलेले नवीन घटक इतके अस्थिर असतात की कधीकधी फक्त काही अणूच प्रमाणात ते मिळतात. त्यामुळे त्यांचे संश्लेषण आणि वैशिष्ट्यीकरण करण्यासाठी अत्याधुनिक महागडी उपकरणे आणि प्रयोगशाळा आवश्यक असतात. असे कार्य स्पर्धात्मक भावनेने जगातील काही प्रयोगशाळांमध्येच केले जाते. वैज्ञानिक, नवीन घटकावर विश्वासार्ह माहिती गोळा करण्यापूर्वी, कधीकधी त्याच्या शोधासाठी दावा करण्यासाठी प्रलोभनास बळी पडतात. उदाहरणार्थ, अमेरिकन आणि सोव्हिएत वैज्ञानिकांनी दोघांनीही घटक १०४ च्या शोधासाठी श्रेय घेतले. अमेरिकनांनी त्याला रदरफोर्डियम असे नाव दिले तर सोव्हिएतांनी त्याला कुर्चाटोव्हियम असे नाव दिले. अशा समस्या टाळण्यासाठी, आययूपीएसीने शिफारस केली आहे की नवीन घटकाचा शोध सिद्ध होईपर्यंत आणि त्याचे नाव अधिकृतपणे मान्य होईपर्यंत, संख्यात्मक मूळे वापरून अणुक्रमांकावरून थेट एक पद्धतशीर नामकरण काढले जावे. ० आणि संख्या $1-9$ साठीची ही मूळे सारणी ३.४ मध्ये दर्शविली आहेत. अणुक्रमांक बनविणाऱ्या अंकांच्या क्रमाने मूळे एकत्र ठेवली जातात आणि शेवटी “ium” जोडले जाते. $Z$ १०० पेक्षा जास्त असलेल्या घटकांसाठी आययूपीएसी नावे सारणी ३.५ मध्ये दर्शविली आहेत.
सारणी ३.४ घटकांच्या आययूपीएसी नामकरणासाठी संकेत
| अंक | नाव | संक्षेप |
|---|---|---|
| 0 | nil | $\mathrm{n}$ |
| 1 | un | $\mathrm{u}$ |
| 2 | bi | $\mathrm{b}$ |
| 3 | tri | $\mathrm{t}$ |
| 4 | quad | $\mathrm{q}$ |
| 5 | pent | $\mathrm{p}$ |
| 6 | hex | $\mathrm{h}$ |
| 7 | sept | $\mathrm{s}$ |
| 8 | oct | $\mathrm{o}$ |
| 9 | enn | $\mathrm{e}$ |
सारणी ३.५ अणुक्रमांक १०० पेक्षा जास्त असलेल्या घटकांची नामकरण पद्धत
| अणु क्रमांक | आययूपीएसी नामकरणानुसार नाव | चिन्ह | आययूपीएसी अधिकृत नाव | आययूपीएसी चिन्ह |
|---|---|---|---|---|
| 101 | Unnilunium | Unu | Mendelevium | $\mathrm{Md}$ |
| 102 | Unnilbium | Unb | Nobelium | No |
| 103 | Unniltrium | Unt | Lawrencium | $\mathrm{Lr}$ |
| 104 | Unnilquadium | Unq | Rutherfordium | $\mathrm{Rf}$ |
| 105 | Unnilpentium | Unp | Dubnium | $\mathrm{Db}$ |
| 106 | Unnilhexium | Unh | Seaborgium | $\mathrm{Sg}$ |
| 107 | Unnilseptium | Uns | Bohrium | $\mathrm{Bh}$ |
| 108 | Unniloctium | Uno | Hassium | $\mathrm{Hs}$ |
| 109 | Unnilennium | Une | Meitnerium | $\mathrm{Mt}$ |
| 110 | Ununnillium | Uun | Darmstadtium | $\mathrm{Ds}$ |
| 111 | Unununnium | Uuu | Rontgenium | $\mathrm{Rg}$ |
| 112 | Ununbium | Uub | Copernicium | $\mathrm{Cn}$ |
| 113 | Ununtrium | Uut | Nihonium | $\mathrm{Nh}$ |
| 114 | Ununquadium | Uuq | Flerovium | $\mathrm{Fl}$ |
| 115 | Ununpentium | Uup | Moscovium | $\mathrm{Mc}$ |
| 116 | Ununhexium | Uuh | Livermorium | $\mathrm{Lv}$ |
| 117 | Ununseptium | Uus | Tennessine | $\mathrm{Ts}$ |
| 118 | Ununoctium | Uuo | Oganesson | $\mathrm{Og}$ |
अशाप्रकारे, नवीन घटकाला प्रथम तीन अक्षरे असलेल्या चिन्हासह एक तात्पुरते नाव मिळते. नंतर आययूपीएसीच्या प्रत्येक देशातील प्रतिनिधींच्या मतदानाने कायम नाव आणि चिन्ह दिले जाते. कायम नावामध्ये तो घटक ज्या देशात (किंवा देशाच्या राज्यात) शोधला गेला तो देश प्रतिबिंबित होऊ शकतो किंवा एखाद्या उल्लेखनीय वैज्ञानिकाला श्र








