धडा 08 रेडॉक्स प्रतिक्रिया
“जिथे ऑक्सिडेशन आहे, तिथे नेहमीच रिडक्शन असते. रसायनशास्त्र मूलतः रेडॉक्स प्रणालींचा अभ्यास आहे.”
रसायनशास्त्र विविध प्रकारच्या द्रव्यांचा आणि एका प्रकारच्या द्रव्याचे दुसऱ्या प्रकारात रूपांतर होण्याचा अभ्यास करते. द्रव्याचे एका प्रकारातून दुसऱ्या प्रकारात रूपांतर विविध प्रकारच्या अभिक्रियांद्वारे होते. अशा अभिक्रियांपैकी एक महत्त्वाची श्रेणी म्हणजे रेडॉक्स अभिक्रिया. अनेक भौतिक तसेच जैविक घटना रेडॉक्स अभिक्रियांशी संबंधित आहेत. या अभिक्रियांचा औषधनिर्मिती, जैविक, औद्योगिक, धातुशास्त्रीय आणि कृषीक्षेत्रात मोठ्या प्रमाणावर उपयोग होतो. घरगुती, वाहतूक आणि इतर व्यावसायिक हेतूंसाठी ऊर्जा मिळवण्यासाठी विविध प्रकारच्या इंधनांचे ज्वलन, अत्यंत क्रियाशील धातू आणि अधातूंच्या निष्कर्षणासाठीच्या विद्युतरासायनिक प्रक्रिया, कॉस्टिक सोडा सारख्या रासायनिक संयुगांचे उत्पादन, कोरड्या आणि ओल्या बॅटरींचे कार्य आणि धातूंचे संक्षारण या सर्व गोष्टी रेडॉक्स प्रक्रियांच्या कक्षेत येतात, यावरून या अभिक्रियांचे महत्त्व स्पष्ट होते. अलीकडे, हायड्रोजन इकॉनॉमी (इंधन म्हणून द्रव हायड्रोजनचा वापर) आणि ‘ओझोन होल’चा विकास यासारख्या पर्यावरणीय समस्या देखील रेडॉक्स घटनेखाली येऊ लागल्या आहेत.
८.१ रेडॉक्स अभिक्रियांची शास्त्रीय संकल्पना - ऑक्सिडेशन आणि रिडक्शन अभिक्रिया
मूळतः, एखाद्या मूलद्रव्याला किंवा संयुगाला ऑक्सिजनची भर घालण्याच्या प्रक्रियेस ऑक्सिडेशन असे संबोधले जात असे. वातावरणात डायऑक्सिजनच्या उपस्थितीमुळे (२०%), अनेक मूलद्रव्ये त्यासोबत संयोग पावतात आणि त्यांचे ऑक्साईड स्वरूपात पृथ्वीवर सामान्यतः आढळण्याचे हे एक प्रमुख कारण आहे. ऑक्सिडेशनच्या मर्यादित व्याख्येनुसार खालील अभिक्रिया ऑक्सिडेशन प्रक्रियांचे प्रतिनिधित्व करतात:
$$2 \mathrm{Mg}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{MgO}(\mathrm{s}) \tag{8.1}$$
$$\mathrm{S}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow \mathrm{SO_2}(\mathrm{~g}) \tag{8.2}$$
अभिक्रिया (८.१) आणि (८.२) मध्ये, मॅग्नेशियम आणि सल्फर या मूलद्रव्यांमध्ये ऑक्सिजनची भर पडल्यामुळे त्यांचे ऑक्सिडेशन होते. त्याचप्रमाणे, मिथेनमध्ये ऑक्सिजनची भर पडल्यामुळे त्याचे ऑक्सिडेशन होते.
$$\mathrm{CH} _{4}(\mathrm{~g})+2 \mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g})+2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{7.3}$$
अभिक्रिया (८.३) चे काळजीपूर्वक परीक्षण केल्यास, ज्यामध्ये हायड्रोजनची जागा ऑक्सिजनने घेतली आहे, त्यामुळे रसायनशास्त्रज्ञांना ऑक्सिडेशनची पुनर्व्याख्या हायड्रोजन काढून टाकण्याच्या दृष्टीने करण्यास प्रवृत्त केले आणि म्हणूनच, ऑक्सिडेशन या शब्दाचा दायरा एखाद्या पदार्थातून हायड्रोजन काढून टाकण्यासह समाविष्ट करण्यासाठी विस्तारित करण्यात आला. खालील उदाहरण ही आणखी एक अभिक्रिया आहे जिथे हायड्रोजन काढून टाकणे देखील ऑक्सिडेशन अभिक्रिया म्हणून उद्धृत केले जाऊ शकते.
$$ \begin{equation*} 2 \mathrm{H_2} \mathrm{~S}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{~S}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \tag{8.4} \end{equation*} $$
रसायनशास्त्रज्ञांचे ज्ञान वाढत गेल्याने, (७.१ ते ७.४) प्रमाणेच अशा अभिक्रियांसाठी ऑक्सिडेशन हा शब्द विस्तारित करणे स्वाभाविक होते, ज्यामध्ये ऑक्सिजन नसून इतर विद्युतऋणात्मक मूलद्रव्ये समाविष्ट असतात. मॅग्नेशियमचे फ्लोरिन, क्लोरीन आणि सल्फर इत्यादींसोबत ऑक्सिडेशन खालील अभिक्रियांनुसार होते:
$$\operatorname{Mg}(\mathrm{s})+\mathrm{F_2} (\mathrm{~g}) \rightarrow \operatorname{MgF_2} (s) \tag{8.5}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{Cl_2} (g) \rightarrow \mathrm{MgCl_2} (s) \tag{8.6}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{S} (s) \rightarrow \operatorname{MgS}(\mathrm{s}) \tag{8.7}$$
अभिक्रिया (७.५ ते ७.७) यांना ऑक्सिडेशन अभिक्रियांच्या छत्राखाली समाविष्ट केल्याने रसायनशास्त्रज्ञांना केवळ हायड्रोजन काढून टाकणेच नव्हे तर विद्युतधनात्मक मूलद्रव्ये काढून टाकणे देखील ऑक्सिडेशन म्हणून विचारात घेण्यास प्रवृत्त केले. अशाप्रकारे अभिक्रिया:
$$ 2 \mathrm{~K_4} \left[ \mathrm{Fe} ( \mathrm{CN})_{6} \right] ( \mathrm{aq}) + \mathrm{H_2} \mathrm{O_2} ( \mathrm{aq}) \rightarrow 2 \mathrm{~K_3} \left[\mathrm{Fe}( \mathrm{CN})_6 \right] ( \mathrm{aq}) + 2 \mathrm{KOH} ( \mathrm{aq}) $$
याचा अर्थ पोटॅशियम फेरोसायनाइडचे पोटॅशियम फेरिसायनाइडमध्ये रूपांतर होण्यापूर्वी त्यातून विद्युतधनात्मक मूलद्रव्य पोटॅशियम काढून टाकल्यामुळे ऑक्सिडेशन होते असे लावला जातो. सारांश म्हणजे, “ऑक्सिडेशन” ही संज्ञा एखाद्या पदार्थात ऑक्सिजन/विद्युतऋणात्मक मूलद्रव्याची भर घालणे किंवा एखाद्या पदार्थातून हायड्रोजन/विद्युतधनात्मक मूलद्रव्य काढून टाकणे अशी व्याख्या केली जाते.
सुरुवातीला, रिडक्शन ही एखाद्या संयुगातून ऑक्सिजन काढून टाकण्याची प्रक्रिया म्हणून विचारात घेतली जात असे. तथापि, रिडक्शन या संज्ञेचा दायरा आजकाल एखाद्या पदार्थातून ऑक्सिजन/विद्युतऋणात्मक मूलद्रव्य काढून टाकणे किंवा एखाद्या पदार्थात हायड्रोजन/विद्युतधनात्मक मूलद्रव्याची भर घालणे यासह विस्तारित करण्यात आला आहे.
वर दिलेल्या व्याख्येनुसार, रिडक्शन प्रक्रियांची खालील उदाहरणे आहेत:
$$2 \mathrm{HgO}(\mathrm{s}) \xrightarrow{\Delta} 2 \mathrm{Hg}(\mathrm{l})+\mathrm{O_2}(\mathrm{~g}) \tag{8.8}$$
(मर्क्युरिक ऑक्साईडमधून ऑक्सिजन काढून टाकणे)
$$2 \mathrm{FeCl_3}(\mathrm{aq})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{FeCl_2}(\mathrm{aq})+2 \mathrm{HCl}(\mathrm{aq}) \tag{8.9}$$
(विद्युतऋणात्मक मूलद्रव्य, क्लोरीनचे फेरिक क्लोराईडमधून काढून टाकणे)
$$\mathrm{CH_2}=\mathrm{CH_2}(\mathrm{~g})+\mathrm{H_2}(\mathrm{~g}) \rightarrow \mathrm{H_3} \mathrm{C}-\mathrm{CH_3}(\mathrm{~g})\tag{8.10}$$
(हायड्रोजनची भर घालणे)
$$2 \mathrm{HgCl_2}(\mathrm{aq})+\mathrm{SnCl_2}(\mathrm{aq}) \rightarrow \mathrm{Hg_2} \mathrm{Cl_2}(\mathrm{~s})+\mathrm{SnCl_4}(\mathrm{aq})\tag{8.11}$$
(मर्क्युरिक क्लोराईडमध्ये पाराची भर घालणे)
अभिक्रिया (८.११) मध्ये, स्टॅनस क्लोराईडचे स्टॅनिक क्लोराईडमध्ये एकाच वेळी ऑक्सिडेशन देखील होत आहे कारण त्यात विद्युतऋणात्मक मूलद्रव्य क्लोरीनची भर पडते. लवकरच हे लक्षात आले की ऑक्सिडेशन आणि रिडक्शन नेहमी एकाच वेळी घडतात (वर दिलेल्या सर्व समीकरणांचे पुनःपरीक्षण केल्यास हे स्पष्ट होईल), म्हणूनच, रासायनिक अभिक्रियांच्या या वर्गासाठी “रेडॉक्स” हा शब्द तयार करण्यात आला.
समस्या ८.१
खाली दिलेल्या अभिक्रियांमध्ये, ऑक्सिडेशन आणि रिडक्शन होणाऱ्या प्रजाती ओळखा:
(i) $\mathrm{H_2} \mathrm{~S}$ (g) $+\mathrm{Cl_2}$ (g) $\rightarrow 2 \mathrm{HCl}$ (g) $+\mathrm{S}$ (s)
(ii) $3 \mathrm{Fe_3} \mathrm{O_4}$ (s) $+8 \mathrm{Al}$ (s) $\rightarrow 9 \mathrm{Fe}$ (s) $+4 \mathrm{Al_2} \mathrm{O_3}(\mathrm{~s})$
(iii) $2 \mathrm{Na}$ (s) $+\mathrm{H_2}$ (g) $\rightarrow 2 \mathrm{NaH}$ (s)
उत्तर
(i) $\mathrm{H_2} \mathrm{~S}$ चे ऑक्सिडेशन होते कारण हायड्रोजनमध्ये अधिक विद्युतऋणात्मक मूलद्रव्य, क्लोरीनची भर पडते (किंवा अधिक विद्युतधनात्मक मूलद्रव्य, हायड्रोजन S मधून काढून टाकले जाते). त्यात हायड्रोजनची भर पडल्यामुळे क्लोरीनचे रिडक्शन होते.
(ii) अॅल्युमिनियमचे ऑक्सिडेशन होते कारण त्यात ऑक्सिजनची भर पडते. फेरस फेरिक ऑक्साईड $\left(\mathrm{Fe_3} \mathrm{O_4}\right)$ चे रिडक्शन होते कारण त्यातून ऑक्सिजन काढून टाकले जाते.
(iii) विद्युतऋणात्मकतेच्या संकल्पनेचा काळजीपूर्वक वापर केल्यासच आपण असा निष्कर्ष काढू शकतो की सोडियमचे ऑक्सिडेशन होते आणि हायड्रोजनचे रिडक्शन होते.
येथे निवडलेली अभिक्रिया (iii) आपल्याला रेडॉक्स अभिक्रियांची व्याख्या करण्याच्या दुसऱ्या मार्गाचा विचार करण्यास प्रवृत्त करते.
८.२ इलेक्ट्रॉन स्थानांतरण अभिक्रियांच्या दृष्टीने रेडॉक्स अभिक्रिया
आपण आधीच शिकलो आहोत की खालील अभिक्रिया रेडॉक्स अभिक्रिया आहेत कारण या प्रत्येक अभिक्रियांमध्ये सोडियममध्ये एकतर ऑक्सिजन किंवा अधिक विद्युतऋणात्मक मूलद्रव्याची भर पडल्यामुळे सोडियमचे ऑक्सिडेशन होते.
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaCl}(\mathrm{s})\tag{8.12}$$
$$4 \mathrm{Na}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na_2} \mathrm{O}(\mathrm{s})\tag{8.13}$$
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{S}(\mathrm{s}) \rightarrow \mathrm{Na_2} \mathrm{~S}(\mathrm{~s}) \tag{8.14}$$
त्याच वेळी, क्लोरीन, ऑक्सिजन आणि सल्फर यांचे रिडक्शन होते कारण या प्रत्येकामध्ये विद्युतधनात्मक मूलद्रव्य सोडियमची भर पडली आहे. रासायनिक बंधांच्या आपल्या ज्ञानावरून आपल्याला हे देखील माहित आहे की सोडियम क्लोराईड, सोडियम ऑक्साईड आणि सोडियम सल्फाइड हे आयनिक संयुगे आहेत आणि कदाचित $\mathrm{Na}^{+} \mathrm{Cl}^{-}( \mathrm{s}),\left(\mathrm{Na}^{+} \right)_2 \mathrm{O}^{2-}( \mathrm{s})$, आणि $ \left(\mathrm{Na}^{+} \right)_2$ $\mathrm{S}^{2-}( \mathrm{s})$ असे लिहिणे अधिक योग्य ठरेल. तयार झालेल्या प्रजातींवर विद्युतभार विकसित होणे आपल्याला अभिक्रिया (८.१२ ते ८.१४) खालील पद्धतीने पुन्हा लिहिण्यास सूचित करते:
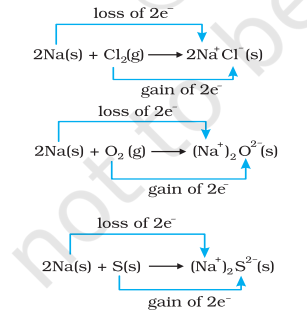
सोयीसाठी, वरील प्रत्येक प्रक्रियेचा दोन स्वतंत्र चरण म्हणून विचार केला जाऊ शकतो, एकामध्ये इलेक्ट्रॉनचे नुकसान होते आणि दुसऱ्यामध्ये इलेक्ट्रॉनचा लाभ होतो. उदाहरण म्हणून, आपण यापैकी एक, म्हणजे सोडियम क्लोराईडची निर्मिती, याचे आणखी सविस्तर वर्णन करू शकतो.
$2 \mathrm{Na}(\mathrm{s}) \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
$\mathrm{Cl_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{Cl}^{-}(\mathrm{g})$
वरील प्रत्येक चरणाला अर्ध-अभिक्रिया म्हणतात, जी स्पष्टपणे इलेक्ट्रॉनचा सहभाग दर्शवते. अर्ध-अभिक्रियांची बेरीज एकूण अभिक्रिया देते:
$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na}^{+} \mathrm{Cl}^{-}(\mathrm{s})$ किंवा $2 \mathrm{NaCl}(\mathrm{s})$
अभिक्रिया ८.१२ ते ८.१४ सूचित करतात की ज्या अर्ध-अभिक्रियांमध्ये इलेक्ट्रॉनचे नुकसान होते त्यांना ऑक्सिडेशन अभिक्रिया म्हणतात. त्याचप्रमाणे, ज्या अर्ध-अभिक्रियांमध्ये इलेक्ट्रॉनचा लाभ होतो त्यांना रिडक्शन अभिक्रिया म्हणतात. येथे हे नमूद करणे अप्रासंगिक होणार नाही की ऑक्सिडेशन आणि रिडक्शनची व्याख्या करण्याची नवीन पद्धत केवळ शास्त्रीय कल्पनेनुसार प्रजातींचे वर्तन आणि इलेक्ट्रॉन-स्थानांतरण बदलातील त्यांचा परस्परसंबंध स्थापित करूनच प्राप्त झाली आहे. अभिक्रिया (८.१२ ते ८.१४) मध्ये, सोडियम, ज्याचे ऑक्सिडेशन होते, ते रिड्युसिंग एजंट म्हणून कार्य करते कारण ते त्याच्याशी संवाद साधणाऱ्या प्रत्येक मूलद्रव्याला इलेक्ट्रॉन दान करते आणि अशाप्रकारे त्यांचे रिडक्शन करण्यास मदत करते. क्लोरीन, ऑक्सिजन आणि सल्फर यांचे रिडक्शन होते आणि ते ऑक्सिडायझिंग एजंट म्हणून कार्य करतात कारण हे सोडियमकडून इलेक्ट्रॉन स्वीकारतात. सारांश म्हणजे, आपण असे नमूद करू शकतो की
ऑक्सिडेशन: कोणत्याही प्रजातीद्वारे इलेक्ट्रॉन(चे) नुकसान.
रिडक्शन: कोणत्याही प्रजातीद्वारे इलेक्ट्रॉन(चा) लाभ.
ऑक्सिडायझिंग एजंट: इलेक्ट्रॉन(चे) स्वीकारकर्ता.
रिड्युसिंग एजंट: इलेक्ट्रॉन(चे) दाता.
समस्या ८.२
हे सिद्ध करा की अभिक्रिया: $2 \mathrm{Na}(\mathrm{s})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaH}$ (s) ही एक रेडॉक्स बदल आहे.
उत्तर
वरील अभिक्रियेत तयार झालेले संयुग आयनिक संयुग असल्यामुळे, ज्याचे प्रतिनिधित्व $\mathrm{Na}^{+} \mathrm{H}^{-}$(s) असे देखील केले जाऊ शकते, यावरून असे सूचित होते की या प्रक्रियेतील एक अर्ध-अभिक्रिया आहे:
$2 \mathrm{Na}(\mathrm{s}) \quad \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
आणि दुसरी अर्ध-अभिक्रिया आहे:
$\mathrm{H_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{H}^{-}(\mathrm{g})$
परीक्षणाखालील अभिक्रियेचे दोन अर्ध-अभिक्रियांमध्ये विभाजन केल्याने आपोआपच हे स्पष्ट होते की येथे सोडियमचे ऑक्सिडेशन होते आणि हायड्रोजनचे रिडक्शन होते, म्हणून, संपूर्ण अभिक्रिया ही एक रेडॉक्स बदल आहे.
८.२.१ स्पर्धात्मक इलेक्ट्रॉन स्थानांतरण अभिक्रिया
आकृती ८.१ मध्ये दाखवल्याप्रमाणे, धात्विक जस्ताची एक पट्टी कॉपर नायट्रेटच्या जलीय द्रावणात सुमारे एक तास ठेवा. आपल्याला हे लक्षात येईल की पट्टीवर तांबेरी रंगाचे धात्विक तांबे जमा होते आणि द्रावणाचा निळा रंग नाहीसा होतो. $\mathrm{Zn}^{2+}$ आयनांची निर्मिती उत्पादनांमध्ये सहजपणे ओळखता येते जेव्हा $\mathrm{Cu}^{2+}$ मुळे द्रावणाचा निळा रंग नाहीसा होतो. जर हायड्रोजन सल्फाइड वायू $\mathrm{Zn}^{2+}$ आयन असलेल्या रंगहीन द्रावणातून पास केला, तर द्रावण अमोनियासह आम्लारी बनवल्यावर पांढऱ्या जस्त सल्फाइड, $\mathrm{ZnS}$ ची उपस्थिती दिसू शकते.
धात्विक जस्त आणि कॉपर नायट्रेटच्या जलीय द्रावण यांच्यातील अभिक्रिया आहे:
$$\mathrm{Zn}(\mathrm{s})+\mathrm{Cu}^{2+}(\mathrm{aq}) \rightarrow \mathrm{Zn}^{2+}(\mathrm{aq})+\mathrm{Cu}(\mathrm{s}) \tag{8.15}$$
अभिक्रिया (८.१५) मध्ये, जस्ताने इलेक्ट्रॉन गमावले आहेत $Zn^{2+}$ तयार करण्यासाठी आणि म्हणून, जस्ताचे ऑक्सिडेशन होते. स्पष्टपणे, आता जर जस्ताचे ऑक्सिडेशन झाले, इलेक्ट्रॉन सोडले, तर काहीतरी रिडक्शन पावले पाहिजे, जस्ताने गमावलेले इलेक्ट्रॉन स्वीकारले पाहिजेत. कॉपर आयन जस्ताकडून इलेक्ट्रॉन मिळवून रिडक्शन पावते.
अभिक्रिया (८.१५) खालीलप्रमाणे पुन्हा लिहिता येईल:
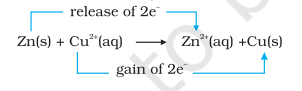
या टप्प्यावर आपण समीकरण (८.१५) द्वारे दर्शविलेल्या अभिक्रियेसाठी समतोलाची स्थिती तपासू शकतो. या हेतूसाठी, धात्विक तांब्याची एक पट्टी जस्त सल्फेट द्रावणात ठेवू. कोणतीही दृश्यमान अभिक्रिया दिसत नाही आणि कॉप्रिक सल्फाइड, CuS चा काळा रंग तयार करण्यासाठी द्रावणातून $\mathrm{H_2} \mathrm{~S}$ वायू पास करून $\mathrm{Cu}^{2+}$ आयनांची उपस्थिती शोधण्याचा प्रयत्न यशस्वी होत नाही. कॉप्रिक सल्फाइडची विद्राव्यता इतकी कमी आहे की ही एक अत्यंत संवेदनशील चाचणी आहे; तरीही तयार झालेल्या $\mathrm{Cu}^{2+}$ चे प्रमाण शोधता येत नाही. अशाप्रकारे आपण असा निष्कर्ष काढतो की अभिक्रिया (८.१५) साठी समतोलाची स्थिती अभिक्रियाकांवर उत्पादनांना मोठ्या प्रमाणात पसंत करते.
आता इलेक्ट्रॉन स्थानांतरण अभिक्रिया तांब्याच्या धातू आणि पाण्यातील सिल्व्हर नायट्रेट द्रावणापर्यंत वाढवू आणि आकृती ८.२ मध्ये दाखवल्याप्रमाणे एक संयोजन तयार करू. अभिक्रियेमुळे:
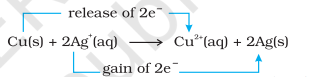
येथे, $\mathrm{Cu}(\mathrm{s})$ चे $\mathrm{Cu}^{2+}(\mathrm{aq})$ मध्ये ऑक्सिडेशन होते आणि $\mathrm{Ag}^{+}(\mathrm{aq})$ चे $\mathrm{Ag}(\mathrm{s})$ मध्ये रिडक्शन होते. समतोल उत्पादनांना $\mathrm{Cu}^{2+}(\mathrm{aq})$ आणि $\mathrm{Ag}(\mathrm{s})$ मोठ्या प्रमाणात पसंत करतो.
याउलट, निकेल सल्फेट द्रावणात ठेवलेल्या धात्विक कोबाल्टची अभिक्रिया देखील तुलना करूया. येथे घडणारी अभिक्रिया आहे:
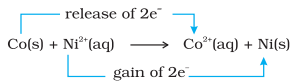
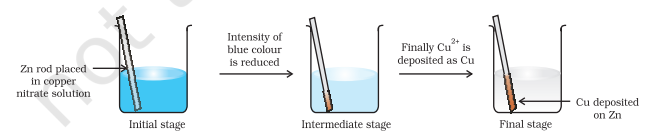
आकृती ८.१ जस्त आणि कॉपर नायट्रेटच्या जलीय द्रावण यांच्यातील रेडॉक्स अभिक्रिया बीकरमध्ये घडत आहे.
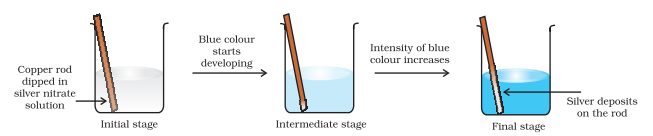
आकृती ८.२ तांबे आणि सिल्व्हर नायट्रेटच्या जलीय द्रावण यांच्यातील रेडॉक्स अभिक्रिया बीकरमध्ये घडत आहे
समतोलावर, रासायनिक चाचण्यांवरून असे दिसून येते की $\mathrm{Ni}^{2+}(\mathrm{aq})$ आणि $\mathrm{Co}^{2+}(\mathrm{aq})$ दोन्ही मध्यम प्रमाणात उपस्थित आहेत. या प्रकरणात, एकतर अभिक्रियाक $\left[\mathrm{Co}(\mathrm{s})\right.$ आणि $\left.\mathrm{Ni}^{2+}(\mathrm{aq})\right]$ किंवा उत्पादने $\left[\mathrm{Co}^{2+}(\mathrm{aq})\right.$ आणि $\left.\mathrm{Ni}(\mathrm{s})\right]$ यांना मोठ्या प्रमाणात पसंत केले जात नाही.
इलेक्ट्रॉन सोडण्याची ही स्पर्धा आपल्याला आम्लांमधील प्रोटॉन सोडण्याच्या स्पर्धेची आठवण करून देते. ही साधर्म्य सूचित करते की आपण एक सारणी विकसित करू शकतो ज्यामध्ये धातू आणि त्यांचे आयन त्यांची इलेक्ट्रॉन सोडण्याची प्रवृत्ती यावर आधारित सूचीबद्ध केले जातात जसे आपण आम्लांच्या बाबतीत आम्लांची ताकद दर्शवण्यासाठी करतो. खरं तर आपण आधीच काही तुलना केली आहे. तुलनेद्वारे आपल्याला हे कळले आहे की जस्त तांब्याला इलेक्ट्रॉन सोडतो आणि तांबे सिल्व्हरला इलेक्ट्रॉन सोडते आणि म्हणून, धातूंची इलेक्ट्रॉन सोडण्याची प्रवृत्ती या क्रमाने आहे: $\mathrm{Zn}>\mathrm{Cu}>\mathrm{Ag}$. आम्ही आमची यादी अधिक विस्तृत करू इच्छितो आणि धातू क्रियाकलाप मालिका किंवा विद्युतरासायनिक मालिका रचू इच्छितो. विविध धातूंमधील इलेक्ट्रॉन्ससाठीची स्पर्धा आपल्याला गॅल्व्हानिक सेल नावाच्या सेलच्या वर्गाची रचना करण्यास मदत करते ज्यामध्ये रासायनिक अभिक्रिया विद्युत ऊर्जेचा स्रोत बनतात. आपण या सेलबद्दल अधिक XII वीत अभ्यास करू.
८.३ ऑक्सिडेशन संख्या
इलेक्ट्रॉन स्थानांतरणाचे एक कमी स्पष्ट उदाहरण हायड्रोजन ऑक्सिजनसोबत संयोग पावून पाणी तयार करते तेव्हा अनुभवले जाते:
$$2 \mathrm{H_2}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{H_2} \mathrm{O}(\mathrm{l})\tag{8.18}$$
त्याच्या दृष्टिकोनात सोपे नसले तरी, आपण $\mathrm{H}$ अणूला $\mathrm{H_2}$ मधील तटस्थ (शून्य) स्थितीतून $\mathrm{H_2} \mathrm{O}$ मधील धनात्मक स्थितीत जाताना पाहू शकतो, $\mathrm{O}$ अणू $\mathrm{O_2}$ मधील शून्य स्थितीतून $\mathrm{H_2} \mathrm{O}$ मधील द्विऋणात्मक स्थितीत जातो. असे गृहीत धरले जाते की $\mathrm{H}$ वरून $\mathrm{O}$ वर इलेक्ट्रॉन स्थानांतरण होते आणि परिणामी $\mathrm{H_2}$ चे ऑक्सिडेशन होते आणि $\mathrm{O_2}$ चे रिडक्शन होते.
तथापि, जसे आपण नंतर पाहू, विद्युतभार स्थानांतरण केवळ आंशिक आहे आणि कदाचित $\mathrm{H}$ द्वारे इलेक्ट्रॉनचे संपूर्ण नुकसान आणि O द्वारे लाभ यापेक्षा इलेक्ट्रॉन शिफ्ट म्हणून वर्णन करणे अधिक योग्य ठरेल. समीकरण (८.१८) बाबत येथे जे सांगितले गेले आहे ते सहसंयुज संयुगे समाविष्ट असलेल्या इतर अनेक अभिक्रियांसाठी खरे असू शकते. या वर्गातील अभिक्रियांची दोन उदाहरणे आहेत:
$$\mathrm{H_2}(\mathrm{~s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{HCl}(\mathrm{g})\tag{8.19}$$
आणि,
$$\mathrm{CH_4}(\mathrm{~g})+4 \mathrm{Cl_2}(\mathrm{~g}) \rightarrow \mathrm{CCl_4}(\mathrm{l})+4 \mathrm{HCl}(\mathrm{g})\tag{8.20}$$
सहसंयुज संयुगांची निर्मिती समाविष्ट असलेल्या रासायनिक अभिक्रियांमध्ये इलेक्ट्रॉन शिफ्टचा मागोवा ठेवण्यासाठी, ऑक्सिडेशन संख्या वापरण्याची एक अधिक व्यावहारिक पद्धत विकसित करण्यात आली आहे. या पद्धतीमध्ये, नेहमी असे गृहीत धरले जाते की कमी विद्युतऋणात्मक अणूपासून अधिक विद्युतऋणात्मक अणूकडे इलेक्ट्रॉनचे संपूर्ण स्थानांतरण होते. उदाहरणार्थ, आपण अभिक्रियेचा भाग बनणाऱ्या प्रत्येक अणूवरील विद्युतभार दर्शवण्यासाठी समीकरणे (८.१८ ते ८.२०) पुन्हा लिहितो:
$$ \begin{array}{cccc} 2 \stackrel{0}{\mathrm{H_2}}(\mathrm{~g}) + \stackrel{0}{\mathrm{O_2}}(\mathrm{~g}) & \rightarrow & 2 \stackrel{+1}{\mathrm{H_2}} \stackrel{-2}{\mathrm{O}}(\mathrm{l}) \tag{8.21} \end{array} $$
$$ \begin{array}{llll} \stackrel {0}{\mathrm{H_2}}(\mathrm{~s}) + \stackrel{0}{\mathrm{Cl_2}}(\mathrm{~g}) & \rightarrow & 2 \stackrel{+1-1}{\mathrm{HCl}}(\mathrm{g}) \tag{8.22} \end{array} $$
$$ \begin{array}{cccc} \stackrel{-4 +1}{\mathrm{CH_4}}(\mathrm{~g}) + & 4 \stackrel{0}{\mathrm{Cl_2}}(\mathrm{~g}) \rightarrow & \stackrel{+4 -1}{\mathrm{C}\mathrm{Cl_4}} (\mathrm{l})+4 \stackrel{+1 -1 }{\mathrm{H } \mathrm{Cl}} (\mathrm{g})\tag{8.23} \end{array} $$
हे जोर देऊन सांगता येईल की इलेक्ट्रॉन स्थानांतरणाची धारणा केवळ हिशोब ठेवण्याच्या हेतूने केली जाते आणि या युनिटमध्ये नंतरच्या टप्प्यावर हे स्पष्ट होईल की ते रेडॉक्स अभिक्रियांच्या सोप्या वर्णनाकडे नेतो.
ऑक्सिडेशन संख्या एखाद्या संयुगातील मूलद्रव्याची ऑक्सिडेशन स्थिती दर्शवते जी नियमांच्या संचानुसार निश्चित केली जाते जी या आधारावर तयार केली जाते की सहसंयुज बंधातील इलेक्ट्रॉन जोडी पूर्णपणे अधिक विद्युतऋणात्मक मूलद्रव्याशी संबंधित असते.
एखाद्या संयुग/आयनमध्ये कोणते मूलद्रव्य दुसऱ्यापेक्षा अधिक विद्युतऋणात्मक आहे हे नेहमी लक्षात ठेवणे किंवा सहज कळणे शक्य नसते. म्हणून, एखाद्या संयुग/








