इकाई 10 हॅलोअल्केन्स आणि हॅलोअरीन्स
हॅलोजनयुक्त संयुगे मातीतील जीवाणूंद्वारे विघटन होण्यास प्रतिरोधक असल्यामुळे पर्यावरणात टिकून राहतात.
अलिफॅटिक किंवा सुगंधी हायड्रोकार्बनमधील हायड्रोजन अणू(ची) जागी हॅलोजन अणू(ची) प्रतिस्थापना केल्यास अनुक्रमे अल्किल हॅलाइड (हॅलोअल्केन) आणि आरिल हॅलाइड (हॅलोअरीन) तयार होतात. हॅलोअल्केन्समध्ये अल्किल गटाच्या sp³ संकरित कार्बन अणूशी हॅलोजन अणू(ची) जोडलेली असते तर हॅलोअरीन्समध्ये आरिल गटाच्या sp² संकरित कार्बन अणू(शी) हॅलोजन अणू(ची) जोडलेली असतात. अनेक हॅलोजनयुक्त सेंद्रिय संयुगे निसर्गात आढळतात आणि त्यापैकी काही वैद्यकीयदृष्ट्या उपयुक्त आहेत. या वर्गातील संयुगांना उद्योगात तसेच दैनंदिन जीवनात मोठ्या प्रमाणात उपयोग आहे. ते तुलनेने अध्रुवीय संयुगांसाठी द्रावक म्हणून आणि विस्तृत श्रेणीतील सेंद्रिय संयुगांच्या संश्लेषणासाठी प्रारंभिक साहित्य म्हणून वापरले जातात. सूक्ष्मजीवांद्वारे तयार होणारे क्लोरीनयुक्त प्रतिजैविक, क्लोरॅम्फेनिकॉल, टायफॉइड ज्वराच्या उपचारासाठी अत्यंत प्रभावी आहे. आपले शरीर आयोडीनयुक्त संप्रेरक, थायरॉक्सिन तयार करते, ज्याच्या कमतरतेमुळे गलगंड नावाचा रोग होतो. कृत्रिम हॅलोजन संयुगे, उदा. क्लोरोक्विन मलेरियाच्या उपचारासाठी वापरली जाते; हॅलोथेन शस्त्रक्रिया दरम्यान भूल देण्यासाठी वापरले जाते. काही पूर्णतः फ्लोरिनेटेड संयुगे शस्त्रक्रियेत संभाव्य रक्त पर्याय म्हणून विचारात घेतली जात आहेत.
या इकाईमध्ये, तुम्ही ऑर्गॅनोहॅलोजन संयुगांच्या तयार करण्याच्या महत्त्वाच्या पद्धती, भौतिक आणि रासायनिक गुणधर्म आणि उपयोगांचा अभ्यास कराल.
10.1 वर्गीकरण
हॅलोअल्केन्स आणि हॅलोअरीन्सचे वर्गीकरण खालीलप्रमाणे केले जाऊ शकते:
10.1.1 हॅलोजन अणूंच्या संख्येच्या आधारे
त्यांच्या रचनेत एक, दोन किंवा अधिक हॅलोजन अणू आहेत यावर अवलंबून त्यांचे मोनो, डाय, किंवा पॉलीहॅलोजन (ट्राय-, टेट्रा- इ.) संयुगे असे वर्गीकरण केले जाऊ शकते. उदाहरणार्थ,

मोनोहॅलोसंयुगांचे पुढे हॅलोजन ज्या कार्बन अणूशी बंधित आहे त्या कार्बन अणूच्या संकरणाच्या आधारे वर्गीकरण केले जाऊ शकते, जसे खाली चर्चा केली आहे.
10.1.2 $\mathbf{s p}^{\mathbf{3}} \mathbf{~C}-\mathbf{X}$ बंध असलेली संयुगे (X= F, Cl, Br, I)
या वर्गात समाविष्ट आहेत
(अ) अल्किल हॅलाइड्स किंवा हॅलोअल्केन्स ( $\mathbf{R}-\mathbf{X}$ )
अल्किल हॅलाइड्समध्ये, हॅलोजन अणू अल्किल गटाशी $(\mathrm{R})$ बंधित असतो. ते $\mathrm{C} _{\mathrm{n}} \mathrm{H} _{2 \mathrm{n}+1} \mathrm{X}$ द्वारे दर्शविलेल्या समसंरचन मालिकेची निर्मिती करतात. हॅलोजन ज्या कार्बनशी जोडलेले आहे त्या कार्बनाच्या स्वरूपानुसार त्यांचे पुढे प्राथमिक, द्वितीयक किंवा तृतीयक असे वर्गीकरण केले जाते. जर अल्किल हॅलाइडमध्ये हॅलोजन प्राथमिक कार्बन अणूशी जोडलेले असेल, तर अल्किल हॅलाइडला प्राथमिक अल्किल हॅलाइड किंवा ($1^{\circ}$) अल्किल हॅलाइड म्हणतात. त्याचप्रमाणे, जर हॅलोजन द्वितीयक किंवा तृतीयक कार्बन अणूशी जोडलेले असेल, तर अल्किल हॅलाइडला अनुक्रमे द्वितीयक अल्किल हॅलाइड ($2^{\circ}$) आणि तृतीयक ($3^{\circ}$) अल्किल हॅलाइड म्हणतात.

(ब) अलायलिक हॅलाइड्स
ही अशी संयुगे आहेत ज्यामध्ये हॅलोजन अणू कार्बन-कार्बन दुहेरी बंध $(\mathrm{C}=\mathrm{C})$ च्या समीप असलेल्या $s p^{3}$-संकरित कार्बन अणूशी बंधित असतो म्हणजेच अलायलिक कार्बनशी.

(क) बेंझिलिक हॅलाइड्स
ही अशी संयुगे आहेत ज्यामध्ये हॅलोजन अणू सुगंधी वलयाशी जोडलेल्या $s p^{3}$-संकरित कार्बन अणूशी बंधित असतो.

10.1.3 $\boldsymbol{s p}^{2} \mathrm{C}-\mathrm{X}$ बंध असलेली संयुगे
या वर्गात समाविष्ट आहेत:
(अ) विनायलिक हॅलाइड्स
ही अशी संयुगे आहेत ज्यामध्ये हॅलोजन अणू कार्बन-कार्बन दुहेरी बंध $(\mathrm{C}=\mathrm{C})$ च्या $s p^{2}$-संकरित कार्बन अणूशी बंधित असतो.

(ब) आरिल हॅलाइड्स
ही अशी संयुगे आहेत ज्यामध्ये हॅलोजन अणू थेट सुगंधी वलयाच्या $s p^{2}$-संकरित कार्बन अणूशी बंधित असतो.

10.2 नामकरण
हॅलोजनेटेड संयुगांचे वर्गीकरण शिकल्यानंतर, आता ही संयुगे कशी नावे दिली जातात ते शिकूया. अल्किल हॅलाइड्सची सामान्य नावे अल्किल गटाचे नाव देऊन त्यानंतर हॅलाइडचे नाव देऊन तयार केली जातात. IUPAC नामकरण पद्धतीमध्ये, अल्किल हॅलाइड्सचे नाव हॅलो-प्रतिस्थापित हायड्रोकार्बन्स असे दिले जाते. बेंझिनच्या मोनो हॅलोजन प्रतिस्थापित व्युत्पन्नांसाठी, सामान्य आणि IUPAC नावे सारखीच असतात. डायहॅलोजन व्युत्पन्नांसाठी, सामान्य पद्धतीत $o^{-,}, m_{-}, p$ - उपसर्ग वापरले जातात परंतु IUPAC पद्धतीमध्ये, जसे तुम्ही इयत्ता XI मध्ये शिकलात, तेथे 1,$2 ; 1,3$ आणि 1,4 अंक वापरले जातात.

समान प्रकारचे हॅलोजन अणू असलेल्या डायहॅलोअल्केन्सचे नाव अल्किलिडीन किंवा अल्किलीन डायहॅलाइड्स असे दिले जाते. दोन्ही हॅलोजन अणू असलेल्या डायहॅलो-संयुगांचे पुढे जेमिनल हॅलाइड्स किंवा जेम-डायहॅलाइड्स असे वर्गीकरण केले जाते जेव्हा दोन्ही हॅलोजन अणू साखळीच्या एकाच कार्बन अणूवर उपस्थित असतात आणि व्हिसिनल हॅलाइड्स किंवा व्हिक-डायहॅलाइड्स असे वर्गीकरण केले जाते जेव्हा हॅलोजन अणू समीप कार्बन अणूंवर उपस्थित असतात. सामान्य नाव पद्धतीत, जेम-डायहॅलाइड्सचे नाव अल्किलिडीन हॅलाइड्स असे आणि व्हिक-डायहॅलाइड्सचे नाव अल्किलीन डायहॅलाइड्स असे दिले जाते. IUPAC पद्धतीमध्ये, त्यांचे नाव डायहॅलोअल्केन्स असे दिले जाते.
हॅलोसंयुगांची काही सामान्य उदाहरणे तक्ता 10.1 मध्ये नमूद केली आहेत.

उदाहरण 10.1
$\mathrm{C_5} \mathrm{H_11} \mathrm{Br}$ हे आण्विक सूत्र असलेल्या सर्व आठ संरचनात्मक समावयवांची रचना काढा. प्रत्येक समावयवाचे IUPAC पद्धतीनुसार नाव द्या आणि त्यांचे प्राथमिक, द्वितीयक किंवा तृतीयक ब्रोमाइड असे वर्गीकरण करा.
उकल
| $\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{CH}_2 \mathrm{CH}_2 \mathrm{CH}_2 \mathrm{Br}$ | 1-ब्रोमोपेन्टेन (1 $\left.{ }^{\circ}\right)$ |
|---|---|
| $\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{CH}_2 \mathrm{CH}(\mathrm{Br}) \mathrm{CH}_3$ | 2-ब्रोमोपेन्टेन $\left(2^{\circ}\right)$ |
| $\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{CH}(\mathrm{Br}) \mathrm{CH}_2 \mathrm{CH}_3$ | 3-ब्रोमोपेन्टेन (2 $\left.{ }^{\circ}\right)$ |
| $\left(\mathrm{CH}_3\right)_2 \mathrm{CHCH}_2 \mathrm{CH}_2 \mathrm{Br}$ | 1-ब्रोमो-3-मेथिलब्युटेन (1 $\left.{ }^{\circ}\right)$ |
| $\left(\mathrm{CH}_3\right)_2 \mathrm{CHCHBrCH}_3$ | 2-ब्रोमो-3-मेथिलब्युटेन(2 $\left.{ }^{\circ}\right)$ |
| $\left(\mathrm{CH}_3\right)_2 \mathrm{CBrCH}_2 \mathrm{CH}_3$ | 2-ब्रोमो-2-मेथिलब्युटेन $\left(3^{\circ}\right)$ |
| $\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{CH}\left(\mathrm{CH}_3\right) \mathrm{CH}_2 \mathrm{Br}$ | 1-ब्रोमो-2-मेथिलब्युटेन(1 $\left.{ }^{\circ}\right)$ |
| $\left(\mathrm{CH}_3\right)_3 \mathrm{CCH}_2 \mathrm{Br}$ | 1-ब्रोमो-2,2-डायमेथिलप्रोपेन (1 $\left.{ }^{\circ}\right)$ |
उदाहरण 10.2 खालील संयुगांची IUPAC नावे लिहा:

उकल
(i) 4-ब्रोमोपेन्ट-2-ईन
(ii) 3-ब्रोमो-2-मेथिलब्युट-1-ईन
(iii) 4-ब्रोमो-3-मेथिलपेन्ट-2-ईन
(iv) 1-ब्रोमो-2-मेथिलब्युट-2-ईन
(v) 1-ब्रोमोब्युट-2-ईन
(vi) 3-ब्रोमो-2-मेथिलप्रोपीन
10.3 C-X बंधाचे स्वरूप
हॅलोजन अणू कार्बनपेक्षा अधिक विद्युतऋण असल्याने, अल्किल हॅलाइडचा कार्बन-हॅलोजन बंध ध्रुवीकृत असतो; कार्बन अणूवर आंशिक धनभार असतो तर हॅलोजन अणूवर आंशिक ऋणभार असतो.
आपण नियतकालिक सारणीतील गटात खाली जाताना, हॅलोजन अणूचा आकार वाढतो. फ्लोरिन अणू सर्वात लहान आणि आयोडिन अणू सर्वात मोठा असतो. परिणामी कार्बन-हॅलोजन बंध लांबी देखील $\mathrm{C}-\mathrm{F}$ ते $\mathrm{C}-\mathrm{I}$ पर्यंत वाढते. काही विशिष्ट बंध लांबी, बंध एन्थाल्पी आणि द्विध्रुवीय आघूर्ण तक्ता 10.2 मध्ये दिले आहेत.
अल्किल हॅलाइड्स अल्कोहोलपासून सर्वोत्तम तयार केले जातात, जी सहज उपलब्ध असतात.
तक्ता 10.2: कार्बन-हॅलोजन (C—X) बंध लांबी, बंध एन्थाल्पी आणि द्विध्रुवीय आघूर्ण
| बंध | बंध लांबी/pm | C-X बंध एन्थाल्पी/ kJmol ${ }^{-1}$ | द्विध्रुवीय आघूर्ण/डेबाई |
|---|---|---|---|
| $\mathrm{CH}_3-\mathrm{F}$ | 139 | 452 | 1.847 |
| $\mathrm{CH}_3-\mathrm{Cl}$ | 178 | 351 | 1.860 |
| $\mathrm{CH}_3-\mathrm{Br}$ | 193 | 293 | 1.830 |
| $\mathrm{CH}_3-\mathrm{I}$ | 214 | 234 | 1.636 |
10.4 हॅलोअल्केन्स तयार करण्याच्या पद्धती
10.4.1 अल्कोहोलपासून
अल्कोहोलचा हायड्रॉक्सिल गट संहत हॅलोजन ऍसिड, फॉस्फरस हॅलाइड किंवा थायोनिल क्लोराईडसह अभिक्रिया करताना हॅलोजनद्वारे बदलला जातो. थायोनिल क्लोराईड प्राधान्य दिले जाते कारण या अभिक्रियेत अल्किल हॅलाइड वायू $\mathrm{SO_2}$ आणि $\mathrm{HCl}$ सह तयार होते. दोन्ही वायू उत्पादने बाहेर पडू शकतात, म्हणून, अभिक्रिया शुद्ध अल्किल हॅलाइड्स देते. प्राथमिक आणि द्वितीयक अल्कोहोलच्या $\mathrm{HCl}$ सह अभिक्रियांसाठी उत्प्रेरकाची उपस्थिती, $\mathrm{ZnCl_2}$ आवश्यक असते. तृतीयक अल्कोहोलसह, अभिक्रिया फक्त संहत $\mathrm{HCl}$ सह अल्कोहोल खोलीच्या तापमानात हलवून केली जाते. $\mathrm{HBr}(48 %)$ सह सतत उकळत ठेवून अल्किल ब्रोमाइड तयार करण्यासाठी वापरले जाते. R-I चे चांगले उत्पादन 95% ऑर्थोफॉस्फोरिक ऍसिडमध्ये सोडियम किंवा पोटॅशियम आयोडाईडसह अल्कोहोल गरम करून मिळवता येते. दिलेल्या हॅलोऍसिडसह अल्कोहोलची अभिक्रियाशीलतेची क्रमवारी $3^{\circ}>2^{\circ}>1^{\circ}$ आहे. फॉस्फरस ट्रायब्रोमाइड आणि ट्रायआयोडाइड सहसा रेड फॉस्फरसची ब्रोमिन आणि आयोडिनसह अनुक्रमे अभिक्रिया करून इन सिटू (अभिक्रिया मिश्रणात तयार) तयार केले जातात.
$$ \begin{aligned} & \mathrm{R}-\mathrm{OH}+\mathrm{HCl} \xrightarrow{\mathrm{ZnCl_2}} \mathrm{R}-\mathrm{Cl}+\mathrm{H_2} \mathrm{O} \\ & \mathrm{R}-\mathrm{OH}+\mathrm{NaBr}+\mathrm{H_2} \mathrm{SO_4} \longrightarrow \mathrm{R}-\mathrm{Br}+\mathrm{NaHSO_4}+\mathrm{H_2} \mathrm{O} \\ & 3 \mathrm{R}-\mathrm{OH}+\mathrm{PX_3} \longrightarrow 3 \mathrm{R}-\mathrm{X}+\mathrm{H_3} \mathrm{PO_3} \quad(\mathrm{X}=\mathrm{Cl}, \mathrm{Br}) \\ & \mathrm{R}-\mathrm{OH}+\mathrm{PCl_5} \longrightarrow \mathrm{R}-\mathrm{Cl}+\mathrm{POCl_3}+\mathrm{HCl} \\ & \mathrm{R}-\mathrm{OH}+\frac{\mathrm{red} \mathrm{P} / \mathrm{X_2}}{\mathrm{X_2}=\mathrm{Br_2}, \mathrm{I_2}} \mathrm{R}-\mathrm{X} \\ & \mathrm{R}-\mathrm{OH}+\mathrm{SOCl_2} \longrightarrow \mathrm{R}-\mathrm{Cl}+\mathrm{SO_2}+\mathrm{HCl} \end{aligned} $$
अल्किल क्लोराईड तयार करणे एकतर अल्कोहोलच्या द्रावणातून कोरडा हायड्रोजन क्लोराईड वायू पास करून किंवा अल्कोहोल आणि संहत जलीय हॅलोजन ऍसिडचे मिश्रण गरम करून केले जाते.
वरील पद्धती फिनॉल्ससाठी लागू होत नाहीत कारण फिनॉल्समधील कार्बन-ऑक्सिजन बंधात आंशिक दुहेरी बंध वैशिष्ट्य असते आणि एकल बंधापेक्षा मजबूत असल्यामुळे तोडणे कठीण असते.
10.4.2 हायड्रोकार्बनपासून
(I) अल्केन्सपासून मुक्त मूलगामी हॅलोजनेशनद्वारे
अल्केन्सचे मुक्त मूलगामी क्लोरीनेशन किंवा ब्रोमिनेशन समावयवी मोनो- आणि पॉलीहॅलोअल्केन्सचे जटिल मिश्रण देते, जे शुद्ध संयुगे म्हणून वेगळे करणे कठीण असते. परिणामी, कोणत्याही एकल संयुगाचे उत्पादन कमी असते.
$\mathrm{CH_3}\mathrm{CH_2}\mathrm{CH_2}\mathrm{CH_3} \xrightarrow[ \text {or heat}]{\mathrm{Cl_2} \text {/UV} \quad \text {light}} \mathrm{CH_3}\mathrm{CH_2}\mathrm{CH_2}\mathrm{CH_2}\mathrm{Cl_2} + \mathrm{CH_3}\mathrm{CH_2}\mathrm{CHCl}\mathrm{CH_3} $
(II) अल्केन्सपासून
(i) हायड्रोजन हॅलाइड्सची बेरीज: अल्कीन हायड्रोजन क्लोराईड, हायड्रोजन ब्रोमाइड किंवा हायड्रोजन आयोडाइडसह अभिक्रिया करून संबंधित अल्किल हॅलाइडमध्ये रूपांतरित केले जाते.
प्रोपीन दोन उत्पादने देते, तथापि मार्कोव्हनिकोव्हच्या नियमानुसार फक्त एक प्रबळ असते. (इकाई 13, इयत्ता XI)
$$ \mathrm{CH_3} \mathrm{CH}=\mathrm{CH_2}+\mathrm{H}-\mathrm{I} \longrightarrow \underset {\text{minor}}{\mathrm{CH_3} \mathrm{CH_2} \mathrm{CH_2} \mathrm{I}} + \underset{ \text{major }}{\mathrm{CH_3} \mathrm{CHICH_3}} $$
(ii) हॅलोजन्सची बेरीज: प्रयोगशाळेत, $\mathrm{CCl}_{4}$ मधील ब्रोमिनची बेरीज अल्कीनमध्ये केल्याने ब्रोमिनचा लालसर तपकिरी रंग निघून जाणे हे रेणूमध्ये दुहेरी बंध शोधण्यासाठी एक महत्त्वाची पद्धत आहे. बेरीजमुळे व्हिक-डायब्रोमाइड्सचे संश्लेषण होते, जे रंगहीन असतात (इकाई 9, इयत्ता XI).

उदाहरण 10.3
$\left(\mathrm{CH_3}\right)_{2} \mathrm{CHCH_2} \mathrm{CH_3}$ च्या मुक्त मूलगामी मोनोक्लोरीनेशनवर तयार होण्याची अपेक्षा असलेल्या सर्व संभाव्य मोनोक्लोरो संरचनात्मक समावयव ओळखा.
उकल
दिलेल्या रेणूमध्ये, चार वेगवेगळ्या प्रकारचे हायड्रोजन अणू आहेत. या हायड्रोजन अणूंची प्रतिस्थापना खालीलप्रमाणे देईल
| $\left(\mathrm{CH_3}\right)_{2} \mathrm{CHCH_2} \mathrm{CH_2} \mathrm{Cl}$ | $\left(\mathrm{CH_3}\right)_{2} \mathrm{CHCH}(\mathrm{Cl}) \mathrm{CH_3}$ |
|---|---|
| $\left(\mathrm{CH_3}\right)_{2} \mathrm{C}(\mathrm{Cl}) \mathrm{CH_2} \mathrm{CH_3}$ | $\mathrm{CH_3} \mathrm{CH}\left(\mathrm{CH_2} \mathrm{Cl_2} \mathrm{CH_2} \mathrm{CH_3}\right).$ |
10.4.3 हॅलोजन विनिमय
अल्किल आयोडाइड्स सहसा कोरड्या ॲसिटोनमध्ये NaI सह अल्किल क्लोराइड/ब्रोमाइडच्या अभिक्रियेद्वारे तयार केले जातात. या अभिक्रियेला फिंकेलस्टाइन अभिक्रिया म्हणतात.
$$ \begin{aligned} & \mathrm{R}-\mathrm{X}+\mathrm{NaI} \longrightarrow \mathrm{R}-\mathrm{I}+\mathrm{NaX} \\ & \mathrm{X}=\mathrm{Cl}, \mathrm{Br} \end{aligned} $$
अशाप्रकारे तयार झालेले NaCl किंवा NaBr कोरड्या ॲसिटोनमध्ये बसते. हे ली शॅटेलियरच्या तत्त्वानुसार पुढच्या अभिक्रियेला सुलभ करते. अल्किल फ्लोराइड्सचे संश्लेषण $\mathrm{AgF}, \mathrm{Hg}_2 \mathrm{~F}_2, \mathrm{CoF}_2$ किंवा $\mathrm{SbF}_3$ सारख्या धातूच्या फ्लोराईडच्या उपस्थितीत अल्किल क्लोराईड/ब्रोमाइड गरम करून सर्वोत्तम साध्य केले जाते. या अभिक्रियेला $\mathrm{Swarts}$ अभिक्रिया म्हणतात.
$$ \mathrm{H}_3 \mathrm{C}-\mathrm{Br}+\mathrm{AgF} \longrightarrow \mathrm{H}_3 \mathrm{C}-\mathrm{F}+\mathrm{AgBr} $$
उदाहरण 6.3 $\left(\mathrm{CH}_3\right)_2 \mathrm{CHCH}_2 \mathrm{CH}_3$ च्या मुक्त मूलगामी मोनोक्लोरीनेशनवर तयार होण्याची अपेक्षा असलेल्या सर्व संभाव्य मोनोक्लोरो संरचनात्मक समावयव ओळखा.
उकल
दिलेल्या रेणूमध्ये, चार वेगवेगळ्या प्रकारचे हायड्रोजन अणू आहेत. या हायड्रोजन अणूंची प्रतिस्थापना खालीलप्रमाणे देईल
$\left(\mathrm{CH} _{3}\right) _{2} \mathrm{CHCH} _{2} \mathrm{CH} _{2} \mathrm{Cl}$,
$\left(\mathrm{CH} _{3}\right) _{2} \mathrm{CHCH}(\mathrm{Cl}) \mathrm{CH} _{3}$,
$\left(\mathrm{CH} _{3}\right) _{2} \mathrm{C}(\mathrm{Cl}) \mathrm{CH} _{2} \mathrm{CH} _{3}$,
$\mathrm{CH} _{3} \mathrm{CH}\left(\mathrm{CH} _{2} \mathrm{Cl}\right) \mathrm{CH} _{2} \mathrm{CH} _{3}$
10.5 हॅलोअरीन्स तयार करणे
(i) हायड्रोकार्बनपासून इलेक्ट्रोफिलिक प्रतिस्थापनद्वारे आरिल क्लोराइड्स आणि ब्रोमाइड्स अनुक्रमे क्लोरीन आणि ब्रोमिनसह आरिन्सचे लोह किंवा लोह(III) क्लोराईड सारख्या लुईस ऍसिड उत्प्रेरकांच्या उपस्थितीत इलेक्ट्रोफिलिक प्रतिस्थापन करून सहज तयार केले जाऊ शकतात.

ऑर्थो आणि पॅरा समावयव त्यांच्या द्रावणांकातील मोठ्या फरकामुळे सहज वेगळे केले जाऊ शकतात. आयोडिनसह अभिक्रिया स्वभावतः प्रतिवर्ती असतात आणि आयोडिनेशन दरम्यान तयार झालेला $\mathrm{HI}$ ऑक्सिडाइज करण्यासाठी ऑक्सिडायझिंग एजंट ($\left(\mathrm{HNO_3}\right).$, $\mathrm{HIO_4}$) ची उपस्थिती आवश्यक असते. फ्लोरिनच्या उच्च अभिक्रियाशीलतेमुळे फ्लोरो संयुगे या पद्धतीने तयार केली जात नाहीत.
(ii) ॲमाइन्सपासून सँडमायरच्या अभिक्रियेद्वारे
जेव्हा प्राथमिक सुगंधी ॲमीन, थंड जलीय खनिज ऍसिडमध्ये विरघळलेली किंवा निलंबित केलेली असते, तेव्हा तिच्यावर सोडियम नायट्राईटची क्रिया केली जाते, तेव्हा डायझोनियम क्षार तयार होतो. ताजे तयार केलेल्या डायझोनियम क्षाराचे द्रावण क्युप्रस क्लोराईड किंवा क्युप्रस ब्रोमाइडसह मिसळल्यास डायझोनियम गटाची जागा $-\mathrm{Cl}$ किंवा $-\mathrm{Br}$ ने घेतली जाते.

डायझोनियम गटाची जागा आयोडिनने घेण्यासाठी क्युप्रस हॅलाइडची उपस्थिती आवश्यक नसते आणि ते फक्त डायझोनियम क्षार पोटॅशियम आयोडाईडसह हलवून केले जाते.

उदाहरण 10.4 खालील अभिक्रियांची उत्पादने लिहा:

उकल

10.6 भौतिक गुणधर्म
अल्किल हॅलाइड्स शुद्ध असताना रंगहीन असतात. तथापि, ब्रोमाइड्स आणि आयोडाइड्स प्रकाशात आल्यावर रंग विकसित करतात. अनेक अस्थिर हॅलोजन संयुगांना गोड वास येतो.
द्रावणांक आणि उत्कलनांक
मिथिल क्लोराईड, मिथिल ब्रोमाइड, इथिल क्लोराईड आणि काही क्लोरोफ्लोरोमिथेन्स खोलीच्या तापमानात वायू असतात. उच्च सदस्य द्रव किंवा घन असतात. जसे आपण आधीच शिकलो आहोत, सेंद्रिय हॅलोजन संयुगांचे रेणू सामान्यतः ध्रुवीय असतात. मूळ हायड्रोकार्बनच्या तुलनेत अधिक ध्रुवीयता तसेच उच्च आण्विक वस्तुमानामुळे, हॅलोजन व्युत्पन्नांमध्ये आंतर-आण्विक आकर्षण शक्ती (द्विध्रुव-द्विध्रुव आणि व्हॅन डर वाल्स) अधिक मजबूत असतात. म्हणूनच तुलनेय आण्विक वस्तुमान असलेल्या हायड्रोकार्बन्सपेक्षा क्लोराइड्स, ब्रोमाइड्स आणि आयोडाइड्सचे उत्कलनांक लक्षणीयरीत्या जास्त असतात.
रेणू आकाराने मोठे होतात आणि अधिक इलेक्ट्रॉन असतात तसतसे आकर्षण शक्ती मजबूत होतात. विविध हॅलाइड्सच्या उत्कलनांकातील बदलाचा नमुना आकृती 10.1 मध्ये दर्शविला आहे. समान अल्किल गटासाठी, अल्किल हॅलाइड्सचे उत्कलनांक खालील क्रमाने कमी होतात: $\mathrm{RI}>\mathrm{RBr}>\mathrm{RCl}>\mathrm{RF}$. याचे कारण असे की हॅलोजन अणूचा आकार आणि वस्तुमान वाढल्याने व्हॅन डर वाल्स शक्तींची तीव्रता वाढते.
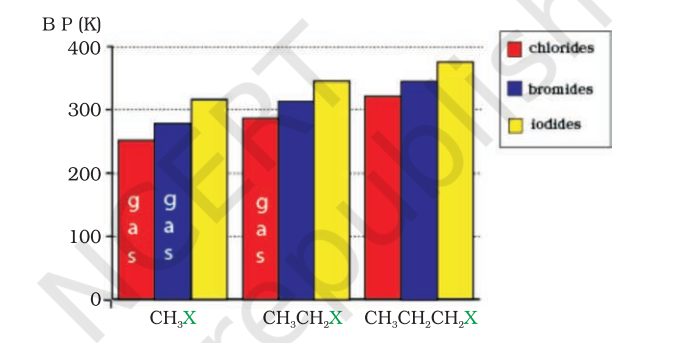
आकृती 10.1: काही अल्किल हॅलाइड्सच्या उत्कलनांकांची तुलना
शाखायुक्तता वाढल्याने समावयवी हॅलोअल्केन्सचे उत्कलनांक कमी होतात (इकाई 12, इयत्ता XI). उदाहरणार्थ, 2-ब्रोमो-2- मेथिलप्रोपेनचे उत्कलनांक तीन समावयवांपैकी सर्वात कमी असते.
$\mathrm{CH_3} \mathrm{CH_2} \mathrm{CH_2} \mathrm{CH_2} \mathrm{Br}$
समावयवी डायहॅलोबेंझिन्सचे उत्कलनांक जवळजवळ सारखेच असतात. तथापि, पॅरा-समावयव त्यांच्या ऑर्थो- आणि मेटा-समावयवांच्या तुलनेत उच्च द्रावणांकाचे असतात. हे पॅरा-समावयवांच्या सममितीमुळे आहे जे ऑर्थो- आणि मेटा-समावयवांच्या तुलनेत स्फटिक जाळीत चांगले बसते.

घनता
हायड्रोकार्बन्सचे ब्रोमो, आयोडो आणि पॉलीक्लोरो व्युत्पन्न पाण्यापेक्षा जड असतात. कार्बन अणूंची संख्या, हॅलोजन अणूंची संख्या आणि हॅलोजन अणूंचे अणु








