ଅଧ୍ୟାୟ 08 ରେଡକ୍ସ ପ୍ରତିକ୍ରିୟା
“ଯେଉଁଠାରେ ଅମ୍ଳୀକରଣ ଅଛି, ସେଠାରେ ସର୍ବଦା ପ୍ରତିକ୍ରିୟା ଅଛି ରସାୟନ ବିଜ୍ଞାନ ମୂଳତଃ ରେଡକ୍ସ ପ୍ରଣାଳୀର ଏକ ଅଧ୍ୟୟନ।”
ରସାୟନ ବିଜ୍ଞାନ ବିଭିନ୍ନ ପ୍ରକାରର ପଦାର୍ଥ ଏବଂ ଗୋଟିଏ ପ୍ରକାରର ପଦାର୍ଥକୁ ଅନ୍ୟ ପ୍ରକାରରେ ପରିବର୍ତ୍ତନ ସହିତ ଜଡିତ। ବିଭିନ୍ନ ପ୍ରକାରର ପ୍ରତିକ୍ରିୟା ମାଧ୍ୟମରେ ଗୋଟିଏ ପ୍ରକାରର ପଦାର୍ଥରୁ ଅନ୍ୟ ପ୍ରକାରରେ ରୂପାନ୍ତରଣ ଘଟେ। ଏହିପରି ପ୍ରତିକ୍ରିୟାର ଏକ ଗୁରୁତ୍ୱପୂର୍ଣ୍ଣ ଶ୍ରେଣୀ ହେଉଛି ରେଡକ୍ସ ପ୍ରତିକ୍ରିୟା। ଅନେକ ଘଟଣା, ଯାହା ଭୌତିକ ଏବଂ ଜୈବିକ ଉଭୟ, ରେଡକ୍ସ ପ୍ରତିକ୍ରିୟା ସହିତ ଜଡିତ। ଏହି ପ୍ରତିକ୍ରିୟାଗୁଡିକ ଫାର୍ମାସ୍ୟୁଟିକାଲ୍, ଜୈବିକ, ଶିଳ୍ପ, ଧାତୁବିଜ୍ଞାନ ଏବଂ କୃଷି କ୍ଷେତ୍ରରେ ବ୍ୟାପକ ଭାବରେ ବ୍ୟବହୃତ ହୁଏ। ଘରୋଇ, ପରିବହନ ଏବଂ ଅନ୍ୟାନ୍ୟ ବାଣିଜ୍ୟିକ ଉଦ୍ଦେଶ୍ୟରେ ଶକ୍ତି ପାଇଁ ବିଭିନ୍ନ ପ୍ରକାରର ଇନ୍ଧନ ଜଳିବା, ଅତ୍ୟଧିକ ପ୍ରତିକ୍ରିୟାଶୀଳ ଧାତୁ ଏବଂ ଅଧାତୁ ଉଦ୍ଧାରଣ ପାଇଁ ବିଦ୍ୟୁତ୍ ରାସାୟନିକ ପ୍ରକ୍ରିୟା, କଷ୍ଟିକ ସୋଡା ପରି ରାସାୟନିକ ଯୌଗିକ ଉତ୍ପାଦନ, ଶୁଷ୍କ ଏବଂ ଆର୍ଦ୍ର ବ୍ୟାଟେରୀର କାର୍ଯ୍ୟ ଏବଂ ଧାତୁର କ୍ଷୟ ରେଡକ୍ସ ପ୍ରକ୍ରିୟାର ପରିସର ମଧ୍ୟରେ ପଡିଥାଏ ବୋଲି ଏହି ପ୍ରତିକ୍ରିୟାଗୁଡିକର ଗୁରୁତ୍ୱ ସ୍ପଷ୍ଟ ହୋଇଥାଏ। ସମ୍ପ୍ରତି, ହାଇଡ୍ରୋଜେନ୍ ଇକୋନୋମି (ଇନ୍ଧନ ଭାବରେ ତରଳ ହାଇଡ୍ରୋଜେନ୍ ବ୍ୟବହାର) ଏବଂ ‘ଓଜୋନ୍ ହୋଲ୍’ ର ବିକାଶ ପରି ପରିବେଶ ସମ୍ବନ୍ଧୀୟ ବିଷୟଗୁଡିକ ରେଡକ୍ସ ଘଟଣା ଅଧୀନରେ ଆସିବା ଆରମ୍ଭ କରିଛି।
8.1 ରେଡକ୍ସ ପ୍ରତିକ୍ରିୟାର ଶାସ୍ତ୍ରୀୟ ଧାରଣା - ଅମ୍ଳୀକରଣ ଏବଂ ପ୍ରତିକ୍ରିୟା ପ୍ରତିକ୍ରିୟା
ମୂଳତଃ, ଅମ୍ଳୀକରଣ ଶବ୍ଦଟି ଏକ ମୌଳିକ କିମ୍ବା ଏକ ଯୌଗିକରେ ଅମ୍ଳଜାନ ଯୋଗ କରିବା ପାଇଁ ବ୍ୟବହୃତ ହେଉଥିଲା। ବାୟୁମଣ୍ଡଳରେ ଡାଇଅକ୍ସିଜେନ୍ ଉପସ୍ଥିତି ହେତୁ (20%), ଅନେକ ମୌଳିକ ଏହା ସହିତ ମିଶ୍ରିତ ହୁଏ ଏବଂ ଏହା ହେଉଛି ମୁଖ୍ୟ କାରଣ ଯାହା ହେତୁ ସେଗୁଡିକ ସାଧାରଣତଃ ପୃଥିବୀରେ ସେମାନଙ୍କର ଅକ୍ସାଇଡ୍ ରୂପରେ ଦେଖାଯାଆନ୍ତି। ନିମ୍ନଲିଖିତ ପ୍ରତିକ୍ରିୟାଗୁଡିକ ଅମ୍ଳୀକରଣର ସୀମିତ ସଂଜ୍ଞା ଅନୁଯାୟୀ ଅମ୍ଳୀକରଣ ପ୍ରକ୍ରିୟାକୁ ପ୍ରତିନିଧିତ୍ୱ କରେ:
$$2 \mathrm{Mg}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{MgO}(\mathrm{s}) \tag{8.1}$$
$$\mathrm{S}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow \mathrm{SO_2}(\mathrm{~g}) \tag{8.2}$$
ପ୍ରତିକ୍ରିୟା (8.1) ଏବଂ (8.2) ରେ, ମ୍ୟାଗ୍ନେସିୟମ୍ ଏବଂ ସଲ୍ଫର୍ ମୌଳିକଗୁଡିକ ସେମାନଙ୍କରେ ଅମ୍ଳଜାନ ଯୋଗ ହେତୁ ଅମ୍ଳୀକୃତ ହୋଇଛି। ସେହିପରି, ମିଥେନ୍ ଏହାରେ ଅମ୍ଳଜାନ ଯୋଗ ହେତୁ ଅମ୍ଳୀକୃତ ହୋଇଛି।
$$\mathrm{CH} _{4}(\mathrm{~g})+2 \mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g})+2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{7.3}$$
ପ୍ରତିକ୍ରିୟା (8.3) ର ଏକ ସତର୍କ ପରୀକ୍ଷଣ ଯେଉଁଥିରେ ହାଇଡ୍ରୋଜେନ୍ ଅମ୍ଳଜାନ ଦ୍ୱାରା ପ୍ରତିସ୍ଥାପିତ ହୋଇଛି, ରସାୟନବିତ୍ମାନଙ୍କୁ ଏହାରୁ ହାଇଡ୍ରୋଜେନ୍ ଅପସାରଣ ଦୃଷ୍ଟିରୁ ଅମ୍ଳୀକରଣକୁ ପୁନର୍ବ୍ୟାଖ୍ୟା କରିବାକୁ ପ୍ରେରଣା ଦେଇଥିଲା ଏବଂ ତେଣୁ, ଅମ୍ଳୀକରଣ ଶବ୍ଦର ପରିସର ଏକ ପଦାର୍ଥରୁ ହାଇଡ୍ରୋଜେନ୍ ଅପସାରଣକୁ ଅନ୍ତର୍ଭୁକ୍ତ କରିବା ପାଇଁ ବିସ୍ତାରିତ ହୋଇଥିଲା। ନିମ୍ନଲିଖିତ ଉଦାହରଣଟି ଅନ୍ୟ ଏକ ପ୍ରତିକ୍ରିୟା ଯେଉଁଠାରେ ହାଇଡ୍ରୋଜେନ୍ ଅପସାରଣକୁ ଏକ ଅମ୍ଳୀକରଣ ପ୍ରତିକ୍ରିୟା ଭାବରେ ଉଲ୍ଲେଖ କରାଯାଇପାରେ।
$$ \begin{equation*} 2 \mathrm{H_2} \mathrm{~S}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{~S}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \tag{8.4} \end{equation*} $$
ରସାୟନବିତ୍ମାନଙ୍କର ଜ୍ଞାନ ବୃଦ୍ଧି ପାଇଲେ, (7.1 ରୁ 7.4) ସଦୃଶ ପ୍ରତିକ୍ରିୟାଗୁଡିକ ପାଇଁ ଅମ୍ଳୀକରଣ ଶବ୍ଦଟି ବିସ୍ତାର କରିବା ସ୍ୱାଭାବିକ ଥିଲା, ଯାହାକି ଅମ୍ଳଜାନକୁ ନୁହେଁ କିନ୍ତୁ ଅନ୍ୟାନ୍ୟ ବିଦ୍ୟୁତ୍-ଋଣାତ୍ମକ ମୌଳିକଗୁଡିକୁ ଅନ୍ତର୍ଭୁକ୍ତ କରେ ନାହିଁ। ଫ୍ଲୁରିନ୍, କ୍ଲୋରିନ୍ ଏବଂ ସଲ୍ଫର୍ ଇତ୍ୟାଦି ସହିତ ମ୍ୟାଗ୍ନେସିୟମ୍ ର ଅମ୍ଳୀକରଣ ନିମ୍ନଲିଖିତ ପ୍ରତିକ୍ରିୟା ଅନୁଯାୟୀ ଘଟେ:
$$\operatorname{Mg}(\mathrm{s})+\mathrm{F_2} (\mathrm{~g}) \rightarrow \operatorname{MgF_2} (s) \tag{8.5}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{Cl_2} (g) \rightarrow \mathrm{MgCl_2} (s) \tag{8.6}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{S} (s) \rightarrow \operatorname{MgS}(\mathrm{s}) \tag{8.7}$$
ପ୍ରତିକ୍ରିୟା 7.5 ରୁ 7.7) କୁ ଅମ୍ଳୀକରଣ ପ୍ରତିକ୍ରିୟାର ପରିସର ମଧ୍ୟରେ ସମ୍ମିଳିତ କରିବା ରସାୟନବିତ୍ମାନଙ୍କୁ କେବଳ ହାଇଡ୍ରୋଜେନ୍ ଅପସାରଣକୁ ନୁହେଁ ବରଂ ବିଦ୍ୟୁତ୍-ଧନାତ୍ମକ ମୌଳିକଗୁଡିକର ଅପସାରଣକୁ ଅମ୍ଳୀକରଣ ଭାବରେ ବିଚାର କରିବାକୁ ଉତ୍ସାହିତ କଲା। ତେଣୁ ପ୍ରତିକ୍ରିୟା:
$$ 2 \mathrm{~K_4} \left[ \mathrm{Fe} ( \mathrm{CN})_{6} \right] ( \mathrm{aq}) + \mathrm{H_2} \mathrm{O_2} ( \mathrm{aq}) \rightarrow 2 \mathrm{~K_3} \left[\mathrm{Fe}( \mathrm{CN})_6 \right] ( \mathrm{aq}) + 2 \mathrm{KOH} ( \mathrm{aq}) $$
କୁ ପୋଟାସିୟମ୍ ଫେରୋସାଇନାଇଡ୍ ପୋଟାସିୟମ୍ ଫେରିସାଇନାଇଡ୍ ରେ ପରିବର୍ତ୍ତନ ହେବା ପୂର୍ବରୁ ବିଦ୍ୟୁତ୍-ଧନାତ୍ମକ ମୌଳିକ ପୋଟାସିୟମ୍ ଅପସାରଣ ହେତୁ ଅମ୍ଳୀକରଣ ଭାବରେ ବ୍ୟାଖ୍ୟା କରାଯାଏ। ସାରାଂଶରେ, “ଅମ୍ଳୀକରଣ” ଶବ୍ଦଟି ଏକ ପଦାର୍ଥରେ ଅମ୍ଳଜାନ/ବିଦ୍ୟୁତ୍-ଋଣାତ୍ମକ ମୌଳିକ ଯୋଗ କିମ୍ବା ଏକ ପଦାର୍ଥରୁ ହାଇଡ୍ରୋଜେନ୍/ବିଦ୍ୟୁତ୍-ଧନାତ୍ମକ ମୌଳିକ ଅପସାରଣ ଭାବରେ ସଂଜ୍ଞାୟିତ ହୋଇଛି।
ଆରମ୍ଭରେ, ପ୍ରତିକ୍ରିୟାକୁ ଏକ ଯୌଗିକରୁ ଅମ୍ଳଜାନ ଅପସାରଣ ଭାବରେ ବିବେଚନା କରାଯାଉଥିଲା। ତଥାପି, ପ୍ରତିକ୍ରିୟା ଶବ୍ଦଟି ଏବେ ଏକ ପଦାର୍ଥରୁ ଅମ୍ଳଜାନ/ବିଦ୍ୟୁତ୍-ଋଣାତ୍ମକ ମୌଳିକ ଅପସାରଣ କିମ୍ବା ଏକ ପଦାର୍ଥରେ ହାଇଡ୍ରୋଜେନ୍/ବିଦ୍ୟୁତ୍-ଧନାତ୍ମକ ମୌଳିକ ଯୋଗକୁ ଅନ୍ତର୍ଭୁକ୍ତ କରିବା ପାଇଁ ବିସ୍ତାରିତ ହୋଇଛି।
ଉପରେ ଦିଆଯାଇଥିବା ସଂଜ୍ଞା ଅନୁଯାୟୀ, ନିମ୍ନଲିଖିତଗୁଡିକ ପ୍ରତିକ୍ରିୟା ପ୍ରକ୍ରିୟାର ଉଦାହରଣ:
$$2 \mathrm{HgO}(\mathrm{s}) \xrightarrow{\Delta} 2 \mathrm{Hg}(\mathrm{l})+\mathrm{O_2}(\mathrm{~g}) \tag{8.8}$$
(ମର୍କ୍ୟୁରିକ୍ ଅକ୍ସାଇଡ୍ ରୁ ଅମ୍ଳଜାନ ଅପସାରଣ)
$$2 \mathrm{FeCl_3}(\mathrm{aq})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{FeCl_2}(\mathrm{aq})+2 \mathrm{HCl}(\mathrm{aq}) \tag{8.9}$$
(ବିଦ୍ୟୁତ୍-ଋଣାତ୍ମକ ମୌଳିକ, ଫେରିକ୍ କ୍ଲୋରାଇଡ୍ ରୁ କ୍ଲୋରିନ୍ ଅପସାରଣ)
$$\mathrm{CH_2}=\mathrm{CH_2}(\mathrm{~g})+\mathrm{H_2}(\mathrm{~g}) \rightarrow \mathrm{H_3} \mathrm{C}-\mathrm{CH_3}(\mathrm{~g})\tag{8.10}$$
(ହାଇଡ୍ରୋଜେନ୍ ଯୋଗ)
$$2 \mathrm{HgCl_2}(\mathrm{aq})+\mathrm{SnCl_2}(\mathrm{aq}) \rightarrow \mathrm{Hg_2} \mathrm{Cl_2}(\mathrm{~s})+\mathrm{SnCl_4}(\mathrm{aq})\tag{8.11}$$
(ମର୍କ୍ୟୁରିକ୍ କ୍ଲୋରାଇଡ୍ ରେ ପାରଦ ଯୋଗ)
ପ୍ରତିକ୍ରିୟା (8.11) ରେ ସ୍ଟାନସ୍ କ୍ଲୋରାଇଡ୍ ର ସ୍ଟାନିକ୍ କ୍ଲୋରାଇଡ୍ ରେ ସମକାଳୀନ ଅମ୍ଳୀକରଣ ମଧ୍ୟ ଘଟୁଛି କାରଣ ଏଥିରେ ବିଦ୍ୟୁତ୍-ଋଣାତ୍ମକ ମୌଳିକ କ୍ଲୋରିନ୍ ଯୋଗ ହୋଇଛି। ଶୀଘ୍ର ଅନୁଭବ କରାଗଲା ଯେ ଅମ୍ଳୀକରଣ ଏବଂ ପ୍ରତିକ୍ରିୟା ସର୍ବଦା ସମକାଳୀନ ଭାବରେ ଘଟେ (ଉପରେ ଦିଆଯାଇଥିବା ସମସ୍ତ ସମୀକରଣକୁ ପୁନର୍ବାର ପରୀକ୍ଷା କରି ସ୍ପଷ୍ଟ ହେବ), ତେଣୁ, ରାସାୟନିକ ପ୍ରତିକ୍ରିୟାର ଏହି ଶ୍ରେଣୀ ପାଇଁ “ରେଡକ୍ସ” ଶବ୍ଦଟି ଗଠିତ ହୋଇଥିଲା।
ସମସ୍ୟା 8.1
ନିମ୍ନଲିଖିତ ପ୍ରତିକ୍ରିୟାରେ, ଅମ୍ଳୀକରଣ ଏବଂ ପ୍ରତିକ୍ରିୟା ଅଧୀନରେ ଥିବା ପ୍ରଜାତିଗୁଡିକୁ ଚିହ୍ନଟ କର:
(i) $\mathrm{H_2} \mathrm{~S}$ (g) $+\mathrm{Cl_2}$ (g) $\rightarrow 2 \mathrm{HCl}$ (g) $+\mathrm{S}$ (s)
(ii) $3 \mathrm{Fe_3} \mathrm{O_4}$ (s) $+8 \mathrm{Al}$ (s) $\rightarrow 9 \mathrm{Fe}$ (s) $+4 \mathrm{Al_2} \mathrm{O_3}(\mathrm{~s})$
(iii) $2 \mathrm{Na}$ (s) $+\mathrm{H_2}$ (g) $\rightarrow 2 \mathrm{NaH}$ (s)
ସମାଧାନ
(i) $\mathrm{H_2} \mathrm{~S}$ ଅମ୍ଳୀକୃତ ହୋଇଛି କାରଣ ଏକ ଅଧିକ ବିଦ୍ୟୁତ୍-ଋଣାତ୍ମକ ମୌଳିକ, କ୍ଲୋରିନ୍ ହାଇଡ୍ରୋଜେନ୍ ରେ ଯୋଗ ହୋଇଛି (କିମ୍ବା ଏକ ଅଧିକ ବିଦ୍ୟୁତ୍-ଧନାତ୍ମକ ମୌଳିକ, ହାଇଡ୍ରୋଜେନ୍ S ରୁ ଅପସାରିତ ହୋଇଛି)। ହାଇଡ୍ରୋଜେନ୍ ଯୋଗ ହେତୁ କ୍ଲୋରିନ୍ ପ୍ରତିକ୍ରିୟାଶୀଳ ହୋଇଛି।
(ii) ଆଲୁମିନିୟମ୍ ଅମ୍ଳୀକୃତ ହୋଇଛି କାରଣ ଏଥିରେ ଅମ୍ଳଜାନ ଯୋଗ ହୋଇଛି। ଫେରସ୍ ଫେରିକ୍ ଅକ୍ସାଇଡ୍ $\left(\mathrm{Fe_3} \mathrm{O_4}\right)$ ପ୍ରତିକ୍ରିୟାଶୀଳ ହୋଇଛି କାରଣ ଏଥିରୁ ଅମ୍ଳଜାନ ଅପସାରିତ ହୋଇଛି।
(iii) ବିଦ୍ୟୁତ୍-ଋଣାତ୍ମକତାର ଧାରଣାର ସତର୍କ ପ୍ରୟୋଗ କେବଳ ଆମେ ଅନୁମାନ କରିପାରିବା ଯେ ସୋଡିୟମ୍ ଅମ୍ଳୀକୃତ ହୋଇଛି ଏବଂ ହାଇଡ୍ରୋଜେନ୍ ପ୍ରତିକ୍ରିୟାଶୀଳ ହୋଇଛି।
ଏଠାରେ ବଛାଯାଇଥିବା ପ୍ରତିକ୍ରିୟା (iii) ଆମକୁ ରେଡକ୍ସ ପ୍ରତିକ୍ରିୟାକୁ ସଂଜ୍ଞାୟିତ କରିବାର ଅନ୍ୟ ଏକ ଉପାୟ ଦିଗରେ ଚିନ୍ତା କରିବାକୁ ପ୍ରେରଣା ଦେଇଥାଏ।
8.2 ଇଲେକ୍ଟ୍ରନ୍ ସ୍ଥାନାନ୍ତରଣ ପ୍ରତିକ୍ରିୟା ଦୃଷ୍ଟିରୁ ରେଡକ୍ସ ପ୍ରତିକ୍ରିୟା
ଆମେ ପୂର୍ବରୁ ଶିଖିଛୁ ଯେ ପ୍ରତିକ୍ରିୟାଗୁଡିକ ରେଡକ୍ସ ପ୍ରତିକ୍ରିୟା କାରଣ ଏହି ପ୍ରତିକ୍ରିୟା ପ୍ରତ୍ୟେକରେ ସୋଡିୟମ୍ ଅମ୍ଳଜାନ କିମ୍ବା ସୋଡିୟମ୍ ରେ ଅଧିକ ବିଦ୍ୟୁତ୍-ଋଣାତ୍ମକ ମୌଳିକ ଯୋଗ ହେତୁ ଅମ୍ଳୀକୃତ ହୋଇଛି।
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaCl}(\mathrm{s})\tag{8.12}$$
$$4 \mathrm{Na}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na_2} \mathrm{O}(\mathrm{s})\tag{8.13}$$
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{S}(\mathrm{s}) \rightarrow \mathrm{Na_2} \mathrm{~S}(\mathrm{~s}) \tag{8.14}$$
ସମକାଳୀନ ଭାବରେ, କ୍ଲୋରିନ୍, ଅମ୍ଳଜାନ ଏବଂ ସଲ୍ଫର୍ ପ୍ରତିକ୍ରିୟାଶୀଳ ହୋଇଛି କାରଣ ଏହି ପ୍ରତ୍ୟେକରେ, ବିଦ୍ୟୁତ୍-ଧନାତ୍ମକ ମୌଳିକ ସୋଡିୟମ୍ ଯୋଗ ହୋଇଛି। ରାସାୟନିକ ବନ୍ଧନ ବିଷୟରେ ଆମର ଜ୍ଞାନରୁ ଆମେ ଜାଣୁ ଯେ ସୋଡିୟମ୍ କ୍ଲୋରାଇଡ୍, ସୋଡିୟମ୍ ଅକ୍ସାଇଡ୍ ଏବଂ ସୋଡିୟମ୍ ସଲ୍ଫାଇଡ୍ ଆୟନିକ୍ ଯୌଗିକ ଏବଂ ବୋଧହୁଏ ଭଲ ଭାବରେ $\mathrm{Na}^{+} \mathrm{Cl}^{-}( \mathrm{s}),\left(\mathrm{Na}^{+} \right)_2 \mathrm{O}^{2-}( \mathrm{s})$, ଏବଂ $ \left(\mathrm{Na}^{+} \right)_2$ $\mathrm{S}^{2-}( \mathrm{s})$ ଭାବରେ ଲିଖିତ। ଉତ୍ପାଦିତ ପ୍ରଜାତି ଉପରେ ଚାର୍ଜ୍ ର ବିକାଶ ଆମକୁ ପ୍ରତିକ୍ରିୟା (8.12 ରୁ 8.14) ନିମ୍ନଲିଖିତ ପଦ୍ଧତିରେ ପୁନର୍ଲେଖନ କରିବାକୁ ସୂଚିତ କରେ:
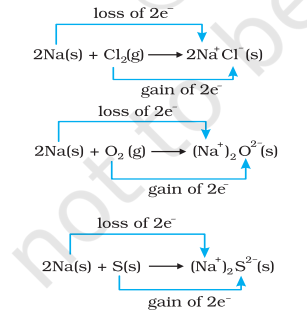
ସୁବିଧା ପାଇଁ, ଉପରୋକ୍ତ ପ୍ରତ୍ୟେକ ପ୍ରକ୍ରିୟାକୁ ଦୁଇଟି ଅଲଗା ପଦକ୍ଷେପ ଭାବରେ ବିବେଚନା କରାଯାଇପାରେ, ଗୋଟିଏ ଇଲେକ୍ଟ୍ରନ୍ ହରାଇବା ଏବଂ ଅନ୍ୟଟି ଇଲେକ୍ଟ୍ରନ୍ ଲାଭ କରିବା ସହିତ ଜଡିତ। ଏକ ଉଦାହରଣ ଭାବରେ, ଆମେ ଏଥିରୁ ଗୋଟିଏକୁ ଆହୁରି ବିସ୍ତୃତ ଭାବରେ ବର୍ଣ୍ଣନା କରିପାରିବା, କୁହନ୍ତୁ, ସୋଡିୟମ୍ କ୍ଲୋରାଇଡ୍ ଗଠନ।
$2 \mathrm{Na}(\mathrm{s}) \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
$\mathrm{Cl_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{Cl}^{-}(\mathrm{g})$
ଉପରୋକ୍ତ ପ୍ରତ୍ୟେକ ପଦକ୍ଷେପକୁ ଏକ ଅର୍ଦ୍ଧ ପ୍ରତିକ୍ରିୟା କୁହାଯାଏ, ଯାହା ସ୍ପଷ୍ଟ ଭାବରେ ଇଲେକ୍ଟ୍ରନ୍ ର ସମ୍ପୃକ୍ତତା ଦର୍ଶାଏ। ଅର୍ଦ୍ଧ ପ୍ରତିକ୍ରିୟାର ସମଷ୍ଟି ସାମଗ୍ରିକ ପ୍ରତିକ୍ରିୟା ଦେଇଥାଏ:
$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na}^{+} \mathrm{Cl}^{-}(\mathrm{s})$ କିମ୍ବା $2 \mathrm{NaCl}(\mathrm{s})$
ପ୍ରତିକ୍ରିୟା 8.12 ରୁ 8.14 ସୂଚିତ କରେ ଯେ ଇଲେକ୍ଟ୍ରନ୍ ହରାଇବା ସହିତ ଜଡିତ ଅର୍ଦ୍ଧ ପ୍ରତିକ୍ରିୟାଗୁଡିକୁ ଅମ୍ଳୀକରଣ ପ୍ରତିକ୍ରିୟା କୁହାଯାଏ। ସେହିପରି, ଇଲେକ୍ଟ୍ରନ୍ ଲାଭ କରିବା ସହିତ ଜଡିତ ଅର୍ଦ୍ଧ ପ୍ରତିକ୍ରିୟାଗୁଡିକୁ ପ୍ରତିକ୍ରିୟା ପ୍ରତିକ୍ରିୟା କୁହାଯାଏ। ଏଠାରେ ଉଲ୍ଲେଖ କରିବା ଅପ୍ରାସଙ୍ଗିକ ହୋଇନପାରେ ଯେ ଅମ୍ଳୀକରଣ ଏବଂ ପ୍ରତିକ୍ରିୟାକୁ ସଂଜ୍ଞାୟିତ କରିବାର ନୂତନ ଉପାୟ ଶାସ୍ତ୍ରୀୟ ଧାରଣା ଅନୁଯାୟୀ ପ୍ରଜାତିର ଆଚରଣ ଏବଂ ଇଲେକ୍ଟ୍ରନ୍-ସ୍ଥାନାନ୍ତରଣ ପରିବର୍ତ୍ତନରେ ସେମାନଙ୍କର ପାରସ୍ପରିକ କ୍ରିୟା ମଧ୍ୟରେ ଏକ ସମ୍ପର୍କ ସ୍ଥାପନ କରି ହାସଲ କରାଯାଇଛି। ପ୍ରତିକ୍ରିୟା (8.12 ରୁ 8.14) ରେ ସୋଡିୟମ୍, ଯାହା ଅମ୍ଳୀକୃତ ହୋଇଛି, ଏକ ପ୍ରତିକ୍ରିୟାଶୀଳ ଏଜେଣ୍ଟ୍ ଭାବରେ କାର୍ଯ୍ୟ କରେ କାରଣ ଏହା ଏହା ସହିତ ପାରସ୍ପରିକ କ୍ରିୟା କରୁଥିବା ପ୍ରତ୍ୟେକ ମୌଳିକକୁ ଇଲେକ୍ଟ୍ରନ୍ ଦାନ କରେ ଏବଂ ତେଣୁ ସେମାନଙ୍କୁ ପ୍ରତିକ୍ରିୟାଶୀଳ କରିବାରେ ସାହାଯ୍ୟ କରେ। କ୍ଲୋରିନ୍, ଅମ୍ଳଜାନ ଏବଂ ସଲ୍ଫର୍ ପ୍ରତିକ୍ରିୟାଶୀଳ ହୋଇଛି ଏବଂ ଅମ୍ଳୀକରଣ ଏଜେଣ୍ଟ୍ ଭାବରେ କାର୍ଯ୍ୟ କରେ କାରଣ ଏଗୁଡିକ ସୋଡିୟମ୍ ରୁ ଇଲେକ୍ଟ୍ରନ୍ ଗ୍ରହଣ କରେ। ସାରାଂଶରେ, ଆମେ ଉଲ୍ଲେଖ କରିପାରିବା ଯେ
ଅମ୍ଳୀକରଣ: ଯେକୌଣସି ପ୍ରଜାତି ଦ୍ୱାରା ଇଲେକ୍ଟ୍ରନ୍ (ଗୁଡିକ) ହରାଇବା।
ପ୍ରତିକ୍ରିୟା: ଯେକୌଣସି ପ୍ରଜାତି ଦ୍ୱାରା ଇଲେକ୍ଟ୍ରନ୍ (ଗୁଡିକ) ଲାଭ କରିବା।
ଅମ୍ଳୀକରଣ ଏଜେଣ୍ଟ୍: ଇଲେକ୍ଟ୍ରନ୍ (ଗୁଡିକ) ର ଗ୍ରହୀତା।
ପ୍ରତିକ୍ରିୟାଶୀଳ ଏଜେଣ୍ଟ୍: ଇଲେକ୍ଟ୍ରନ୍ (ଗୁଡିକ) ର ଦାତା।
ସମସ୍ୟା 8.2
ଯୁକ୍ତି ଦର୍ଶାଅ ଯେ ପ୍ରତିକ୍ରିୟା: $2 \mathrm{Na}(\mathrm{s})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaH}$ (s) ଏକ ରେଡକ୍ସ ପରିବର୍ତ୍ତନ।
ସମାଧାନ
ଉପରୋକ୍ତ ପ୍ରତିକ୍ରିୟାରେ ଯେହେତୁ ଗଠିତ ଯୌଗିକଟି ଏକ ଆୟନିକ୍ ଯୌଗିକ, ଯାହାକି $\mathrm{Na}^{+} \mathrm{H}^{-}$(s) ଭାବରେ ମଧ୍ୟ ପ୍ରତିନିଧିତ୍ୱ କରାଯାଇପାରେ, ଏହା ସୂଚିତ କରେ ଯେ ଏହି ପ୍ରକ୍ରିୟାରେ ଗୋଟିଏ ଅର୍ଦ୍ଧ ପ୍ରତିକ୍ରିୟା ହେଉଛି:
$2 \mathrm{Na}(\mathrm{s}) \quad \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
ଏବଂ ଅନ୍ୟ ଅର୍ଦ୍ଧ ପ୍ରତିକ୍ରିୟା ହେଉଛି:
$\mathrm{H_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{H}^{-}(\mathrm{g})$
ପରୀକ୍ଷା ଅଧୀନରେ ଥିବା ପ୍ରତିକ୍ରିୟାକୁ ଦୁଇଟି ଅର୍ଦ୍ଧ ପ୍ରତିକ୍ରିୟାରେ ବିଭାଜନ କରିବା ସ୍ୱୟଂଚାଳିତ ଭାବରେ ପ୍ରକାଶ କରେ ଯେ ଏଠାରେ ସୋଡିୟମ୍ ଅମ୍ଳୀକୃତ ହୋଇଛି ଏବଂ ହାଇଡ୍ରୋଜେନ୍ ପ୍ରତିକ୍ରିୟାଶୀଳ ହୋଇଛି, ତେଣୁ, ସମ୍ପୂର୍ଣ୍ଣ ପ୍ରତିକ








