ਅਧਿਆਇ 04 ਰਸਾਇਣਕ ਬੰਧਨ ਅਤੇ ਅਣਵੀ ਬਣਤਰ
“ਵਿਗਿਆਨੀ ਨਿਰੰਤਰ ਨਵੇਂ ਯੌਗਿਕਾਂ ਦੀ ਖੋਜ ਕਰ ਰਹੇ ਹਨ, ਉਹਨਾਂ ਬਾਰੇ ਤੱਥਾਂ ਨੂੰ ਕ੍ਰਮਬੱਧ ਢੰਗ ਨਾਲ ਵਿਵਸਥਿਤ ਕਰਦੇ ਹਨ, ਮੌਜੂਦਾ ਗਿਆਨ ਨਾਲ ਵਿਆਖਿਆ ਕਰਨ ਦੀ ਕੋਸ਼ਿਸ਼ ਕਰਦੇ ਹਨ, ਪਹਿਲਾਂ ਦੇ ਵਿਚਾਰਾਂ ਨੂੰ ਸੋਧਣ ਜਾਂ ਨਵੇਂ ਦੇਖੇ ਗਏ ਤੱਥਾਂ ਦੀ ਵਿਆਖਿਆ ਲਈ ਸਿਧਾਂਤਾਂ ਨੂੰ ਵਿਕਸਿਤ ਕਰਨ ਲਈ ਸੰਗਠਿਤ ਕਰਦੇ ਹਨ।”
ਪਦਾਰਥ ਇੱਕ ਜਾਂ ਵੱਖ-ਵੱਖ ਕਿਸਮ ਦੇ ਤੱਤਾਂ ਤੋਂ ਬਣਿਆ ਹੁੰਦਾ ਹੈ। ਸਾਧਾਰਨ ਹਾਲਤਾਂ ਵਿੱਚ ਕੋਈ ਹੋਰ ਤੱਤ ਕੁਦਰਤ ਵਿੱਚ ਇੱਕ ਸੁਤੰਤਰ ਪਰਮਾਣੂ ਦੇ ਰੂਪ ਵਿੱਚ ਮੌਜੂਦ ਨਹੀਂ ਹੁੰਦਾ, ਸਿਵਾਏ ਨੋਬਲ ਗੈਸਾਂ ਦੇ। ਹਾਲਾਂਕਿ, ਪਰਮਾਣੂਆਂ ਦਾ ਇੱਕ ਸਮੂਹ ਇੱਕ ਪ੍ਰਜਾਤੀ ਦੇ ਰੂਪ ਵਿੱਚ ਇਕੱਠੇ ਮੌਜੂਦ ਹੋਣਾ ਪਾਇਆ ਜਾਂਦਾ ਹੈ ਜਿਸਦੇ ਖਾਸ ਗੁਣ ਹੁੰਦੇ ਹਨ। ਪਰਮਾਣੂਆਂ ਦੇ ਅਜਿਹੇ ਸਮੂਹ ਨੂੰ ਅਣੂ ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਸਪੱਸ਼ਟ ਹੈ ਕਿ ਕੁਝ ਸ਼ਕਤੀ ਹੋਣੀ ਚਾਹੀਦੀ ਹੈ ਜੋ ਇਨ੍ਹਾਂ ਘਟਕ ਪਰਮਾਣੂਆਂ ਨੂੰ ਅਣੂਆਂ ਵਿੱਚ ਇਕੱਠਾ ਰੱਖਦੀ ਹੈ। ਆਕਰਸ਼ਕ ਸ਼ਕਤੀ ਜੋ ਵੱਖ-ਵੱਖ ਘਟਕਾਂ (ਪਰਮਾਣੂ, ਆਇਨ, ਆਦਿ) ਨੂੰ ਵੱਖ-ਵੱਖ ਰਸਾਇਣਕ ਪ੍ਰਜਾਤੀਆਂ ਵਿੱਚ ਇਕੱਠਾ ਰੱਖਦੀ ਹੈ, ਉਸਨੂੰ ਰਸਾਇਣਕ ਬੰਧਨ ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਕਿਉਂਕਿ ਰਸਾਇਣਕ ਯੌਗਿਕਾਂ ਦਾ ਨਿਰਮਾਣ ਵੱਖ-ਵੱਖ ਤਰੀਕਿਆਂ ਨਾਲ ਵੱਖ-ਵੱਖ ਤੱਤਾਂ ਦੇ ਪਰਮਾਣੂਆਂ ਦੇ ਸੁਮੇਲ ਦੇ ਨਤੀਜੇ ਵਜੋਂ ਹੁੰਦਾ ਹੈ, ਇਸ ਨਾਲ ਬਹੁਤ ਸਾਰੇ ਸਵਾਲ ਉਠਦੇ ਹਨ। ਪਰਮਾਣੂ ਕਿਉਂ ਜੁੜਦੇ ਹਨ? ਸਿਰਫ ਕੁਝ ਖਾਸ ਸੁਮੇਲ ਹੀ ਕਿਉਂ ਸੰਭਵ ਹਨ? ਕੁਝ ਪਰਮਾਣੂ ਕਿਉਂ ਜੁੜਦੇ ਹਨ ਜਦਕਿ ਕੁਝ ਹੋਰ ਨਹੀਂ ਜੁੜਦੇ? ਅਣੂਆਂ ਦੀ ਨਿਸ਼ਚਿਤ ਆਕ੍ਰਿਤੀ ਕਿਉਂ ਹੁੰਦੀ ਹੈ? ਅਜਿਹੇ ਸਵਾਲਾਂ ਦੇ ਜਵਾਬ ਦੇਣ ਲਈ ਵੱਖ-ਵੱਖ ਸਿਧਾਂਤ ਅਤੇ ਧਾਰਨਾਵਾਂ ਸਮੇਂ-ਸਮੇਂ ‘ਤੇ ਸਾਹਮਣੇ ਲਿਆਂਦੀਆਂ ਗਈਆਂ ਹਨ। ਇਹ ਹਨ ਕੋਸਲ-ਲਿਊਇਸ ਦਾ ਦ੍ਰਿਸ਼ਟੀਕੋਣ, ਵੈਲੈਂਸ ਸ਼ੈਲ ਇਲੈਕਟ੍ਰੌਨ ਪੇਅਰ ਪ੍ਰਤੀਕਰਸ਼ਣ (VSEPR) ਸਿਧਾਂਤ, ਵੈਲੈਂਸ ਬਾਂਡ (VB) ਸਿਧਾਂਤ ਅਤੇ ਅਣਵੀ ਆਰਬਿਟਲ (MO) ਸਿਧਾਂਤ। ਵੈਲੈਂਸ ਦੇ ਵੱਖ-ਵੱਖ ਸਿਧਾਂਤਾਂ ਦਾ ਵਿਕਾਸ ਅਤੇ ਰਸਾਇਣਕ ਬੰਧਨਾਂ ਦੀ ਪ੍ਰਕਿਰਤੀ ਦੀ ਵਿਆਖਿਆ ਪਰਮਾਣੂ ਦੀ ਬਣਤਰ, ਤੱਤਾਂ ਦੀ ਇਲੈਕਟ੍ਰੌਨਿਕ ਵਿਵਸਥਾ ਅਤੇ ਆਵਰਤੀ ਸਾਰਣੀ ਦੀ ਸਮਝ ਵਿੱਚ ਹੋਈਆਂ ਤਰੱਕੀਆਂ ਨਾਲ ਨਜ਼ਦੀਕੀ ਤੌਰ ‘ਤੇ ਸੰਬੰਧਿਤ ਰਹੀ ਹੈ। ਹਰੇਕ ਪ੍ਰਬੰਧ ਹੋਰ ਸਥਿਰ ਹੋਣ ਦੀ ਪ੍ਰਵਿਰਤੀ ਰੱਖਦਾ ਹੈ ਅਤੇ ਬੰਧਨ ਪ੍ਰਬੰਧ ਦੀ ਊਰਜਾ ਨੂੰ ਘਟਾ ਕੇ ਸਥਿਰਤਾ ਪ੍ਰਾਪਤ ਕਰਨ ਦੀ ਕੁਦਰਤ ਦਾ ਤਰੀਕਾ ਹੈ।
4.1 ਰਸਾਇਣਕ ਬੰਧਨ ਲਈ ਕੋਸਲ-ਲਿਊਇਸ ਦਾ ਦ੍ਰਿਸ਼ਟੀਕੋਣ
ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੇ ਸੰਦਰਭ ਵਿੱਚ ਰਸਾਇਣਕ ਬੰਧਨ ਦੇ ਨਿਰਮਾਣ ਦੀ ਵਿਆਖਿਆ ਕਰਨ ਲਈ, ਬਹੁਤ ਸਾਰੇ ਯਤਨ ਕੀਤੇ ਗਏ, ਪਰ ਇਹ ਸਿਰਫ 1916 ਵਿੱਚ ਸੀ ਜਦੋਂ ਕੋਸਲ ਅਤੇ ਲਿਊਇਸ ਸਫਲਤਾਪੂਰਵਕ ਸੰਤੋਖਜਨਕ ਵਿਆਖਿਆ ਦੇਣ ਵਿੱਚ ਸਫਲ ਹੋਏ। ਉਹ ਵੈਲੈਂਸ ਦੀ ਕੁਝ ਤਾਰਕਿਕ ਵਿਆਖਿਆ ਪ੍ਰਦਾਨ ਕਰਨ ਵਾਲੇ ਪਹਿਲੇ ਵਿਅਕਤੀ ਸਨ ਜੋ ਨੋਬਲ ਗੈਸਾਂ ਦੀ ਨਿਸ਼ਕਿਰਿਆਤਾ ‘ਤੇ ਆਧਾਰਿਤ ਸੀ।
ਲਿਊਇਸ ਨੇ ਪਰਮਾਣੂ ਨੂੰ ਇੱਕ ਧਨਾਤਮਕ ਚਾਰਜ ਵਾਲੇ ‘ਕਰਨਲ’ (ਨਿਊਕਲੀਅਸ ਅਤੇ ਅੰਦਰੂਨੀ ਇਲੈਕਟ੍ਰੌਨਾਂ) ਅਤੇ ਬਾਹਰੀ ਸ਼ੈਲ ਦੇ ਰੂਪ ਵਿੱਚ ਦਰਸਾਇਆ ਜੋ ਅੱਠ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਅਧਿਕਤਮ ਸੰਖਿਆ ਨੂੰ ਸਮਾ ਸਕਦਾ ਹੈ। ਉਸਨੇ ਇਹ ਹੋਰ ਧਾਰਨਾ ਬਣਾਈ ਕਿ ਇਹ ਅੱਠ ਇਲੈਕਟ੍ਰੌਨ ਇੱਕ ਘਣ ਦੇ ਕੋਨਿਆਂ ‘ਤੇ ਕਬਜ਼ਾ ਕਰਦੇ ਹਨ ਜੋ ‘ਕਰਨਲ’ ਨੂੰ ਘੇਰਦੇ ਹਨ। ਇਸ ਤਰ੍ਹਾਂ ਸੋਡੀਅਮ ਦਾ ਇੱਕ ਬਾਹਰੀ ਸ਼ੈਲ ਇਲੈਕਟ੍ਰੌਨ ਘਣ ਦੇ ਇੱਕ ਕੋਨੇ ‘ਤੇ ਕਬਜ਼ਾ ਕਰੇਗਾ, ਜਦਕਿ ਨੋਬਲ ਗੈਸ ਦੇ ਮਾਮਲੇ ਵਿੱਚ ਸਾਰੇ ਅੱਠ ਕੋਨੇ ਕਬਜ਼ੇ ਵਿੱਚ ਹੋਣਗੇ। ਇਲੈਕਟ੍ਰੌਨਾਂ ਦਾ ਇਹ ਅੱਠਕ, ਇੱਕ ਖਾਸ ਤੌਰ ‘ਤੇ ਸਥਿਰ ਇਲੈਕਟ੍ਰੌਨਿਕ ਵਿਵਸਥਾ ਨੂੰ ਦਰਸਾਉਂਦਾ ਹੈ। ਲਿਊਇਸ ਨੇ ਇਹ ਪ੍ਰਸਤਾਵਿਤ ਕੀਤਾ ਕਿ ਪਰਮਾਣੂ ਸਥਿਰ ਅੱਠਕ ਪ੍ਰਾਪਤ ਕਰਦੇ ਹਨ ਜਦੋਂ ਉਹ ਰਸਾਇਣਕ ਬੰਧਨਾਂ ਦੁਆਰਾ ਜੁੜੇ ਹੁੰਦੇ ਹਨ। ਸੋਡੀਅਮ ਅਤੇ ਕਲੋਰੀਨ ਦੇ ਮਾਮਲੇ ਵਿੱਚ, ਇਹ ਸੋਡੀਅਮ ਤੋਂ ਕਲੋਰੀਨ ਵਿੱਚ ਇੱਕ ਇਲੈਕਟ੍ਰੌਨ ਦੇ ਤਬਾਦਲੇ ਦੁਆਰਾ ਹੋ ਸਕਦਾ ਹੈ ਜਿਸ ਨਾਲ $\mathrm{Na}^+$ ਅਤੇ $\mathrm{Cl}^{-}$ ਆਇਨ ਪ੍ਰਾਪਤ ਹੁੰਦੇ ਹਨ। ਹੋਰ ਅਣੂਆਂ ਜਿਵੇਂ ਕਿ $ \mathrm{Cl}_2, \mathrm{H}_2, \mathrm{~F}_2 $, ਆਦਿ ਦੇ ਮਾਮਲੇ ਵਿੱਚ, ਬੰਧਨ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਇੱਕ ਜੋੜੀ ਦੀ ਸਾਂਝ ਕਰਕੇ ਬਣਦਾ ਹੈ। ਇਸ ਪ੍ਰਕਿਰਿਆ ਵਿੱਚ ਹਰੇਕ ਪਰਮਾਣੂ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦਾ ਇੱਕ ਸਥਿਰ ਬਾਹਰੀ ਅੱਠਕ ਪ੍ਰਾਪਤ ਕਰਦਾ ਹੈ।
ਲਿਊਇਸ ਚਿੰਨ੍ਹ: ਇੱਕ ਅਣੂ ਦੇ ਨਿਰਮਾਣ ਵਿੱਚ, ਸਿਰਫ ਬਾਹਰੀ ਸ਼ੈਲ ਦੇ ਇਲੈਕਟ੍ਰੌਨ ਰਸਾਇਣਕ ਸੁਮੇਲ ਵਿੱਚ ਹਿੱਸਾ ਲੈਂਦੇ ਹਨ ਅਤੇ ਉਹਨਾਂ ਨੂੰ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨ ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਅੰਦਰੂਨੀ ਸ਼ੈਲ ਦੇ ਇਲੈਕਟ੍ਰੌਨ ਚੰਗੀ ਤਰ੍ਹਾਂ ਸੁਰੱਖਿਅਤ ਹੁੰਦੇ ਹਨ ਅਤੇ ਆਮ ਤੌਰ ‘ਤੇ ਸੁਮੇਲ ਪ੍ਰਕਿਰਿਆ ਵਿੱਚ ਸ਼ਾਮਲ ਨਹੀਂ ਹੁੰਦੇ। ਜੀ.ਐਨ. ਲਿਊਇਸ, ਇੱਕ ਅਮਰੀਕੀ ਰਸਾਇਣ ਵਿਗਿਆਨੀ ਨੇ ਇੱਕ ਪਰਮਾਣੂ ਵਿੱਚ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨਾਂ ਨੂੰ ਦਰਸਾਉਣ ਲਈ ਸਧਾਰਨ ਨੋਟੇਸ਼ਨ ਪੇਸ਼ ਕੀਤੇ। ਇਹਨਾਂ ਨੋਟੇਸ਼ਨਾਂ ਨੂੰ ਲਿਊਇਸ ਚਿੰਨ੍ਹ ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਉਦਾਹਰਨ ਲਈ, ਦੂਜੀ ਅਵਧੀ ਦੇ ਤੱਤਾਂ ਲਈ ਲਿਊਇਸ ਚਿੰਨ੍ਹ ਹੇਠਾਂ ਦਿੱਤੇ ਅਨੁਸਾਰ ਹਨ:

ਲਿਊਇਸ ਚਿੰਨ੍ਹਾਂ ਦਾ ਮਹੱਤਵ: ਚਿੰਨ੍ਹ ਦੇ ਆਲੇ-ਦੁਆਲੇ ਬਿੰਦੀਆਂ ਦੀ ਸੰਖਿਆ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਸੰਖਿਆ ਨੂੰ ਦਰਸਾਉਂਦੀ ਹੈ। ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਇਹ ਸੰਖਿਆ ਤੱਤ ਦੀ ਆਮ ਜਾਂ ਸਮੂਹ ਵੈਲੈਂਸ ਦੀ ਗਣਨਾ ਕਰਨ ਵਿੱਚ ਮਦਦ ਕਰਦੀ ਹੈ। ਤੱਤਾਂ ਦੀ ਸਮੂਹ ਵੈਲੈਂਸ ਆਮ ਤੌਰ ‘ਤੇ ਲਿਊਇਸ ਚਿੰਨ੍ਹਾਂ ਵਿੱਚ ਬਿੰਦੀਆਂ ਦੀ ਸੰਖਿਆ ਜਾਂ 8 ਘਟਾਓ ਬਿੰਦੀਆਂ ਜਾਂ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਸੰਖਿਆ ਦੇ ਬਰਾਬਰ ਹੁੰਦੀ ਹੈ।
ਕੋਸਲ ਨੇ, ਰਸਾਇਣਕ ਬੰਧਨ ਨਾਲ ਸੰਬੰਧਿਤ, ਹੇਠ ਲਿਖੇ ਤੱਥਾਂ ਵੱਲ ਧਿਆਨ ਖਿੱਚਿਆ:
- ਆਵਰਤੀ ਸਾਰਣੀ ਵਿੱਚ, ਬਹੁਤ ਜ਼ਿਆਦਾ ਇਲੈਕਟ੍ਰੋਨੈਗੇਟਿਵ ਹੈਲੋਜਨ ਅਤੇ ਬਹੁਤ ਜ਼ਿਆਦਾ ਇਲੈਕਟ੍ਰੋਪੋਜ਼ਿਟਿਵ ਖਾਰੀ ਧਾਤਾਂ ਨੋਬਲ ਗੈਸਾਂ ਦੁਆਰਾ ਵੱਖ ਕੀਤੀਆਂ ਗਈਆਂ ਹਨ;
- ਇੱਕ ਹੈਲੋਜਨ ਪਰਮਾਣੂ ਤੋਂ ਇੱਕ ਨਕਾਰਾਤਮਕ ਆਇਨ ਅਤੇ ਇੱਕ ਖਾਰੀ ਧਾਤ ਪਰਮਾਣੂ ਤੋਂ ਇੱਕ ਧਨਾਤਮਕ ਆਇਨ ਦਾ ਨਿਰਮਾਣ ਸੰਬੰਧਿਤ ਪਰਮਾਣੂਆਂ ਦੁਆਰਾ ਇੱਕ ਇਲੈਕਟ੍ਰੌਨ ਦੇ ਲਾਭ ਅਤੇ ਨੁਕਸਾਨ ਨਾਲ ਜੁੜਿਆ ਹੋਇਆ ਹੈ;
- ਇਸ ਤਰ੍ਹਾਂ ਬਣੇ ਨਕਾਰਾਤਮਕ ਅਤੇ ਧਨਾਤਮਕ ਆਇਨ ਸਥਿਰ ਨੋਬਲ ਗੈਸ ਇਲੈਕਟ੍ਰੌਨਿਕ ਵਿਵਸਥਾਵਾਂ ਪ੍ਰਾਪਤ ਕਰਦੇ ਹਨ। ਨੋਬਲ ਗੈਸਾਂ (ਹੀਲੀਅਮ ਨੂੰ ਛੱਡ ਕੇ ਜਿਸਦੇ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦਾ ਇੱਕ ਜੋੜਾ ਹੁੰਦਾ ਹੈ) ਦੀ ਬਾਹਰੀ ਸ਼ੈਲ ਵਿਵਸਥਾ ਅੱਠ (ਅੱਠਕ) ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਖਾਸ ਤੌਰ ‘ਤੇ ਸਥਿਰ ਹੁੰਦੀ ਹੈ, $n s^{2} n p^{6}$।
- ਨਕਾਰਾਤਮਕ ਅਤੇ ਧਨਾਤਮਕ ਆਇਨ ਇਲੈਕਟ੍ਰੋਸਟੈਟਿਕ ਆਕਰਸ਼ਣ ਦੁਆਰਾ ਸਥਿਰ ਹੁੰਦੇ ਹਨ।
ਉਦਾਹਰਨ ਲਈ, ਉਪਰੋਕਤ ਯੋਜਨਾ ਅਨੁਸਾਰ, ਸੋਡੀਅਮ ਅਤੇ ਕਲੋਰੀਨ ਤੋਂ $\mathrm{NaCl}$ ਦਾ ਨਿਰਮਾਣ, ਇਸ ਤਰ੍ਹਾਂ ਵਿਆਖਿਆ ਕੀਤਾ ਜਾ ਸਕਦਾ ਹੈ:
| $\mathrm{Na}$ | $\rightarrow$ | $\mathrm{Na}^{+}+\mathrm{e}^{-}$ |
| $[\mathrm{Ne}] 3 \mathrm{~s}^{1}$ | $[\mathrm{Ne}]$ | |
| $\mathrm{Cl}+\mathrm{e}^{-}$ | $\rightarrow$ | $\mathrm{Cl}^{-}$ |
| $[\mathrm{Ne}] 3 s^{2} 3 p^{5}$ | $[\mathrm{Ne}] 3 s^{2} 3 p^{6}$ ਜਾਂ $[\mathrm{Ar}]$ | |
| $\mathrm{Na}^{+}+\mathrm{Cl}^{-}$ | $\rightarrow$ | $\mathrm{NaCl}$ ਜਾਂ $\mathrm{Na}^{+} \mathrm{Cl}^{-}$ |
ਇਸੇ ਤਰ੍ਹਾਂ $\mathrm{CaF}_{2}$ ਦੇ ਨਿਰਮਾਣ ਨੂੰ ਇਸ ਤਰ੍ਹਾਂ ਦਰਸਾਇਆ ਜਾ ਸਕਦਾ ਹੈ:
| $\mathrm{Ca}$ | $\rightarrow$ | $\mathrm{Ca}^{2+}+2 \mathrm{e}^{-}$ |
| $[\mathrm{Ar}] 4 s^{2}$ | $[\mathrm{Ar}]$ | |
| $\mathrm{F}+\mathrm{e}^{-}$ | $\rightarrow$ | $\mathrm{F}^{-}$ |
| $[\mathrm{He}] 2 s^{2} 2 p^{5}$ | $[\mathrm{He}] 2 s^{2} 2 p^{6}$ ਜਾਂ $[\mathrm{Ne}]$ | |
| $\mathrm{Ca}^{2+}+2 \mathrm{~F}^{-}$ | $\rightarrow$ | $\mathrm{CaF}_2$ ਜਾਂ $\mathrm{Ca}^{2+}\left(\mathrm{F}^{-}\right)_2$ |
ਬੰਧਨ, ਧਨਾਤਮਕ ਅਤੇ ਨਕਾਰਾਤਮਕ ਆਇਨਾਂ ਵਿਚਕਾਰ ਇਲੈਕਟ੍ਰੋਸਟੈਟਿਕ ਆਕਰਸ਼ਣ ਦੇ ਨਤੀਜੇ ਵਜੋਂ ਬਣਿਆ, ਨੂੰ ਇਲੈਕਟ੍ਰੋਵੈਲੈਂਟ ਬੰਧਨ ਕਿਹਾ ਜਾਂਦਾ ਸੀ। ਇਸ ਤਰ੍ਹਾਂ ਇਲੈਕਟ੍ਰੋਵੈਲੈਂਸ ਆਇਨ ‘ਤੇ ਇਕਾਈ ਚਾਰਜ(ਆਂ) ਦੀ ਸੰਖਿਆ ਦੇ ਬਰਾਬਰ ਹੁੰਦਾ ਹੈ। ਇਸ ਤਰ੍ਹਾਂ, ਕੈਲਸ਼ੀਅਮ ਨੂੰ ਦੋ ਦਾ ਧਨਾਤਮਕ ਇਲੈਕਟ੍ਰੋਵੈਲੈਂਸ ਦਿੱਤਾ ਜਾਂਦਾ ਹੈ, ਜਦਕਿ ਕਲੋਰੀਨ ਨੂੰ ਇੱਕ ਦਾ ਨਕਾਰਾਤਮਕ ਇਲੈਕਟ੍ਰੋਵੈਲੈਂਸ ਦਿੱਤਾ ਜਾਂਦਾ ਹੈ।
ਕੋਸਲ ਦੇ ਪ੍ਰਸਤਾਵ ਇਲੈਕਟ੍ਰੌਨ ਤਬਾਦਲੇ ਦੁਆਰਾ ਆਇਨ-ਨਿਰਮਾਣ ਅਤੇ ਆਇਨਿਕ ਕ੍ਰਿਸਟਲੀਨ ਯੌਗਿਕਾਂ ਦੇ ਨਿਰਮਾਣ ਬਾਰੇ ਆਧੁਨਿਕ ਧਾਰਨਾਵਾਂ ਲਈ ਆਧਾਰ ਪ੍ਰਦਾਨ ਕਰਦੇ ਹਨ। ਉਸਦੇ ਵਿਚਾਰ ਆਇਨਿਕ ਯੌਗਿਕਾਂ ਦੀ ਸਮਝ ਅਤੇ ਪ੍ਰਬੰਧਨ ਵਿੱਚ ਬਹੁਤ ਮਹੱਤਵਪੂਰਨ ਸਾਬਤ ਹੋਏ ਹਨ। ਉਸੇ ਸਮੇਂ ਉਸਨੇ ਇਸ ਤੱਥ ਨੂੰ ਮਾਨਤਾ ਦਿੱਤੀ ਕਿ ਬਹੁਤ ਸਾਰੇ ਯੌਗਿਕ ਇਨ੍ਹਾਂ ਧਾਰਨਾਵਾਂ ਵਿੱਚ ਫਿੱਟ ਨਹੀਂ ਬੈਠਦੇ ਸਨ।
4.1.1 ਅੱਠਕ ਨਿਯਮ
ਕੋਸਲ ਅਤੇ ਲਿਊਇਸ ਨੇ 1916 ਵਿੱਚ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਰਸਾਇਣਕ ਸੁਮੇਲ ਦਾ ਇੱਕ ਮਹੱਤਵਪੂਰਨ ਸਿਧਾਂਤ ਵਿਕਸਿਤ ਕੀਤਾ ਜਿਸਨੂੰ ਰਸਾਇਣਕ ਬੰਧਨ ਦਾ ਇਲੈਕਟ੍ਰੌਨਿਕ ਸਿਧਾਂਤ ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਇਸ ਅਨੁਸਾਰ, ਪਰਮਾਣੂ ਆਪਣੀਆਂ ਵੈਲੈਂਸ ਸ਼ੈਲਾਂ ਵਿੱਚ ਇੱਕ ਅੱਠਕ ਪ੍ਰਾਪਤ ਕਰਨ ਲਈ ਇੱਕ ਪਰਮਾਣੂ ਤੋਂ ਦੂਜੇ ਪਰਮਾਣੂ ਵਿੱਚ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੇ ਤਬਾਦਲੇ (ਲਾਭ ਜਾਂ ਨੁਕਸਾਨ) ਜਾਂ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਸਾਂਝ ਕਰਕੇ ਜੁੜ ਸਕਦੇ ਹਨ। ਇਸਨੂੰ ਅੱਠਕ ਨਿਯਮ ਕਿਹਾ ਜਾਂਦਾ ਹੈ।
4.1.2 ਸਹਿਸੰਯੋਜਕ ਬੰਧਨ
ਲੈਂਗਮੁਇਰ (1919) ਨੇ ਅੱਠਕ ਦੀ ਸਥਿਰ ਘਣਾਕਾਰ ਵਿਵਸਥਾ ਦੇ ਵਿਚਾਰ ਨੂੰ ਛੱਡ ਕੇ ਅਤੇ ਸਹਿਸੰਯੋਜਕ ਬੰਧਨ ਸ਼ਬਦ ਦੀ ਸ਼ੁਰੂਆਤ ਕਰਕੇ ਲਿਊਇਸ ਦੇ ਪ੍ਰਸਤਾਵਾਂ ਨੂੰ ਸੁਧਾਰਿਆ। ਲਿਊਇਸ-ਲੈਂਗਮੁਇਰ ਸਿਧਾਂਤ ਨੂੰ ਕਲੋਰੀਨ ਅਣੂ, $\mathrm{Cl}_2$ ਦੇ ਨਿਰਮਾਣ ‘ਤੇ ਵਿਚਾਰ ਕਰਕੇ ਸਮਝਿਆ ਜਾ ਸਕਦਾ ਹੈ। ਇਲੈਕਟ੍ਰੌਨਿਕ ਵਿਵਸਥਾ, $[\mathrm{Ne}] 3 s^2 3 p^5$ ਵਾਲਾ $\mathrm{Cl}$ ਪਰਮਾਣੂ, ਆਰਗਨ ਵਿਵਸਥਾ ਤੋਂ ਇੱਕ ਇਲੈਕਟ੍ਰੌਨ ਘੱਟ ਹੈ। $\mathrm{Cl}_2$ ਅਣੂ ਦਾ ਨਿਰਮਾਣ ਦੋ ਕਲੋਰੀਨ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਇੱਕ ਜੋੜੀ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਸਾਂਝ ਦੇ ਸੰਦਰਭ ਵਿੱਚ ਸਮਝਿਆ ਜਾ ਸਕਦਾ ਹੈ, ਹਰੇਕ ਕਲੋਰੀਨ ਪਰਮਾਣੂ ਸਾਂਝੀ ਜੋੜੀ ਵਿੱਚ ਇੱਕ ਇਲੈਕਟ੍ਰੌਨ ਦਾ ਯੋਗਦਾਨ ਪਾਉਂਦਾ ਹੈ। ਇਸ ਪ੍ਰਕਿਰਿਆ ਵਿੱਚ ਦੋਵੇਂ ਕਲੋਰੀਨ ਪਰਮਾਣੂ ਨਜ਼ਦੀਕੀ ਨੋਬਲ ਗੈਸ (ਭਾਵ, ਆਰਗਨ) ਦਾ ਬਾਹਰੀ ਸ਼ੈਲ ਅੱਠਕ ਪ੍ਰਾਪਤ ਕਰਦੇ ਹਨ।

ਦੋ Cl ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਸਹਿਸੰਯੋਜਕ ਬੰਧਨ
ਬਿੰਦੀਆਂ ਇਲੈਕਟ੍ਰੌਨਾਂ ਨੂੰ ਦਰਸਾਉਂਦੀਆਂ ਹਨ। ਅਜਿਹੀਆਂ ਬਣਤਰਾਂ ਨੂੰ ਲਿਊਇਸ ਡੌਟ ਬਣਤਰਾਂ ਵਜੋਂ ਜਾਣਿਆ ਜਾਂਦਾ ਹੈ।
ਲਿਊਇਸ ਡੌਟ ਬਣਤਰਾਂ ਹੋਰ ਅਣੂਆਂ ਲਈ ਵੀ ਲਿਖੀਆਂ ਜਾ ਸਕਦੀਆਂ ਹਨ, ਜਿਸ ਵਿੱਚ ਜੁੜਨ ਵਾਲੇ ਪਰਮਾਣੂ ਇੱਕੋ ਜਿਹੇ ਜਾਂ ਵੱਖਰੇ ਹੋ ਸਕਦੇ ਹਨ। ਮਹੱਤਵਪੂਰਨ ਸ਼ਰਤਾਂ ਇਹ ਹਨ ਕਿ:
- ਹਰੇਕ ਬੰਧਨ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਇੱਕ ਇਲੈਕਟ੍ਰੌਨ ਜੋੜੀ ਦੀ ਸਾਂਝ ਦੇ ਨਤੀਜੇ ਵਜੋਂ ਬਣਦਾ ਹੈ।
- ਹਰੇਕ ਜੁੜਨ ਵਾਲਾ ਪਰਮਾਣੂ ਸਾਂਝੀ ਜੋੜੀ ਵਿੱਚ ਘੱਟੋ-ਘੱਟ ਇੱਕ ਇਲੈਕਟ੍ਰੌਨ ਦਾ ਯੋਗਦਾਨ ਪਾਉਂਦਾ ਹੈ।
- ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਸਾਂਝ ਦੇ ਨਤੀਜੇ ਵਜੋਂ ਜੁੜਨ ਵਾਲੇ ਪਰਮਾਣੂ ਬਾਹਰੀ ਸ਼ੈਲ ਨੋਬਲ ਗੈਸ ਵਿਵਸਥਾਵਾਂ ਪ੍ਰਾਪਤ ਕਰਦੇ ਹਨ।
- ਇਸ ਤਰ੍ਹਾਂ ਪਾਣੀ ਅਤੇ ਕਾਰਬਨ ਟੈਟ੍ਰਾਕਲੋਰਾਈਡ ਅਣੂਆਂ ਵਿੱਚ, ਸਹਿਸੰਯੋਜਕ ਬੰਧਨਾਂ ਦਾ ਨਿਰਮਾਣ ਇਸ ਤਰ੍ਹਾਂ ਦਰਸਾਇਆ ਜਾ ਸਕਦਾ ਹੈ:

ਇਸ ਤਰ੍ਹਾਂ, ਜਦੋਂ ਦੋ ਪਰਮਾਣੂ ਇੱਕ ਇਲੈਕਟ੍ਰੌਨ ਜੋੜੀ ਸਾਂਝੀ ਕਰਦੇ ਹਨ ਤਾਂ ਉਹ ਇੱਕ ਸਿੰਗਲ ਸਹਿਸੰਯੋਜਕ ਬੰਧਨ ਦੁਆਰਾ ਜੁੜੇ ਹੋਏ ਕਿਹੇ ਜਾਂਦੇ ਹਨ। ਬਹੁਤ ਸਾਰੇ ਯੌਗਿਕਾਂ ਵਿੱਚ ਸਾਡੇ ਕੋਲ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਬਹੁਵਚਨ ਬੰਧਨ ਹੁੰਦੇ ਹਨ। ਬਹੁਵਚਨ ਬੰਧਨਾਂ ਦਾ ਨਿਰਮਾਣ ਦੋ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਇੱਕ ਤੋਂ ਵੱਧ ਇਲੈਕਟ੍ਰੌਨ ਜੋੜੀਆਂ ਦੀ ਸਾਂਝ ਦੀ ਕਲਪਨਾ ਕਰਦਾ ਹੈ। ਜੇਕਰ ਦੋ ਪਰਮਾਣੂ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀਆਂ ਦੋ ਜੋੜੀਆਂ ਸਾਂਝੀਆਂ ਕਰਦੇ ਹਨ, ਤਾਂ ਉਹਨਾਂ ਵਿਚਕਾਰ ਸਹਿਸੰਯੋਜਕ ਬੰਧਨ ਨੂੰ ਡਬਲ ਬਾਂਡ ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਉਦਾਹਰਨ ਲਈ, ਕਾਰਬਨ ਡਾਈਆਕਸਾਈਡ ਅਣੂ ਵਿੱਚ, ਸਾਡੇ ਕੋਲ ਕਾਰਬਨ ਅਤੇ ਆਕਸੀਜਨ ਪਰਮਾਣੂਆਂ ਵਿਚਕਾਰ ਦੋ ਡਬਲ ਬਾਂਡ ਹਨ। ਇਸੇ ਤਰ੍ਹਾਂ ਈਥੀਨ ਅਣੂ ਵਿੱਚ ਦੋ ਕਾਰਬਨ ਪਰਮਾਣੂ ਇੱਕ ਡਬਲ ਬਾਂਡ ਦੁਆਰਾ ਜੁੜੇ ਹੁੰਦੇ ਹਨ।

$\mathrm{C} _{2} \mathrm{H} _{4}$ ਅਣੂ
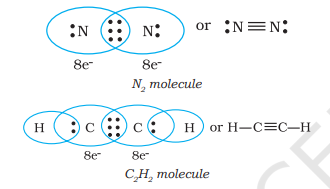
ਜਦੋਂ ਜੁੜਨ ਵਾਲੇ ਪਰਮਾਣੂ ਤਿੰਨ ਇਲੈਕਟ੍ਰ੍ਨ ਜੋੜੀਆਂ ਸਾਂਝੀਆਂ ਕਰਦੇ ਹਨ ਜਿਵੇਂ ਕਿ $N_{2}$ ਅਣੂ ਵਿੱਚ ਦੋ ਨਾਈਟ੍ਰੋਜਨ ਪਰਮਾਣੂਆਂ ਅਤੇ ਈਥਾਈਨ ਅਣੂ ਵਿੱਚ ਦੋ ਕਾਰਬਨ ਪਰਮਾਣੂਆਂ ਦੇ ਮਾਮਲੇ ਵਿੱਚ, ਇੱਕ ਟ੍ਰਿਪਲ ਬਾਂਡ ਬਣਦਾ ਹੈ।
4.1.3 ਸਧਾਰਨ ਅਣੂਆਂ ਦੀ ਲਿਊਇਸ ਨੁਮਾਇੰਦਗੀ (ਲਿਊਇਸ ਬਣਤਰਾਂ)
ਲਿਊਇਸ ਡੌਟ ਬਣਤਰਾਂ ਸਾਂਝੀਆਂ ਇਲੈਕਟ੍ਰੌਨ ਜੋੜੀਆਂ ਅਤੇ ਅੱਠਕ ਨਿਯਮ ਦੇ ਸੰਦਰਭ ਵਿੱਚ ਅਣੂਆਂ ਅਤੇ ਆਇਨਾਂ ਵਿੱਚ ਬੰਧਨ ਦੀ ਇੱਕ ਤਸਵੀਰ ਪ੍ਰਦਾਨ ਕਰਦੀਆਂ ਹਨ। ਜਦਕਿ ਅਜਿਹੀ ਤਸਵੀਰ ਇੱਕ ਅਣੂ ਦੇ ਬੰਧਨ ਅਤੇ ਵਿਵਹਾਰ ਨੂੰ ਪੂਰੀ ਤਰ੍ਹਾਂ ਨਹੀਂ ਸਮਝਾ ਸਕਦੀ, ਇਹ ਇੱਕ ਅਣੂ ਦੇ ਨਿਰਮਾਣ ਅਤੇ ਗੁਣਾਂ ਨੂੰ ਬਹੁਤ ਹੱਦ ਤੱਕ ਸਮਝਣ ਵਿੱਚ ਮਦਦ ਕਰਦੀ ਹੈ। ਇਸ ਲਈ, ਅਣੂਆਂ ਦੀਆਂ ਲਿਊਇਸ ਡੌਟ ਬਣਤਰਾਂ ਲਿਖਣਾ ਬਹੁਤ ਲਾਭਦਾਇਕ ਹੈ। ਲਿਊਇਸ ਡੌਟ ਬਣਤਰਾਂ ਹੇਠ ਲਿਖੇ ਕਦਮ ਅਪਣਾ ਕੇ ਲਿਖੀਆਂ ਜਾ ਸਕਦੀਆਂ ਹਨ:
- ਬਣਤਰਾਂ ਲਿਖਣ ਲਈ ਲੋੜੀਂਦੇ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਕੁੱਲ ਸੰਖਿਆ ਜੁੜਨ ਵਾਲੇ ਪਰਮਾਣੂਆਂ ਦੇ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨਾਂ ਨੂੰ ਜੋੜ ਕੇ ਪ੍ਰਾਪਤ ਕੀਤੀ ਜਾਂਦੀ ਹੈ। ਉਦਾਹਰਨ ਲਈ, $\mathrm{CH}_{4}$ ਅਣੂ ਵਿੱਚ ਬੰਧਨ ਲਈ ਅੱਠ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨ ਉਪਲਬਧ ਹਨ (ਕਾਰਬਨ ਤੋਂ 4 ਅਤੇ ਚਾਰ ਹਾਈਡ੍ਰੋਜਨ ਪਰਮਾਣੂਆਂ ਤੋਂ 4)।
- ਨਕਾਰਾਤਮਕ ਆਇਨਾਂ ਲਈ, ਹਰੇਕ ਨਕਾਰਾਤਮਕ ਚਾਰਜ ਦਾ ਮਤਲਬ ਹੋਵੇਗਾ ਇੱਕ ਇਲੈਕਟ੍ਰੌਨ ਦਾ ਜੋੜ। ਧਨਾਤਮਕ ਆਇਨਾਂ ਲਈ, ਹਰੇਕ ਧਨਾਤਮਕ ਚਾਰਜ ਦਾ ਨਤੀਜਾ ਵੈਲੈਂਸ ਇਲੈਕਟ੍ਰੌਨਾਂ ਦੀ ਕੁੱਲ ਸੰਖਿਆ ਵਿੱਚੋਂ ਇੱਕ ਇਲੈਕਟ੍ਰੌਨ ਦੀ ਘਟਾਓ ਹੋਵੇਗਾ। ਉਦਾਹਰਨ ਲਈ, $CO_3^{2-}$ ਆਇਨ ਲਈ, ਦੋ ਨਕਾਰਾਤਮ








