ਅਧਿਆਇ 08 ਰੈਡੌਕਸ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ
“ਜਿੱਥੇ ਆਕਸੀਕਰਨ ਹੁੰਦਾ ਹੈ, ਉੱਥੇ ਹਮੇਸ਼ਾ ਰਿਡਕਸ਼ਨ ਹੁੰਦੀ ਹੈ। ਰਸਾਇਣ ਵਿਗਿਆਨ ਅਸਲ ਵਿੱਚ ਰੈਡੌਕਸ ਪ੍ਰਣਾਲੀਆਂ ਦਾ ਅਧਿਐਨ ਹੈ।”
ਰਸਾਇਣ ਵਿਗਿਆਨ ਪਦਾਰਥ ਦੀਆਂ ਕਿਸਮਾਂ ਅਤੇ ਇੱਕ ਕਿਸਮ ਦੇ ਪਦਾਰਥ ਦਾ ਦੂਜੇ ਵਿੱਚ ਬਦਲਾਅ ਨਾਲ ਸੰਬੰਧਿਤ ਹੈ। ਪਦਾਰਥ ਦਾ ਇੱਕ ਕਿਸਮ ਤੋਂ ਦੂਜੇ ਕਿਸਮ ਵਿੱਚ ਰੂਪਾਂਤਰਨ ਵੱਖ-ਵੱਖ ਕਿਸਮਾਂ ਦੀਆਂ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਰਾਹੀਂ ਹੁੰਦਾ ਹੈ। ਅਜਿਹੀਆਂ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਦੀ ਇੱਕ ਮਹੱਤਵਪੂਰਨ ਸ਼੍ਰੇਣੀ ਰੈਡੌਕਸ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਹੈ। ਕਈ ਘਟਨਾਵਾਂ, ਭੌਤਿਕ ਅਤੇ ਜੀਵ-ਵਿਗਿਆਨਿਕ ਦੋਵੇਂ, ਰੈਡੌਕਸ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਨਾਲ ਸੰਬੰਧਿਤ ਹਨ। ਇਹ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਫਾਰਮਾਸਿਊਟੀਕਲ, ਜੀਵ-ਵਿਗਿਆਨਿਕ, ਉਦਯੋਗਿਕ, ਧਾਤ-ਵਿਗਿਆਨਿਕ ਅਤੇ ਖੇਤੀਬਾੜੀ ਖੇਤਰਾਂ ਵਿੱਚ ਵਿਆਪਕ ਉਪਯੋਗ ਰੱਖਦੀਆਂ ਹਨ। ਇਹਨਾਂ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਦੀ ਮਹੱਤਤਾ ਇਸ ਤੱਥ ਤੋਂ ਸਪੱਸ਼ਟ ਹੈ ਕਿ ਘਰੇਲੂ, ਆਵਾਜਾਈ ਅਤੇ ਹੋਰ ਵਪਾਰਕ ਉਦੇਸ਼ਾਂ ਲਈ ਊਰਜਾ ਪ੍ਰਾਪਤ ਕਰਨ ਲਈ ਵੱਖ-ਵੱਖ ਕਿਸਮਾਂ ਦੇ ਬਾਲਣਾਂ ਦਾ ਸਾੜਨਾ, ਬਹੁਤ ਕਿਰਿਆਸ਼ੀਲ ਧਾਤਾਂ ਅਤੇ ਅਧਾਤਾਂ ਦੇ ਨਿਕਾਸ ਲਈ ਇਲੈਕਟ੍ਰੋਕੈਮੀਕਲ ਪ੍ਰਕਿਰਿਆਵਾਂ, ਕਾਸਟਿਕ ਸੋਡਾ ਵਰਗੇ ਰਸਾਇਣਿਕ ਯੋਗਿਕਾਂ ਦਾ ਨਿਰਮਾਣ, ਸੁੱਕੀ ਅਤੇ ਗਿੱਲੀ ਬੈਟਰੀਆਂ ਦਾ ਸੰਚਾਲਨ ਅਤੇ ਧਾਤਾਂ ਦਾ ਜੰਗ ਲੱਗਣਾ ਰੈਡੌਕਸ ਪ੍ਰਕਿਰਿਆਵਾਂ ਦੇ ਦਾਇਰੇ ਵਿੱਚ ਆਉਂਦੇ ਹਨ। ਹਾਲ ਹੀ ਵਿੱਚ, ਹਾਈਡ੍ਰੋਜਨ ਇਕਨਾਮੀ (ਬਾਲਣ ਦੇ ਰੂਪ ਵਿੱਚ ਤਰਲ ਹਾਈਡ੍ਰੋਜਨ ਦਾ ਉਪਯੋਗ) ਅਤੇ ‘ਓਜ਼ੋਨ ਹੋਲ’ ਦੇ ਵਿਕਾਸ ਵਰਗੇ ਵਾਤਾਵਰਣਕ ਮੁੱਦੇ ਰੈਡੌਕਸ ਘਟਨਾ ਅਧੀਨ ਸ਼ਾਮਲ ਹੋਣੇ ਸ਼ੁਰੂ ਹੋ ਗਏ ਹਨ।
8.1 ਰੈਡੌਕਸ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਦਾ ਸ਼ਾਸਤਰੀ ਵਿਚਾਰ - ਆਕਸੀਕਰਨ ਅਤੇ ਰਿਡਕਸ਼ਨ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ
ਮੂਲ ਰੂਪ ਵਿੱਚ, ਆਕਸੀਕਰਨ ਸ਼ਬਦ ਦੀ ਵਰਤੋਂ ਕਿਸੇ ਤੱਤ ਜਾਂ ਯੋਗਿਕ ਵਿੱਚ ਆਕਸੀਜਨ ਦੇ ਜੋੜਨ ਨੂੰ ਦਰਸਾਉਣ ਲਈ ਕੀਤੀ ਜਾਂਦੀ ਸੀ। ਵਾਯੂਮੰਡਲ ਵਿੱਚ ਡਾਈਆਕਸੀਜਨ ਦੀ ਮੌਜੂਦਗੀ (20%) ਕਾਰਨ, ਬਹੁਤ ਸਾਰੇ ਤੱਤ ਇਸ ਨਾਲ ਜੁੜ ਜਾਂਦੇ ਹਨ ਅਤੇ ਇਹ ਮੁੱਖ ਕਾਰਨ ਹੈ ਕਿ ਉਹ ਆਮ ਤੌਰ ‘ਤੇ ਧਰਤੀ ‘ਤੇ ਆਪਣੇ ਆਕਸਾਈਡਾਂ ਦੇ ਰੂਪ ਵਿੱਚ ਮਿਲਦੇ ਹਨ। ਹੇਠ ਲਿਖੀਆਂ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਆਕਸੀਕਰਨ ਦੀ ਸੀਮਿਤ ਪਰਿਭਾਸ਼ਾ ਅਨੁਸਾਰ ਆਕਸੀਕਰਨ ਪ੍ਰਕਿਰਿਆਵਾਂ ਨੂੰ ਦਰਸਾਉਂਦੀਆਂ ਹਨ:
$$2 \mathrm{Mg}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{MgO}(\mathrm{s}) \tag{8.1}$$
$$\mathrm{S}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow \mathrm{SO_2}(\mathrm{~g}) \tag{8.2}$$
ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ (8.1) ਅਤੇ (8.2) ਵਿੱਚ, ਤੱਤ ਮੈਗਨੀਸ਼ੀਅਮ ਅਤੇ ਸਲਫਰ ਉਹਨਾਂ ਵਿੱਚ ਆਕਸੀਜਨ ਦੇ ਜੋੜਨ ਕਾਰਨ ਆਕਸੀਕ੍ਰਿਤ ਹੁੰਦੇ ਹਨ। ਇਸੇ ਤਰ੍ਹਾਂ, ਮੀਥੇਨ ਇਸ ਵਿੱਚ ਆਕਸੀਜਨ ਦੇ ਜੋੜਨ ਕਾਰਨ ਆਕਸੀਕ੍ਰਿਤ ਹੁੰਦੀ ਹੈ।
$$\mathrm{CH} _{4}(\mathrm{~g})+2 \mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g})+2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{7.3}$$
ਪ੍ਰਤੀਕਿਰਿਆ (8.3) ਦੀ ਸਾਵਧਾਨੀ ਨਾਲ ਜਾਂਚ, ਜਿਸ ਵਿੱਚ ਹਾਈਡ੍ਰੋਜਨ ਨੂੰ ਆਕਸੀਜਨ ਨਾਲ ਬਦਲਿਆ ਗਿਆ ਹੈ, ਨੇ ਰਸਾਇਣ ਵਿਗਿਆਨੀਆਂ ਨੂੰ ਇਸ ਤੋਂ ਹਾਈਡ੍ਰੋਜਨ ਦੇ ਹਟਾਉਣ ਦੇ ਰੂਪ ਵਿੱਚ ਆਕਸੀਕਰਨ ਦੀ ਮੁੜ ਵਿਆਖਿਆ ਕਰਨ ਲਈ ਪ੍ਰੇਰਿਤ ਕੀਤਾ ਅਤੇ, ਇਸ ਲਈ, ਆਕਸੀਕਰਨ ਸ਼ਬਦ ਦੇ ਦਾਇਰੇ ਨੂੰ ਕਿਸੇ ਪਦਾਰਥ ਤੋਂ ਹਾਈਡ੍ਰੋਜਨ ਦੇ ਹਟਾਉਣ ਨੂੰ ਸ਼ਾਮਲ ਕਰਨ ਲਈ ਵਿਸਤਾਰਿਤ ਕੀਤਾ ਗਿਆ। ਹੇਠ ਲਿਖੀ ਦ੍ਰਿਸ਼ਟਾਂਤ ਇੱਕ ਹੋਰ ਪ੍ਰਤੀਕਿਰਿਆ ਹੈ ਜਿੱਥੇ ਹਾਈਡ੍ਰੋਜਨ ਦਾ ਹਟਾਉਣਾ ਵੀ ਇੱਕ ਆਕਸੀਕਰਨ ਪ੍ਰਤੀਕਿਰਿਆ ਵਜੋਂ ਦਰਸਾਇਆ ਜਾ ਸਕਦਾ ਹੈ।
$$ \begin{equation*} 2 \mathrm{H_2} \mathrm{~S}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{~S}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \tag{8.4} \end{equation*} $$
ਰਸਾਇਣ ਵਿਗਿਆਨੀਆਂ ਦੇ ਗਿਆਨ ਵਿੱਚ ਵਾਧੇ ਨਾਲ, (7.1 ਤੋਂ 7.4) ਵਰਗੀਆਂ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਲਈ ਆਕਸੀਕਰਨ ਸ਼ਬਦ ਨੂੰ ਵਿਸਤਾਰਿਤ ਕਰਨਾ ਸੁਭਾਵਿਕ ਸੀ, ਜਿਨ੍ਹਾਂ ਵਿੱਚ ਆਕਸੀਜਨ ਸ਼ਾਮਲ ਨਹੀਂ ਹੁੰਦਾ ਪਰ ਹੋਰ ਇਲੈਕਟ੍ਰੋਨੇਗੇਟਿਵ ਤੱਤ ਸ਼ਾਮਲ ਹੁੰਦੇ ਹਨ। ਫਲੋਰੀਨ, ਕਲੋਰੀਨ ਅਤੇ ਸਲਫਰ ਆਦਿ ਨਾਲ ਮੈਗਨੀਸ਼ੀਅਮ ਦਾ ਆਕਸੀਕਰਨ ਹੇਠ ਲਿਖੀਆਂ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਅਨੁਸਾਰ ਹੁੰਦਾ ਹੈ:
$$\operatorname{Mg}(\mathrm{s})+\mathrm{F_2} (\mathrm{~g}) \rightarrow \operatorname{MgF_2} (s) \tag{8.5}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{Cl_2} (g) \rightarrow \mathrm{MgCl_2} (s) \tag{8.6}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{S} (s) \rightarrow \operatorname{MgS}(\mathrm{s}) \tag{8.7}$$
ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ (7.5 ਤੋਂ 7.7) ਨੂੰ ਆਕਸੀਕਰਨ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਦੇ ਦਾਇਰੇ ਵਿੱਚ ਸ਼ਾਮਲ ਕਰਨ ਨੇ ਰਸਾਇਣ ਵਿਗਿਆਨੀਆਂ ਨੂੰ ਨਾ ਸਿਰਫ਼ ਹਾਈਡ੍ਰੋਜਨ ਦੇ ਹਟਾਉਣ ਨੂੰ ਆਕਸੀਕਰਨ ਵਜੋਂ ਮੰਨਣ ਲਈ ਪ੍ਰੇਰਿਤ ਕੀਤਾ, ਬਲਕਿ ਇਲੈਕਟ੍ਰੋਪੋਜ਼ਿਟਿਵ ਤੱਤਾਂ ਦੇ ਹਟਾਉਣ ਨੂੰ ਵੀ ਆਕਸੀਕਰਨ ਵਜੋਂ ਮੰਨਣ ਲਈ ਪ੍ਰੇਰਿਤ ਕੀਤਾ। ਇਸ ਲਈ ਪ੍ਰਤੀਕਿਰਿਆ:
$$ 2 \mathrm{~K_4} \left[ \mathrm{Fe} ( \mathrm{CN})_{6} \right] ( \mathrm{aq}) + \mathrm{H_2} \mathrm{O_2} ( \mathrm{aq}) \rightarrow 2 \mathrm{~K_3} \left[\mathrm{Fe}( \mathrm{CN})_6 \right] ( \mathrm{aq}) + 2 \mathrm{KOH} ( \mathrm{aq}) $$
ਨੂੰ ਪੋਟਾਸ਼ੀਅਮ ਫੈਰੋਸਾਇਨਾਈਡ ਤੋਂ ਇਲੈਕਟ੍ਰੋਪੋਜ਼ਿਟਿਵ ਤੱਤ ਪੋਟਾਸ਼ੀਅਮ ਦੇ ਹਟਾਉਣ ਕਾਰਨ ਆਕਸੀਕਰਨ ਵਜੋਂ ਵਿਆਖਿਆਤ ਕੀਤਾ ਜਾਂਦਾ ਹੈ, ਇਸ ਤੋਂ ਪਹਿਲਾਂ ਕਿ ਇਹ ਪੋਟਾਸ਼ੀਅਮ ਫੈਰਿਸਾਇਨਾਈਡ ਵਿੱਚ ਬਦਲ ਜਾਵੇ। ਸੰਖੇਪ ਵਿੱਚ, “ਆਕਸੀਕਰਨ” ਸ਼ਬਦ ਨੂੰ ਕਿਸੇ ਪਦਾਰਥ ਵਿੱਚ ਆਕਸੀਜਨ/ਇਲੈਕਟ੍ਰੋਨੇਗੇਟਿਵ ਤੱਤ ਦੇ ਜੋੜਨ ਜਾਂ ਕਿਸੇ ਪਦਾਰਥ ਤੋਂ ਹਾਈਡ੍ਰੋਜਨ/ਇਲੈਕਟ੍ਰੋਪੋਜ਼ਿਟਿਵ ਤੱਤ ਦੇ ਹਟਾਉਣ ਵਜੋਂ ਪਰਿਭਾਸ਼ਿਤ ਕੀਤਾ ਗਿਆ ਹੈ।
ਸ਼ੁਰੂਆਤ ਵਿੱਚ, ਰਿਡਕਸ਼ਨ ਨੂੰ ਕਿਸੇ ਯੋਗਿਕ ਤੋਂ ਆਕਸੀਜਨ ਦੇ ਹਟਾਉਣ ਵਜੋਂ ਮੰਨਿਆ ਜਾਂਦਾ ਸੀ। ਹਾਲਾਂਕਿ, ਰਿਡਕਸ਼ਨ ਸ਼ਬਦ ਨੂੰ ਇਨ੍ਹਾਂ ਦਿਨਾਂ ਵਿੱਚ ਕਿਸੇ ਪਦਾਰਥ ਤੋਂ ਆਕਸੀਜਨ/ਇਲੈਕਟ੍ਰੋਨੇਗੇਟਿਵ ਤੱਤ ਦੇ ਹਟਾਉਣ ਜਾਂ ਕਿਸੇ ਪਦਾਰਥ ਵਿੱਚ ਹਾਈਡ੍ਰੋਜਨ/ਇਲੈਕਟ੍ਰੋਪੋਜ਼ਿਟਿਵ ਤੱਤ ਦੇ ਜੋੜਨ ਨੂੰ ਸ਼ਾਮਲ ਕਰਨ ਲਈ ਵਿਸਤਾਰਿਤ ਕੀਤਾ ਗਿਆ ਹੈ।
ਉੱਪਰ ਦਿੱਤੀ ਪਰਿਭਾਸ਼ਾ ਅਨੁਸਾਰ, ਹੇਠ ਲਿਖੇ ਰਿਡਕਸ਼ਨ ਪ੍ਰਕਿਰਿਆਵਾਂ ਦੇ ਉਦਾਹਰਨ ਹਨ:
$$2 \mathrm{HgO}(\mathrm{s}) \xrightarrow{\Delta} 2 \mathrm{Hg}(\mathrm{l})+\mathrm{O_2}(\mathrm{~g}) \tag{8.8}$$
(ਮਰਕਿਊਰਿਕ ਆਕਸਾਈਡ ਤੋਂ ਆਕਸੀਜਨ ਦਾ ਹਟਾਉਣਾ)
$$2 \mathrm{FeCl_3}(\mathrm{aq})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{FeCl_2}(\mathrm{aq})+2 \mathrm{HCl}(\mathrm{aq}) \tag{8.9}$$
(ਇਲੈਕਟ੍ਰੋਨੇਗੇਟਿਵ ਤੱਤ, ਕਲੋਰੀਨ ਦਾ ਫੈਰਿਕ ਕਲੋਰਾਈਡ ਤੋਂ ਹਟਾਉਣਾ)
$$\mathrm{CH_2}=\mathrm{CH_2}(\mathrm{~g})+\mathrm{H_2}(\mathrm{~g}) \rightarrow \mathrm{H_3} \mathrm{C}-\mathrm{CH_3}(\mathrm{~g})\tag{8.10}$$
(ਹਾਈਡ੍ਰੋਜਨ ਦਾ ਜੋੜ)
$$2 \mathrm{HgCl_2}(\mathrm{aq})+\mathrm{SnCl_2}(\mathrm{aq}) \rightarrow \mathrm{Hg_2} \mathrm{Cl_2}(\mathrm{~s})+\mathrm{SnCl_4}(\mathrm{aq})\tag{8.11}$$
(ਮਰਕਿਊਰਿਕ ਕਲੋਰਾਈਡ ਵਿੱਚ ਪਾਰੇ ਦਾ ਜੋੜ)
ਪ੍ਰਤੀਕਿਰਿਆ (8.11) ਵਿੱਚ ਸਟੈਨਸ ਕਲੋਰਾਈਡ ਦਾ ਸਟੈਨਿਕ ਕਲੋਰਾਈਡ ਵਿੱਚ ਇਸ ਵਿੱਚ ਇਲੈਕਟ੍ਰੋਨੇਗੇਟਿਵ ਤੱਤ ਕਲੋਰੀਨ ਦੇ ਜੋੜਨ ਕਾਰਨ ਇਕੱਠਾ ਆਕਸੀਕਰਨ ਵੀ ਹੋ ਰਿਹਾ ਹੈ। ਇਹ ਜਲਦੀ ਹੀ ਅਹਿਸਾਸ ਹੋ ਗਿਆ ਕਿ ਆਕਸੀਕਰਨ ਅਤੇ ਰਿਡਕਸ਼ਨ ਹਮੇਸ਼ਾ ਇਕੱਠੇ ਹੁੰਦੇ ਹਨ (ਜਿਵੇਂ ਕਿ ਉੱਪਰ ਦਿੱਤੇ ਸਾਰੇ ਸਮੀਕਰਨਾਂ ਦੀ ਮੁੜ ਜਾਂਚ ਕਰਕੇ ਸਪੱਸ਼ਟ ਹੋਵੇਗਾ), ਇਸ ਲਈ, ਰਸਾਇਣਿਕ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਦੀ ਇਸ ਸ਼੍ਰੇਣੀ ਲਈ “ਰੈਡੌਕਸ” ਸ਼ਬਦ ਘੜਿਆ ਗਿਆ ਸੀ।
ਸਮੱਸਿਆ 8.1
ਹੇਠ ਲਿਖੀਆਂ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਵਿੱਚ, ਆਕਸੀਕ੍ਰਿਤ ਅਤੇ ਰਿਡਿਊਸ ਹੋ ਰਹੀਆਂ ਸਪੀਸੀਜ਼ ਦੀ ਪਛਾਣ ਕਰੋ:
(i) $\mathrm{H_2} \mathrm{~S}$ (g) $+\mathrm{Cl_2}$ (g) $\rightarrow 2 \mathrm{HCl}$ (g) $+\mathrm{S}$ (s)
(ii) $3 \mathrm{Fe_3} \mathrm{O_4}$ (s) $+8 \mathrm{Al}$ (s) $\rightarrow 9 \mathrm{Fe}$ (s) $+4 \mathrm{Al_2} \mathrm{O_3}(\mathrm{~s})$
(iii) $2 \mathrm{Na}$ (s) $+\mathrm{H_2}$ (g) $\rightarrow 2 \mathrm{NaH}$ (s)
ਹੱਲ
(i) $\mathrm{H_2} \mathrm{~S}$ ਆਕਸੀਕ੍ਰਿਤ ਹੁੰਦਾ ਹੈ ਕਿਉਂਕਿ ਹਾਈਡ੍ਰੋਜਨ ਵਿੱਚ ਇੱਕ ਵਧੇਰੇ ਇਲੈਕਟ੍ਰੋਨੇਗੇਟਿਵ ਤੱਤ, ਕਲੋਰੀਨ ਜੋੜਿਆ ਜਾਂਦਾ ਹੈ (ਜਾਂ ਇੱਕ ਵਧੇਰੇ ਇਲੈਕਟ੍ਰੋਪੋਜ਼ਿਟਿਵ ਤੱਤ, ਹਾਈਡ੍ਰੋਜਨ ਨੂੰ S ਤੋਂ ਹਟਾ ਦਿੱਤਾ ਗਿਆ ਹੈ)। ਕਲੋਰੀਨ ਇਸ ਵਿੱਚ ਹਾਈਡ੍ਰੋਜਨ ਦੇ ਜੋੜਨ ਕਾਰਨ ਰਿਡਿਊਸ ਹੁੰਦੀ ਹੈ।
(ii) ਐਲੂਮੀਨੀਅਮ ਆਕਸੀਕ੍ਰਿਤ ਹੁੰਦਾ ਹੈ ਕਿਉਂਕਿ ਇਸ ਵਿੱਚ ਆਕਸੀਜਨ ਜੋੜਿਆ ਜਾਂਦਾ ਹੈ। ਫੈਰਸ ਫੈਰਿਕ ਆਕਸਾਈਡ $\left(\mathrm{Fe_3} \mathrm{O_4}\right)$ ਰਿਡਿਊਸ ਹੁੰਦਾ ਹੈ ਕਿਉਂਕਿ ਇਸ ਤੋਂ ਆਕਸੀਜਨ ਹਟਾ ਦਿੱਤਾ ਗਿਆ ਹੈ।
(iii) ਇਲੈਕਟ੍ਰੋਨੇਗੇਟਿਵਿਟੀ ਦੀ ਧਾਰਨਾ ਦੀ ਸਾਵਧਾਨੀ ਨਾਲ ਵਰਤੋਂ ਨਾਲ ਹੀ ਅਸੀਂ ਅਨੁਮਾਨ ਲਗਾ ਸਕਦੇ ਹਾਂ ਕਿ ਸੋਡੀਅਮ ਆਕਸੀਕ੍ਰਿਤ ਹੁੰਦਾ ਹੈ ਅਤੇ ਹਾਈਡ੍ਰੋਜਨ ਰਿਡਿਊਸ ਹੁੰਦਾ ਹੈ।
ਇੱਥੇ ਚੁਣੀ ਗਈ ਪ੍ਰਤੀਕਿਰਿਆ (iii) ਸਾਨੂੰ ਰੈਡੌਕਸ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਨੂੰ ਪਰਿਭਾਸ਼ਿਤ ਕਰਨ ਦੇ ਇੱਕ ਹੋਰ ਤਰੀਕੇ ਬਾਰੇ ਸੋਚਣ ਲਈ ਪ੍ਰੇਰਿਤ ਕਰਦੀ ਹੈ।
8.2 ਇਲੈਕਟ੍ਰਾਨ ਟ੍ਰਾਂਸਫਰ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਦੇ ਰੂਪ ਵਿੱਚ ਰੈਡੌਕਸ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ
ਅਸੀਂ ਪਹਿਲਾਂ ਹੀ ਸਿੱਖ ਚੁੱਕੇ ਹਾਂ ਕਿ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਰੈਡੌਕਸ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਹਨ ਕਿਉਂਕਿ ਇਹਨਾਂ ਵਿੱਚੋਂ ਹਰੇਕ ਪ੍ਰਤੀਕਿਰਿਆ ਵਿੱਚ ਸੋਡੀਅਮ ਆਕਸੀਕ੍ਰਿਤ ਹੁੰਦਾ ਹੈ ਕਿਉਂਕਿ ਸੋਡੀਅਮ ਵਿੱਚ ਆਕਸੀਜਨ ਜਾਂ ਵਧੇਰੇ ਇਲੈਕਟ੍ਰੋਨੇਗੇਟਿਵ ਤੱਤ ਜੋੜਿਆ ਜਾਂਦਾ ਹੈ।
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaCl}(\mathrm{s})\tag{8.12}$$
$$4 \mathrm{Na}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na_2} \mathrm{O}(\mathrm{s})\tag{8.13}$$
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{S}(\mathrm{s}) \rightarrow \mathrm{Na_2} \mathrm{~S}(\mathrm{~s}) \tag{8.14}$$
ਇਕੱਠੇ ਹੀ, ਕਲੋਰੀਨ, ਆਕਸੀਜਨ ਅਤੇ ਸਲਫਰ ਰਿਡਿਊਸ ਹੁੰਦੇ ਹਨ ਕਿਉਂਕਿ ਇਹਨਾਂ ਵਿੱਚੋਂ ਹਰੇਕ ਵਿੱਚ, ਇਲੈਕਟ੍ਰੋਪੋਜ਼ਿਟਿਵ ਤੱਤ ਸੋਡੀਅਮ ਜੋੜਿਆ ਗਿਆ ਹੈ। ਰਸਾਇਣਿਕ ਬੰਧਨ ਬਾਰੇ ਸਾਡੇ ਗਿਆਨ ਤੋਂ ਅਸੀਂ ਇਹ ਵੀ ਜਾਣਦੇ ਹਾਂ ਕਿ ਸੋਡੀਅਮ ਕਲੋਰਾਈਡ, ਸੋਡੀਅਮ ਆਕਸਾਈਡ ਅਤੇ ਸੋਡੀਅਮ ਸਲਫਾਈਡ ਆਇਨਿਕ ਯੋਗਿਕ ਹਨ ਅਤੇ ਸ਼ਾਇਦ ਬਿਹਤਰ ਰੂਪ ਵਿੱਚ $\mathrm{Na}^{+} \mathrm{Cl}^{-}( \mathrm{s}),\left(\mathrm{Na}^{+} \right)_2 \mathrm{O}^{2-}( \mathrm{s})$, ਅਤੇ $ \left(\mathrm{Na}^{+} \right)_2$ $\mathrm{S}^{2-}( \mathrm{s})$ ਵਜੋਂ ਲਿਖੇ ਜਾ ਸਕਦੇ ਹਨ। ਪੈਦਾ ਹੋਈਆਂ ਸਪੀਸੀਜ਼ ‘ਤੇ ਚਾਰਜਾਂ ਦਾ ਵਿਕਾਸ ਸਾਨੂੰ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ (8.12 ਤੋਂ 8.14) ਨੂੰ ਹੇਠ ਲਿਖੇ ਢੰਗ ਨਾਲ ਮੁੜ ਲਿਖਣ ਲਈ ਸੁਝਾਅ ਦਿੰਦਾ ਹੈ:
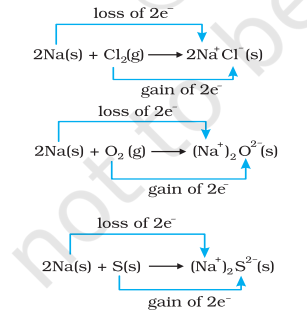
ਸੁਵਿਧਾ ਲਈ, ਉੱਪਰਲੀਆਂ ਵਿੱਚੋਂ ਹਰੇਕ ਪ੍ਰਕਿਰਿਆ ਨੂੰ ਦੋ ਵੱਖਰੇ ਕਦਮਾਂ ਵਜੋਂ ਮੰਨਿਆ ਜਾ ਸਕਦਾ ਹੈ, ਇੱਕ ਵਿੱਚ ਇਲੈਕਟ੍ਰਾਨਾਂ ਦਾ ਨੁਕਸਾਨ ਅਤੇ ਦੂਜੇ ਵਿੱਚ ਇਲੈਕਟ੍ਰਾਨਾਂ ਦਾ ਲਾਭ ਸ਼ਾਮਲ ਹੁੰਦਾ ਹੈ। ਇੱਕ ਦ੍ਰਿਸ਼ਟਾਂਤ ਵਜੋਂ, ਅਸੀਂ ਇਹਨਾਂ ਵਿੱਚੋਂ ਇੱਕ ਨੂੰ ਹੋਰ ਵਿਸਤਾਰ ਨਾਲ ਦਰਸਾ ਸਕਦੇ ਹਾਂ, ਮੰਨ ਲਓ, ਸੋਡੀਅਮ ਕਲੋਰਾਈਡ ਦਾ ਬਣਨਾ।
$2 \mathrm{Na}(\mathrm{s}) \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
$\mathrm{Cl_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{Cl}^{-}(\mathrm{g})$
ਉੱਪਰਲੇ ਵਿੱਚੋਂ ਹਰੇਕ ਕਦਮ ਨੂੰ ਅੱਧੀ ਪ੍ਰਤੀਕਿਰਿਆ ਕਿਹਾ ਜਾਂਦਾ ਹੈ, ਜੋ ਸਪੱਸ਼ਟ ਤੌਰ ‘ਤੇ ਇਲੈਕਟ੍ਰਾਨਾਂ ਦੀ ਸ਼ਮੂਲੀਅਤ ਦਰਸਾਉਂਦੀ ਹੈ। ਅੱਧੀਆਂ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਦਾ ਜੋੜ ਕੁੱਲ ਪ੍ਰਤੀਕਿਰਿਆ ਦਿੰਦਾ ਹੈ:
$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na}^{+} \mathrm{Cl}^{-}(\mathrm{s})$ ਜਾਂ $2 \mathrm{NaCl}(\mathrm{s})$
ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ 8.12 ਤੋਂ 8.14 ਸੁਝਾਅ ਦਿੰਦੀਆਂ ਹਨ ਕਿ ਅੱਧੀਆਂ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਜਿਨ੍ਹਾਂ ਵਿੱਚ ਇਲੈਕਟ੍ਰਾਨਾਂ ਦਾ ਨੁਕਸਾਨ ਸ਼ਾਮਲ ਹੁੰਦਾ ਹੈ, ਉਹਨਾਂ ਨੂੰ ਆਕਸੀਕਰਨ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਇਸੇ ਤਰ੍ਹਾਂ, ਅੱਧੀਆਂ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਜਿਨ੍ਹਾਂ ਵਿੱਚ ਇਲੈਕਟ੍ਰਾਨਾਂ ਦਾ ਲਾਭ ਸ਼ਾਮਲ ਹੁੰਦਾ ਹੈ, ਉਹਨਾਂ ਨੂੰ ਰਿਡਕਸ਼ਨ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਕਿਹਾ ਜਾਂਦਾ ਹੈ। ਇਹ ਇੱਥੇ ਸੰਦਰਭ ਤੋਂ ਬਾਹਰ ਨਹੀਂ ਹੋ ਸਕਦਾ ਕਿ ਆਕਸੀਕਰਨ ਅਤੇ ਰਿਡਕਸ਼ਨ ਨੂੰ ਪਰਿਭਾਸ਼ਿਤ ਕਰਨ ਦੇ ਨਵੇਂ ਤਰੀਕੇ ਨੂੰ ਸ਼ਾਸਤਰੀ ਵਿਚਾਰ ਅਨੁਸਾਰ ਸਪੀਸੀਜ਼ ਦੇ ਵਿਵਹਾਰ ਅਤੇ ਇਲੈਕਟ੍ਰਾਨ-ਟ੍ਰਾਂਸਫਰ ਬਦਲਾਅ ਵਿੱਚ ਉਹਨਾਂ ਦੇ ਪਰਸਪਰ ਕ੍ਰਿਆ ਦੇ ਵਿਚਕਾਰ ਸੰਬੰਧ ਸਥਾਪਿਤ ਕਰਕੇ ਹੀ ਪ੍ਰਾਪਤ ਕੀਤਾ ਗਿਆ ਹੈ। ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ (8.12 ਤੋਂ 8.14) ਵਿੱਚ ਸੋਡੀਅਮ, ਜੋ ਆਕਸੀਕ੍ਰਿਤ ਹੁੰਦਾ ਹੈ, ਇੱਕ ਰਿਡਿਊਸਿੰਗ ਏਜੰਟ ਵਜੋਂ ਕੰਮ ਕਰਦਾ ਹੈ ਕਿਉਂਕਿ ਇਹ ਇਸ ਨਾਲ ਪਰਸਪਰ ਕ੍ਰਿਆ ਕਰਨ ਵਾਲੇ ਹਰੇਕ ਤੱਤ ਨੂੰ ਇਲੈਕਟ੍ਰਾਨ ਦਾਨ ਕਰਦਾ ਹੈ ਅਤੇ ਇਸ ਤਰ੍ਹਾਂ ਉਹਨਾਂ ਨੂੰ ਘਟਾਉਣ ਵਿੱਚ ਮਦਦ ਕਰਦਾ ਹੈ। ਕਲੋਰੀਨ, ਆਕਸੀਜਨ ਅਤੇ ਸਲਫਰ ਰਿਡਿਊਸ ਹੁੰਦੇ ਹਨ ਅਤੇ ਆਕਸੀਕਾਰਕ ਏਜੰਟਾਂ ਵਜੋਂ ਕੰਮ ਕਰਦੇ ਹਨ ਕਿਉਂਕਿ ਇਹ ਸੋਡੀਅਮ ਤੋਂ ਇਲੈਕਟ੍ਰਾਨ ਗ੍ਰਹਿਣ ਕਰਦੇ ਹਨ। ਸੰਖੇਪ ਵਿੱਚ, ਅਸੀਂ ਦਰਸਾ ਸਕਦੇ ਹਾਂ ਕਿ
ਆਕਸੀਕਰਨ: ਕਿਸੇ ਵੀ ਸਪੀਸੀਜ਼ ਦੁਆਰਾ ਇਲੈਕਟ੍ਰਾਨ(ਆਂ) ਦਾ ਨੁਕਸਾਨ।
ਰਿਡਕਸ਼ਨ: ਕਿਸੇ ਵੀ ਸਪੀਸੀਜ਼ ਦੁਆਰਾ ਇਲੈਕਟ੍ਰਾਨ(ਆਂ) ਦਾ ਲਾਭ।
ਆਕਸੀਕਾਰਕ ਏਜੰਟ: ਇਲੈਕਟ੍ਰਾਨ(ਆਂ) ਦਾ ਗ੍ਰਹਿਣ ਕਰਨ ਵਾਲਾ।
ਰਿਡਿਊਸਿੰਗ ਏਜੰਟ: ਇਲੈਕਟ੍ਰਾਨ(ਆਂ) ਦਾ ਦਾਤਾ।
ਸਮੱਸਿਆ 8.2
ਦਰਸਾਓ ਕਿ ਪ੍ਰਤੀਕਿਰਿਆ: $2 \mathrm{Na}(\mathrm{s})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaH}$ (s) ਇੱਕ ਰੈਡੌਕਸ ਬਦਲਾਅ ਹੈ।
ਹੱਲ
ਕਿਉਂਕਿ ਉੱਪਰਲੀ ਪ੍ਰਤੀਕਿਰਿਆ ਵਿੱਚ ਬਣਿਆ ਯੋਗਿਕ ਇੱਕ ਆਇਨਿਕ ਯੋਗਿਕ ਹੈ, ਜਿਸ ਨੂੰ $\mathrm{Na}^{+} \mathrm{H}^{-}$(s) ਵਜੋਂ ਵੀ ਦਰਸਾਇਆ ਜਾ ਸਕਦਾ ਹੈ, ਇਹ ਸੁਝਾਅ ਦਿੰਦਾ ਹੈ ਕਿ ਇਸ ਪ੍ਰਕਿਰਿਆ ਵਿੱਚ ਇੱਕ ਅੱਧੀ ਪ੍ਰਤੀਕਿਰਿਆ ਹੈ:
$2 \mathrm{Na}(\mathrm{s}) \quad \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
ਅਤੇ ਦੂਜੀ ਅੱਧੀ ਪ੍ਰਤੀਕਿਰਿਆ ਹੈ:
$\mathrm{H_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{H}^{-}(\mathrm{g})$
ਜਾਂਚ ਅਧੀਨ ਪ੍ਰਤੀਕਿਰਿਆ ਦਾ ਦੋ ਅੱਧੀਆਂ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ ਵਿੱਚ ਵੰਡਣਾ ਆਪਣੇ ਆਪ ਹੀ ਦਰਸਾਉਂਦਾ ਹੈ ਕਿ ਇੱਥੇ ਸੋਡੀਅਮ ਆਕਸੀਕ੍ਰਿਤ ਹੁੰਦਾ ਹੈ ਅਤੇ ਹਾਈਡ੍ਰੋਜਨ ਰਿਡਿਊਸ ਹੁੰਦਾ ਹੈ, ਇਸ ਲਈ, ਪੂਰੀ ਪ੍ਰਤੀਕਿਰਿਆ ਇੱਕ ਰੈਡੌਕਸ ਬਦਲਾਅ ਹੈ।
8.2.1 ਮੁਕਾਬਲੇਬਾਜ਼ ਇਲੈਕਟ੍ਰਾਨ ਟ੍ਰਾਂਸਫਰ ਪ੍ਰਤੀਕਿਰਿਆਵਾਂ
ਤਾਂਬੇ ਦੇ ਨਾਈਟ੍ਰੇਟ ਦੇ ਜਲੀ ਘੋਲ ਵਿੱਚ ਧਾਤਵੀ ਜ਼ਿੰਕ ਦੀ ਇੱਕ ਪੱਟੀ ਰੱਖੋ ਜਿਵੇਂ ਕਿ ਚਿੱਤਰ 8.1 ਵਿੱਚ ਦਰਸਾਇਆ ਗਿਆ ਹੈ, ਲਗਭਗ ਇੱਕ ਘੰਟੇ ਲਈ। ਤੁਸੀਂ ਦੇਖ ਸਕਦੇ ਹੋ ਕਿ ਪੱਟੀ ਲਾਲ-ਰੰਗੀ ਧਾਤਵੀ ਤਾਂਬੇ ਨਾਲ ਲੇਪਿਤ ਹੋ ਜਾਂਦੀ ਹੈ ਅਤੇ ਘੋਲ ਦਾ ਨੀਲਾ ਰੰਗ ਗਾਇਬ ਹੋ ਜਾਂਦਾ ਹੈ। $\mathrm{Zn}^{2+}$ ਆਇਨਾਂ ਦਾ ਬਣਨਾ ਉਤਪਾਦਾਂ ਵਿੱਚੋਂ ਆਸਾਨੀ ਨਾਲ ਪਛਾਣਿਆ ਜਾ ਸਕਦਾ ਹੈ ਜਦੋਂ $\mathrm{Cu}^{2+}$ ਕਾਰਨ ਘੋਲ ਦਾ ਨੀਲਾ ਰੰਗ ਗਾਇਬ ਹੋ ਜਾਂਦਾ ਹੈ। ਜੇਕਰ ਹਾਈਡ੍ਰੋਜਨ ਸਲਫਾਈਡ ਗੈਸ ਨੂੰ $\mathrm{Zn}^{2+}$ ਆਇਨਾਂ ਵਾਲੇ ਬੇਰੰਗ ਘੋਲ ਵਿੱਚੋਂ ਲੰਘਾਇਆ ਜਾਂਦਾ ਹੈ, ਤਾਂ ਘੋਲ ਨੂੰ ਅਮੋਨੀਆ ਨਾਲ ਖਾਰੀ ਬਣਾਉਣ ‘ਤੇ ਸਫ਼ੇਦ ਜ਼ਿੰਕ ਸਲਫਾਈਡ, $\mathrm{ZnS}$ ਦਿਖਾਈ ਦੇ ਸਕਦਾ ਹੈ।
ਧਾਤਵੀ ਜ਼ਿੰਕ ਅਤੇ ਤਾਂਬੇ ਦੇ ਨਾਈਟ੍ਰੇਟ ਦੇ ਜਲੀ ਘੋਲ ਵਿਚਕਾਰ ਪ੍ਰਤੀਕਿਰਿਆ ਹੈ:
$$\mathrm{Zn}(\mathrm{s})+\mathrm{Cu}^{2+}(\mathrm{aq}) \rightarrow \mathrm{Zn}^{2+}(\mathrm{aq})+\mathrm{Cu}(\mathrm{s}) \tag{8.15}$$
ਪ੍ਰਤੀਕਿਰਿਆ (8.15) ਵਿੱਚ, ਜ਼ਿੰਕ ਨੇ $Zn^{2+}$ ਬਣਾਉਣ ਲਈ ਇਲੈਕਟ੍ਰਾਨ ਗੁਆ ਦਿੱਤੇ ਹਨ ਅਤੇ, ਇਸ ਲਈ, ਜ਼ਿੰਕ ਆਕਸੀਕ੍ਰਿਤ ਹੁੰਦਾ ਹੈ। ਸਪੱਸ਼ਟ ਤੌਰ ‘ਤੇ, ਹੁਣ ਜੇਕਰ ਜ਼ਿੰਕ ਆਕਸੀਕ੍ਰਿਤ ਹੁੰਦਾ ਹੈ, ਇਲੈਕਟ੍ਰਾਨ ਛੱਡਦਾ ਹੈ, ਤਾਂ ਕੁਝ ਰਿਡਿਊਸ ਹੋਣਾ ਚਾਹੀਦਾ ਹੈ, ਜ਼ਿੰਕ ਦੁਆਰਾ ਗੁਆਚੇ ਇਲੈਕਟ੍ਰਾਨਾਂ ਨੂੰ ਗ੍ਰਹਿਣ ਕਰਦਾ ਹੈ। ਤਾਂਬੇ ਦਾ ਆਇਨ ਜ਼ਿੰਕ ਤੋਂ ਇਲੈਕਟ੍ਰਾਨ ਪ੍ਰਾਪਤ ਕਰਕੇ ਰਿਡਿਊਸ ਹੁੰਦਾ ਹੈ।
ਪ੍ਰਤੀਕਿਰਿਆ (8.15) ਨੂੰ ਇਸ ਤਰ੍ਹਾਂ ਮੁੜ ਲਿਖਿਆ ਜਾ ਸਕਦਾ ਹੈ:
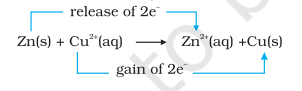
ਇਸ ਪੜਾਅ ‘ਤੇ ਅਸੀਂ ਸਮੀਕਰਨ (8.15) ਦੁਆਰਾ ਦਰਸਾਈ ਗਈ ਪ੍ਰਤੀਕਿਰਿਆ ਲਈ ਸੰਤੁਲਨ ਦੀ ਅਵਸਥਾ ਦੀ ਜਾਂਚ ਕਰ ਸਕਦੇ ਹਾਂ। ਇਸ ਉਦੇਸ਼ ਲਈ, ਆਓ ਜ਼ਿੰਕ ਸਲਫੇਟ ਘੋਲ ਵਿੱਚ ਧਾਤਵੀ ਤਾਂਬੇ ਦੀ ਇੱਕ ਪ








