అధ్యాయం 03 లక్షణాలలో మూలకాలు మరియు ఆవర్తన వర్గీకరణ
“ఆవర్తన పట్టిక సూత్రప్రాయంగా మరియు ఆచరణాత్మకంగా రసాయన శాస్త్రంలో అత్యంత ముఖ్యమైన భావన అని చెప్పవచ్చు. ఇది విద్యార్థులకు రోజువారీ ఆధారం, వృత్తిపరులకు పరిశోధనకు కొత్త మార్గాలను సూచిస్తుంది మరియు మొత్తం రసాయన శాస్త్రం యొక్క సంక్షిప్తమైన వ్యవస్థీకరణను అందిస్తుంది. రసాయన మూలకాలు యాదృచ్ఛిక సమూహాలు కాకుండా, పోకడలను ప్రదర్శించి, కుటుంబాలలో కలిసి ఉంటాయనే వాస్తవానికి ఇది ఒక గొప్ప ప్రదర్శన. ప్రాథమిక రసాయన నిర్మాణ ఖండాలు, రసాయన మూలకాల నుండి ప్రపంచం ఎలా నిర్మితమైందో విప్పి చూడాలనుకునే ఎవరికైనా ఆవర్తన పట్టిక పట్ల అవగాహన అత్యవసరం.”
గ్లెన్ టి. సీబోర్గ్
ఈ యూనిట్లో, ఆవర్తన పట్టిక యొక్క చారిత్రక అభివృద్ధిని, అది ఈ రోజు ఉన్నట్లుగా మరియు ఆధునిక ఆవర్తన నియమాన్ని మనం అధ్యయనం చేస్తాము. పరమాణువుల ఎలక్ట్రాన్ విన్యాసం యొక్క తార్కిక పరిణామంగా ఆవర్తన వర్గీకరణ ఎలా అనుసరిస్తుందో కూడా మనం నేర్చుకుంటాము. చివరగా, మూలకాల భౌతిక మరియు రసాయన ధర్మాలలోని కొన్ని ఆవర్తన పోకడలను మనం పరిశీలిస్తాము.
3.1 మూలకాలను వర్గీకరించడం ఎందుకు అవసరం?
మూలకాలు అన్ని రకాల పదార్థాల ప్రాథమిక ప్రమాణాలు అని ఇప్పటికే మనకు తెలుసు. 1800లో, కేవలం 31 మూలకాలు మాత్రమే తెలుసు. 1865 నాటికి, గుర్తించబడిన మూలకాల సంఖ్య రెట్టింపు కంటే ఎక్కువగా 63కి చేరుకుంది. ప్రస్తుతం 114 మూలకాలు తెలుసు. వాటిలో, ఇటీవల కనుగొనబడిన మూలకాలు మానవ నిర్మితమైనవి. కొత్త మూలకాలను సంశ్లేషణ చేయడానికి ప్రయత్నాలు కొనసాగుతున్నాయి. ఇంత పెద్ద సంఖ్యలో మూలకాలతో, ఈ మూలకాల అన్నింటి రసాయన శాస్త్రాన్ని మరియు వాటి అసంఖ్యాక సమ్మేళనాలను వ్యక్తిగతంగా అధ్యయనం చేయడం చాలా కష్టం. ఈ సమస్యను సులభతరం చేయడానికి, శాస్త్రవేత్తలు మూలకాలను వర్గీకరించడం ద్వారా వారి జ్ఞానాన్ని వ్యవస్థీకరించే వ్యవస్థాపూర్వక మార్గాన్ని వెతికారు. ఇది మూలకాల గురించి తెలిసిన రసాయన వాస్తవాలను హేతుబద్ధీకరించడమే కాకుండా, మరింత అధ్యయనం చేయడానికి కొత్త వాటిని కూడా అంచనా వేయగలదు.
3.2 ఆవర్తన వర్గీకరణ యొక్క ఉద్భవం
మూలకాలను సమూహాలుగా వర్గీకరించడం మరియు ఆవర్తన నియమం మరియు ఆవర్తన పట్టిక యొక్క అభివృద్ధి అనేది అనేక శాస్త్రవేత్తలు వారి పరిశీలనలు మరియు ప్రయోగాల ద్వారా సంపాదించిన జ్ఞానాన్ని వ్యవస్థీకరించడం యొక్క పరిణామాలు. జర్మన్ రసాయన శాస్త్రవేత్త, జోహాన్ డోబెరైనర్ 1800ల ప్రారంభంలో మూలకాల ధర్మాల మధ్య పోకడల ఆలోచనను మొదటిసారిగా పరిగణించాడు. 1829 నాటికి అతను అనేక మూలకాల సమూహాల (త్రయాలు) భౌతిక మరియు రసాయన ధర్మాల మధ్య సారూప్యతను గమనించాడు. ప్రతి సందర్భంలో, ప్రతి త్రయం యొక్క మధ్య మూలకం యొక్క పరమాణు భారం ఇతర రెండింటి పరమాణు భారాల మధ్య సగం దూరంలో ఉంటుందని అతను గమనించాడు (పట్టిక 3.1). అలాగే మధ్య మూలకం యొక్క ధర్మాలు ఇతర రెండు సభ్యుల కంటే మధ్యలో ఉండేవి.
పట్టిక 3.1 డోబెరైనర్ యొక్క త్రయాలు
| మూలకం | పరమాణు భారం | మూలకం | పరమాణు భారం | మూలకం | పరమాణు భారం |
|---|---|---|---|---|---|
| $\mathbf{L i}$ | 7 | $\mathbf{C a}$ | 40 | $\mathbf{C l}$ | 35.5 |
| $\mathbf{N a}$ | 23 | $\mathbf{S r}$ | 88 | $\mathbf{B r}$ | 80 |
| $\mathbf{K}$ | 39 | $\mathbf{B a}$ | 137 | $\mathbf{I}$ | 127 |
డోబెరైనర్ సంబంధం, త్రయాల నియమం అని పిలువబడుతుంది, కేవలం కొన్ని మూలకాలకు మాత్రమే పనిచేసినట్లు కనిపించినందున, అది యాదృచ్ఛికం అని తిరస్కరించబడింది. మూలకాలను వర్గీకరించడానికి తదుపరి నివేదించబడిన ప్రయత్నం ఒక ఫ్రెంచ్ భూవిజ్ఞాన శాస్త్రవేత్త, A.E.B. డి ఛాన్కోర్టోయిస్ చేత 1862లో చేయబడింది. అతను అప్పటికి తెలిసిన మూలకాలను పరమాణు భారాల పెరుగుదల క్రమంలో అమర్చాడు మరియు ధర్మాల ఆవర్తన పునరావృత్తిని ప్రదర్శించడానికి మూలకాల స్థూపాకార పట్టికను తయారు చేసాడు. ఇది కూడా ఎక్కువ శ్రద్ధను ఆకర్షించలేదు. ఆంగ్ల రసాయన శాస్త్రవేత్త, జాన్ అలెగ్జాండర్ న్యూలాండ్స్ 1865లో అష్టకాల నియమాన్ని ప్రతిపాదించాడు. అతను మూలకాలను వాటి పరమాణు భారాల పెరుగుదల క్రమంలో అమర్చాడు మరియు ప్రతి ఎనిమిదవ మూలకం మొదటి మూలకం వలె ధర్మాలను కలిగి ఉందని గమనించాడు (పట్టిక 3.2). ఈ సంబంధం సంగీతం యొక్క అష్టకాలలో ప్రతి ఎనిమిదవ స్వరం మొదటి స్వరాన్ని పోలి ఉండటం లాంటిది. న్యూలాండ్స్ యొక్క అష్టకాల నియమం కాల్షియం వరకు మాత్రమే మూలకాలకు నిజమని తెలుసుకోవడమైనది. అతని ఆలోచన ఆ సమయంలో విస్తృతంగా అంగీకరించబడనప్పటికీ, అతని పనికి, తరువాత 1887లో రాయల్ సొసైటీ, లండన్ చేత డేవీ మెడల్ ను పొందాడు.
ఆవర్తన నియమం, ఈ రోజు మనకు తెలిసినట్లుగా, దాని అభివృద్ధికి రష్యన్ రసాయన శాస్త్రవేత్త, డిమిత్రి మెండలీవ్ (1834-1907) మరియు జర్మన్ రసాయన శాస్త్రవేత్త, లోథార్ మేయర్ (1830-1895) కు ఋణపడి ఉంది.
స్వతంత్రంగా పనిచేస్తూ, ఇద్దరు రసాయన శాస్త్రవేత్తలు 1869లో మూలకాలను వాటి పరమాణు భారాల పెరుగుదల క్రమంలో అమర్చినప్పుడు, భౌతిక మరియు రసాయన ధర్మాలలో సారూప్యతలు క్రమం తప్పకుండా కనిపిస్తాయని ప్రతిపాదించారు. లోథార్ మేయర్ పరమాణు ఘనపరిమాణం, ద్రవీభవన స్థానం మరియు క్వథన స్థానం వంటి భౌతిక ధర్మాలను పరమాణు భారానికి వ్యతిరేకంగా గీసాడు మరియు ఆవర్తనంగా పునరావృతమయ్యే నమూనాను పొందాడు. న్యూలాండ్స్ కాకుండా, లోథార్ మేయర్ ఆ పునరావృత నమూనా యొక్క పొడవులో మార్పును గమనించాడు. 1868 నాటికి, లోథార్ మేయర్ ఆధునిక ఆవర్తన పట్టికను దగ్గరగా పోలి ఉండే మూలకాల పట్టికను అభివృద్ధి చేసాడు. అయినప్పటికీ, ఆధునిక ఆవర్తన పట్టిక అభివృద్ధికి సాధారణంగా గుర్తింపు పొందిన శాస్త్రవేత్త డిమిత్రి మెండలీవ్ పని తరువాత వరకు అతని పని ప్రచురించబడలేదు.
పట్టిక 3.2 న్యూలాండ్స్ యొక్క అష్టకాలు
| మూలకం | $\mathbf{L i}$ | $\mathbf{B e}$ | $\mathbf{B}$ | $\mathbf{C}$ | $\mathbf{N}$ | $\mathbf{O}$ | $\mathbf{F}$ |
|---|---|---|---|---|---|---|---|
| పర. భా. | 7 | 9 | 11 | 12 | 14 | 16 | 19 |
| మూలకం | $\mathbf{N a}$ | $\mathbf{M g}$ | $\mathbf{A l}$ | $\mathbf{S i}$ | $\mathbf{P}$ | $\mathbf{S}$ | $\mathbf{C l}$ |
| పర. భా. | 23 | 24 | 27 | 29 | 31 | 32 | 35.5 |
| మూలకం | $\mathbf{K}$ | $\mathbf{C a}$ | |||||
| పర. భా. | 39 | 40 |
డోబెరైనర్ ఆవర్తన సంబంధం అధ్యయనాన్ని ప్రారంభించగా, ఆవర్తన నియమాన్ని మొదటిసారిగా ప్రచురించడానికి బాధ్యత వహించిన వ్యక్తి మెండలీవ్. ఇది ఈ క్రింది విధంగా పేర్కొంది:
మూలకాల ధర్మాలు వాటి పరమాణు భారాల ఆవర్తన ప్రమేయం.
మెండలీవ్ మూలకాలను పరమాణు భారాల పెరుగుదల క్రమంలో ఒక పట్టిక యొక్క సమాంతర వరుసలు మరియు నిలువు నిలువు వరుసలలో ఇటువంటి విధంగా అమర్చాడు, ఒకే విధమైన ధర్మాలు కలిగిన మూలకాలు ఒకే నిలువు నిలువు వరుస లేదా సమూహాన్ని ఆక్రమించాయి. మెండలీవ్ యొక్క మూలకాలను వర్గీకరించే వ్యవస్థ లోథార్ మేయర్ కంటే మరింత వివరణాత్మకమైనది. అతను ఆవర్తనత యొక్క ప్రాముఖ్యతను పూర్తిగా గుర్తించాడు మరియు మూలకాలను వర్గీకరించడానికి విస్తృత శ్రేణి భౌతిక మరియు రసాయన ధర్మాలను ఉపయోగించాడు. ప్రత్యేకించి, మెండలీవ్ మూలకాలచే ఏర్పడిన సమ్మేళనాల అనుభావిక సూత్రాలు మరియు ధర్మాలలోని సారూప్యతలపై ఆధారపడ్డాడు. పరమాణు భారం యొక్క క్రమం కఠినంగా పాటించబడితే, కొన్ని మూలకాలు అతని వర్గీకరణ పథకంలో సరిపోలవని అతను గ్రహించాడు. పరమాణు కొలతలు తప్పుగా ఉండవచ్చని భావించి, పరమాణు భారాల క్రమాన్ని విస్మరించాడు మరియు ఒకే విధమైన ధర్మాలు కలిగిన మూలకాలను కలిపి ఉంచాడు. ఉదాహరణకు, టెలూరియం (సమూహం VI) కంటే తక్కువ పరమాణు భారం కలిగిన అయోడిన్, ధర్మాలలోని సారూప్యతల కారణంగా (Fig. 3.1), ఫ్లోరిన్, క్లోరిన్, బ్రోమిన్ తో పాటు సమూహం VIIలో ఉంచబడింది. అదే సమయంలో, ఒకే విధమైన ధర్మాలు కలిగిన మూలకాలను ఒకే సమూహంలో అమర్చడం అనే అతని ప్రాథమిక లక్ష్యాన్ని కొనసాగిస్తూ, కొన్ని మూలకాలు ఇంకా కనుగొనబడలేదని మరియు, అందువల్ల, పట్టికలో అనేక ఖాళీలను వదిలివేసాడని ప్రతిపాదించాడు. ఉదాహరణకు, గాలియం మరియు జెర్మేనియం రెండూ మెండలీవ్ తన ఆవర్తన పట్టికను ప్రచురించిన సమయంలో తెలియదు. అతను అల్యూమినియం క్రింద మరియు సిలికాన్ క్రింద ఒక ఖాళీని వదిలివేసాడు మరియు ఈ మూలకాలను ఏక-అల్యూమినియం మరియు ఏక-సిలికాన్ అని పిలిచాడు. మెండలీవ్ గాలియం మరియు జెర్మేనియం యొక్క ఉనికిని మాత్రమే కాకుండా, వాటి కొన్ని సాధారణ భౌతిక ధర్మాలను కూడా వివరించాడు. ఈ మూలకాలు తరువాత కనుగొనబడ్డాయి. ఈ మూలకాల కోసం మెండలీవ్ అంచనా వేసిన కొన్ని ధర్మాలు మరియు ప్రయోగాత్మకంగా కనుగొనబడినవి పట్టిక 3.3లో పేర్కొనబడ్డాయి.
మెండలీవ్ యొక్క పరిమాణాత్మక అంచనాల ధైర్యం మరియు వాటి చివరికి విజయం అతన్ని మరియు అతని ఆవర్తన పట్టికను ప్రసిద్ధి చేసింది. 1905లో ప్రచురించబడిన మెండలీవ్ యొక్క ఆవర్తన పట్టిక Fig. 3.1లో చూపబడింది.
పట్టిక 3.3 ఏక-అల్యూమినియం (గాలియం) మరియు ఏక-సిలికాన్ (జెర్మేనియం) మూలకాల కోసం మెండలీవ్ యొక్క అంచనాలు
| ధర్మం | ఏక-అల్యూమినియం (అంచనా) | గాలియం (కనుగొనబడింది) | ఏక-సిలికాన్ (అంచనా) | జెర్మేనియం (కనుగొనబడింది) |
|---|---|---|---|---|
| పరమాణు భారం | 68 | 70 | 72 | 72.6 |
| సాంద్రత/(గ్రా/సెం.మీ $\mathbf{)}$ | 5.9 | 5.94 | 5.5 | 5.36 |
| ద్రవీభవన స్థానం/కె | $\mathrm{Low}$ | 302.93 | $\mathrm{High}$ | 1231 |
| ఆక్సైడ్ సూత్రం | $\mathrm{E}_2 \mathrm{O}_3$ | $\mathrm{Ga}_2 \mathrm{O}_3$ | $\mathrm{EO}_{2}$ | $\mathrm{GeO}_{2}$ |
| క్లోరైడ్ సూత్రం | $\mathrm{E} \mathrm{Cl}_{3}$ | $\mathrm{GaCl}_{3}$ | $\mathrm{ECl}_{4}$ | $\mathrm{GeCl}_{4}$ |
సమూహాలు మరియు శ్రేణులలో మూలకాల ఆవర్తన వ్యవస్థ

Fig. 3.1 మెండలీవ్ యొక్క ఆవర్తన పట్టిక ముందుగా ప్రచురించబడింది
3.3 ఆధునిక ఆవర్తన నియమం మరియు ఆవర్తన పట్టిక యొక్క ప్రస్తుత రూపం
మెండలీవ్ తన ఆవర్తన పట్టికను అభివృద్ధి చేసినప్పుడు, రసాయన శాస్త్రవేత్తలకు పరమాణువు యొక్క అంతర్గత నిర్మాణం గురించి ఏమీ తెలియదని మనం గుర్తుంచుకోవాలి. అయినప్పటికీ, $20^{\text {th }}$ శతాబ్దం ప్రారంభం పరమాణు కణాల గురించి సిద్ధాంతాలలో గాఢమైన అభివృద్ధిని చూసింది. 1913లో, ఆంగ్ల భౌతిక శాస్త్రవేత్త, హెన్రీ మోస్లే మూలకాల లక్షణ $X$-కిరణ వర్ణపటాలలో క్రమబద్ధతలను గమనించాడు. $\sqrt{v}$ (ఇక్కడ $V$ అనేది $X$-కిరణాల పౌనఃపున్యం) ను పరమాణు సంఖ్య $(Z)$ కు వ్యతిరేకంగా గీయడం వల్ల సరళ రేఖ వచ్చింది మరియు $\sqrt{v}$ vs పరమాణు ద్రవ్యరాశి ప్లాట్ కాదు. అతను పరమాణు సంఖ్య ఒక మూలకం యొక్క దాని పరమాణు ద్రవ్యరాశి కంటే మరింత ప్రాథమికమైన ధర్మం అని తద్వారా చూపించాడు. మెండలీవ్ యొక్క ఆవర్తన నియమం, అందువల్ల, తదనుగుణంగా సవరించబడింది. ఇది ఆధునిక ఆవర్తన నియమం అని పిలువబడుతుంది మరియు ఇలా పేర్కొనవచ్చు:
మూలకాల భౌతిక మరియు రసాయన ధర్మాలు వాటి పరమాణు సంఖ్యల ఆవర్తన ప్రమేయాలు.
ఆవర్తన నియమం 94 సహజంగా సంభవించే మూలకాల మధ్య ముఖ్యమైన సారూప్యతలను వెల్లడించింది (నెప్ట్యూనియం మరియు ప్లూటోనియం యాక్టినియం మరియు ప్రోటోయాక్టినియం వలె యురేనియం ఖనిజం - పిచ్బ్లెండ్లో కూడా కనిపిస్తాయి). ఇది అకర్బన రసాయన శాస్త్రంలో పునరుజ్జీవన ఆసక్తిని ప్రేరేపించింది మరియు కృత్రిమంగా ఉత్పత్తి చేయబడిన చిన్న జీవితకాలం గల మూలకాల సృష్టితో ప్రస్తుతం కొనసాగింది.
పరమాణు సంఖ్య కేంద్రక ఆవేశానికి (అనగా, ప్రోటాన్ల సంఖ్య) లేదా తటస్థ పరమాణువులోని ఎలక్ట్రాన్ల సంఖ్యకు సమానం అని మీరు గుర్తు చేసుకోవచ్చు. మూలకాల ఆవర్తనతలో క్వాంటం సంఖ్యలు మరియు ఎలక్ట్రాన్ విన్యాసాల ప్రాముఖ్యతను ఊహించడం సులభం. వాస్తవానికి, ఎలక్ట్రాన్ విన్యాసాలలో ఆవర్తన వైవిధ్యం యొక్క పరిణామం ఆవర్తన నియమం అని ఇప్పుడు గుర్తించబడింది, ఇది నిజంగా మూలకాలు మరియు వాటి సమ్మేళనాల భౌతిక మరియు రసాయన ధర్మాలను నిర్ణయిస్తుంది.
ఆవర్తన పట్టిక యొక్క అనేక రూపాలు సమయానికి సమయానికి రూపొందించబడ్డాయి. కొన్ని రూపాలు రసాయన ప్రతిచర్యలు మరియు సంయోజకతను నొక్కి చెబుతాయి, మరికొన్ని మూలకాల ఎలక్ట్రాన్ విన్యాసాన్ని నొక్కి చెబుతాయి. ఒక ఆధునిక వెర్షన్, మూలకాల ఆవర్తన పట్టిక యొక్క “దీర్ఘ రూపం” (Fig. 3.2), అత్యంత సౌకర్యవంతమైనది మరియు విస్తృతంగా ఉపయోగించబడుతుంది. సమాంతర వరుసలు (మెండలీవ్ శ్రేణులు అని పిలిచాడు) ఆవర్తనాలు మరియు నిలువు నిలువు వరుసలు, సమూహాలు అని పిలువబడతాయి. వాటి పరమాణువులలో ఒకే విధమైన బాహ్య ఎలక్ట్రాన్ విన్యాసాలు కలిగిన మూలకాలు నిలువు నిలువు వరుసలలో అమర్చబడతాయి, వీటిని సమూహాలు లేదా కుటుంబాలు అంటారు. ఇంటర్నేషనల్ యూనియన్ ఆఫ్ ప్యూర్ అండ్ అప్లైడ్ కెమిస్ట్రీ (IUPAC) యొక్క సిఫార్సు ప్రకారం, సమూహాలు 1 నుండి 18 వరకు సంఖ్యాబద్ధం చేయబడ్డాయి, సమూహాల IA … VIIA, VIII, IB … VIIB మరియు 0 యొక్క పాత సంజ్ఞామానాన్ని భర్తీ చేస్తాయి.
మొత్తం ఏడు ఆవర్తనాలు ఉన్నాయి. ఆవర్తన సంఖ్య ఆవర్తనంలోని మూలకాల అత్యధిక ప్రధాన క్వాంటం సంఖ్య $(n)$ కు అనుగుణంగా ఉంటుంది. మొదటి ఆవర్తనం 2 మూలకాలను కలిగి ఉంటుంది. తదుపరి ఆవర్తనాలు వరుసగా $8,8,18,18$ మరియు 32 మూలకాలను కలిగి ఉంటాయి. ఏడవ ఆవర్తనం అసంపూర్ణంగా ఉంది మరియు ఆరవ ఆవర్తనం వలె 32 మూలకాల సైద్ధాంతిక గరిష్టంను (క్వాంటం సంఖ్యల ఆధారంగా) కలిగి ఉంటుంది. ఈ రూపంలోని ఆవర్తన పట్టికలో, ఆరవ మరియు ఏడవ ఆవర్తనాల యొక్క 14 మూలకాలు (లాంథనాయిడ్లు మరియు యాక్టినాయిడ్లు, వరుసగా) దిగువన ప్రత్యేక ప్యానెల్లలో ఉంచబడ్డాయి[^0].
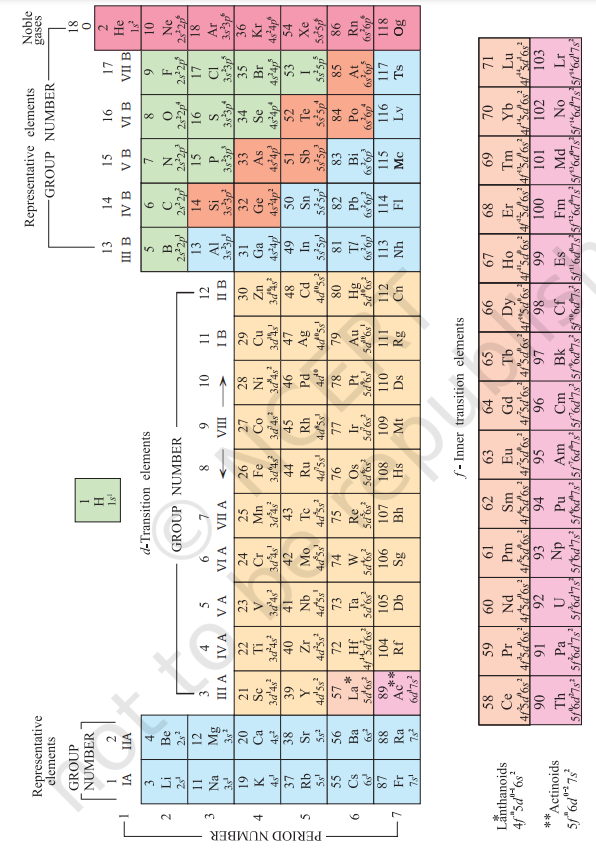
Fig. 3.2 వాటి పరమాణు సంఖ్యలు మరియు భూస్థితి బాహ్య ఎలక్ట్రాన్ విన్యాసాలతో మూలకాల ఆవర్తన పట్టిక యొక్క దీర్ఘ రూపం. సమూహాలు 1984 IUPAC సిఫార్సులకు అనుగుణంగా 1-18 గా సంఖ్యాబద్ధం చేయబడ్డాయి. ఈ సంజ్ఞామానం మూలకాల కోసం IA–VIIA, VIII, IB–VIIB మరియు 0 యొక్క పాత నంబరింగ్ పథకాన్ని భర్తీ చేస్తుంది.








