అధ్యాయం 04 రసాయన బంధం మరియు పరమాణు నిర్మాణం
“శాస్త్రవేత్తలు నిరంతరం కొత్త సమ్మేళనాలను కనుగొంటూ, వాటి గురించిన వాస్తవాలను క్రమబద్ధంగా అమర్చుతూ, ఇప్పటికే ఉన్న జ్ఞానంతో వివరించడానికి ప్రయత్నిస్తూ, మునుపటి అభిప్రాయాలను సవరించడానికి లేదా కొత్తగా గమనించిన వాస్తవాలను వివరించడానికి సిద్ధాంతాలను రూపొందించడానికి నిర్వహిస్తారు.”
పదార్థం ఒకటి లేదా వివిధ రకాల మూలకాలతో రూపొందించబడింది. సాధారణ పరిస్థితుల్లో, ఉదాత్త వాయువులు మినహా, ఏ ఇతర మూలకం ప్రకృతిలో స్వతంత్ర అణువుగా ఉండదు. అయితే, అణువుల సమూహం ఒకే జాతిగా కలిసి ఉండటం, వాటికి స్వంతమైన లక్షణాలతో కనుగొనబడింది. అటువంటి అణువుల సమూహాన్ని అణువు అంటారు. స్పష్టంగా, ఈ అణువులను కలిపి ఉంచే ఏదో ఒక శక్తి ఉండాలి. వివిధ రసాయన జాతులలో వివిధ భాగాలను (అణువులు, అయాన్లు మొదలైనవి) కలిపి ఉంచే ఆకర్షణ శక్తిని రసాయన బంధం అంటారు. వివిధ మూలకాల అణువులు వివిధ రీతుల్లో కలిసి రసాయన సమ్మేళనాలు ఏర్పడటం వలన, ఇది అనేక ప్రశ్నలను రేకెత్తిస్తుంది. అణువులు ఎందుకు కలుస్తాయి? కేవలం కొన్ని కలయికలు మాత్రమే ఎందుకు సాధ్యమవుతాయి? కొన్ని అణువులు కలిస్తే, మరికొన్ని ఎందుకు కలవవు? అణువులు ఎందుకు నిర్దిష్ట ఆకారాలను కలిగి ఉంటాయి? అటువంటి ప్రశ్నలకు సమాధానం ఇవ్వడానికి వివిధ సిద్ధాంతాలు మరియు భావనలు సమయానుగుణంగా ముందుకు తీసుకువచ్చారు. ఇవి కోసెల్-లూయిస్ విధానం, వాలెన్స్ షెల్ ఎలక్ట్రాన్ జత వికర్షణ (VSEPR) సిద్ధాంతం, వాలెన్స్ బాండ్ (VB) సిద్ధాంతం మరియు మాలిక్యులర్ ఆర్బిటల్ (MO) సిద్ధాంతం. వాలెన్స్ యొక్క వివిధ సిద్ధాంతాల పరిణామం మరియు రసాయన బంధాల స్వభావం యొక్క వివరణ అణువు నిర్మాణం, మూలకాల ఎలక్ట్రానిక్ విన్యాసం మరియు ఆవర్తన పట్టిక యొక్క అవగాహనలోని అభివృద్ధులతో దగ్గరి సంబంధం కలిగి ఉంది. ప్రతి వ్యవస్థ మరింత స్థిరంగా ఉండటానికి ప్రయత్నిస్తుంది మరియు బంధం స్థిరత్వాన్ని పొందడానికి వ్యవస్థ యొక్క శక్తిని తగ్గించే ప్రకృతి యొక్క మార్గం.
4.1 రసాయన బంధానికి కోసెల్-లూయిస్ విధానం
రసాయన బంధం ఏర్పడటాన్ని ఎలక్ట్రాన్ల పరంగా వివరించడానికి, అనేక ప్రయత్నాలు చేయబడ్డాయి, కానీ 1916లో కోసెల్ మరియు లూయిస్ స్వతంత్రంగా సంతృప్తికరమైన వివరణను ఇవ్వడంలో విజయం సాధించినప్పుడు మాత్రమే ఇది సాధ్యమైంది. ఉదాత్త వాయువుల నిష్క్రియాత్మకతపై ఆధారపడిన వాలెన్స్ యొక్క తార్కిక వివరణను అందించిన వారు మొదటివారు.
లూయిస్ అణువును ధనాత్మకంగా చార్జ్ చేయబడిన ‘కెర్నల్’ (న్యూక్లియస్ ప్లస్ లోపలి ఎలక్ట్రాన్లు) మరియు గరిష్టంగా ఎనిమిది ఎలక్ట్రాన్లను కలిగి ఉండే బాహ్య షెల్ పరంగా చిత్రీకరించాడు. ఇంకా, ఈ ఎనిమిది ఎలక్ట్రాన్లు ‘కెర్నల్’ చుట్టూ ఉన్న ఘనం యొక్క మూలలను ఆక్రమిస్తాయని ఊహించాడు. అందువలన, సోడియం యొక్క ఒకే బాహ్య షెల్ ఎలక్ట్రాన్ ఘనం యొక్క ఒక మూలను ఆక్రమిస్తుంది, అయితే ఉదాత్త వాయువు విషయంలో అన్ని ఎనిమిది మూలలు ఆక్రమించబడతాయి. ఈ ఎలక్ట్రాన్ల అష్టకం, ప్రత్యేకంగా స్థిరమైన ఎలక్ట్రానిక్ అమరికను సూచిస్తుంది. లూయిస్ పోస్ట్యులేట్ చేసినదేమిటంటే, అణువులు రసాయన బంధాల ద్వారా లింక్ చేయబడినప్పుడు స్థిరమైన అష్టకాన్ని సాధిస్తాయి. సోడియం మరియు క్లోరిన్ విషయంలో, ఇది సోడియం నుండి క్లోరిన్కు ఒక ఎలక్ట్రాన్ బదిలీ ద్వారా జరగవచ్చు, తద్వారా $\mathrm{Na}^+$ మరియు $\mathrm{Cl}^{-}$ అయాన్లను ఇస్తుంది. $ \mathrm{Cl}_2, \mathrm{H}_2, \mathrm{~F}_2 $ మొదలైన ఇతర అణువుల విషయంలో, బంధం అణువుల మధ్య ఒక జత ఎలక్ట్రాన్లను పంచుకోవడం ద్వారా ఏర్పడుతుంది. ఈ ప్రక్రియలో ప్రతి అణువు ఎలక్ట్రాన్ల స్థిరమైన బాహ్య అష్టకాన్ని పొందుతుంది.
లూయిస్ చిహ్నాలు: ఒక అణువు ఏర్పడటంలో, బాహ్య షెల్ ఎలక్ట్రాన్లు మాత్రమే రసాయన కలయికలో పాల్గొంటాయి మరియు అవి వాలెన్స్ ఎలక్ట్రాన్లుగా పిలువబడతాయి. లోపలి షెల్ ఎలక్ట్రాన్లు బాగా రక్షించబడతాయి మరియు సాధారణంగా కలయిక ప్రక్రియలో చేర్చబడవు. అమెరికన్ రసాయన శాస్త్రవేత్త జి.ఎన్. లూయిస్ ఒక అణువులో వాలెన్స్ ఎలక్ట్రాన్లను సూచించడానికి సాధారణ సంజ్ఞలను పరిచయం చేశాడు. ఈ సంజ్ఞలను లూయిస్ చిహ్నాలు అంటారు. ఉదాహరణకు, రెండవ కాలం మూలకాల కోసం లూయిస్ చిహ్నాలు క్రింది విధంగా ఉన్నాయి:

లూయిస్ చిహ్నాల ప్రాముఖ్యత : చిహ్నం చుట్టూ ఉన్న చుక్కల సంఖ్య వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను సూచిస్తుంది. వాలెన్స్ ఎలక్ట్రాన్ల ఈ సంఖ్య మూలకం యొక్క సాధారణ లేదా గ్రూప్ వాలెన్స్ను లెక్కించడంలో సహాయపడుతుంది. మూలకాల గ్రూప్ వాలెన్స్ సాధారణంగా లూయిస్ చిహ్నాలలోని చుక్కల సంఖ్యకు సమానంగా ఉంటుంది లేదా 8 మైనస్ చుక్కల సంఖ్య లేదా వాలెన్స్ ఎలక్ట్రాన్లు.
రసాయన బంధానికి సంబంధించి, కోసెల్ ఈ క్రింది వాస్తవాలకు దృష్టి పెట్టాడు:
- ఆవర్తన పట్టికలో, అత్యంత ఎలక్ట్రోనెగటివ్ హాలోజన్లు మరియు అత్యంత ఎలక్ట్రోపాజిటివ్ క్షార లోహాలు ఉదాత్త వాయువుల ద్వారా వేరు చేయబడతాయి;
- హాలోజన్ అణువు నుండి ప్రతికూల అయాన్ మరియు క్షార లోహ అణువు నుండి ధనాత్మక అయాన్ ఏర్పడటం సంబంధిత అణువుల ద్వారా ఎలక్ట్రాన్ పొందడం మరియు కోల్పోవడంతో సంబంధం కలిగి ఉంటుంది;
- ఈ విధంగా ఏర్పడిన ప్రతికూల మరియు ధనాత్మక అయాన్లు స్థిరమైన ఉదాత్త వాయు వాయు ఎలక్ట్రానిక్ విన్యాసాలను పొందుతాయి. ఉదాత్త వాయువులు (హీలియం మినహా, ఇది ఎలక్ట్రాన్ల యుగ్మాన్ని కలిగి ఉంటుంది) ఎనిమిది (అష్టకం) ఎలక్ట్రాన్ల ప్రత్యేకంగా స్థిరమైన బాహ్య షెల్ విన్యాసాన్ని కలిగి ఉంటాయి, $n s^{2} n p^{6}$.
- ప్రతికూల మరియు ధనాత్మక అయాన్లు ఎలెక్ట్రోస్టాటిక్ ఆకర్షణ ద్వారా స్థిరపడతాయి.
ఉదాహరణకు, సోడియం మరియు క్లోరిన్ నుండి $\mathrm{NaCl}$ ఏర్పడటం, పై పథకం ప్రకారం, ఇలా వివరించవచ్చు:
| $\mathrm{Na}$ | $\rightarrow$ | $\mathrm{Na}^{+}+\mathrm{e}^{-}$ |
| $[\mathrm{Ne}] 3 \mathrm{~s}^{1}$ | $[\mathrm{Ne}]$ | |
| $\mathrm{Cl}+\mathrm{e}^{-}$ | $\rightarrow$ | $\mathrm{Cl}^{-}$ |
| $[\mathrm{Ne}] 3 s^{2} 3 p^{5}$ | $[\mathrm{Ne}] 3 s^{2} 3 p^{6}$ or $[\mathrm{Ar}]$ | |
| $\mathrm{Na}^{+}+\mathrm{Cl}^{-}$ | $\rightarrow$ | $\mathrm{NaCl}$ or $\mathrm{Na}^{+} \mathrm{Cl}^{-}$ |
అదేవిధంగా $\mathrm{CaF}_{2}$ ఏర్పడటాన్ని ఇలా చూపవచ్చు:
| $\mathrm{Ca}$ | $\rightarrow$ | $\mathrm{Ca}^{2+}+2 \mathrm{e}^{-}$ |
| $[\mathrm{Ar}] 4 s^{2}$ | $[\mathrm{Ar}]$ | |
| $\mathrm{F}+\mathrm{e}^{-}$ | $\rightarrow$ | $\mathrm{F}^{-}$ |
| $[\mathrm{He}] 2 s^{2} 2 p^{5}$ | $[\mathrm{He}] 2 s^{2} 2 p^{6}$ or $[\mathrm{Ne}]$ | |
| $\mathrm{Ca}^{2+}+2 \mathrm{~F}^{-}$ | $\rightarrow$ | $\mathrm{CaF}_2$ or $\mathrm{Ca}^{2+}\left(\mathrm{F}^{-}\right)_2$ |
ధనాత్మక మరియు ప్రతికూల అయాన్ల మధ్య ఎలెక్ట్రోస్టాటిక్ ఆకర్షణ ఫలితంగా ఏర్పడిన బంధం ఎలెక్ట్రోవాలెంట్ బంధం అని పిలువబడింది. అందువలన, ఎలెక్ట్రోవాలెన్స్ అయాన్పై యూనిట్ ఛార్జ్(ల) సంఖ్యకు సమానం. అందువలన, కాల్షియం రెండు ధనాత్మక ఎలెక్ట్రోవాలెన్స్ను కేటాయించబడింది, అయితే క్లోరిన్ ఒక ప్రతికూల ఎలెక్ట్రోవాలెన్స్ను కలిగి ఉంటుంది.
ఎలక్ట్రాన్ బదిలీ ద్వారా అయాన్-ఏర్పాటు మరియు అయానిక్ స్ఫటిక సమ్మేళనాల ఏర్పాటు గురించి ఆధునిక భావనలకు కోసెల్ యొక్క పోస్ట్యులేషన్లు ఆధారాన్ని అందిస్తాయి. అయానిక్ సమ్మేళనాల అవగాహన మరియు వ్యవస్థీకరణలో అతని అభిప్రాయాలు గొప్ప విలువగా నిరూపించబడ్డాయి. అదే సమయంలో, పెద్ద సంఖ్యలో సమ్మేళనాలు ఈ భావనలకు సరిపోలని వాస్తవాన్ని అతను గుర్తించాడు.
4.1.1 అష్టక నియమం
1916లో కోసెల్ మరియు లూయిస్ రసాయన బంధం యొక్క ఎలక్ట్రానిక్ సిద్ధాంతం అని పిలువబడే అణువుల మధ్య రసాయన కలయిక యొక్క ముఖ్యమైన సిద్ధాంతాన్ని అభివృద్ధి చేశారు. దీని ప్రకారం, అణువులు వాలెన్స్ ఎలక్ట్రాన్లను ఒక అణువు నుండి మరొక అణువుకు బదిలీ చేయడం ద్వారా (పొందడం లేదా కోల్పోవడం) లేదా వాలెన్స్ షెల్లలో అష్టకాన్ని కలిగి ఉండటానికి వాలెన్స్ ఎలక్ట్రాన్లను పంచుకోవడం ద్వారా కలిసి ఉంటాయి. దీనిని అష్టక నియమం అంటారు.
4.1.2 సమయోజనీయ బంధం
లాంగ్ముయిర్ (1919) అష్టకం యొక్క స్థిరమైన ఘనాకార అమరిక యొక్క ఆలోచనను విస్మరించడం ద్వారా మరియు సమయోజనీయ బంధం అనే పదాన్ని పరిచయం చేయడం ద్వారా లూయిస్ పోస్ట్యులేషన్లను శుద్ధి చేశాడు. క్లోరిన్ అణువు $\mathrm{Cl}_2$ ఏర్పడటాన్ని పరిగణనలోకి తీసుకోవడం ద్వారా లూయిస్-లాంగ్ముయిర్ సిద్ధాంతాన్ని అర్థం చేసుకోవచ్చు. ఎలక్ట్రానిక్ విన్యాసం $[\mathrm{Ne}] 3 s^2 3 p^5$తో $\mathrm{Cl}$ అణువు, ఆర్గాన్ విన్యాసానికి ఒక ఎలక్ట్రాన్ తక్కువగా ఉంటుంది. $\mathrm{Cl}_2$ అణువు ఏర్పడటం రెండు క్లోరిన్ అణువుల మధ్య ఒక జత ఎలక్ట్రాన్లను పంచుకోవడం పరంగా అర్థం చేసుకోవచ్చు, ప్రతి క్లోరిన్ అణువు పంచుకున్న జతకు ఒక ఎలక్ట్రాన్ని సహకరిస్తుంది. ఈ ప్రక్రియలో రెండు క్లోరిన్ అణువులు సమీపంలోని ఉదాత్త వాయువు (అనగా, ఆర్గాన్) యొక్క బాహ్య షెల్ అష్టకాన్ని పొందుతాయి.

రెండు Cl అణువుల మధ్య సమయోజనీయ బంధం
చుక్కలు ఎలక్ట్రాన్లను సూచిస్తాయి. అటువంటి నిర్మాణాలను లూయిస్ డాట్ నిర్మాణాలు అంటారు.
లూయిస్ డాట్ నిర్మాణాలు ఇతర అణువులకు కూడా వ్రాయవచ్చు, దీనిలో కలిపే అణువులు ఒకేలా లేదా భిన్నంగా ఉండవచ్చు. ముఖ్యమైన షరతులు:
- ప్రతి బంధం అణువుల మధ్య ఒక ఎలక్ట్రాన్ జతను పంచుకోవడం ఫలితంగా ఏర్పడుతుంది.
- కలిపే ప్రతి అణువు పంచుకున్న జతకు కనీసం ఒక ఎలక్ట్రాన్ని సహకరిస్తుంది.
- ఎలక్ట్రాన్లను పంచుకోవడం ఫలితంగా కలిపే అణువులు బాహ్య షెల్ ఉదాత్త వాయు విన్యాసాలను పొందుతాయి.
- అందువలన నీరు మరియు కార్బన్ టెట్రాక్లోరైడ్ అణువులలో, సమయోజనీయ బంధాల ఏర్పాటును ఇలా సూచించవచ్చు:

అందువలన, రెండు అణువులు ఒక ఎలక్ట్రాన్ జతను పంచుకున్నప్పుడు, అవి ఒకే సమయోజనీయ బంధం ద్వారా కలిసి ఉన్నాయని చెప్పబడుతుంది. అనేక సమ్మేళనాలలో మనకు అణువుల మధ్య బహుళ బంధాలు ఉన్నాయి. బహుళ బంధాల ఏర్పాటు రెండు అణువుల మధ్య ఒకటి కంటే ఎక్కువ ఎలక్ట్రాన్ జతలను పంచుకోవడాన్ని ఊహించుకుంటుంది. రెండు అణువులు రెండు జతల ఎలక్ట్రాన్లను పంచుకుంటే, వాటి మధ్య సమయోజనీయ బంధాన్ని డబుల్ బాండ్ అంటారు. ఉదాహరణకు, కార్బన్ డయాక్సైడ్ అణువులో, కార్బన్ మరియు ఆక్సిజన్ అణువుల మధ్య మనకు రెండు డబుల్ బంధాలు ఉన్నాయి. అదేవిధంగా ఇథీన్ అణువులో రెండు కార్బన్ అణువులు డబుల్ బంధం ద్వారా కలిసి ఉంటాయి..

$\mathrm{C} _{2} \mathrm{H} _{4}$ అణువు
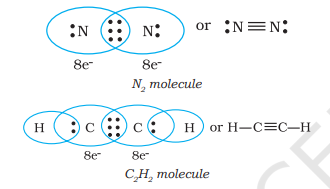
కలిపే అణువులు మూడు ఎలక్ట్రాన్ జతలను పంచుకున్నప్పుడు, $N_{2}$ అణువులోని రెండు నైట్రోజన్ అణువుల విషయంలో మరియు ఇథైన్ అణువులోని రెండు కార్బన్ అణువుల విషయంలో, ట్రిపుల్ బాండ్ ఏర్పడుతుంది.
4.1.3 సాధారణ అణువుల లూయిస్ ప్రాతినిధ్యం (లూయిస్ నిర్మాణాలు)
లూయిస్ డాట్ నిర్మాణాలు పంచుకున్న ఎలక్ట్రాన్ జతలు మరియు అష్టక నియమం పరంగా అణువులు మరియు అయాన్లలో బంధం యొక్క చిత్రాన్ని అందిస్తాయి. అటువంటి చిత్రం ఒక అణువు యొక్క బంధం మరియు ప్రవర్తనను పూర్తిగా వివరించకపోవచ్చు, అయినప్పటికీ ఇది ఒక అణువు యొక్క ఏర్పాటు మరియు లక్షణాలను పెద్ద మేరకు అర్థం చేసుకోవడంలో సహాయపడుతుంది. అందువలన, అణువుల లూయిస్ డాట్ నిర్మాణాలను వ్రాయడం చాలా ఉపయోగకరంగా ఉంటుంది. లూయిస్ డాట్ నిర్మాణాలు క్రింది దశలను స్వీకరించడం ద్వారా వ్రాయవచ్చు:
- నిర్మాణాలను వ్రాయడానికి అవసరమైన మొత్తం ఎలక్ట్రాన్ల సంఖ్య కలిపే అణువుల వాలెన్స్ ఎలక్ట్రాన్లను జోడించడం ద్వారా పొందబడుతుంది. ఉదాహరణకు, $\mathrm{CH}_{4}$ అణువులో బంధం కోసం ఎనిమిది వాలెన్స్ ఎలక్ట్రాన్లు అందుబాటులో ఉన్నాయి (కార్బన్ నుండి 4 మరియు నాలుగు హైడ్రోజన్ అణువుల నుండి 4).
- ప్రతికూల అయాన్ల కోసం, ప్రతి ప్రతికూల ఛార్జ్ అంటే ఒక ఎలక్ట్రాన్ జోడించడం. ధనాత్మక అయాన్ల కోసం, ప్రతి ధనాత్మక ఛార్జ్ వాలెన్స్ ఎలక్ట్రాన్ల మొత్తం సంఖ్య నుండి ఒక ఎలక్ట్రాన్ని తీసివేయడానికి దారి తీస్తుంది. ఉదాహరణకు, $CO_3^{2-}$ అయాన్ కోసం, రెండు ప్రతికూల ఛార్జీలు తటస్థ అణువుల ద్వారా అందించిన వాటి కంటే రెండు అదనపు ఎలక్ట్రాన్లు ఉన్నాయని సూచిస్తాయి. $\mathrm{NH}_{4}^{+}$ అయాన్ కోసం, ఒక ధనాత్మక ఛార్జ్ తటస్థ అణువుల సమూహం నుండి ఒక ఎలక్ట్రాన్ నష్టాన్ని సూచిస్తుంది.
- కలిపే అణువుల రసాయన చిహ్నాలను తెలుసుకోవడం మరియు సమ్మేళనం యొక్క అస్థిపంజర నిర్మాణం (తెలిసిన లేదా తెలివిగా ఊహించిన) గురించి జ్ఞానం కలిగి ఉండటం, మొత్తం బంధాలకు అనులోమానుపాతంలో అణువుల మధ్య బంధం పంచుకున్న జతలుగా మొత్తం ఎలక్ట్రాన్ల సంఖ్యను పంపిణీ చేయడం సులభం.
- సాధారణంగా తక్కువ ఎలక్ట్రోనెగటివ్ అణువు అణువు/అయాన్లో కేంద్ర స్థానాన్ని ఆక్రమిస్తుంది. ఉదాహరణకు $\mathrm{NF}_3$ మరియు $CO_3^{2-}$లో, నైట్రోజన్ మరియు కార్బన్ కేంద్ర అణువులు అయితే ఫ్లోరిన్ మరియు ఆక్సిజన్ టెర్మినల్ స్థానాలను ఆక్రమిస్తాయి.
- సింగిల్ బాండ్ల కోసం పంచుకున్న ఎలక్ట్రాన్ జతలను లెక్కించిన తర్వాత, మిగిలిన ఎలక్ట్రాన్ జతలు బహుళ బంధం కోసం ఉపయోగించబడతాయి లేదా ఒంటరి జతలుగా ఉంటాయి. ప్రాథమిక అవసరం ఏమిటంటే ప్రతి బంధిత అణువు ఎలక్ట్రాన్ల అష్టకాన్ని పొందుతుంది.
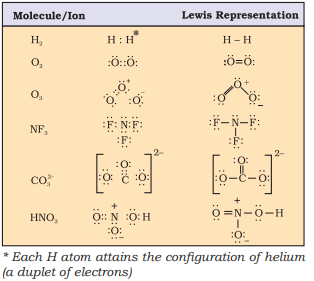
కొన్ని అణువులు/అయాన్ల లూయిస్ ప్రాతినిధ్యాలు పట్టిక 4.1లో ఇవ్వబడ్డాయి.
పట్టిక 4.1 కొన్ని అణువుల లూయిస్ ప్రాతినిధ్యం
సమస్య 4.1
$\mathrm{CO}$ అణువు యొక్క లూయిస్ డాట్ నిర్మాణాన్ని వ్రాయండి.
పరిష్కారం
దశ 1. కార్బన్ మరియు ఆక్సిజన్ అణువుల వాలెన్స్ ఎలక్ట్రాన్ల మొత్తం సంఖ్యను లెక్కించండి. కార్బన్ మరియు ఆక్సిజన్ అణువుల బాహ్య (వాలెన్స్) షెల్ విన్యాసాలు వరుసగా: $2 s^{2} 2 p^{2}$ మరియు $2 s^{2} 2 p^{4}$. అందుబాటులో ఉన్న వాలెన్స్ ఎలక్ట్రాన్లు $4+6=10$.
దశ 2. $\mathrm{CO}$ యొక్క అస్థిపంజర నిర్మాణం ఇలా వ్రాయబడింది: C O
దశ 3. $\mathrm{C}$ మరియు $\mathrm{O}$ మధ్య ఒకే బంధాన్ని (ఒక పంచుకున్న ఎలక్ట్రాన్ జత) గీయండి మరియు $\mathrm{O}$పై అష్టకాన్ని పూర్తి చేయండి, మిగిలిన రెండు ఎలక్ట్రాన్లు $\mathrm{C}$పై ఒంటరి జత.
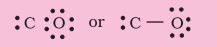
ఇది కార్బన్పై అష్టకాన్ని పూర్తి చేయదు మరియు అందువలన మనం $\mathrm{C}$ మరియు $\mathrm{O}$ అణువుల మధ్య బహుళ బంధానికి (ఈ సందర్భంలో ట్రిపుల్ బంధం) ఆశ్రయించాలి. ఇది రెండు అణువులకు అష్టక నియమం షరతును సంతృప్తిపరుస్తుంది.
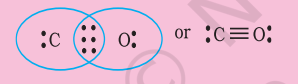
సమస్య 4.2
నైట్రైట్ అయాన్ యొక్క లూయిస్ నిర్మాణాన్ని వ్రాయండి, $\mathrm{NO}_{2}^{-}$.
పరిష్కారం








