అధ్యాయం 08 రెడాక్స్ చర్యలు
“ఆక్సీకరణం ఉన్న చోట, తగ్గింపు ఎల్లప్పుడూ ఉంటుంది. రసాయన శాస్త్రం ముఖ్యంగా రెడాక్స్ వ్యవస్థల అధ్యయనం.”
రసాయన శాస్త్రం వివిధ రకాల పదార్థాలను మరియు ఒక రకమైన పదార్థం మరొక రకంగా మారే మార్పును వ్యవహరిస్తుంది. ఒక రకమైన పదార్థం మరొక రకంగా మార్పు చెందడం వివిధ రకాల చర్యల ద్వారా జరుగుతుంది. అటువంటి చర్యలలో ఒక ముఖ్యమైన వర్గం రెడాక్స్ చర్యలు. అనేక దృగ్విషయాలు, భౌతికమైనవి మరియు జీవసంబంధమైనవి కూడా, రెడాక్స్ చర్యలకు సంబంధించినవి. ఈ చర్యలు ఫార్మాస్యూటికల్, జీవశాస్త్ర, పారిశ్రామిక, లోహశాస్త్ర మరియు వ్యవసాయ రంగాలలో విస్తృతంగా ఉపయోగించబడతాయి. ఈ చర్యల ప్రాముఖ్యత వాటి నుండి స్పష్టంగా తెలుస్తుంది: గృహ, రవాణా మరియు ఇతర వాణిజ్య ప్రయోజనాల కోసం శక్తి పొందడానికి వివిధ రకాల ఇంధనాల దహనం, అత్యంత చర్యాశీల లోహాలు మరియు అలోహాల సంగ్రహణ కోసం విద్యుత్ రసాయన ప్రక్రియలు, కాస్టిక్ సోడా వంటి రసాయన సమ్మేళనాల తయారీ, ఎండిన మరియు తడి బ్యాటరీల పనితీరు మరియు లోహాల క్షయం వంటివి రెడాక్స్ ప్రక్రియల పరిధిలోకి వస్తాయి. ఇటీవల, హైడ్రోజన్ ఎకనామీ (ద్రవ హైడ్రోజన్ ఇంధనంగా ఉపయోగం) మరియు ‘ఓజోన్ హోల్’ అభివృద్ధి వంటి పర్యావరణ సమస్యలు రెడాక్స్ దృగ్విషయం కింద కనిపించడం ప్రారంభించాయి.
8.1 రెడాక్స్ చర్యల శాస్త్రీయ భావన - ఆక్సీకరణ మరియు తగ్గింపు చర్యలు
మొదట్లో, ఆక్సీకరణ అనే పదం ఒక మూలకం లేదా సమ్మేళనానికి ఆక్సిజన్ జోడించడాన్ని వివరించడానికి ఉపయోగించబడింది. వాతావరణంలో డైఆక్సిజన్ ఉండటం వలన (20%), అనేక మూలకాలు దానితో కలిసిపోతాయి మరియు ఇది వాటి ఆక్సైడ్ల రూపంలో సాధారణంగా భూమిపై కనిపించడానికి ప్రధాన కారణం. ఆక్సీకరణం యొక్క పరిమిత నిర్వచనం ప్రకారం కింది చర్యలు ఆక్సీకరణ ప్రక్రియలను సూచిస్తాయి:
$$2 \mathrm{Mg}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{MgO}(\mathrm{s}) \tag{8.1}$$
$$\mathrm{S}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow \mathrm{SO_2}(\mathrm{~g}) \tag{8.2}$$
చర్యలు (8.1) మరియు (8.2)లో, మెగ్నీషియం మరియు సల్ఫర్ మూలకాలు వాటికి ఆక్సిజన్ జోడించబడినందున ఆక్సీకరణం చెందాయి. అదేవిధంగా, మీథేన్ దానికి ఆక్సిజన్ జోడించబడినందున ఆక్సీకరణం చెందుతుంది.
$$\mathrm{CH} _{4}(\mathrm{~g})+2 \mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g})+2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{7.3}$$
చర్య (8.3)ను జాగ్రత్తగా పరిశీలించినప్పుడు, దాని నుండి హైడ్రోజన్ ఆక్సిజన్ ద్వారా భర్తీ చేయబడింది, ఇది రసాయన శాస్త్రవేత్తలను హైడ్రోజన్ను తొలగించడం పరంగా ఆక్సీకరణాన్ని తిరిగి వివరించడానికి ప్రేరేపించింది మరియు అందువలన, ఆక్సీకరణం అనే పదం యొక్క పరిధి ఒక పదార్థం నుండి హైడ్రోజన్ను తొలగించడాన్ని కూడా చేర్చడానికి విస్తరించబడింది. హైడ్రోజన్ తొలగింపును ఆక్సీకరణ చర్యగా కూడా ఉదహరించగల మరొక చర్య కింది వివరణ:
$$ \begin{equation*} 2 \mathrm{H_2} \mathrm{~S}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{~S}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \tag{8.4} \end{equation*} $$
రసాయన శాస్త్రవేత్తల జ్ఞానం పెరిగిన కొద్దీ, ఆక్సిజన్ను కలిగి ఉండని కానీ ఇతర విద్యుదృణ మూలకాలను కలిగి ఉన్న (7.1 నుండి 7.4) వంటి చర్యల కోసం ఆక్సీకరణ పదాన్ని విస్తరించడం సహజం. మెగ్నీషియం యొక్క ఆక్సీకరణం ఫ్లోరిన్, క్లోరిన్ మరియు సల్ఫర్ మొదలైన వాటితో కింది చర్యల ప్రకారం జరుగుతుంది:
$$\operatorname{Mg}(\mathrm{s})+\mathrm{F_2} (\mathrm{~g}) \rightarrow \operatorname{MgF_2} (s) \tag{8.5}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{Cl_2} (g) \rightarrow \mathrm{MgCl_2} (s) \tag{8.6}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{S} (s) \rightarrow \operatorname{MgS}(\mathrm{s}) \tag{8.7}$$
చర్యలు (7.5 నుండి 7.7)ని ఆక్సీకరణ చర్యల పరిధిలో చేర్చడం రసాయన శాస్త్రవేత్తలను హైడ్రోజన్ తొలగింపు మాత్రమే కాకుండా, విద్యుద్ధన మూలకాల తొలగింపును కూడా ఆక్సీకరణంగా పరిగణించడానికి ప్రోత్సహించింది. అందువలన చర్య:
$$ 2 \mathrm{~K_4} \left[ \mathrm{Fe} ( \mathrm{CN})_{6} \right] ( \mathrm{aq}) + \mathrm{H_2} \mathrm{O_2} ( \mathrm{aq}) \rightarrow 2 \mathrm{~K_3} \left[\mathrm{Fe}( \mathrm{CN})_6 \right] ( \mathrm{aq}) + 2 \mathrm{KOH} ( \mathrm{aq}) $$
పొటాషియం ఫెర్రోసైనైడ్ పొటాషియం ఫెర్రిసైనైడ్గా మారడానికి ముందు విద్యుద్ధన మూలకం పొటాషియం తొలగించబడినందున ఆక్సీకరణంగా అర్థం చేసుకోబడింది. సంగ్రహంగా చెప్పాలంటే, “ఆక్సీకరణం” అనే పదం ఒక పదార్థానికి ఆక్సిజన్/విద్యుదృణ మూలకం జోడించడం లేదా ఒక పదార్థం నుండి హైడ్రోజన్/విద్యుద్ధన మూలకం తొలగించడం అని నిర్వచించబడింది.
మొదట్లో, తగ్గింపు ఒక సమ్మేళనం నుండి ఆక్సిజన్ను తొలగించడంగా పరిగణించబడింది. అయితే, ఈ రోజుల్లో తగ్గింపు అనే పదం ఒక పదార్థం నుండి ఆక్సిజన్/విద్యుదృణ మూలకం తొలగించడం లేదా ఒక పదార్థానికి హైడ్రోజన్/విద్యుద్ధన మూలకం జోడించడం వరకు విస్తరించబడింది.
పైన ఇచ్చిన నిర్వచనం ప్రకారం, తగ్గింపు ప్రక్రియలకు ఉదాహరణలు క్రింది విధంగా ఉన్నాయి:
$$2 \mathrm{HgO}(\mathrm{s}) \xrightarrow{\Delta} 2 \mathrm{Hg}(\mathrm{l})+\mathrm{O_2}(\mathrm{~g}) \tag{8.8}$$
(మెర్క్యూరిక్ ఆక్సైడ్ నుండి ఆక్సిజన్ తొలగింపు)
$$2 \mathrm{FeCl_3}(\mathrm{aq})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{FeCl_2}(\mathrm{aq})+2 \mathrm{HCl}(\mathrm{aq}) \tag{8.9}$$
(విద్యుదృణ మూలకం, క్లోరిన్ తొలగింపు ఫెర్రిక్ క్లోరైడ్ నుండి)
$$\mathrm{CH_2}=\mathrm{CH_2}(\mathrm{~g})+\mathrm{H_2}(\mathrm{~g}) \rightarrow \mathrm{H_3} \mathrm{C}-\mathrm{CH_3}(\mathrm{~g})\tag{8.10}$$
(హైడ్రోజన్ జోడింపు)
$$2 \mathrm{HgCl_2}(\mathrm{aq})+\mathrm{SnCl_2}(\mathrm{aq}) \rightarrow \mathrm{Hg_2} \mathrm{Cl_2}(\mathrm{~s})+\mathrm{SnCl_4}(\mathrm{aq})\tag{8.11}$$
(మెర్క్యూరిక్ క్లోరైడ్కు పాదరసం జోడింపు)
చర్య (8.11)లో, స్టానస్ క్లోరైడ్ నుండి స్టానిక్ క్లోరైడ్కు ఏకకాలంలో ఆక్సీకరణం కూడా జరుగుతోంది, ఎందుకంటే దానికి విద్యుదృణ మూలకం క్లోరిన్ జోడించబడింది. ఆక్సీకరణం మరియు తగ్గింపు ఎల్లప్పుడూ ఏకకాలంలో జరుగుతాయని త్వరలో గుర్తించబడింది (పైన ఇచ్చిన అన్ని సమీకరణాలను తిరిగి పరిశీలించడం ద్వారా స్పష్టంగా తెలుస్తుంది), అందువలన, ఈ రసాయన చర్యల తరగతికి “రెడాక్స్” అనే పదం ఏర్పడింది.
సమస్య 8.1
క్రింద ఇవ్వబడిన చర్యలలో, ఆక్సీకరణం మరియు తగ్గింపు చెందుతున్న జాతులను గుర్తించండి:
(i) $\mathrm{H_2} \mathrm{~S}$ (g) $+\mathrm{Cl_2}$ (g) $\rightarrow 2 \mathrm{HCl}$ (g) $+\mathrm{S}$ (s)
(ii) $3 \mathrm{Fe_3} \mathrm{O_4}$ (s) $+8 \mathrm{Al}$ (s) $\rightarrow 9 \mathrm{Fe}$ (s) $+4 \mathrm{Al_2} \mathrm{O_3}(\mathrm{~s})$
(iii) $2 \mathrm{Na}$ (s) $+\mathrm{H_2}$ (g) $\rightarrow 2 \mathrm{NaH}$ (s)
పరిష్కారం
(i) $\mathrm{H_2} \mathrm{~S}$ ఆక్సీకరణం చెందుతుంది ఎందుకంటే మరింత విద్యుదృణ మూలకం, క్లోరిన్ హైడ్రోజన్కు జోడించబడింది (లేదా మరింత విద్యుద్ధన మూలకం, హైడ్రోజన్ S నుండి తొలగించబడింది). క్లోరిన్ దానికి హైడ్రోజన్ జోడించబడినందున తగ్గింపు చెందుతుంది.
(ii) అల్యూమినియం ఆక్సీకరణం చెందుతుంది ఎందుకంటే దానికి ఆక్సిజన్ జోడించబడింది. ఫెర్రస్ ఫెర్రిక్ ఆక్సైడ్ $\left(\mathrm{Fe_3} \mathrm{O_4}\right)$ తగ్గింపు చెందుతుంది ఎందుకంటే దాని నుండి ఆక్సిజన్ తొలగించబడింది.
(iii) విద్యుదృణత యొక్క భావనను జాగ్రత్తగా వర్తింపజేస్తే మాత్రమే సోడియం ఆక్సీకరణం చెందుతుందని మరియు హైడ్రోజన్ తగ్గింపు చెందుతుందని మేము నిర్ధారించవచ్చు.
ఇక్కడ ఎంచుకున్న చర్య (iii) రెడాక్స్ చర్యలను నిర్వచించడానికి మరొక మార్గం పరంగా ఆలోచించమని మాకు ప్రేరేపిస్తుంది.
8.2 ఎలక్ట్రాన్ బదిలీ చర్యల పరంగా రెడాక్స్ చర్యలు
ఈ చర్యలలో ప్రతి ఒక్కదానిలో సోడియంకు ఆక్సిజన్ లేదా మరింత విద్యుదృణ మూలకం జోడించబడినందున సోడియం ఆక్సీకరణం చెందుతుంది కాబట్టి ఈ చర్యలు రెడాక్స్ చర్యలు అని మనం ఇప్పటికే తెలుసుకున్నాము.
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaCl}(\mathrm{s})\tag{8.12}$$
$$4 \mathrm{Na}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na_2} \mathrm{O}(\mathrm{s})\tag{8.13}$$
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{S}(\mathrm{s}) \rightarrow \mathrm{Na_2} \mathrm{~S}(\mathrm{~s}) \tag{8.14}$$
ఏకకాలంలో, క్లోరిన్, ఆక్సిజన్ మరియు సల్ఫర్ తగ్గింపు చెందుతాయి ఎందుకంటే వాటిలో ప్రతి ఒక్కదానికి, విద్యుద్ధన మూలకం సోడియం జోడించబడింది. రసాయన బంధం గురించి మన జ్ఞానం నుండి సోడియం క్లోరైడ్, సోడియం ఆక్సైడ్ మరియు సోడియం సల్ఫైడ్ అయానిక్ సమ్మేళనాలు మరియు బహుశా $\mathrm{Na}^{+} \mathrm{Cl}^{-}( \mathrm{s}),\left(\mathrm{Na}^{+} \right)_2 \mathrm{O}^{2-}( \mathrm{s})$, మరియు $ \left(\mathrm{Na}^{+} \right)_2$ $\mathrm{S}^{2-}( \mathrm{s})$గా బాగా వ్రాయబడతాయని కూడా మనకు తెలుసు. ఉత్పత్తి చేయబడిన జాతులపై ఆవేశాల అభివృద్ధి మనల్ని చర్యలను (8.12 నుండి 8.14) కింది పద్ధతిలో తిరిగి వ్రాయమని సూచిస్తుంది:
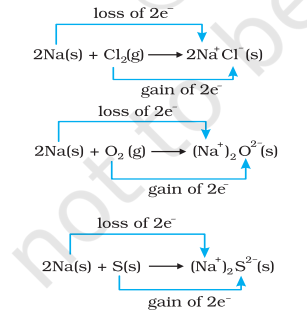
సౌలభ్యం కోసం, పై ప్రక్రియలలో ప్రతి ఒక్కదానిని రెండు వేర్వేరు దశలుగా పరిగణించవచ్చు, ఒకటి ఎలక్ట్రాన్ల కోల్పోవడం మరియు మరొకటి ఎలక్ట్రాన్లను పొందడం. ఒక వివరణగా, వీటిలో ఒకదానిని, అంటే, సోడియం క్లోరైడ్ ఏర్పడటాన్ని మనం మరింత వివరించవచ్చు.
$2 \mathrm{Na}(\mathrm{s}) \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
$\mathrm{Cl_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{Cl}^{-}(\mathrm{g})$
పైన ఉన్న ప్రతి దశను అర్ధచర్య అంటారు, ఇది ఎలక్ట్రాన్ల పాల్గొనడాన్ని స్పష్టంగా చూపుతుంది. అర్ధచర్యల మొత్తం మొత్తం చర్యను ఇస్తుంది:
$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na}^{+} \mathrm{Cl}^{-}(\mathrm{s})$ లేదా $2 \mathrm{NaCl}(\mathrm{s})$
చర్యలు 8.12 నుండి 8.14 సూచించేది ఎలక్ట్రాన్ల కోల్పోవడం ఉన్న అర్ధచర్యలను ఆక్సీకరణ చర్యలు అంటారు. అదేవిధంగా, ఎలక్ట్రాన్లను పొందడం ఉన్న అర్ధచర్యలను తగ్గింపు చర్యలు అంటారు. ఆక్సీకరణం మరియు తగ్గింపును నిర్వచించే కొత్త మార్గం శాస్త్రీయ భావన ప్రకారం జాతుల ప్రవర్తన మరియు ఎలక్ట్రాన్-బదిలీ మార్పులో వాటి పరస్పర చర్య మధ్య సంబంధాన్ని ఏర్పరచడం ద్వారా మాత్రమే సాధించబడిందని ఇక్కడ ప్రస్తావించడం సందర్భోచితం కాకపోవచ్చు. చర్యలలో (8.12 నుండి 8.14) ఆక్సీకరణం చెందిన సోడియం, రిడ్యూసింగ్ ఏజెంట్గా పనిచేస్తుంది ఎందుకంటే ఇది దానితో పరస్పర చర్య చేసే ప్రతి మూలకానికి ఎలక్ట్రాన్ను దానం చేస్తుంది మరియు అందువలన వాటిని తగ్గించడంలో సహాయపడుతుంది. క్లోరిన్, ఆక్సిజన్ మరియు సల్ఫర్ తగ్గింపు చెందుతాయి మరియు ఆక్సీకరణ కారకాలుగా పనిచేస్తాయి ఎందుకంటే ఇవి సోడియం నుండి ఎలక్ట్రాన్లను అంగీకరిస్తాయి. సంగ్రహంగా చెప్పాలంటే, మనం ఇలా ప్రస్తావించవచ్చు
ఆక్సీకరణం: ఏదైనా జాతి ద్వారా ఎలక్ట్రాన్(ల) కోల్పోవడం.
తగ్గింపు: ఏదైనా జాతి ద్వారా ఎలక్ట్రాన్(ల)ను పొందడం.
ఆక్సీకరణ కారకం: ఎలక్ట్రాన్(ల) యొక్క గ్రహీత.
రిడ్యూసింగ్ ఏజెంట్: ఎలక్ట్రాన్(ల) యొక్క దాత.
సమస్య 8.2
చర్య: $2 \mathrm{Na}(\mathrm{s})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaH}$ (s) ఒక రెడాక్స్ మార్పు అని న్యాయసమ్మతం చేయండి.
పరిష్కారం
పై చర్యలో ఏర్పడిన సమ్మేళనం ఒక అయానిక్ సమ్మేళనం కాబట్టి, దీనిని $\mathrm{Na}^{+} \mathrm{H}^{-}$(s)గా కూడా సూచించవచ్చు, ఇది ఈ ప్రక్రియలో ఒక అర్ధచర్య:
$2 \mathrm{Na}(\mathrm{s}) \quad \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
మరియు మరొక అర్ధచర్య:
$\mathrm{H_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{H}^{-}(\mathrm{g})$
పరీక్షలో ఉన్న చర్యను రెండు అర్ధచర్యలుగా విభజించడం స్వయంచాలకంగా ఇక్కడ సోడియం ఆక్సీకరణం చెందుతుందని మరియు హైడ్రోజన్ తగ్గింపు చెందుతుందని బహిర్గతం చేస్తుంది, అందువలన, పూర్తి చర్య ఒక రెడాక్స్ మార్పు.
8.2.1 పోటీ ఎలక్ట్రాన్ బదిలీ చర్యలు
మెటాలిక్ జింక్ యొక్క ఒక పట్టీని ఫిగ్ 8.1లో చూపిన విధంగా కాపర్ నైట్రేట్ యొక్క జలద్రావణంలో ఒక గంట పాటు ఉంచండి. పట్టీ ఎరుపు రంగు మెటాలిక్ కాపర్తో పూత పూయబడిందని మరియు ద్రావణం యొక్క నీలం రంగు అదృశ్యమవుతుందని మీరు గమనించవచ్చు. $\mathrm{Zn}^{2+}$ అయాన్ల ఏర్పాటు $\mathrm{Cu}^{2+}$ వల్ల ద్రావణం యొక్క నీలం రంగు అదృశ్యమైనప్పుడు సులభంగా నిర్ధారించబడుతుంది. హైడ్రోజన్ సల్ఫైడ్ వాయువును $\mathrm{Zn}^{2+}$ అయాన్లను కలిగి ఉన్న రంగులేని ద్రావణం ద్వారా పంపినట్లయితే, తెల్లటి జింక్ సల్ఫైడ్, $\mathrm{ZnS}$ యొక్క రంగు ద్రావణాన్ని అమ్మోనియాతో క్షారంగా చేసినప్పుడు కనిపించవచ్చు.
మెటాలిక్ జింక్ మరియు కాపర్ నైట్రేట్ యొక్క జలద్రావణం మధ్య చర్య:
$$\mathrm{Zn}(\mathrm{s})+\mathrm{Cu}^{2+}(\mathrm{aq}) \rightarrow \mathrm{Zn}^{2+}(\mathrm{aq})+\mathrm{Cu}(\mathrm{s}) \tag{8.15}$$
చర్య (8.15)లో, జింక్ $Zn^{2+}$ ఏర్పడటానికి ఎలక్ట్రాన్లను కోల్పోయింది మరియు, అందువలన, జింక్ ఆక్సీకరణం చెందుతుంది. స్పష్టంగా, ఇప్పుడు జింక్ ఆక్సీకరణం చెందినట్లయితే, ఎలక్ట్రాన్లను విడుదల చేస్తే, జింక్ కోల్పోయిన ఎలక్ట్రాన్లను అంగీకరించడం ద్వారా తగ్గించబడే ఏదో ఉండాలి. కాపర్ అయాన్ జింక్ నుండి ఎలక్ట్రాన్లను పొందడం ద్వారా తగ్గింపు చెందుతుంది.
చర్య (8.15) ఇలా తిరిగి వ్రాయవచ్చు:
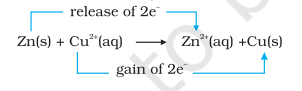
ఈ దశలో మనం సమీకరణం (8.15) ద్వారా సూచించబడిన చర్యకు సమతౌల్య స్థితిని పరిశోధించవచ్చు. ఈ ప్రయోజనం కోసం, జింక్ సల్ఫేట్ ద్రావణంలో మెటాలిక్ కాపర్ యొక్క ఒక పట్టీని ఉంచండి. ఎలాంటి దృశ్యమాన చర్య గమనించబడదు మరియు $\mathrm{Cu}^{2+}$ అయాన్ల ఉనికిని గుర్తించడానికి ప్రయత్నం $\mathrm{H_2} \mathrm{~S}$ వాయువును ద్రావణం ద్వారా పంపడం ద్వారా క్యుప్రిక్ సల్ఫైడ్, CuS యొక్క నలుపు రంగును ఉత్పత్తి చేయడం విజయవంతం కాదు. క్యుప్రిక్ సల్ఫైడ్ చాలా తక్కువ ద్రావణీయతను కలిగి ఉంటుంది, ఇది చాలా సున్నితమైన పరీక్ష; అయినప్పటికీ, ఏర్పడిన $\mathrm{Cu}^{2+}$ మొత్తాన్ని గుర్తించలేము. అందువలన, చర్య (8.15)కు సమతౌల్య స్థితి ప్రతిచర్యకారుల కంటే ఉత్పన్నాలను చాలా ఎక్కువగా అనుకూలంగా ఉంటుందని మేము నిర్ధారించాము.
ఇప్పుడు ఎలక్ట్రాన్ బదిలీ చర్యను కాపర్ లోహం మరియు వెండి నైట్రేట్ ద్రావణం వరకు విస్తరించి, ఫిగ్ 8.2లో చూపిన విధంగా ఒక సెటప్ను ఏర్పాటు చేద్దాం. చర్య వలన ద్రావణం నీలం రంగును అభివృద్ధి చేస్తుంది:
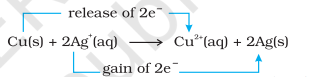
ఇక్కడ, $\mathrm{Cu}(\mathrm{s})$ $\mathrm{Cu}^{2+}(\mathrm{aq})$కి ఆక్సీకరణం చెందుతుంది మరియు $\mathrm{Ag}^{+}(\mathrm{aq})$ $\mathrm{Ag}(\mathrm{s})$కి తగ్గింపు చెందుతుంది. సమతౌల్యం ఉత్పన్నాలు $\mathrm{Cu}^{2+}(\mathrm{aq})$ మరియు $\mathrm{Ag}(\mathrm{s})$ను చాలా అనుకూలంగా ఉంటుంది.
వ్యత్యాసం ద్వారా, నికెల్ సల్ఫేట్ ద్రావణంలో ఉంచబడిన మెటాలిక్ కోబాల్ట్ చర్యను కూడా పోల్చి చూద్దాం. ఇక్కడ జరిగే చర్య:
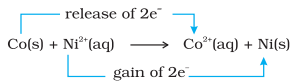
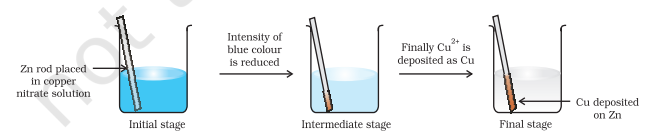
Fig. 8.1 జింక్ మరియు కాపర్ నైట్రేట్ యొక్క జలద్రావణం మధ్య రెడాక్స్ చర్య బీకర్లో జరుగుతుంది.
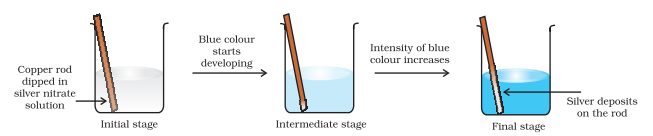
Fig. 8.2 కాపర్ మరియు వెండి నైట్రేట్ యొక్క జలద్రావణం మధ్య రెడాక్స్ చర్య బీకర్లో జరుగుతుంది
సమతౌల్య స్థితిలో, రసాయన పరీక్షలు $\mathrm{Ni}^{2+}(\mathrm{aq})$ మరియు $\mathrm{Co}^{2+}(\mathrm{aq})$ రెండూ మధ్యస్థ గాఢతలలో ఉన్నాయని బహిర్గతం చేస్తాయి. ఈ సందర్భంలో, ప్రతిచర్యకారులు $\left[\mathrm{Co}(\mathrm{s})\right.$ మరియు $\left.\mathrm{Ni}^{2+}(\mathrm{aq})\right]$ లేదా ఉత్పన్నాలు $\left[\mathrm{Co}^{2+}(\mathrm{aq})\right.$ మరియు $\left.\mathrm{Ni}(\mathrm{s})\right]$ చాలా అనుకూలంగా లేవు.
ఎలక్ట్రాన్ల విడుదల కోసం ఈ పోటీ ప్రోటాన్ల విడుదల కోసం ఆమ్లాల మధ్య పోటీని మనకు గుర్తు చేస్తుంది. ఈ సారూప్యత ఆమ్లాల బలాన్ని సూచించడానికి ఆమ్లాల విషయంలో మనం చేస్తున్నట్లుగా లోహాలు మరియు వాటి అయాన్లను ఎలక్ట్రాన్లను విడుదల చేయడానికి వాటి ధోరణి ఆధారంగా జాబితా చేయబడిన పట్టికను మనం అభివృద్ధి చేయవచ్చని సూచిస్తుంది. వాస్తవానికి మనం ఇప్పటికే కొన్ని పోలికలు చేసాము. పోలిక ద్వారా జింక్ కాపర్కు ఎలక్ట్రాన్లను విడుదల చేస్తుందని మరియు కాపర్ వెండికి ఎలక్ట్రాన్లను విడుదల చేస్తుందని మనకు తెలుసు మరియు, అందువలన, లోహాల ఎలక్ట్రాన్ విడుదల ధోరణి క్రమంలో ఉంటుంది: $\mathrm{Zn}>\mathrm{Cu}>\mathrm{Ag}$. మన జాబితాను మరింత విస్తృతంగా చేయడానికి మరియు లోహ క్రియాశీల శ్రేణి లేదా విద్యుత్ రసాయన శ్రేణిని రూపకల్పన చేయడానికి మేము ఇష్టపడతాము. వివిధ లోహాల మధ్య ఎలక్ట్రాన్ల కోసం పోటీ గాల్వానిక్ సెల్లు అని పిలువబడే సెల్ల తరగతిని రూపకల్పన చేయడంలో మాకు సహాయపడుతుంది, దీనిలో రసాయన చర్యలు విద్యుత్ శక్తి యొక్క మూలంగా మారతాయి. క్లాస్ XIIలో ఈ సెల్ల గురించి మనం మరింత అధ్యయనం చేస్తాము.
8.3 ఆక్సీకరణ సంఖ్య
ఎలక్ట్రాన్ బదిలీ యొక్క తక్కువ స్పష్టమైన ఉదాహరణ హైడ్రోజన్ ఆక్సిజన్తో కల








