باب 03 عناصر کی درجہ بندی اور خواص میں دوری
“دوری جدول بلا شبہ کیمیا میں سب سے اہم تصور ہے، اصولی اور عملی دونوں اعتبار سے۔ یہ طلباء کے لیے روزمرہ کی سہارا ہے، پیشہ ور افراد کے لیے تحقیق کے نئے راستے تجویز کرتا ہے، اور یہ پوری کیمیا کا ایک مختصر انتظام فراہم کرتا ہے۔ یہ اس حقیقت کا ایک قابل ذکر مظاہرہ ہے کہ کیمیائی عناصر وجودوں کا ایک بے ترتیب جھنڈ نہیں ہیں بلکہ رجحانات ظاہر کرتے ہیں اور خاندانوں میں اکٹھے پائے جاتے ہیں۔ دوری جدول کا شعور ہر اس شخص کے لیے ضروری ہے جو دنیا کو سلجھانا چاہتا ہے اور یہ دیکھنا چاہتا ہے کہ یہ کیمیا کے بنیادی بلڈنگ بلاکس، یعنی کیمیائی عناصر سے کیسے تعمیر ہوئی ہے۔”
گلین ٹی سی بورگ
اس یونٹ میں، ہم دوری جدول کی تاریخی ترقی جیسا کہ آج ہے اور جدید دوری قانون کا مطالعہ کریں گے۔ ہم یہ بھی سیکھیں گے کہ ایٹموں کی الیکٹرانک ترتیب کے منطقی نتیجے کے طور پر دوری درجہ بندی کیسے ہوتی ہے۔ آخر میں، ہم عناصر کے طبیعی اور کیمیائی خواص میں کچھ دوری رجحانات کا جائزہ لیں گے۔
3.1 ہمیں عناصر کی درجہ بندی کیوں کرنے کی ضرورت ہے؟
ہم اب تک جانتے ہیں کہ عناصر ہر قسم کے مادے کی بنیادی اکائیاں ہیں۔ 1800 میں، صرف 31 عناصر معلوم تھے۔ 1865 تک، شناخت شدہ عناصر کی تعداد دوگنی سے زیادہ ہو کر 63 ہو گئی تھی۔ فی الحال 114 عناصر معلوم ہیں۔ ان میں سے، حال ہی میں دریافت ہونے والے عناصر انسان ساختہ ہیں۔ نئے عناصر ترکیب کرنے کی کوششیں جاری ہیں۔ اتنی بڑی تعداد میں عناصر کے ساتھ ان تمام عناصر اور ان کے لاتعداد مرکبات کی کیمیا کا انفرادی طور پر مطالعہ کرنا بہت مشکل ہے۔ اس مسئلے کو آسان بنانے کے لیے، سائنسدانوں نے عناصر کی درجہ بندی کر کے اپنے علم کو منظم کرنے کے نظامی طریقے کی تلاش کی۔ نہ صرف یہ کہ یہ عناصر کے بارے میں معلوم کیمیائی حقائق کو معقول بنائے گا، بلکہ مزید مطالعہ کے لیے نئے عناصر کی پیش گوئی بھی کرے گا۔
3.2 دوری درجہ بندی کی ابتدا
عناصر کو گروپوں میں درجہ بندی کرنا اور دوری قانون اور دوری جدول کی ترقی متعدد سائنسدانوں کے مشاہدات اور تجربات سے حاصل ہونے والے علم کو نظامی بنانے کے نتائج ہیں۔ جرمن کیمیا دان، جوہان ڈوبرائنر 1800 کی دہائی کے اوائل میں عناصر کے خواص میں رجحانات کے خیال پر غور کرنے والے پہلے شخص تھے۔ 1829 تک انہوں نے تین عناصر کے کئی گروپوں (تثلیث) کے طبیعی اور کیمیائی خواص میں مماثلت نوٹ کی۔ ہر معاملے میں، انہوں نے دیکھا کہ ہر تثلیث کے درمیانی عنصر کا ایٹمی وزن دوسرے دو کے ایٹمی وزن کے تقریباً درمیانی نصف راستے پر تھا (جدول 3.1)۔ نیز درمیانی عنصر کے خواص دوسرے دو اراکین کے درمیان تھے۔
جدول 3.1 ڈوبرائنر کی تثلیثیں
| عنصر | ایٹمی وزن | عنصر | ایٹمی وزن | عنصر | ایٹمی وزن |
|---|---|---|---|---|---|
| $\mathbf{L i}$ | 7 | $\mathbf{C a}$ | 40 | $\mathbf{C l}$ | 35.5 |
| $\mathbf{N a}$ | 23 | $\mathbf{S r}$ | 88 | $\mathbf{B r}$ | 80 |
| $\mathbf{K}$ | 39 | $\mathbf{B a}$ | 137 | $\mathbf{I}$ | 127 |
چونکہ ڈوبرائنر کے تعلق، جسے قانون تثلیث کہا جاتا ہے، صرف چند عناصر کے لیے کام کرتا دکھائی دیا، اسے اتفاق سمجھ کر رد کر دیا گیا۔ عناصر کی درجہ بندی کی اگلی رپورٹ شدہ کوشش ایک فرانسیسی ماہر ارضیات، اے ای بی ڈی شانکورٹوئس نے 1862 میں کی۔ انہوں نے اس وقت کے معلوم عناصر کو بڑھتے ہوئے ایٹمی وزن کے ترتیب میں ترتیب دیا اور خواص کی دوری تکرار کو ظاہر کرنے کے لیے عناصر کا ایک اسطوانی جدول بنایا۔ اس نے بھی زیادہ توجہ حاصل نہیں کی۔ انگریز کیمیا دان، جان الیگزنڈر نیولینڈز نے 1865 میں قانون ہشتک (آکٹیو) پیش کیا۔ انہوں نے عناصر کو ان کے بڑھتے ہوئے ایٹمی وزن کے ترتیب میں ترتیب دیا اور نوٹ کیا کہ ہر آٹھواں عنصر پہلے عنصر کی طرح خواص رکھتا ہے (جدول 3.2)۔ تعلق بالکل ایسا تھا جیسے موسیقی کے ہشتک میں ہر آٹھواں سر پہلے سر سے مشابہ ہوتا ہے۔ نیولینڈز کا قانون ہشتک صرف کیلشیم تک کے عناصر کے لیے سچ دکھائی دیا۔ اگرچہ اس وقت ان کا خیال وسیع پیمانے پر قبول نہیں کیا گیا تھا، انہیں ان کے کام کے لیے بعد میں 1887 میں رائل سوسائٹی، لندن کے ذریعے ڈیوی میڈل سے نوازا گیا۔
دوری قانون، جیسا کہ ہم آج جانتے ہیں، اس کی ترقی روسی کیمیا دان، دمیتری مینڈیلیف (1834-1907) اور جرمن کیمیا دان، لوٹھر میئر (1830-1895) کے مرہون منت ہے۔
آزادانہ طور پر کام کرتے ہوئے، دونوں کیمیا دانوں نے 1869 میں تجویز کیا کہ عناصر کو ان کے بڑھتے ہوئے ایٹمی وزن کے ترتیب میں ترتیب دینے پر، باقاعدہ وقفوں پر طبیعی اور کیمیائی خواص میں مماثلتیں ظاہر ہوتی ہیں۔ لوٹھر میئر نے طبیعی خواص جیسے ایٹمی حجم، پگھلنے کا نقطہ اور ابلنے کا نقطہ کو ایٹمی وزن کے خلاف پلاٹ کیا اور ایک دوری طور پر دہرائی جانے والا نمونہ حاصل کیا۔ نیولینڈز کے برعکس، لوٹھر میئر نے اس دہرائے جانے والے نمونے کی لمبائی میں تبدیلی دیکھی۔ 1868 تک، لوٹھر میئر نے عناصر کا ایک جدول تیار کر لیا تھا جو جدید دوری جدول سے قریب سے ملتا جلتا ہے۔ تاہم، ان کا کام دمیتری مینڈیلیف کے کام کے بعد تک شائع نہیں ہوا، جو سائنسدان عام طور پر جدید دوری جدول کی ترقی کا سہرا دیا جاتا ہے۔
جدول 3.2 نیولینڈز کے ہشتک
| عنصر | $\mathbf{L i}$ | $\mathbf{B e}$ | $\mathbf{B}$ | $\mathbf{C}$ | $\mathbf{N}$ | $\mathbf{O}$ | $\mathbf{F}$ |
|---|---|---|---|---|---|---|---|
| ایٹمی وزن | 7 | 9 | 11 | 12 | 14 | 16 | 19 |
| عنصر | $\mathbf{N a}$ | $\mathbf{M g}$ | $\mathbf{A l}$ | $\mathbf{S i}$ | $\mathbf{P}$ | $\mathbf{S}$ | $\mathbf{C l}$ |
| ایٹمی وزن | 23 | 24 | 27 | 29 | 31 | 32 | 35.5 |
| عنصر | $\mathbf{K}$ | $\mathbf{C a}$ | |||||
| ایٹمی وزن | 39 | 40 |
جبکہ ڈوبرائنر نے دوری تعلق کا مطالعہ شروع کیا، یہ مینڈیلیف تھے جو پہلی بار دوری قانون شائع کرنے کے ذمہ دار تھے۔ یہ مندرجہ ذیل بیان کرتا ہے:
عناصر کے خواص ان کے ایٹمی وزنوں کا ایک دوری فعل ہیں۔
مینڈیلیف نے عناصر کو بڑھتے ہوئے ایٹمی وزن کے ترتیب میں ایک جدول کی افقی قطاروں اور عمودی کالموں میں اس طرح ترتیب دیا کہ ایک جیسے خواص رکھنے والے عناصر ایک ہی عمودی کالم یا گروپ میں آئے۔ مینڈیلیف کے عناصر کی درجہ بندی کا نظام لوٹھر میئر کے نظام سے زیادہ تفصیلی تھا۔ انہوں نے دوریت کی اہمیت کو پوری طرح پہچانا اور عناصر کی درجہ بندی کے لیے طبیعی اور کیمیائی خواص کی وسیع رینج استعمال کی۔ خاص طور پر، مینڈیلیف عناصر کے بنائے گئے مرکبات کے تجرباتی فارمولوں اور خواص میں مماثلتوں پر انحصار کرتے تھے۔ انہوں نے محسوس کیا کہ اگر ایٹمی وزن کا ترتیب سختی سے پیروی کیا جائے تو کچھ عناصر ان کی درجہ بندی کے اسکیم میں فٹ نہیں بیٹھتے۔ انہوں نے ایٹمی وزن کے ترتیب کو نظر انداز کر دیا، یہ سوچتے ہوئے کہ ایٹمی پیمائشیں غلط ہو سکتی ہیں، اور ایک جیسے خواص والے عناصر کو اکٹھا رکھا۔ مثال کے طور پر، آیوڈین جو ٹیلوریم (گروپ VI) سے کم ایٹمی وزن رکھتا ہے، خواص میں مماثلتوں کی وجہ سے فلورین، کلورین، برومین کے ساتھ گروپ VII میں رکھا گیا (شکل 3.1)۔ اسی وقت، ایک ہی گروپ میں ایک جیسے خواص والے عناصر کو ترتیب دینے کے اپنے بنیادی مقصد کو برقرار رکھتے ہوئے، انہوں نے تجویز کیا کہ کچھ عناصر ابھی تک نامعلوم تھے اور اس لیے، انہوں نے جدول میں کئی خالی جگہیں چھوڑ دیں۔ مثال کے طور پر، گیلیم اور جرمینیم دونوں اس وقت نامعلوم تھے جب مینڈیلیف نے اپنا دوری جدول شائع کیا۔ انہوں نے ایلومینیم کے نیچے اور سلیکون کے نیچے خالی جگہ چھوڑی، اور ان عناصر کو ایکا-ایلومینیم اور ایکا-سلیکون کہا۔ مینڈیلیف نے نہ صرف گیلیم اور جرمینیم کے وجود کی پیش گوئی کی، بلکہ ان کے کچھ عمومی طبیعی خواص بھی بیان کیے۔ یہ عناصر بعد میں دریافت ہوئے۔ ان عناصر کے لیے مینڈیلیف کی طرف سے پیش گوئی کردہ کچھ خواص اور تجرباتی طور پر پائے گئے خواص کی فہرست جدول 3.3 میں دی گئی ہے۔
مینڈیلیف کی مقداری پیش گوئیوں کی جرات اور ان کی حتمی کامیابی نے انہیں اور ان کے دوری جدول کو مشہور کر دیا۔ مینڈیلیف کا دوری جدول جو 1905 میں شائع ہوا، شکل 3.1 میں دکھایا گیا ہے۔
جدول 3.3 عناصر ایکا-ایلومینیم (گیلیم) اور ایکا-سلیکون (جرمینیم) کے لیے مینڈیلیف کی پیش گوئیاں
| خاصیت | ایکا-ایلومینیم (پیش گوئی) | گیلیم (پایا گیا) | ایکا-سلیکون (پیش گوئی) | جرمینیم (پایا گیا) |
|---|---|---|---|---|
| ایٹمی وزن | 68 | 70 | 72 | 72.6 |
| کثافت/(گرام/سی ایم $\mathbf{)}$ | 5.9 | 5.94 | 5.5 | 5.36 |
| پگھلنے کا نقطہ/K | $\mathrm{Low}$ | 302.93 | $\mathrm{High}$ | 1231 |
| آکسائیڈ کا فارمولا | $\mathrm{E}_2 \mathrm{O}_3$ | $\mathrm{Ga}_2 \mathrm{O}_3$ | $\mathrm{EO}_{2}$ | $\mathrm{GeO}_{2}$ |
| کلورائیڈ کا فارمولا | $\mathrm{E} \mathrm{Cl}_{3}$ | $\mathrm{GaCl}_{3}$ | $\mathrm{ECl}_{4}$ | $\mathrm{GeCl}_{4}$ |
عناصر کا دوری نظام گروپوں اور سیریز میں

شکل 3.1 مینڈیلیف کا دوری جدول جو پہلے شائع ہوا
3.3 جدید دوری قانون اور دوری جدول کی موجودہ شکل
ہمیں ذہن میں رکھنا چاہیے کہ جب مینڈیلیف نے اپنا دوری جدول تیار کیا، تو کیمیا دان ایٹم کی اندرونی ساخت کے بارے میں کچھ نہیں جانتے تھے۔ تاہم، $20^{\text {th }}$ صدی کے آغاز نے ذیلی ایٹمی ذرات کے نظریات میں گہری ترقی دیکھی۔ 1913 میں، انگریز ماہر طبیعیات، ہنری موزلی نے عناصر کی خصوصی $X$-رے سپیکٹرا میں باقاعدگیاں دیکھیں۔ $\sqrt{v}$ (جہاں $V$ $X$-رے کی تعدد ہے) کا ایٹمی نمبر $(Z)$ کے خلاف پلاٹ ایک سیدھی لکیر دیتا ہے نہ کہ $\sqrt{v}$ بمقابلہ ایٹمی کمیت کا پلاٹ۔ اس طرح انہوں نے دکھایا کہ ایٹمی نمبر ایک عنصر کی اس کی ایٹمی کمیت سے زیادہ بنیادی خاصیت ہے۔ مینڈیلیف کے دوری قانون کو، لہذا، اس کے مطابق ترمیم کیا گیا۔ اسے جدید دوری قانون کے نام سے جانا جاتا ہے اور اسے اس طرح بیان کیا جا سکتا ہے:
عناصر کے طبیعی اور کیمیائی خواص ان کے ایٹمی نمبروں کے دوری افعال ہیں۔
دوری قانون نے 94 قدرتی طور پر پائے جانے والے عناصر (نیپٹونیم اور پلوٹونیم ایکٹینیم اور پروٹوایکٹینیم کی طرح پچ بلینڈ - یورینیم کے ایک سنگ معدن میں بھی پائے جاتے ہیں) کے درمیان اہم مماثلتیں ظاہر کیں۔ اس نے غیر نامیاتی کیمیا میں تجدید شدہ دلچسپی کو تحریک دی اور مصنوعی طور پر تیار کردہ مختصر العمر عناصر کی تخلیق کے ساتھ حال تک لے آیا ہے۔
آپ کو یاد ہوگا کہ ایٹمی نمبر نیوکلیائی چارج (یعنی، پروٹون کی تعداد) یا غیر جانبدار ایٹم میں الیکٹران کی تعداد کے برابر ہوتا ہے۔ پھر عناصر کی دوریت میں کوانٹم نمبروں اور الیکٹرانک ترتیبات کی اہمیت کو تصور کرنا آسان ہے۔ درحقیقت، اب یہ تسلیم کیا جاتا ہے کہ دوری قانون بنیادی طور پر الیکٹرانک ترتیبات میں دوری تغیر کا نتیجہ ہے، جو واقعی عناصر اور ان کے مرکبات کے طبیعی اور کیمیائی خواص کا تعین کرتی ہیں۔
وقتاً فوقتاً دوری جدول کی متعدد شکلیں تیار کی گئی ہیں۔ کچھ شکلیں کیمیائی رد عمل اور والینس پر زور دیتی ہیں، جبکہ دوسری عناصر کی الیکٹرانک ترتیب پر زور دیتی ہیں۔ ایک جدید ورژن، جسے عناصر کے دوری جدول کی “طویل شکل” کہا جاتا ہے (شکل 3.2)، سب سے زیادہ آسان اور وسیع پیمانے پر استعمال ہونے والی ہے۔ افقی قطاریں (جنہیں مینڈیلیف نے سیریز کہا) ادوار کہلاتی ہیں اور عمودی کالم، گروپ۔ ایسے عناصر جن کے ایٹموں میں بیرونی الیکٹرانک ترتیب ایک جیسی ہوتی ہے، عمودی کالموں میں ترتیب دیے جاتے ہیں، جنہیں گروپ یا خاندان کہا جاتا ہے۔ انٹرنیشنل یونین آف پیور اینڈ اپلائیڈ کیمسٹری (آئی یو پی اے سی) کی سفارش کے مطابق، گروپوں کو 1 سے 18 تک نمبر دیا گیا ہے، جو گروپوں IA … VIIA, VIII, IB … VIIB اور 0 کی پرانی نوٹیشن کی جگہ لے رہا ہے۔
کل سات ادوار ہیں۔ دور نمبر اس دور میں موجود عناصر کے اعلی ترین پرنسپل کوانٹم نمبر $(n)$ کے مطابق ہوتا ہے۔ پہلے دور میں 2 عناصر ہیں۔ بعد کے ادوار میں بالترتیب $8,8,18,18$ اور 32 عناصر ہوتے ہیں۔ ساتواں دور نامکمل ہے اور چھٹے دور کی طرح نظریاتی طور پر زیادہ سے زیادہ (کوانٹم نمبروں کی بنیاد پر) 32 عناصر ہوں گے۔ دوری جدول کی اس شکل میں، چھٹے اور ساتویں دور دونوں کے 14 عناصر (بالترتیب لیتھنائڈز اور ایکٹینائڈز) نیچے الگ پینلز میں رکھے گئے ہیں[^0]۔
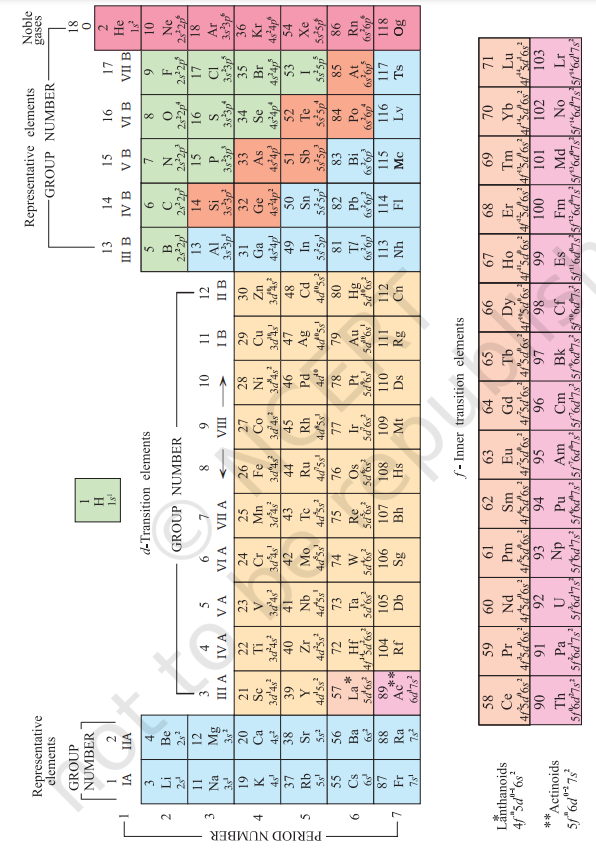
شکل 3.2 عناصر کا دوری جدول کی طویل شکل ان کے ایٹمی نمبروں اور زمینی حالت بیرونی الیکٹرانک ترتیبات کے ساتھ۔ گروپوں کو 1984 کی آئی یو پی اے سی کی سفارشات کے مطابق 1-18 نمبر دیے گئے ہیں۔ یہ نوٹیشن عناصر کے لیے IA–VIIA, VIII, IB–VIIB اور 0 کی پرانی نمبرنگ اسکیم کی جگہ لے رہی ہے۔
3.4 ایٹمی نمبر > 100 والے عناصر کی نامگذاری
نئے عناصر کی نامگذاری روایتی طور پر دریافت کنندہ (یا دریافت کنندگان) کی مراعات رہی ہے اور تجویز کردہ نام کو آئی یو پی اے سی نے توثیق کی۔ حالیہ برسوں میں اس نے کچھ تنازعہ پیدا کیا ہے۔ بہت زیادہ ایٹمی نمبر والے نئے عناصر اتنا غیر مستحکم ہوتے ہیں کہ صرف بہت کم مقدار، کبھی کبھار ان کے صرف چند ایٹم حاصل ہوتے ہیں۔ ان کی ترکیب اور خصوصیات، لہذا، انتہائی جدید مہنگی سامان اور لیبارٹری کی ضرورت ہوتی ہے۔ ایسا کام مسابقتی جذبے کے ساتھ صرف دنیا کی کچھ لیبارٹریز میں کیا جاتا ہے۔ سائنسدان، نئے عنصر پر قابل اعتماد ڈیٹا جمع کرنے سے پہلے، کبھی کبھی اس کی دریافت کا دعویٰ کرنے کے لیے لالچ میں آ جاتے ہیں۔ مثال کے طور پر، امریکی اور سوویت سائنسدانوں دونوں نے عنصر 104 دریافت کرنے کا سہرا لینے کا دعویٰ کیا۔ امریکیوں نے اسے ردرفورڈیم کا نام دیا جبکہ سوویت نے اسے کورچاٹوویم کا نام دیا۔ ایسے مسائل سے بچنے کے لیے، آئی یو پی اے سی نے سفارش کی ہے کہ جب تک کسی نئے عنصر کی دریافت ثابت نہ ہو جائے، اور اس کا نام سرکاری طور پر تسلیم نہ کر لیا جائے، ایک نظامی نامگذاری براہ راست عنصر کے ایٹمی نمبر سے 0 اور نمبروں $1-9$ کے عددی جڑوں کا استعمال کرتے ہوئے اخذ کی جائے۔ یہ جدول 3.4 میں دکھائے گئے ہیں۔ جڑوں کو ایٹمی نمبر بنانے والے ہندسوں کے ترتیب میں اکٹھا کیا جاتا ہے اور آخر میں “یم” لگا دیا جاتا ہے۔ $Z$ سے زیادہ ایٹمی نمبر والے عناصر کے لیے آئی یو پی اے سی کے نام جدول 3.5 میں دکھائے گئے ہیں۔
جدول 3.4 عناصر کی آئی یو پی اے سی نامگذاری کے لیے نوٹیشن
| ہندسہ | نام | مخفف |
|---|---|---|
| 0 | nil | $\mathrm{n}$ |
| 1 | un | $\mathrm{u}$ |
| 2 | bi | $\mathrm{b}$ |
| 3 | tri | $\mathrm{t}$ |
| 4 | quad | $\mathrm{q}$ |
| 5 | pent | $\mathrm{p}$ |
| 6 | hex | $\mathrm{h}$ |
| 7 | sept | $\mathrm{s}$ |
| 8 | oct | $\mathrm{o}$ |
| 9 | enn | $\mathrm{e}$ |
جدول 3.5 ایٹمی نمبر 100 سے زیادہ والے عناصر کی نامگذاری
| ایٹمی نمبر | آئی یو پی اے سی نامگذاری کے مطابق نام | علامت | آئی یو پی اے سی سرکاری نام | آئی یو پی اے سی علامت |
|---|---|---|---|---|
| 101 | Unnilunium | Unu | Mendelevium | $\mathrm{Md}$ |
| 102 | Unnilbium | Unb | Nobelium | No |
| 103 | Unniltrium | Unt | Lawrencium | $\mathrm{Lr}$ |
| 104 | Unnilquadium | Unq | Rutherfordium | $\mathrm{Rf}$ |
| 105 | Unnilpentium | Unp | Dubnium | $\mathrm{Db}$ |
| 106 | Unnilhexium | Unh | Seaborgium | $\mathrm{Sg}$ |
| 107 | Unnilseptium | Uns | Bohrium | $\mathrm{Bh}$ |
| 108 | Unniloctium | Uno | Hassium | $\mathrm{Hs}$ |
| 109 | Unnilennium | Une | Meitnerium | $\mathrm{Mt}$ |
| 110 | Ununnillium | Uun | Darmstadtium | $\mathrm{Ds}$ |
| 111 | Unununnium | Uuu | Rontgenium | $\mathrm{Rg}$ |
| 112 | Ununbium | Uub | Copernicium | $\mathrm{Cn}$ |
| 113 | Ununtrium | Uut | Nihonium | $\mathrm{Nh}$ |
| 114 | Ununquadium | Uuq | Flerovium | $\mathrm{Fl}$ |
| 115 | Ununpentium | Uup | Moscovium | $\mathrm{Mc}$ |
| 116 | Ununhexium | Uuh | Livermorium | $\mathrm{Lv}$ |
| 117 | Ununseptium | Uus | Tennessine | $\mathrm{Ts}$ |
| 118 | Ununoctium | Uuo | Oganesson | $\mathrm{Og}$ |
اس طرح، نئے عنصر کو پہلے ایک عارضی نام ملتا ہے، جس کی علامت تین حروف پر مشتمل ہوتی ہے۔ بعد میں مستقل نام اور علامت ہر ملک کے آئی یو پی اے سی نمائندوں کے ووٹ سے دی جاتی ہے۔ مستقل نام اس ملک (یا ملک کی ریاست) کو ظاہر کر سکتا ہے جس میں عنصر دریافت ہوا، یا کسی قابل ذکر سائنسدان کو خراج تحسین پیش کر سکتا ہے۔ اب تک، ایٹمی نمبر 118 تک کے عناصر دریافت ہو چکے ہیں۔ تمام عناصر کے سرکاری نام آئی یو پی اے سی نے اعلان کر دیے ہیں۔
مسئلہ 3.1
ایٹمی نمبر 120 والے عنصر کے لیے آئی یو پی اے سی نام اور علامت کیا ہوگی؟
حل
جدول 3.4 سے، 1، 2 اور 0 کے لیے جڑیں بالترتیب un، bi اور nil ہیں۔ لہذا، علامت اور نام بالترتیب Ubn اور unbinilium ہیں۔
3.5 عناصر کی الیکٹرانک ترتیبات اور دوری جدول
پچھلے یونٹ میں ہم نے سیکھا ہے کہ ایٹم میں ایک الیکٹران چار کوانٹم نمبروں کے سیٹ کی خصوصیت رکھتا ہے، اور پرنسپل کوانٹم نمبر ( $n$ ) مرکزی توانائی کی سطح کو بیان کرتا ہے جسے شیل کہا جاتا ہے۔ ہم نے مختلف ذیلی شیلوں میں، جنہیں مدار (s, p, $d, f)$ بھی کہا جاتا ہے، میں الیکٹران بھرنے کے بارے میں بھی مطالعہ کیا ہے۔ ایٹم کے مداروں میں الیکٹران کی تقسیم کو اس کی الیکٹرانک ترتیب کہا جاتا ہے۔ دوری جدول میں کسی عنصر کی جگہ آخری بھرے گئے مدار کے کوانٹم نمبروں کو ظاہر کرتی ہے۔ اس حصے میں ہم عناصر کی الیکٹرانک ترتیبات اور دوری جدول کی طویل شکل کے درمیان براہ راست تعلق دیکھیں گے۔
(الف) ادوار میں الیکٹرانک ترتیبات
دور بیرونی یا والینس شیل کے $n$ کی قدر کو ظاہر کرتا ہے۔ دوسرے لفظوں میں، دوری جدول میں متواتر دور اگلی اعلیٰ پرنسپل توانائی کی سطح $(n=1, n=2$، وغیرہ) بھرنے سے وابستہ ہے۔ یہ آسانی سے دیکھا جا سکتا ہے کہ ہر دور میں عناصر کی تعداد دستیاب ایٹمی مداروں کی تعداد سے دوگنی ہے جو توانائی کی سطح میں بھرے جا رہے ہیں۔ پہلا دور $(n=1)$ سب سے کم سطح (1s) بھرنے سے شروع ہوتا ہے اور اس لیے دو عناصر ہوتے ہیں - ہائیڈروجن $\left(1 s^{1}\right)$ اور ہیلیم $\left(1 s^{2}\right)$ جب پہلی شیل $(K)$ مکمل ہو جاتی ہے۔ دوسرا دور $(n=2)$ لیتھیم سے شروع ہوتا ہے اور تیسرا الیکٹران $2 s$ مدار میں داخل ہوتا ہے۔ اگلا عنصر، بیریلیم کے چار الیکٹران ہوتے ہیں اور اس کی الیکٹرانک ترتیب $1 s^{2} 2 s^{2}$ ہوتی ہے۔ اگلے عنصر بورون سے شروع ہو کر، $2 p$ مدار الیکٹران سے بھر جاتے ہیں جب $L$ شیل نیون $\left(2 s^{2} 2 p^{6}\right)$ پر مکمل ہو جاتی ہے۔ اس طرح دوسرے دور میں 8 عناصر ہیں۔ تیسرا دور $(n=3)$ سوڈیم پر شروع ہوتا ہے، اور شامل ہونے والا الیکٹران $3 s$ مدار میں داخل ہوتا ہے۔ $3 s$ اور $3 p$ مداروں کے متواتر بھرنے سے سوڈیم سے آرگون تک 8 عناصر کا تیسرا دور بنتا ہے۔ چوتھا دور $(n=4)$ پوٹاشیم پر شروع ہوتا ہے، اور شامل ہونے والے الیکٹران $4 s$ مدار کو بھرتے ہیں۔ اب آپ نوٹ کر سکتے ہیں کہ $4 p$ مدار بھرنے سے پہلے، $3 d$ مداروں کو بھرنا توانائیاتی طور پر سازگار ہو جاتا ہے اور ہم عناصر کی نام نہاد $3 d$ منتقلی سیریز سے سامنا کرتے ہیں۔ یہ سکینڈیم $(Z=21)$ سے شروع ہوتی ہے جس کی الیکٹرانک ترتیب $3 d^{1} 4 s^{2}$ ہوتی ہے۔ $3 d$ مدار زنک $(Z=30)$ پر الیکٹرانک ترتیب $3 d^{10} 4 s^{2}$ کے ساتھ بھر جاتے ہیں۔ چوتھا دور کریپٹون پر $4 p$ مداروں کے بھرنے کے ساتھ ختم ہوتا ہے۔ اس چوتھے دور میں ہمارے پاس کل 18 عناصر ہیں۔ پانچواں دور $(n=5)$ روبیڈیم سے شروع ہونے والا چوتھے دور کی طرح ہے اور اس میں $4 d$ منتقلی سیریز شامل ہے جو یٹریم $(Z=39)$ سے شروع ہوتی ہے۔ یہ دور زینون پر $5 p$ مداروں کے بھرنے کے ساتھ ختم ہوتا ہے۔ چھٹا دور $(n=6)$ 32 عناصر پر مشتمل ہے اور متواتر الیکٹران $6 s, 4 f, 5 d$ اور $6 p$ مداروں میں داخل ہوتے ہیں، ترتیب میں - $4 f$ مداروں کا بھرنا سیریم $(Z=58)$ سے شروع ہوتا ہے اور لٹیٹیم $(Z=71)$ پر ختم ہوتا ہے تاکہ $4 f$-اندرونی منتقلی سیریز ملے جو لیتھنائڈ سیریز کہلاتی ہے۔ ساتواں دور $(n=7)$ چھٹے دور کی طرح ہے جس میں $7 s, 5 f, 6 d$ اور $7 p$ مداروں کا متواتر بھرنا شامل ہے اور زیادہ تر انسان ساختہ تابکار عناصر شامل ہیں۔ یہ دور ایٹمی نمبر 118 والے عنصر پر ختم ہوگا جو نوبل گیس خاندان سے تعلق رکھے گا۔ ایکٹینیم $(Z=89)$ کے بعد $5 f$ مداروں کا بھرنا $5 f$-اندرونی منتقلی سیریز دیتا ہے جسے ایکٹینائڈ سیریز کہا جاتا ہے۔ $4 f$ اور $5 f$-اندرونی منتقلی سیریز کے عناصر دوری جدول میں اس کی ساخت کو برقرار رکھنے اور ایک جیسے خواص والے عناصر کو ایک ہی کالم میں رکھنے کے اصول کو محفوظ رکھنے کے لیے الگ رکھے گئے ہیں۔
مسئلہ 3.2
آپ دوری جدول کے $5^{\text {th }}$ دور میں 18 عناصر کی موجودگی کو کیسے جواز پیش کریں








