باب 04 کیمیائی بانڈنگ اور سالماتی ساخت
“سائنسدان مسلسل نئے مرکبات دریافت کر رہے ہیں، ان کے بارے میں حقائق کو منظم ترتیب دے رہے ہیں، موجودہ علم سے وضاحت کرنے کی کوشش کر رہے ہیں، پہلے کے خیالات میں ترمیم کے لیے منظم ہو رہے ہیں یا نئے مشاہدہ شدہ حقائق کی وضاحت کے لیے نظریات تشکیل دے رہے ہیں۔”
مادہ ایک یا مختلف قسم کے عناصر سے بنا ہوتا ہے۔ عام حالات میں کوئی دوسرا عنصر فطری طور پر ایک آزاد ایٹم کے طور پر موجود نہیں ہوتا، سوائے نوبل گیسیز کے۔ تاہم، ایٹموں کا ایک گروہ ایک نوع کے طور پر ایک ساتھ موجود پایا جاتا ہے جس کی خصوصی خصوصیات ہوتی ہیں۔ ایٹموں کے اس گروہ کو سالمہ کہتے ہیں۔ ظاہر ہے کہ کچھ قوت ضرور ہونی چاہیے جو ان تشکیل دینے والے ایٹموں کو سالمات میں ایک ساتھ رکھتی ہو۔ وہ کشش قوت جو مختلف کیمیائی انواع میں مختلف اجزاء (ایٹم، آئن وغیرہ) کو ایک ساتھ رکھتی ہے، کیمیائی بانڈ کہلاتی ہے۔ چونکہ کیمیائی مرکبات کی تشکیل مختلف طریقوں سے مختلف عناصر کے ایٹموں کے ملاپ کے نتیجے میں ہوتی ہے، اس لیے یہ بہت سے سوالات پیدا کرتی ہے۔ ایٹم کیوں ملتے ہیں؟ صرف کچھ مخصوص ملاپ کیوں ممکن ہیں؟ کچھ ایٹم کیوں ملتے ہیں جبکہ کچھ دوسرے نہیں ملتے؟ سالمات کی مخصوص شکلیں کیوں ہوتی ہیں؟ ایسے سوالات کے جواب دینے کے لیے وقتاً فوقتاً مختلف نظریات اور تصورات پیش کیے گئے ہیں۔ یہ ہیں: کوسل-لیوس نقطہ نظر، ویلینس شیل الیکٹران جوڑی دھکیلنے (VSEPR) تھیوری، ویلینس بانڈ (VB) تھیوری اور مالیکیولر اوربیٹل (MO) تھیوری۔ ویلینس کے مختلف نظریات کی ارتقاء اور کیمیائی بانڈز کی نوعیت کی تشریح ایٹم کی ساخت، عناصر کی الیکٹرانک ترتیب اور دوری جدول کی سمجھ میں ترقی کے ساتھ قریب سے وابستہ رہی ہے۔ ہر نظام زیادہ مستحکم ہونے کی کوشش کرتا ہے اور بانڈنگ نظام کی توانائی کو کم کرکے استحکام حاصل کرنے کا فطرت کا طریقہ ہے۔
4.1 کیمیائی بانڈنگ کے لیے کوسل-لیوس نقطہ نظر
الیکٹران کے لحاظ سے کیمیائی بانڈ کی تشکیل کی وضاحت کرنے کے لیے کئی کوششیں کی گئیں، لیکن یہ صرف 1916 میں ہوا جب کوسل اور لیوس آزادانہ طور پر ایک تسلی بخش وضاحت دینے میں کامیاب ہوئے۔ وہ ویلینس کی کچھ منطقی وضاحت فراہم کرنے والے پہلے تھے جو نوبل گیسیز کی غیر فعالیت پر مبنی تھی۔
لیوس نے ایٹم کو مثبت چارج شدہ ‘کرنل’ (مرکزہ اور اندرونی الیکٹران) اور بیرونی خول کے لحاظ سے تصور کیا جو زیادہ سے زیادہ آٹھ الیکٹران گھر سکتا ہے۔ اس نے مزید فرض کیا کہ یہ آٹھ الیکٹران ایک کیوب کے کونوں پر قبضہ کرتے ہیں جو ‘کرنل’ کو گھیرے ہوئے ہیں۔ اس طرح سوڈیم کا ایک بیرونی خول والا الیکٹران کیوب کے ایک کونے پر قبضہ کرے گا، جبکہ نوبل گیس کی صورت میں تمام آٹھ کونے قبضہ میں ہوں گے۔ الیکٹران کا یہ آکٹیٹ، ایک خاص طور پر مستحکم الیکٹرانک ترتیب کی نمائندگی کرتا ہے۔ لیوس نے مفروضہ پیش کیا کہ ایٹم مستحکم آکٹیٹ حاصل کرتے ہیں جب وہ کیمیائی بانڈز سے جڑے ہوتے ہیں۔ سوڈیم اور کلورین کی صورت میں، یہ سوڈیم سے کلورین میں ایک الیکٹران کی منتقلی کے ذریعے ہو سکتا ہے جس کے نتیجے میں $\mathrm{Na}^+$ اور $\mathrm{Cl}^{-}$ آئن ملتے ہیں۔ دوسرے سالمات جیسے $ \mathrm{Cl}_2, \mathrm{H}_2, \mathrm{~F}_2 $ وغیرہ کی صورت میں، بانڈ ایٹموں کے درمیان الیکٹران کے ایک جوڑے کی اشتراک سے بنتا ہے۔ اس عمل میں ہر ایٹم الیکٹران کے ایک مستحکم بیرونی آکٹیٹ کو حاصل کرتا ہے۔
لیوس علامات: ایک سالمہ کی تشکیل میں، صرف بیرونی خول کے الیکٹران کیمیائی ملاپ میں حصہ لیتے ہیں اور انہیں ویلینس الیکٹران کہا جاتا ہے۔ اندرونی خول کے الیکٹران اچھی طرح محفوظ ہوتے ہیں اور عام طور پر ملاپ کے عمل میں شامل نہیں ہوتے۔ جی این لیوس، ایک امریکی کیمیا دان نے ایک ایٹم میں ویلینس الیکٹران کی نمائندگی کے لیے سادہ علامات متعارف کرائیں۔ ان علامات کو لیوس علامات کہا جاتا ہے۔ مثال کے طور پر، دوسرے دور کے عناصر کے لیے لیوس علامات درج ذیل ہیں:

لیوس علامات کی اہمیت: علامت کے اردو گرد نقطوں کی تعداد ویلینس الیکٹران کی تعداد کی نمائندگی کرتی ہے۔ ویلینس الیکٹران کی یہ تعداد عنصر کی عام یا گروپ ویلینس کے حساب میں مدد کرتی ہے۔ عناصر کی گروپ ویلینس عام طور پر یا تو لیوس علامات میں نقطوں کی تعداد کے برابر ہوتی ہے یا 8 مائنس نقطوں یا ویلینس الیکٹران کی تعداد۔
کوسل نے، کیمیائی بانڈنگ کے تعلق سے، درج ذیل حقائق کی طرف توجہ دلائی:
- دوری جدول میں، انتہائی برقی منفی ہیلوجنز اور انتہائی برقی مثبت الکلی دھاتیں نوبل گیسیز سے الگ ہیں؛
- ہیلوجن ایٹم سے منفی آئن اور الکلی دھات کے ایٹم سے مثبت آئن کی تشکیل متعلقہ ایٹموں کے ذریعے ایک الیکٹران کے حصول اور نقصان سے وابستہ ہے؛
- اس طرح بننے والے منفی اور مثبت آئن مستحکم نوبل گیس الیکٹرانک ترتیبات حاصل کرتے ہیں۔ نوبل گیسیز (ہیلیم کے مستثنیٰ جس کے الیکٹران کا جوڑا ہوتا ہے) میں آٹھ (آکٹیٹ) الیکٹران کی ایک خاص طور پر مستحکم بیرونی خول ترتیب ہوتی ہے، $n s^{2} n p^{6}$۔
- منفی اور مثبت آئن برقی ساکن کشش سے مستحکم ہوتے ہیں۔
مثال کے طور پر، سوڈیم اور کلورین سے $\mathrm{NaCl}$ کی تشکیل، مذکورہ بالا اسکیم کے مطابق، اس طرح بیان کی جا سکتی ہے:
| $\mathrm{Na}$ | $\rightarrow$ | $\mathrm{Na}^{+}+\mathrm{e}^{-}$ |
| $[\mathrm{Ne}] 3 \mathrm{~s}^{1}$ | $[\mathrm{Ne}]$ | |
| $\mathrm{Cl}+\mathrm{e}^{-}$ | $\rightarrow$ | $\mathrm{Cl}^{-}$ |
| $[\mathrm{Ne}] 3 s^{2} 3 p^{5}$ | $[\mathrm{Ne}] 3 s^{2} 3 p^{6}$ یا $[\mathrm{Ar}]$ | |
| $\mathrm{Na}^{+}+\mathrm{Cl}^{-}$ | $\rightarrow$ | $\mathrm{NaCl}$ یا $\mathrm{Na}^{+} \mathrm{Cl}^{-}$ |
اسی طرح $\mathrm{CaF}_{2}$ کی تشکیل اس طرح دکھائی جا سکتی ہے:
| $\mathrm{Ca}$ | $\rightarrow$ | $\mathrm{Ca}^{2+}+2 \mathrm{e}^{-}$ |
| $[\mathrm{Ar}] 4 s^{2}$ | $[\mathrm{Ar}]$ | |
| $\mathrm{F}+\mathrm{e}^{-}$ | $\rightarrow$ | $\mathrm{F}^{-}$ |
| $[\mathrm{He}] 2 s^{2} 2 p^{5}$ | $[\mathrm{He}] 2 s^{2} 2 p^{6}$ یا $[\mathrm{Ne}]$ | |
| $\mathrm{Ca}^{2+}+2 \mathrm{~F}^{-}$ | $\rightarrow$ | $\mathrm{CaF}_2$ یا $\mathrm{Ca}^{2+}\left(\mathrm{F}^{-}\right)_2$ |
مثبت اور منفی آئنوں کے درمیان برقی ساکن کشش کے نتیجے میں بننے والے بانڈ کو برقی بانڈ کہا گیا۔ اس طرح برقی ویلینس آئن پر یونٹ چارج(ز) کی تعداد کے برابر ہوتی ہے۔ اس طرح، کیلشیم کو دو کی مثبت برقی ویلینس دی جاتی ہے، جبکہ کلورین کو ایک کی منفی برقی ویلینس دی جاتی ہے۔
کوسل کے مفروضے الیکٹران کی منتقلی کے ذریعے آئن کی تشکیل اور آئنک کرسٹلین مرکبات کی تشکیل کے بارے میں جدید تصورات کی بنیاد فراہم کرتے ہیں۔ آئنک مرکبات کی سمجھ اور نظام سازی میں ان کے خیالات بہت اہم ثابت ہوئے ہیں۔ ساتھ ہی انہوں نے اس حقیقت کو تسلیم کیا کہ بڑی تعداد میں مرکبات ان تصورات میں فٹ نہیں ہوتے۔
4.1.1 آکٹیٹ قاعدہ
کوسل اور لیوس نے 1916 میں ایٹموں کے درمیان کیمیائی ملاپ کا ایک اہم نظریہ تیار کیا جسے کیمیائی بانڈنگ کی الیکٹرانک تھیوری کے نام سے جانا جاتا ہے۔ اس کے مطابق، ایٹم یا تو ویلینس الیکٹران کے ایک ایٹم سے دوسرے ایٹم میں منتقلی (حاصل کرنے یا کھونے) کے ذریعے یا ویلینس الیکٹران کی اشتراک کے ذریعے مل سکتے ہیں تاکہ ان کے ویلینس خولوں میں ایک آکٹیٹ ہو۔ اسے آکٹیٹ قاعدہ کہا جاتا ہے۔
4.1.2 کوویلنٹ بانڈ
لینگمائر (1919) نے آکٹیٹ کی ساکن کیوبیکل ترتیب کے خیال کو ترک کرکے اور کوویلنٹ بانڈ کی اصطلاح متعارف کروا کر لیوس کے مفروضوں کو بہتر کیا۔ لیوس-لینگمائر تھیوری کو کلورین سالمہ، $\mathrm{Cl}_2$ کی تشکیل پر غور کرکے سمجھا جا سکتا ہے۔ $\mathrm{Cl}$ ایٹم الیکٹرانک ترتیب، $[\mathrm{Ne}] 3 s^2 3 p^5$ کے ساتھ، آرگون ترتیب سے ایک الیکٹران کم ہے۔ $\mathrm{Cl}_2$ سالمہ کی تشکیل کو دو کلورین ایٹموں کے درمیان الیکٹران کے ایک جوڑے کی اشتراک کے لحاظ سے سمجھا جا سکتا ہے، ہر کلورین ایٹم مشترکہ جوڑے میں ایک الیکٹران کا حصہ ڈالتا ہے۔ اس عمل میں دونوں کلورین ایٹم قریب ترین نوبل گیس (یعنی آرگون) کے بیرونی خول آکٹیٹ کو حاصل کرتے ہیں۔

دو Cl ایٹموں کے درمیان کوویلنٹ بانڈ
نقطے الیکٹران کی نمائندگی کرتے ہیں۔ ایسی ساختوں کو لیوس ڈاٹ ڈھانچے کہا جاتا ہے۔
لیوس ڈاٹ ڈھانچے دوسرے سالمات کے لیے بھی لکھے جا سکتے ہیں، جن میں ملنے والے ایٹم یکساں یا مختلف ہو سکتے ہیں۔ اہم شرائط یہ ہیں کہ:
- ہر بانڈ ایٹموں کے درمیان الیکٹران کے ایک جوڑے کی اشتراک کے نتیجے میں بنتا ہے۔
- ہر ملنے والا ایٹم مشترکہ جوڑے میں کم از کم ایک الیکٹران کا حصہ ڈالتا ہے۔
- الیکٹران کی اشتراک کے نتیجے میں ملنے والے ایٹم بیرونی خول نوبل گیس ترتیبات حاصل کرتے ہیں۔
- اس طرح پانی اور کاربن ٹیٹرا کلورائیڈ سالمات میں، کوویلنٹ بانڈز کی تشکیل اس طرح ظاہر کی جا سکتی ہے:

اس طرح، جب دو ایٹم ایک الیکٹران جوڑا اشتراک کرتے ہیں تو کہا جاتا ہے کہ وہ ایک سنگل کوویلنٹ بانڈ سے جڑے ہیں۔ بہت سے مرکبات میں ہمارے پاس ایٹموں کے درمیان ملٹی پل بانڈز ہوتے ہیں۔ ملٹی پل بانڈز کی تشکیل دو ایٹموں کے درمیان ایک سے زیادہ الیکٹران جوڑے کی اشتراک کا تصور دیتی ہے۔ اگر دو ایٹم الیکٹران کے دو جوڑے اشتراک کرتے ہیں، تو ان کے درمیان کوویلنٹ بانڈ کو ڈبل بانڈ کہا جاتا ہے۔ مثال کے طور پر، کاربن ڈائی آکسائیڈ سالمہ میں، ہمارے پاس کاربن اور آکسیجن ایٹموں کے درمیان دو ڈبل بانڈز ہیں۔ اسی طرح ایتھین سالمہ میں دو کاربن ایٹم ایک ڈبل بانڈ سے جڑے ہوتے ہیں۔

$\mathrm{C} _{2} \mathrm{H} _{4}$ سالمہ
جب ملنے والے ایٹم تین الیکٹران جوڑے اشتراک کرتے ہیں جیسا کہ $N_{2}$ سالمہ میں دو نائٹروجن ایٹموں اور ایتھائن سالمہ میں دو کاربن ایٹموں کی صورت میں، ایک ٹرپل بانڈ بنتا ہے۔
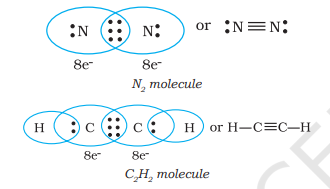
4.1.3 سادہ سالمات کی لیوس نمائندگی (لیوس ڈھانچے)
لیوس ڈاٹ ڈھانچے سالمات اور آئنوں میں بانڈنگ کی تصویر فراہم کرتے ہیں الیکٹران کے مشترکہ جوڑوں اور آکٹیٹ قاعدے کے لحاظ سے۔ اگرچہ ایسی تصویر سالمہ کی بانڈنگ اور رویے کی مکمل وضاحت نہیں کر سکتی، یہ بڑی حد تک سالمہ کی تشکیل اور خصوصیات کو سمجھنے میں مدد کرتی ہے۔ سالمات کے لیوس ڈاٹ ڈھانچے لکھنا، اس لیے، بہت مفید ہے۔ لیوس ڈاٹ ڈھانچے درج ذیل مراحل اپنا کر لکھے جا سکتے ہیں:
- ڈھانچے لکھنے کے لیے درکار الیکٹران کی کل تعداد ملنے والے ایٹموں کے ویلینس الیکٹران کو جوڑ کر حاصل کی جاتی ہے۔ مثال کے طور پر، $\mathrm{CH}_{4}$ سالمہ میں بانڈنگ کے لیے آٹھ ویلینس الیکٹران دستیاب ہیں (کاربن سے 4 اور چار ہائیڈروجن ایٹموں سے 4)۔
- منفی آئنوں کے لیے، ہر منفی چارج کا مطلب ایک الیکٹران کا اضافہ ہوگا۔ مثبت آئنوں کے لیے، ہر مثبت چارج کے نتیجے میں ویلینس الیکٹران کی کل تعداد سے ایک الیکٹران کی تفریق ہوگی۔ مثال کے طور پر، $CO_3^{2-}$ آئن کے لیے، دو منفی چارجز ظاہر کرتے ہیں کہ غیر جانبدار ایٹموں کے ذریعے فراہم کردہ الیکٹران سے دو اضافی الیکٹران ہیں۔ $\mathrm{NH}_{4}^{+}$ آئن کے لیے، ایک مثبت چارج غیر جانبدار ایٹموں کے گروپ سے ایک الیکٹران کے نقصان کی نشاندہی کرتا ہے۔
- ملنے والے ایٹموں کے کیمیائی علامات کو جاننا اور مرکب (معلوم یا ذہانت سے اندازہ لگایا گیا) کی اسکیلیٹل ساخت کا علم ہونا، کل بانڈز کے تناسب میں ایٹموں کے درمیان بانڈنگ مشترکہ جوڑوں کے طور پر الیکٹران کی کل تعداد تقسیم کرنا آسان ہے۔
- عام طور پر سب سے کم برقی منفی ایٹم سالمہ/آئن میں مرکزی مقام پر ہوتا ہے۔ مثال کے طور پر $\mathrm{NF}_3$ اور $CO_3^{2-}$ میں، نائٹروجن اور کاربن مرکزی ایٹم ہیں جبکہ فلورین اور آکسیجن آخری مقامات پر ہیں۔
- سنگل بانڈز کے لیے الیکٹران کے مشترکہ جوڑوں کا حساب لگانے کے بعد، باقی الیکٹران جوڑے یا تو ملٹی پل بانڈنگ کے لیے استعمال ہوتے ہیں یا تنہا جوڑوں کے طور پر رہ جاتے ہیں۔ بنیادی ضرورت یہ ہے کہ ہر بانڈ شدہ ایٹم کو الیکٹران کا آکٹیٹ مل جائے۔
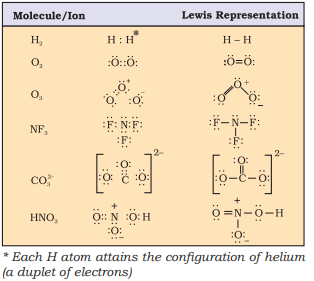
کچھ سالمات/آئنوں کی لیوس نمائندگی جدول 4.1 میں دی گئی ہے۔
جدول 4.1 کچھ سالمات کی لیوس نمائندگی
مسئلہ 4.1
$\mathrm{CO}$ سالمہ کا لیوس ڈاٹ ڈھانچہ لکھیں۔
حل
مرحلہ 1. کاربن اور آکسیجن ایٹموں کے ویلینس الیکٹران کی کل تعداد گنیں۔ کاربن اور آکسیجن ایٹموں کی بیرونی (ویلینس) خول ترتیبات ہیں: $2 s^{2} 2 p^{2}$ اور $2 s^{2} 2 p^{4}$، بالترتیب۔ دستیاب ویلینس الیکٹران $4+6=10$ ہیں۔
مرحلہ 2. $\mathrm{CO}$ کی اسکیلیٹل ساخت اس طرح لکھی گئی ہے: C O
مرحلہ 3. $\mathrm{C}$ اور $\mathrm{O}$ کے درمیان ایک سنگل بانڈ (ایک مشترکہ الیکٹران جوڑا) بنائیں اور $\mathrm{O}$ پر آکٹیٹ مکمل کریں، باقی دو الیکٹران $\mathrm{C}$ پر تنہا جوڑے ہیں۔
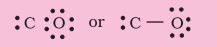
یہ کاربن پر آکٹیٹ مکمل نہیں کرتا اور اس لیے ہمیں $\mathrm{C}$ اور $\mathrm{O}$ ایٹموں کے درمیان ملٹی پل بانڈنگ (اس صورت میں ایک ٹرپل بانڈ) کا سہارا لینا پڑتا ہے۔ یہ دونوں ایٹموں کے لیے آکٹیٹ قاعدے کی شرط کو پورا کرتا ہے۔
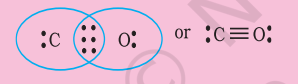
مسئلہ 4.2
نائٹرائٹ آئن، $\mathrm{NO}_{2}^{-}$ کا لیوس ڈھانچہ لکھیں۔
حل
مرحلہ 1. نائٹروجن ایٹم، آکسیجن ایٹموں اور اضافی ایک منفی چارج (ایک الیکٹران کے برابر) کے ویلینس الیکٹران کی کل تعداد گنیں۔
$$ \begin{aligned} & \mathrm{N}\left(2 s^{2} 2 p^{3}\right), \mathrm{O}\left(2 s^{2} 2 p^{4}\right) \\ & 5+(2 \times 6)+ = 17 \text { electrons } \end{aligned} $$
یونٹ منفی چارج کے لیے ایک الیکٹران جمع ہونے پر الیکٹران کی کل تعداد = 17+1 = 18
مرحلہ 2. $\mathrm{NO}_{2}^{-}$ کی اسکیلیٹل ساخت اس طرح لکھی گئی ہے: $\mathrm{O} \quad \mathrm{N} \mathrm{O}$
مرحلہ 3. نائٹروجن اور ہر آکسیجن ایٹم کے درمیان ایک سنگل بانڈ (ایک مشترکہ الیکٹران جوڑا) بنائیں آکسیجن ایٹموں پر آکٹیٹ مکمل کریں۔ تاہم، اگر باقی دو الیکٹران اس پر تنہا جوڑے کی تشکیل دیتے ہیں تو یہ نائٹروجن پر آکٹیٹ مکمل نہیں کرتا۔

لہذا ہمیں نائٹروجن اور ایک آکسیجن ایٹم کے درمیان ملٹی پل بانڈنگ (اس صورت میں ایک ڈبل بانڈ) کا سہارا لینا پڑتا ہے۔ اس سے درج ذیل لیوس ڈاٹ ڈھانچے بنتے ہیں۔
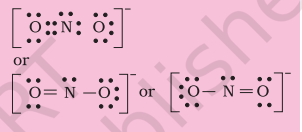
4.1.4 رسمی چارج
لیوس ڈاٹ ڈھانچے، عام طور پر، سالمات کی اصل شکلوں کی نمائندگی نہیں کرتے۔ پولی ایٹومک آئنوں کی صورت میں، خالص چارج آئن کے پاس مجموعی طور پر ہوتا ہے نہ کہ کسی خاص ایٹم کے پاس۔ تاہم، ہر ایٹم پر ایک رسمی چارج تفویض کرنا ممکن ہے۔ پولی ایٹومک سالمہ یا آئن میں کسی ایٹم کا رسمی چارج اس طرح بیان کیا جا سکتا ہے کہ وہ الگ تھلگ یا آزاد حالت میں اس ایٹم کے ویلینس الیکٹران کی تعداد اور لیوس ڈھانچے میں اس ایٹم کو تفویض کردہ الیکٹران کی تعداد کے درمیان فرق ہے۔ اسے اس طرح ظاہر کیا جاتا ہے:

گنتی اس مفروضے پر مبنی ہے کہ سالمہ میں ایٹم ہر مشترکہ جوڑے کے ایک الیکٹران اور تنہا جوڑے کے دونوں الیکٹران کا مالک ہوتا ہے۔
آئیے اوزون سالمہ $\left(\mathrm{O}_3\right)$ پر غور کریں۔ $\mathrm{O}_3$ کا لیوس ڈھانچہ اس طرح بنایا جا سکتا ہے:
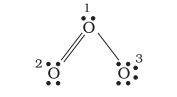
ایٹموں کو 1،2 اور 3 کے طور پر نمبر دیا گیا ہے۔ رسمی چارج:
- مرکزی $\mathrm{O}$ ایٹم نشان زد 1 $=6-2-\frac{1}{2}(6)=+1$
- آخری $\mathrm{O}$ ایٹم نشان زد 2 $=6-4-\frac{1}{2}(4)=0$
- آخری $\mathrm{O}$ ایٹم نشان زد 3 $=6-6-\frac{1}{2}(2)=-1$
لہذا، ہم $\mathrm{O}_{3}$ کو رسمی چارجز کے ساتھ اس طرح ظاہر کرتے ہیں:
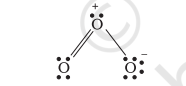
ہمیں یہ سمجھنا چاہیے کہ رسمی چارج سالمہ کے اندر حقیقی چارج علیحدگی کی نشاندہی نہیں کرتے۔ لیوس ڈھانچے میں ایٹموں پر چارجز کی نشاندہی صرف سالمہ میں ویلینس الیکٹران کا حساب رکھنے میں مدد کرتی ہے۔ رسمی چارجز کسی دی گئی نوع کے لیے ممکنہ لیوس ڈھانچوں کی تعداد میں سے کم ترین توانائی والے ڈھانچے کے انتخاب میں مدد کرتے ہیں۔ عام طور پر کم ترین توانائی والا ڈھانچہ وہ ہوتا ہے جس میں ایٹموں پر سب سے چھوٹے رسمی چارجز ہوں۔ رسمی چارج خالص کوویلنٹ نقطہ نظر پر مبنی ایک عنصر ہے جس میں الیکٹران جوڑے ہمسایہ ایٹموں کے درمیان برابر طور پر مشترک ہوتے ہیں۔
4.1.5 آکٹیٹ قاعدے کی حدود
آکٹیٹ قاعدہ، اگرچہ مفید ہے، عالمگیر نہیں ہے۔ یہ زیادہ تر نامیاتی مرکبات کے ڈھانچے کو سمجھنے کے لیے کافی مفید ہے اور یہ بنیادی طور پر دوری جدول کے دوسرے دور کے عناصر پر لاگو ہوتا ہے۔ آکٹیٹ قاعدے کے تین قسم کے استثنیٰ ہیں۔
مرکزی ایٹم کا نامکمل آکٹیٹ
کچھ مرکبات میں، مرکزی ایٹم کے ارد گرد الیکٹران کی تعداد آٹھ سے کم ہوتی ہے۔ یہ خاص طور پر چار سے کم ویلینس الیکٹران رکھنے والے عناصر کے ساتھ معاملہ ہے۔ مثالیں ہیں $\mathrm{LiCl}, \mathrm{BeH}_2$ اور $\mathrm{BCl}_3$۔
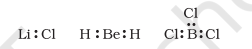
$\mathrm{Li}$، Be اور B کے پاس صرف 1، 2 اور 3 ویلینس الیکٹران ہیں۔ کچھ دوسرے ایسے مرکبات ہیں $\mathrm{AlCl}_3$ اور $\mathrm{BF}_3$۔
طاق الیکٹران والے سالمات
طاق تعداد میں الیکٹران والے سالمات جیسے نائٹرک آکسائیڈ، $\mathrm{NO}$ اور نائٹروجن ڈائی آکسائیڈ، $\mathrm{NO}_2$ میں، آکٹیٹ قاعدہ تمام ایٹموں کے لیے پورا نہیں ہوتا۔
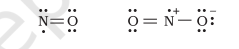
وسیع آکٹیٹ
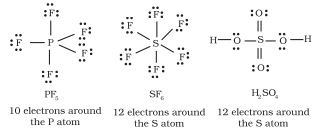
دوری جدول کے تیسرے دور اور اس سے آگے کے عناصر میں، $3 s$ اور $3 p$ اوربیٹلز کے علاوہ، $3 d$ اوربیٹلز بھی بانڈنگ کے لیے دستیاب ہیں۔ ان عناصر کے بہت سے مرکبات میں مرکزی ایٹم کے ارد گرد آٹھ سے زیادہ ویلینس الیکٹران ہوتے ہیں۔ اسے وسیع آکٹیٹ کہا جاتا ہے۔ ظاہر ہے کہ آکٹیٹ قاعدہ ایسی صورتوں میں لاگو نہیں ہوتا۔
ایسے مرکبات کی کچھ مثالیں ہیں: $\mathrm{PF}_5, \mathrm{SF}_6, \mathrm{H}_2 \mathrm{SO}_4$ اور کئی کوآرڈینیشن مرکبات۔
دلچسپ بات یہ ہے کہ سلفر بھی بہت سے مرکبات بناتا ہے جن میں آکٹیٹ قاعدہ پورا ہوتا ہے۔ سلفر ڈائی کلورائیڈ میں، $\mathrm{S}$ ایٹم کے ارد گرد الیکٹران کا آکٹیٹ ہوتا ہے۔
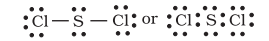
آکٹیٹ تھیوری کے دیگر نقائص
- یہ واضح ہے کہ آکٹیٹ قاعدہ نوبل گیسیز کی کیمیائی غیر فعالیت پر مبنی ہے۔ تاہم، کچھ نوبل گیسیز (مثال کے طور پر زینون اور کرپٹون) بھی آکسیجن اور فلورین کے ساتھ مل کر کئی مرکبات بناتی ہیں جیسے $\mathrm{XeF}_2, \mathrm{KrF}_2, \mathrm{XeOF}_2$ وغیرہ۔
- یہ تھیوری سالمات کی شکل کا حساب نہیں دیتی۔
- یہ سالمات کی نسبتتی استحکام کی وضاحت نہیں کرتی اور سالمہ کی توانائی کے بارے میں مکمل طور پر خاموش ہے۔
4.2 آئنک یا برقی بانڈ
آئنک بانڈ کی تشکیل کے کوسل اور لیوس علاج سے یہ بات سامنے آتی ہے کہ آئنک مرکبات کی تشکیل بنیادی طور پر ان پر منحصر ہوگی:
- متعلقہ غیر جانبدار ایٹموں سے مثبت اور منفی آئنوں کی تشکیل کی آسانی؛
- ٹھوس میں مثبت اور منفی آئنوں کی ترتیب، یعنی کرسٹلین مرکب کی جالی۔
مثبت آئن کی تشکیل میں آئنائزیشن شامل ہے، یعنی غیر جانبدار ایٹم سے الیکٹران(ز) کا ہٹنا اور منفی آئن کی تشکیل میں غیر جانبدار ایٹم میں الیکٹران(ز) کا اضافہ شامل ہے۔
| $\mathrm{M}(\mathrm{g}) $ | $\rightarrow$ | $\mathrm{M}^{+}(\mathrm{g})+\mathrm{e}^{-} ;$ | |
| آئنائزیشن اینتھالپی | |||
| $\mathrm{X}(\mathrm{g})+\mathrm{e}^{-}$ | $\rightarrow$ | $\mathrm{X}^{-}(\mathrm{g}) ;$ | |
| الیکٹران گین اینتھالپی | |||
| $\mathrm{M}^{+}(\mathrm{g})+\mathrm{X}^{-}(\mathrm{g}) \rightarrow$ | $\mathrm{MX}(\mathrm{s})$ |
الیکٹران گین اینتھالپی، $\Delta_{e g} \boldsymbol{H}$، اینتھالپی تبدیلی (یونٹ 3) ہے، جب گیس فیز کا ایٹم اپنی گراؤنڈ اسٹیٹ میں ایک الیکٹران حاصل کرتا ہے۔ الیکٹران گین عمل ایکزو تھرمک یا اینڈو تھرمک ہو سکتا ہے۔ آئنائزیشن، دوسری طرف، ہمیشہ اینڈو تھرمک ہوتی ہے۔ الیکٹران ایفینٹی، الیکٹران گین کے ساتھ ہونے والی توانائی کی تبدیلی کا منفی ہوتا ہے۔
ظاہر ہے کہ آئنک بانڈ نسبتاً کم آئنائزیشن اینتھالپی والے عناصر اور الیکٹران گین اینتھالپی کے نسبتاً زیادہ منفی قدر والے عناصر کے درمیان زیادہ آسانی سے بنیں گے۔
زیادہ تر آئنک مرکبات میں دھاتی عناصر سے ماخوذ مثبت آئن اور غیر دھاتی عناصر سے منفی آئن ہوتے ہیں۔ امونیم آئن، $\mathrm{NH}_{4}^{+}$ (دو غیر دھاتی عناصر سے بنا) ایک استثنیٰ ہے۔ یہ کئی آئنک مرکبات کا مثبت آئن بناتا ہے۔
کرسٹلین حالت میں آئنک مرکبات مثبت اور منفی آئنوں کے منظم تین جہتی ترتیبات پر مشتمل ہوتے ہیں جو کولمبک تعامل توانائیوں سے جڑے ہوتے ہیں۔ یہ مرکبات مختلف کرسٹل ڈھانچوں میں کرسٹلائز ہوتے ہیں جو آئنوں کے سائز، ان کی پیکنگ ترتیبات اور دیگر عوامل سے طے ہوتے ہیں۔ سوڈیم کلورائیڈ، $\mathrm{NaCl}$ (راک سالٹ) کا کرسٹل ڈھانچہ، مثال کے طور پر نیچے دکھایا گیا ہے۔
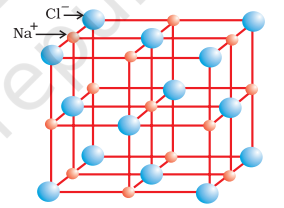
راک سالٹ ڈھانچہ
آئنک ٹھوس میں، الیکٹران گین اینتھالپی اور آئنائزیشن اینتھالپی کا مجموعہ مثبت ہو سکتا ہے لیکن پھر بھی کرسٹل جالی کی تشکیل میں خارج ہونے والی توانائی کی وجہ سے کرسٹل ڈھانچہ مستحکم ہو جاتا ہے۔ مثال کے طور پر: $\mathrm{Na}^{+}(\mathrm{g})$ کی تشکیل کے لیے $\mathrm{Na}(\mathrm{g})$ سے آئنائزیشن اینتھالپی $495.8 \mathrm{~kJ} \mathrm{~mol}^{-1}$ ہے؛ جبکہ تبدیلی $\mathrm{Cl}(\mathrm{g})+\mathrm{e}^{-} \rightarrow$ $\mathrm{Cl}^{-}(\mathrm{g})$ کے لیے الیکٹران گین اینتھالپی، صرف $-348.7 \mathrm{~kJ} \mathrm{~mol}^{-1}$ ہے۔ دونوں کا مجموعہ، $147.1 \mathrm{~kJ} \mathrm{~mol}^{-1}$ $\mathrm{NaCl}(\mathrm{s})\left(-788 \mathrm{~kJ} \mathrm{~mol}^{-1}\right)$ کی جالی کی تشکیل کی اینتھالپی سے زیادہ معاوضہ پاتا ہے۔ لہذا، عمل میں خارج ہون








