باب 08 ریڈاکس تعاملات
“جہاں آکسیکرن ہوتی ہے، وہاں ہمیشہ اِختزال ہوتا ہے۔ کیمیا بنیادی طور پر ریڈاکس نظاموں کا مطالعہ ہے۔”
کیمیا مادے کی مختلف اقسام اور ایک قسم کے مادے کا دوسری قسم میں تبدیلی سے متعلق ہے۔ مادے کا ایک قسم سے دوسری قسم میں تبدیلی مختلف قسم کے تعاملات کے ذریعے ہوتی ہے۔ ایسے تعاملات کی ایک اہم قسم ریڈاکس تعاملات ہیں۔ بہت سے مظاہر، جوہری اور حیاتیاتی دونوں، ریڈاکس تعاملات سے متعلق ہیں۔ یہ تعاملات دوائی سازی، حیاتیاتی، صنعتی، دھات کاری اور زرعی شعبوں میں وسیع پیمانے پر استعمال ہوتے ہیں۔ ان تعاملات کی اہمیت اس حقیقت سے ظاہر ہوتی ہے کہ گھریلو، نقل و حمل اور دیگر تجارتی مقاصد کے لیے توانائی حاصل کرنے کے لیے مختلف قسم کے ایندھن کا جلنا، انتہائی فعال دھاتوں اور غیر دھاتوں کے نکالنے کے لیے برقی کیمیائی عمل، کاسٹک سوڈا جیسے کیمیائی مرکبات کی تیاری، خشک اور تر بیٹریوں کا کام اور دھاتوں کا کٹاؤ ریڈاکس عمل کے دائرہ کار میں آتے ہیں۔ حال ہی میں، ماحولیاتی مسائل جیسے ہائیڈروجن اکانومی (ایندھن کے طور پر مائع ہائیڈروجن کا استعمال) اور ‘اوزون ہول’ کی نشوونما ریڈاکس مظہر کے تحت شمار ہونے لگے ہیں۔
8.1 ریڈاکس تعاملات کا کلاسیکی تصور - آکسیکرن اور اِختزال کے تعاملات
اصل میں، آکسیکرن کی اصطلاح کسی عنصر یا مرکب میں آکسیجن کے اضافے کو بیان کرنے کے لیے استعمال ہوتی تھی۔ فضا میں ڈائی آکسیجن کی موجودگی (20%) کی وجہ سے، بہت سے عناصر اس کے ساتھ مل جاتے ہیں اور یہی بنیادی وجہ ہے کہ وہ عام طور پر زمین پر اپنے آکسائیڈز کی شکل میں پائے جاتے ہیں۔ آکسیکرن کی محدود تعریف کے مطابق درج ذیل تعاملات آکسیکرن کے عمل کی نمائندگی کرتے ہیں:
$$2 \mathrm{Mg}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{MgO}(\mathrm{s}) \tag{8.1}$$
$$\mathrm{S}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow \mathrm{SO_2}(\mathrm{~g}) \tag{8.2}$$
تعاملات (8.1) اور (8.2) میں، میگنیشیم اور گندھک کے عناصر ان میں آکسیجن کے اضافے کی وجہ سے آکسائڈائز ہو جاتے ہیں۔ اسی طرح، میتھین آکسیجن کے اضافے کی وجہ سے آکسائڈائز ہو جاتی ہے۔
$$\mathrm{CH} _{4}(\mathrm{~g})+2 \mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g})+2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{7.3}$$
تعامل (8.3) کا بغور جائزہ، جس میں ہائیڈروجن کو آکسیجن سے بدل دیا گیا ہے، نے کیمیا دانوں کو آکسیکرن کی ازسر نو تشریح اس سے ہائیڈروجن کے ہٹانے کے لحاظ سے کرنے پر مجبور کیا، اور اس لیے، آکسیکرن کی اصطلاح کے دائرہ کار کو کسی مادے سے ہائیڈروجن کے ہٹانے کو شامل کرنے کے لیے وسیع کیا گیا۔ درج ذیل مثال ایک اور تعامل ہے جہاں ہائیڈروجن کا ہٹانا بھی ایک آکسیکرن تعامل کے طور پر پیش کیا جا سکتا ہے۔
$$ \begin{equation*} 2 \mathrm{H_2} \mathrm{~S}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{~S}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \tag{8.4} \end{equation*} $$
جیسے جیسے کیمیا دانوں کا علم بڑھتا گیا، آکسیکرن کی اصطلاح کو (7.1 سے 7.4) جیسے تعاملات کے لیے بڑھانا فطری تھا، جو آکسیجن کو شامل نہیں کرتے بلکہ دیگر برقی منفی عناصر کو شامل کرتے ہیں۔ میگنیشیم کا فلوورین، کلورین اور گندھک وغیرہ کے ساتھ آکسیکرن درج ذیل تعاملات کے مطابق ہوتا ہے:
$$\operatorname{Mg}(\mathrm{s})+\mathrm{F_2} (\mathrm{~g}) \rightarrow \operatorname{MgF_2} (s) \tag{8.5}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{Cl_2} (g) \rightarrow \mathrm{MgCl_2} (s) \tag{8.6}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{S} (s) \rightarrow \operatorname{MgS}(\mathrm{s}) \tag{8.7}$$
تعاملات (7.5 سے 7.7) کو آکسیکرن تعاملات کے دائرے میں شامل کرنے نے کیمیا دانوں کو نہ صرف ہائیڈروجن کے ہٹانے کو آکسیکرن سمجھنے پر اکسایا، بلکہ برقی مثبت عناصر کے ہٹانے کو بھی آکسیکرن سمجھنے پر۔ اس طرح تعامل:
$$ 2 \mathrm{~K_4} \left[ \mathrm{Fe} ( \mathrm{CN})_{6} \right] ( \mathrm{aq}) + \mathrm{H_2} \mathrm{O_2} ( \mathrm{aq}) \rightarrow 2 \mathrm{~K_3} \left[\mathrm{Fe}( \mathrm{CN})_6 \right] ( \mathrm{aq}) + 2 \mathrm{KOH} ( \mathrm{aq}) $$
کو پوٹاشیم فیروسائینائڈ سے برقی مثبت عنصر پوٹاشیم کے ہٹانے کی وجہ سے آکسیکرن کے طور پر تشریح کیا جاتا ہے قبل اس کے کہ یہ پوٹاشیم فیرک سائینائڈ میں تبدیل ہو۔ خلاصہ یہ کہ، “آکسیکرن” کی اصطلاح کو کسی مادے میں آکسیجن/برقی منفی عنصر کے اضافے یا کسی مادے سے ہائیڈروجن/برقی مثبت عنصر کے ہٹانے کے طور پر تعریف کیا جاتا ہے۔
شروع میں، اِختزال کو کسی مرکب سے آکسیجن کے ہٹانے کے طور پر سمجھا جاتا تھا۔ تاہم، اِختزال کی اصطلاح کو آج کل کسی مادے سے آکسیجن/برقی منفی عنصر کے ہٹانے یا کسی مادے میں ہائیڈروجن/برقی مثبت عنصر کے اضافے کو شامل کرنے کے لیے وسیع کیا گیا ہے۔
اوپر دی گئی تعریف کے مطابق، اِختزال کے عمل کی مثالیں درج ذیل ہیں:
$$2 \mathrm{HgO}(\mathrm{s}) \xrightarrow{\Delta} 2 \mathrm{Hg}(\mathrm{l})+\mathrm{O_2}(\mathrm{~g}) \tag{8.8}$$
(مرکورک آکسائیڈ سے آکسیجن کا ہٹانا)
$$2 \mathrm{FeCl_3}(\mathrm{aq})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{FeCl_2}(\mathrm{aq})+2 \mathrm{HCl}(\mathrm{aq}) \tag{8.9}$$
(برقی منفی عنصر، کلورین کا فیرک کلورائیڈ سے ہٹانا)
$$\mathrm{CH_2}=\mathrm{CH_2}(\mathrm{~g})+\mathrm{H_2}(\mathrm{~g}) \rightarrow \mathrm{H_3} \mathrm{C}-\mathrm{CH_3}(\mathrm{~g})\tag{8.10}$$
(ہائیڈروجن کا اضافہ)
$$2 \mathrm{HgCl_2}(\mathrm{aq})+\mathrm{SnCl_2}(\mathrm{aq}) \rightarrow \mathrm{Hg_2} \mathrm{Cl_2}(\mathrm{~s})+\mathrm{SnCl_4}(\mathrm{aq})\tag{8.11}$$
(مرکورک کلورائیڈ میں پارے کا اضافہ)
تعامل (8.11) میں، اسٹینس کلورائیڈ کا اسٹینک کلورائیڈ میں بیک وقت آکسیکرن بھی ہو رہا ہے کیونکہ اس میں برقی منفی عنصر کلورین کا اضافہ ہو رہا ہے۔ جلد ہی یہ احساس ہوا کہ آکسیکرن اور اِختزال ہمیشہ بیک وقت ہوتے ہیں (جیسا کہ اوپر دیے گئے تمام مساواتوں کے دوبارہ جائزے سے ظاہر ہوگا)، اس لیے، کیمیائی تعاملات کی اس قسم کے لیے “ریڈاکس” کا لفظ گڑھا گیا۔
مسئلہ 8.1
نیچے دیے گئے تعاملات میں، آکسائڈائز اور ریڈیوس ہونے والی انواع کی شناخت کریں:
(i) $\mathrm{H_2} \mathrm{~S}$ (g) $+\mathrm{Cl_2}$ (g) $\rightarrow 2 \mathrm{HCl}$ (g) $+\mathrm{S}$ (s)
(ii) $3 \mathrm{Fe_3} \mathrm{O_4}$ (s) $+8 \mathrm{Al}$ (s) $\rightarrow 9 \mathrm{Fe}$ (s) $+4 \mathrm{Al_2} \mathrm{O_3}(\mathrm{~s})$
(iii) $2 \mathrm{Na}$ (s) $+\mathrm{H_2}$ (g) $\rightarrow 2 \mathrm{NaH}$ (s)
حل
(i) $\mathrm{H_2} \mathrm{~S}$ آکسائڈائز ہوتا ہے کیونکہ ہائیڈروجن میں ایک زیادہ برقی منفی عنصر، کلورین کا اضافہ ہوتا ہے (یا ایک زیادہ برقی مثبت عنصر، ہائیڈروجن کو S سے ہٹا دیا جاتا ہے)۔ کلورین ریڈیوس ہوتی ہے کیونکہ اس میں ہائیڈروجن کا اضافہ ہوتا ہے۔
(ii) ایلومینیم آکسائڈائز ہوتا ہے کیونکہ اس میں آکسیجن کا اضافہ ہوتا ہے۔ فیرس فیرک آکسائیڈ $\left(\mathrm{Fe_3} \mathrm{O_4}\right)$ ریڈیوس ہوتا ہے کیونکہ اس سے آکسیجن ہٹا دی جاتی ہے۔
(iii) برقی منفیت کے تصور کے محتاط اطلاق سے ہم صرف یہ نتیجہ نکال سکتے ہیں کہ سوڈیم آکسائڈائز ہوتا ہے اور ہائیڈروجن ریڈیوس ہوتی ہے۔
یہاں منتخب کردہ تعامل (iii) ہمیں ریڈاکس تعاملات کی تعریف کرنے کے دوسرے طریقے کے بارے میں سوچنے پر مجبور کرتا ہے۔
8.2 الیکٹران منتقلی تعاملات کے لحاظ سے ریڈاکس تعاملات
ہم پہلے ہی سیکھ چکے ہیں کہ تعاملات ریڈاکس تعاملات ہیں کیونکہ ان میں سے ہر ایک میں سوڈیم آکسائڈائز ہوتا ہے یا تو آکسیجن کے اضافے کی وجہ سے یا سوڈیم میں زیادہ برقی منفی عنصر کے اضافے کی وجہ سے۔
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaCl}(\mathrm{s})\tag{8.12}$$
$$4 \mathrm{Na}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na_2} \mathrm{O}(\mathrm{s})\tag{8.13}$$
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{S}(\mathrm{s}) \rightarrow \mathrm{Na_2} \mathrm{~S}(\mathrm{~s}) \tag{8.14}$$
بیک وقت، کلورین، آکسیجن اور گندھک ریڈیوس ہوتی ہیں کیونکہ ان میں سے ہر ایک میں برقی مثبت عنصر سوڈیم کا اضافہ ہوا ہے۔ کیمیائی بانڈنگ کے ہمارے علم سے ہم یہ بھی جانتے ہیں کہ سوڈیم کلورائیڈ، سوڈیم آکسائیڈ اور سوڈیم سلفائیڈ آئنک مرکبات ہیں اور شاید بہتر طور پر $\mathrm{Na}^{+} \mathrm{Cl}^{-}( \mathrm{s}),\left(\mathrm{Na}^{+} \right)_2 \mathrm{O}^{2-}( \mathrm{s})$، اور $ \left(\mathrm{Na}^{+} \right)_2$ $\mathrm{S}^{2-}( \mathrm{s})$ کے طور پر لکھے جاتے ہیں۔ پیدا ہونے والی انواع پر چارجز کی نشوونما ہمیں تعاملات (8.12 سے 8.14) کو درج ذیل طریقے سے دوبارہ لکھنے کی ترغیب دیتی ہے:
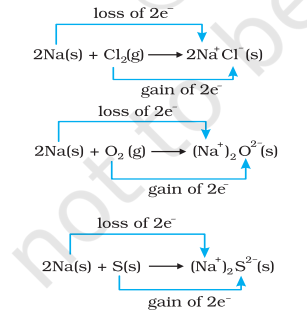
سہولت کے لیے، ان میں سے ہر عمل کو دو الگ الگ مراحل کے طور پر سمجھا جا سکتا ہے، ایک الیکٹران کی کمی اور دوسرا الیکٹران کی حصولی۔ مثال کے طور پر، ہم ان میں سے ایک، یعنی سوڈیم کلورائیڈ کی تشکیل کو مزید تفصیل سے بیان کر سکتے ہیں۔
$2 \mathrm{Na}(\mathrm{s}) \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
$\mathrm{Cl_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{Cl}^{-}(\mathrm{g})$
اوپر کے ہر مرحلے کو نصف تعامل کہا جاتا ہے، جو واضح طور پر الیکٹران کی شمولیت کو ظاہر کرتا ہے۔ نصف تعاملات کا مجموعہ مجموعی تعامل دیتا ہے:
$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na}^{+} \mathrm{Cl}^{-}(\mathrm{s})$ یا $2 \mathrm{NaCl}(\mathrm{s})$
تعاملات 8.12 سے 8.14 بتاتے ہیں کہ الیکٹران کی کمی شامل کرنے والے نصف تعاملات کو آکسیکرن تعاملات کہا جاتا ہے۔ اسی طرح، الیکٹران کی حصولی شامل کرنے والے نصف تعاملات کو اِختزال تعاملات کہا جاتا ہے۔ یہاں یہ ذکر کرنا بے جا نہ ہوگا کہ آکسیکرن اور اِختزال کی تعریف کرنے کا نیا طریقہ صرف کلاسیکی خیال کے مطابق انواع کے رویے اور الیکٹران منتقلی تبدیلی میں ان کی باہمی کارکردگی کے درمیان تعلق قائم کرکے حاصل کیا گیا ہے۔ تعاملات (8.12 سے 8.14) میں سوڈیم، جو آکسائڈائز ہوتا ہے، ایک ریڈیوس ایجنٹ کے طور پر کام کرتا ہے کیونکہ یہ اس کے ساتھ تعامل کرنے والے ہر عنصر کو الیکٹران عطا کرتا ہے اور اس طرح انہیں ریڈیوس کرنے میں مدد کرتا ہے۔ کلورین، آکسیجن اور گندھک ریڈیوس ہوتی ہیں اور آکسائڈائزنگ ایجنٹ کے طور پر کام کرتی ہیں کیونکہ یہ سوڈیم سے الیکٹران قبول کرتی ہیں۔ خلاصہ کرنے کے لیے، ہم ذکر کر سکتے ہیں کہ
آکسیکرن: کسی بھی نوع کی طرف سے الیکٹران(ز) کی کمی۔
اِختزال: کسی بھی نوع کی طرف سے الیکٹران(ز) کی حصولی۔
آکسائڈائزنگ ایجنٹ: الیکٹران(ز) کا قبول کنندہ۔
ریڈیوسنگ ایجنٹ: الیکٹران(ز) کا عطا کنندہ۔
مسئلہ 8.2
ثابت کریں کہ تعامل: $2 \mathrm{Na}(\mathrm{s})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaH}$ (s) ایک ریڈاکس تبدیلی ہے۔
حل
چونکہ اوپر والے تعامل میں بننے والا مرکب ایک آئنک مرکب ہے، جسے $\mathrm{Na}^{+} \mathrm{H}^{-}$(s) کے طور پر بھی ظاہر کیا جا سکتا ہے، یہ بتاتا ہے کہ اس عمل میں ایک نصف تعامل یہ ہے:
$2 \mathrm{Na}(\mathrm{s}) \quad \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
اور دوسرا نصف تعامل یہ ہے:
$\mathrm{H_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{H}^{-}(\mathrm{g})$
جانچ کے تحت تعامل کا دو نصف تعاملات میں تقسیم ہونا خود بخود ظاہر کرتا ہے کہ یہاں سوڈیم آکسائڈائز ہوتا ہے اور ہائیڈروجن ریڈیوس ہوتی ہے، اس لیے، مکمل تعامل ایک ریڈاکس تبدیلی ہے۔
8.2.1 مقابلہ جاتی الیکٹران منتقلی تعاملات
میٹالک زنک کی ایک پٹی کو تانبے کے نائٹریٹ کے آبی محلول میں رکھیں جیسا کہ شکل 8.1 میں دکھایا گیا ہے، تقریباً ایک گھنٹے کے لیے۔ آپ دیکھ سکتے ہیں کہ پٹی سرخ رنگ کی میٹالک تانبے سے ڈھک جاتی ہے اور محلول کا نیلا رنگ غائب ہو جاتا ہے۔ $\mathrm{Zn}^{2+}$ آئنوں کی تشکیل مصنوعات میں سے آسانی سے دیکھی جا سکتی ہے جب $\mathrm{Cu}^{2+}$ کی وجہ سے محلول کا نیلا رنگ غائب ہو جاتا ہے۔ اگر ہائیڈروجن سلفائیڈ گیس کو $\mathrm{Zn}^{2+}$ آئنوں پر مشتمل بے رنگ محلول سے گزارا جائے، تو سفید زنک سلفائیڈ، $\mathrm{ZnS}$ کی ظاہری شکل دیکھی جا سکتی ہے جب محلول کو امونیا سے القلی بنایا جاتا ہے۔
میٹالک زنک اور تانبے کے نائٹریٹ کے آبی محلول کے درمیان تعامل یہ ہے:
$$\mathrm{Zn}(\mathrm{s})+\mathrm{Cu}^{2+}(\mathrm{aq}) \rightarrow \mathrm{Zn}^{2+}(\mathrm{aq})+\mathrm{Cu}(\mathrm{s}) \tag{8.15}$$
تعامل (8.15) میں، زنک نے الیکٹران کھو کر $Zn^{2+}$ بنایا ہے اور، اس لیے، زنک آکسائڈائز ہوتا ہے۔ ظاہر ہے، اب اگر زنک آکسائڈائز ہوتا ہے، الیکٹران چھوڑتا ہے، تو کچھ نہ کچھ ریڈیوس ہونا چاہیے، زنک کے کھوئے ہوئے الیکٹران کو قبول کرتا ہے۔ تانبے کا آئن زنک سے الیکٹران حاصل کرکے ریڈیوس ہوتا ہے۔
تعامل (8.15) کو اس طرح دوبارہ لکھا جا سکتا ہے:
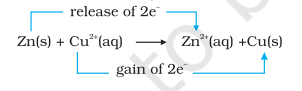
اس مرحلے پر ہم مساوات (8.15) کے ذریعے ظاہر کردہ تعامل کے لیے توازن کی حالت کی تحقیقات کر سکتے ہیں۔ اس مقصد کے لیے، ہم میٹالک تانبے کی ایک پٹی زنک سلفیٹ محلول میں رکھتے ہیں۔ کوئی نظر آنے والا تعامل نظر نہیں آتا اور $\mathrm{Cu}^{2+}$ آئنوں کی موجودگی کا پتہ لگانے کی کوشش، $\mathrm{H_2} \mathrm{~S}$ گیس کو محلول سے گزار کر کیپرک سلفائیڈ، CuS کے سیاہ رنگ کو پیدا کرنے کے لیے، کامیاب نہیں ہوتی۔ کیپرک سلفائیڈ کی اتنی کم حل پزیری ہے کہ یہ ایک انتہائی حساس ٹیسٹ ہے؛ پھر بھی بننے والے $\mathrm{Cu}^{2+}$ کی مقدار کا پتہ نہیں لگایا جا سکتا۔ اس طرح ہم نتیجہ اخذ کرتے ہیں کہ تعامل (8.15) کے لیے توازن کی حالت ری ایکٹنٹس کے مقابلے میں مصنوعات کو بہت زیادہ ترجیح دیتی ہے۔
آئیے اب الیکٹران منتقلی تعامل کو تانبے کی دھات اور سلور نائٹریٹ محلول در آب تک بڑھائیں اور ایک سیٹ اپ ترتیب دیں جیسا کہ شکل 8.2 میں دکھایا گیا ہے۔ محلول $\mathrm{Cu}^{2+}$ آئنوں کی تشکیل کی وجہ سے نیلا رنگ تیار کرتا ہے تعامل کی وجہ سے:
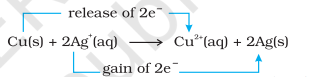
یہاں، $\mathrm{Cu}(\mathrm{s})$ آکسائڈائز ہو کر $\mathrm{Cu}^{2+}(\mathrm{aq})$ بنتا ہے اور $\mathrm{Ag}^{+}(\mathrm{aq})$ ریڈیوس ہو کر $\mathrm{Ag}(\mathrm{s})$ بنتا ہے۔ توازن مصنوعات $\mathrm{Cu}^{2+}(\mathrm{aq})$ اور $\mathrm{Ag}(\mathrm{s})$ کو بہت زیادہ ترجیح دیتا ہے۔
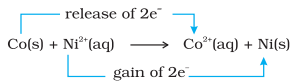
اس کے برعکس، آئیے ہم نکل سلفیٹ محلول میں رکھے گئے میٹالک کوبالٹ کے تعامل کا بھی موازنہ کریں۔ یہاں ہونے والا تعامل یہ ہے:
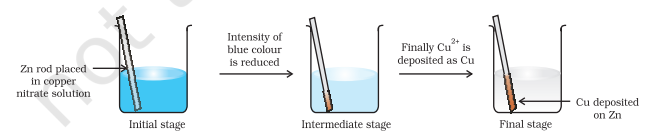
شکل 8.1 زنک اور تانبے کے نائٹریٹ کے آبی محلول کے درمیان ریڈاکس تعامل جو ایک بیکر میں ہو رہا ہے۔
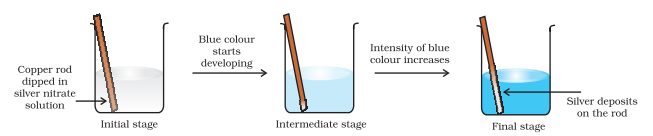
شکل 8.2 تانبے اور سلور نائٹریٹ کے آبی محلول کے درمیان ریڈاکس تعامل جو ایک بیکر میں ہو رہا ہے۔
توازن پر، کیمیائی ٹیسٹ ظاہر کرتے ہیں کہ دونوں $\mathrm{Ni}^{2+}(\mathrm{aq})$ اور $\mathrm{Co}^{2+}(\mathrm{aq})$ معتدل ارتکاز پر موجود ہیں۔ اس صورت میں، نہ تو ری ایکٹنٹس $\left[\mathrm{Co}(\mathrm{s})\right.$ اور $\left.\mathrm{Ni}^{2+}(\mathrm{aq})\right]$ اور نہ ہی مصنوعات $\left[\mathrm{Co}^{2+}(\mathrm{aq})\right.$ اور $\left.\mathrm{Ni}(\mathrm{s})\right]$ کو بہت زیادہ ترجیح حاصل ہے۔
الیکٹران جاری کرنے کے لیے یہ مقابلہ اتفاقاً ہمیں تیزابوں کے درمیان پروٹون جاری کرنے کے مقابلے کی یاد دلاتا ہے۔ یہ مماثلت بتاتی ہے کہ ہم ایک جدول تیار کر سکتے ہیں جس میں دھاتیں اور ان کے آئن ان کے الیکٹران جاری کرنے کے رجحان کی بنیاد پر درج ہوں جیسا کہ ہم تیزابوں کی طاقت بتانے کے لیے تیزابوں کے معاملے میں کرتے ہیں۔ درحقیقت ہم نے پہلے ہی کچھ موازنے کر لیے ہیں۔ موازنے سے ہم نے جانا ہے کہ زنک تانبے کو الیکٹران جاری کرتا ہے اور تانبے سلور کو الیکٹران جاری کرتا ہے اور، اس لیے، دھاتوں کا الیکٹران جاری کرنے کا رجحان ترتیب میں ہے: $\mathrm{Zn}>\mathrm{Cu}>\mathrm{Ag}$۔ ہم اپنی فہرست کو زیادہ وسیع بنانا چاہیں گے اور ایک دھاتی سرگرمی سیریز یا برقی کیمیائی سیریز ڈیزائن کریں گے۔ مختلف دھاتوں کے درمیان الیکٹران کے لیے مقابلہ ہمیں خلیوں کی ایک قسم ڈیزائن کرنے میں مدد کرتا ہے، جسے گیلوانک خلیے کہا جاتا ہے جس میں کیمیائی تعاملات برقی توانائی کا ذریعہ بن جاتے ہیں۔ ہم بارہویں جماعت میں ان خلیوں کے بارے میں مزید پڑھیں گے۔
8.3 آکسیڈیشن نمبر
الیکٹران منتقلی کا ایک کم واضح مثال اس وقت سامنے آتی ہے جب ہائیڈروجن آکسیجن کے ساتھ مل کر پانی بناتی ہے تعامل کے ذریعے:
$$2 \mathrm{H_2}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{H_2} \mathrm{O}(\mathrm{l})\tag{8.18}$$
اگرچہ اس کے نقطہ نظر میں آسان نہیں ہے، پھر بھی ہم $\mathrm{H}$ ایٹم کو $\mathrm{H_2}$ میں غیر جانبدار (صفر) حالت سے $\mathrm{H_2} \mathrm{O}$ میں مثبت حالت میں جاتے ہوئے تصور کر سکتے ہیں، $\mathrm{O}$ ایٹم $\mathrm{O_2}$ میں صفر حالت سے $\mathrm{H_2} \mathrm{O}$ میں دو منفی حالت میں جاتا ہے۔ یہ فرض کیا جاتا ہے کہ $\mathrm{H}$ سے $\mathrm{O}$ تک الیکٹران کی منتقلی ہوتی ہے اور نتیجتاً $\mathrm{H_2}$ آکسائڈائز ہوتا ہے اور $\mathrm{O_2}$ ریڈیوس ہوتا ہے۔
تاہم، جیسا کہ ہم بعد میں دیکھیں گے، چارج منتقلی صرف جزوی ہے اور شاید $\mathrm{H}$ کے ذریعے الیکٹران کی مکمل کمی اور O کے ذریعے حصولی کے بجائے الیکٹران شفٹ کے طور پر بہتر بیان کیا گیا ہے۔ یہاں مساوات (8.18) کے حوالے سے جو کہا گیا ہے وہ شاید کوویلنٹ مرکبات شامل کرنے والے دیگر تعاملات کی ایک اچھی تعداد کے لیے درست ہو سکتا ہے۔ اس قسم کے تعاملات کی دو مثالیں یہ ہیں:
$$\mathrm{H_2}(\mathrm{~s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{HCl}(\mathrm{g})\tag{8.19}$$
اور،
$$\mathrm{CH_4}(\mathrm{~g})+4 \mathrm{Cl_2}(\mathrm{~g}) \rightarrow \mathrm{CCl_4}(\mathrm{l})+4 \mathrm{HCl}(\mathrm{g})\tag{8.20}$$
کوویلنٹ مرکبات کی تشکیل شامل کرنے والے کیمیائی تعاملات میں الیکٹران شفٹ کا حساب رکھنے کے لیے، آکسیڈیشن نمبر استعمال کرنے کا ایک زیادہ عملی طریقہ تیار کیا گیا ہے۔ اس طریقہ کار میں، یہ ہمیشہ فرض کیا جاتا ہے کہ کم برقی منفی ایٹم سے زیادہ برقی منفی ایٹم تک الیکٹران کی مکمل منتقلی ہوتی ہے۔ مثال کے طور پر، ہم مساوات (8.18 سے 8.20) کو دوبارہ لکھتے ہیں تاکہ تعامل کا حصہ بننے والے ہر ایٹم پر چارج دکھایا جا سکے:
$$ \begin{array}{cccc} 2 \stackrel{0}{\mathrm{H_2}}(\mathrm{~g}) + \stackrel{0}{\mathrm{O_2}}(\mathrm{~g}) & \rightarrow & 2 \stackrel{+1}{\mathrm{H_2}} \stackrel{-2}{\mathrm{O}}(\mathrm{l}) \tag{8.21} \end{array} $$
$$ \begin{array}{llll} \stackrel {0}{\mathrm{H_2}}(\mathrm{~s}) + \stackrel{0}{\mathrm{Cl_2}}(\mathrm{~g}) & \rightarrow & 2 \stackrel{+1-1}{\mathrm{HCl}}(\mathrm{g}) \tag{8.22} \end{array} $$
$$ \begin{array}{cccc} \stackrel{-4 +1}{\mathrm{CH_4}}(\mathrm{~g}) + & 4 \stackrel{0}{\mathrm{Cl_2}}(\mathrm{~g}) \rightarrow & \stackrel{+4 -1}{\mathrm{C}\mathrm{Cl_4}} (\mathrm{l})+4 \stackrel{+1 -1 }{\mathrm{H } \mathrm{Cl}} (\mathrm{g})\tag{8.23} \end{array} $$
یہ بات زور دے کر کہی جا سکتی ہے کہ الیکٹران منتقلی کا فرض صرف بک کیپنگ کے مقصد کے لیے کیا گیا ہے اور اس یونٹ میں بعد کے مرحلے پر یہ واضح ہو جائے گا کہ یہ ریڈاکس تعاملات کی سادہ وضاحت کی طرف لے جاتا ہے۔
آکسیڈیشن نمبر کسی مرکب میں کسی عنصر کی آکسیڈیشن حالت کو ظاہر کرتا ہے جو قواعد کے ایک سیٹ کے مطابق معلوم کیا جاتا ہے جو اس بنیاد پر ترتیب دیا گیا ہے کہ کوویلنٹ بانڈ میں الیکٹران جوڑا مکمل طور پر زیادہ برقی منفی عنصر سے تعلق رکھتا ہے۔
یہ ہمیشہ ممکن نہیں ہوتا کہ کسی مرکب/آئن میں آسانی سے یاد رکھیں یا معلوم کریں کہ کون سا عنصر دوسرے سے زیادہ برقی منفی ہے۔ اس لیے، کسی مرکب/آئن میں کسی عنصر کا آکسیڈیشن نمبر معلوم کرنے کے لیے قواعد کا ایک سیٹ ترتیب دیا گیا ہے۔ اگر کسی عنصر کے دو یا دو سے زیادہ ایٹم مالیکیول/آئن میں موجود ہوں جیسے $\mathrm{Na_2} \mathrm{~S_2} \mathrm{O_3} / \mathrm{Cr_2} \mathrm{O_7}^{2-}$، تو اس عنصر کے ایٹم کا آکسیڈیشن نمبر اس عنصر کے تمام ایٹمز کے آکسیڈیشن نمبر کا اوسط ہوگا۔ ہم اس مرحلے پر، آکسیڈیشن نمبر کے حساب کے لیے قواعد بیان کر سکتے ہیں۔ یہ قواعد ہیں:
1. عناصر میں، آزاد یا غیر ملحق حالت میں، ہر ایٹم کا آکسیڈیشن نمبر صفر ہوتا ہے۔ ظاہر ہے $\mathrm{H_2}, \mathrm{O_2}, \mathrm{Cl_2}, \mathrm{O_3}, \mathrm{P_4}, \mathrm{~S_8}, \mathrm{Na}, \mathrm{Mg}, \mathrm{Al}$ میں ہر ایٹم کا آکسیڈیشن نمبر صفر ہے۔
2. صرف ایک ایٹم پر مشتمل آئنوں کے لیے، آکسیڈیشن نمبر آئن پر چارج کے برابر ہوتا ہے۔ اس طرح $\mathrm{Na}^{+}$ آئن کا آکسیڈیشن نمبر $+1, \mathrm{Mg}^{2+}$ آئن، $+2, \mathrm{Fe}^{3+}$ آئن، +3، $\mathrm{Cl}^{-}$ آئن، $-1, \mathrm{O}^{2-}$ آئن، -2؛ اور اسی طرح۔ ان کے مرکبات میں تمام الکلی دھاتوں کا آکسیڈیشن نمبر +1 ہوتا ہے، اور تمام الکالائن ارتھ دھاتوں کا آکسیڈیشن نمبر +2 ہوتا ہے۔ ایلومینیم کو اس کے تمام مرکبات میں +3 کا آکسیڈیشن نمبر رکھنے والا سمجھا جاتا ہے۔
3. زیادہ تر مرکبات میں آکسیجن کا آکسیڈیشن نمبر -2 ہوتا ہے۔ تاہم، ہم یہاں دو قسم کے استثناء سے دوچار ہوتے ہیں۔ ایک پیرآکسائیڈز اور سپرآکسائیڈز کے معاملے میں پیدا ہوتا ہے، آکسیجن کے وہ مرکبات جن میں آکسیجن کے ایٹم براہ راست ایک دوسرے سے جڑے ہوتے ہیں۔ جبکہ پیرآکسائیڈز (مثلاً، $\mathrm{H_2} \mathrm{O_2}$، $\mathrm{Na_2} \mathrm{O_2}$) میں، ہر آکسیجن ایٹم کو -1 کا آکسیڈیشن نمبر تفویض کیا جاتا ہے، سپرآکسائیڈز (مثلاً، $\mathrm{KO_2}, \mathrm{RbO_2}$) میں ہر آکسیجن ایٹم کو $-(1 / 2)$ کا آکسیڈیشن نمبر تفویض کیا جاتا ہے۔ دوسرا استثناء شاذ و نادر ہی ظاہر ہوتا ہے، یعنی جب آکسیجن فلوورین سے بندھی ہوتی ہے۔ ایسے مرکبات میں مثلاً، آکسیجن ڈائی فلوورائیڈ $\left(\mathrm{OF_2}\right)$ اور ڈائی آکسیجن ڈائی فلوورائیڈ $\left(\mathrm{O_2} \mathrm{~F_2}\right)$، آکسیجن کو بالترتیب +2 اور +1 کا آکسیڈیشن نمبر تفویض کیا جاتا ہے۔ آکسیجن کو تفویض کردہ نمبر آکسیجن کی بانڈنگ حالت پر منحصر ہوگا لیکن یہ نمبر اب صرف ایک مثبت عدد ہوگا۔
4. ہائیڈروجن کا آکسیڈیشن نمبر +1 ہوتا ہے، سوائے اس کے کہ جب یہ بائنری مرکبات (یعنی دو عناصر پر مشتمل مرکبات) میں دھاتوں سے بندھا ہو۔ مثال کے طور پر، $\mathrm{LiH}, \mathrm{NaH}$، اور $\mathrm{CaH_2}$ میں، اس کا آکسیڈیشن نمبر -1 ہے۔
5. اس کے تمام مرکبات میں، فلوورین کا آکسیڈیشن نمبر -1 ہوتا ہے۔ دیگر ہیلوجنز ($(\mathrm{Cl}$، $\mathrm{Br}$، اور I) کا بھی آکسیڈیشن نمبر -1 ہوتا ہے، جب وہ اپنے مرکبات میں ہیلائیڈ آئنوں کے طور پر موجود ہوں۔ کلورین، برومین اور آیوڈین جب آکسیجن کے ساتھ ملتے ہیں، مثال کے طور پر آکسیو ایسڈز اور آکسیو اینیونز میں، مثبت آکسیڈیشن نمبر رکھتے ہیں۔
6. کسی مرکب میں تمام ایٹمز کے آکسیڈیشن نمبر کا الجبرائی مجموعہ صفر ہونا چاہیے۔ پولی ایٹومک آئن میں، آئن کے تمام ایٹمز کے آکسیڈیشن نمبروں کا الجبرائی مجموعہ آئن پر چارج کے برابر ہونا چاہیے۔ اس طرح، کاربونیٹ آئن، $\left(\mathrm{CO_3}\right)^{2-}$ میں تین آکسیجن ایٹمز اور ایک کاربن ایٹم کے آکسیڈیشن نمبر کا مجموعہ -2 کے برابر ہونا چاہیے۔
اوپر کے قواعد کے اطلاق سے، ہم کسی مالیکیول یا آئن میں مطلوبہ عنصر کا آکسیڈیشن نمبر معلوم کر سکتے ہیں۔ یہ واضح ہے کہ دھاتی عناصر مثبت آکسیڈیشن نمبر رکھتے ہیں اور غیر دھاتی عناصر مثبت یا منفی آکسیڈیشن نمبر رکھتے ہیں۔ منتقلی عناصر کے ایٹم عام طور پر کئی مثبت آکسیڈیشن حالتیں ظاہر کرتے ہیں۔ ایک نمائندہ عنصر کا سب سے زیادہ آکسیڈیشن نمبر پہلے دو گروپوں کے لیے گروپ نمبر ہے اور دیگر گروپوں کے لیے گروپ نمبر مائنس 10 (پیریڈک ٹیبل کی لمبی شکل کے بعد) ہے۔ اس طرح، اس کا مطلب یہ ہے کہ کسی عنصر کے ایٹم کے ذریعے ظاہر کردہ آکسیڈیشن نمبر کی سب سے زیادہ قدر عام طور پر پیریڈک ٹیبل میں پیریڈ کے پار بڑھتی ہے۔ تیسرے پیریڈ میں، آکسیڈیشن نمبر کی سب سے زیادہ قدر 1 سے 7 تک بدلتی ہے جیسا کہ عناصر کے مرکبات میں نیچے اشارہ کیا گیا ہے۔
ایک اصطلاح جو اکثر آکسیڈیشن نمبر کے ساتھ متبادل طور پر استعمال ہوتی ہے وہ آکسیڈیشن حالت ہے۔ اس طرح $\mathrm{CO_2}$ میں، کاربن کی آکسیڈیشن حالت +4 ہے، جو اس کا آکسیڈیشن نمبر بھی ہے اور اسی طرح آکسیجن کی آکسیڈیشن حالت اور آکسیڈیشن نمبر -2 ہے۔ اس کا مطلب یہ ہے کہ آکسیڈیشن نمبر کسی مرکب میں کسی عنصر کی آکسیڈیشن حالت کو ظاہر کرتا ہے۔
| گروپ | $\mathbf{1}$ | $\mathbf{2}$ | $\mathbf{1 3}$ | $\mathbf{1 4}$ | $\mathbf{1 5}$ | $\mathbf{1 6}$ | $\mathbf{1 7}$ |
|---|---|---|---|---|---|---|---|
| عنصر | $\mathrm{Na}$ | $\mathrm{Mg}$ | $\mathrm{Al}$ | $\mathrm{Si}$ | $\mathrm{P}$ | $\mathrm{S}$ | $\mathrm{Cl}$ |
| مرکب | $\mathrm{NaCl}$ | $\mathrm{MgSO_4}$ | $\mathrm{AlF_3}$ | $\mathrm{SiCl_4}$ | $\mathrm{P_4} \mathrm{O_10}$ |








