یونٹ 10 ہیلو الکینز اور ہیلو ایرینز
ہیلوجنیٹڈ مرکبات ماحول میں اپنی موجودگی برقرار رکھتے ہیں کیونکہ یہ مٹی کے بیکٹیریا کے ذریعے ٹوٹنے کے خلاف مزاحم ہوتے ہیں۔
ایک ایلیفٹک یا ایرومیٹک ہائیڈروکاربن میں ہائیڈروجن ایٹم(ز) کی جگہ ہیلوجن ایٹم(ز) لگنے سے بالترتیب الکیل ہیلائیڈ (ہیلو الکین) اور ایرائل ہیلائیڈ (ہیلو ایرین) بنتے ہیں۔ ہیلو الکینز میں ہیلوجن ایٹم(ز) الکیل گروپ کے sp3 ہائبرڈائزڈ کاربن ایٹم سے جڑے ہوتے ہیں جبکہ ہیلو ایرینز میں ہیلوجن ایٹم(ز) ایرائل گروپ کے sp2 ہائبرڈائزڈ کاربن ایٹم(ز) سے جڑے ہوتے ہیں۔ بہت سے ہیلوجن پر مشتمل نامیاتی مرکبات فطرت میں پائے جاتے ہیں اور ان میں سے کچھ طبی طور پر مفید ہیں۔ مرکبات کی یہ اقسام صنعت کے ساتھ ساتھ روزمرہ کی زندگی میں وسیع پیمانے پر استعمال ہوتی ہیں۔ انہیں نسبتاً غیر قطبی مرکبات کے لیے سالوینٹس کے طور پر اور نامیاتی مرکبات کی وسیع رینج کی ترکیب کے لیے ابتدائی مواد کے طور پر استعمال کیا جاتا ہے۔ کلورین پر مشتمل اینٹی بائیوٹک، کلورامفینیکول، جو خرد حیاتیات کے ذریعے تیار ہوتی ہے، ٹائیفائیڈ بخار کے علاج کے لیے بہت مؤثر ہے۔ ہمارا جسم آیوڈین پر مشتمل ہارمون، تھائیروکسین پیدا کرتا ہے، جس کی کمی سے گائٹر نامی بیماری ہوتی ہے۔ مصنوعی ہیلوجن مرکبات، مثلاً کلوروکوئن ملیریا کے علاج کے لیے استعمال ہوتی ہے؛ ہیلوتھین سرجری کے دوران بے ہوشی کی دوا کے طور پر استعمال ہوتی ہے۔ کچھ مکمل طور پر فلورینیٹڈ مرکبات کو سرجری میں ممکنہ خون کے متبادل کے طور پر غور کیا جا رہا ہے۔
اس یونٹ میں، آپ آرگینوہیلوجن مرکبات کی تیاری کے اہم طریقوں، طبیعی اور کیمیائی خواص اور استعمالات کا مطالعہ کریں گے۔
10.1 درجہ بندی
ہیلو الکینز اور ہیلو ایرینز کو درج ذیل کے مطابق درجہ بند کیا جا سکتا ہے:
10.1.1 ہیلوجن ایٹموں کی تعداد کی بنیاد پر
انہیں مونو، ڈائی، یا پولی ہیلوجن (ٹری-، ٹیٹرا-، وغیرہ) مرکبات کے طور پر درجہ بند کیا جا سکتا ہے، اس بات پر منحصر ہے کہ ان کی ساخت میں ایک، دو یا زیادہ ہیلوجن ایٹم ہیں۔ مثال کے طور پر،

مونو ہیلو مرکبات کو مزید اس بنیاد پر درجہ بند کیا جا سکتا ہے کہ ہیلوجن کس کاربن ایٹم سے جڑا ہوا ہے، جیسا کہ نیچے بحث کی گئی ہے۔
10.1.2 $\mathbf{s p}^{\mathbf{3}} \mathbf{~C}-\mathbf{X}$ بانڈ پر مشتمل مرکبات (X= F, Cl, Br, I)
اس زمرے میں شامل ہیں:
(الف) الکیل ہیلائیڈز یا ہیلو الکینز ($\mathbf{R}-\mathbf{X}$)
الکیل ہیلائیڈز میں، ہیلوجن ایٹم ایک الکیل گروپ $(\mathrm{R})$ سے جڑا ہوتا ہے۔ وہ $\mathrm{C} _{\mathrm{n}} \mathrm{H} _{2 \mathrm{n}+1} \mathrm{X}$ کے ذریعے ظاہر کردہ ہومولوجس سیریز بناتے ہیں۔ انہیں مزید پرائمری، سیکنڈری یا ٹرشری کے طور پر درجہ بند کیا جاتا ہے، اس بنیاد پر کہ ہیلوجن کس قسم کے کاربن سے جڑا ہے۔ اگر ہیلوجن الکیل ہیلائیڈ میں پرائمری کاربن ایٹم سے جڑا ہو، تو الکیل ہیلائیڈ کو پرائمری الکیل ہیلائیڈ یا ($1^{\circ}$) الکیل ہیلائیڈ کہتے ہیں۔ اسی طرح، اگر ہیلوجن سیکنڈری یا ٹرشری کاربن ایٹم سے جڑا ہو، تو الکیل ہیلائیڈ کو بالترتیب سیکنڈری الکیل ہیلائیڈ ($2^{\circ}$) اور ٹرشری ($3^{\circ}$) الکیل ہیلائیڈ کہتے ہیں۔

(ب) ایلائلک ہیلائیڈز
یہ وہ مرکبات ہیں جن میں ہیلوجن ایٹم ایک $s p^{3}$-ہائبرڈائزڈ کاربن ایٹم سے جڑا ہوتا ہے جو کاربن-کاربن ڈبل بانڈ $(\mathrm{C}=\mathrm{C})$ کے متصل ہوتا ہے، یعنی ایک ایلائلک کاربن سے۔

(ج) بینزلک ہیلائیڈز
یہ وہ مرکبات ہیں جن میں ہیلوجن ایٹم ایک $s p^{3}$-ہائبرڈائزڈ کاربن ایٹم سے جڑا ہوتا ہے جو ایک ایرومیٹک رنگ سے منسلک ہوتا ہے۔

10.1.3 $\boldsymbol{s p}^{2} \mathrm{C}-\mathrm{X}$ بانڈ پر مشتمل مرکبات
اس زمرے میں شامل ہیں:
(الف) وینائلک ہیلائیڈز
یہ وہ مرکبات ہیں جن میں ہیلوجن ایٹم کاربن-کاربن ڈبل بانڈ $(\mathrm{C}=\mathrm{C})$ کے ایک $s p^{2}$-ہائبرڈائزڈ کاربن ایٹم سے جڑا ہوتا ہے۔

(ب) ایرائل ہیلائیڈز
یہ وہ مرکبات ہیں جن میں ہیلوجن ایٹم براہ راست ایرومیٹک رنگ کے $s p^{2}$-ہائبرڈائزڈ کاربن ایٹم سے جڑا ہوتا ہے۔

10.2 نامگذاری
ہیلوجنیٹڈ مرکبات کی درجہ بندی سیکھنے کے بعد، اب ہم سیکھتے ہیں کہ ان کے نام کیسے رکھے جاتے ہیں۔ الکیل ہیلائیڈز کے عام نام الکیل گروپ کا نام لے کر پھر ہیلائیڈ کا نام لگا کر بنائے جاتے ہیں۔ آئی یو پی اے سی نظام نامگذاری میں، الکیل ہیلائیڈز کو ہیلو متبادل ہائیڈروکاربنز کے طور پر نامزد کیا جاتا ہے۔ بنزین کے مونو ہیلوجن متبادل مشتقات کے لیے، عام اور آئی یو پی اے سی نام ایک جیسے ہیں۔ ڈائی ہیلوجن مشتقات کے لیے، عام نظام میں سابقے $o^{-,}, m_{-}, p$ استعمال ہوتے ہیں لیکن آئی یو پی اے سی نظام میں، جیسا کہ آپ نے کلاس XI میں سیکھا ہے، ہندسے 1,$2 ; 1,3$ اور 1,4 استعمال ہوتے ہیں۔

ایک جیسے ہیلوجن ایٹموں والے ڈائی ہیلو الکینز کو الکیلائیڈین یا الکیلین ڈائی ہیلائیڈز کہا جاتا ہے۔ دونوں ہیلوجن ایٹموں والے ڈائی ہیلو مرکبات کو مزید جیمینل ہیلائیڈز یا جیم-ڈائی ہیلائیڈز کہا جاتا ہے جب دونوں ہیلوجن ایٹم زنجیر کے ایک ہی کاربن ایٹم پر موجود ہوں اور وِسینل ہیلائیڈز یا وِک-ڈائی ہیلائیڈز کہا جاتا ہے جب ہیلوجن ایٹم متصل کاربن ایٹموں پر موجود ہوں۔ عام نام نظام میں، جیم-ڈائی ہیلائیڈز کو الکیلائیڈین ہیلائیڈز کہا جاتا ہے اور وِسینل ہیلائیڈز کو الکیلین ڈائی ہیلائیڈز کہا جاتا ہے۔ آئی یو پی اے سی نظام میں، انہیں ڈائی ہیلو الکینز کہا جاتا ہے۔
ہیلو مرکبات کی کچھ عام مثالیں جدول 10.1 میں درج ہیں۔

مثال 10.1
ان تمام آٹھ ساختی آئسومرز کے ڈھانچے بنائیں جن کا سالماتی فارمولا $\mathrm{C_5} \mathrm{H_11} \mathrm{Br}$ ہے۔ ہر آئسومر کو آئی یو پی اے سی نظام کے مطابق نام دیں اور انہیں پرائمری، سیکنڈری یا ٹرشری برومائیڈ کے طور پر درجہ بند کریں۔
حل
| $\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{CH}_2 \mathrm{CH}_2 \mathrm{CH}_2 \mathrm{Br}$ | 1-بروموپینٹین (1 $\left.{ }^{\circ}\right)$ |
|---|---|
| $\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{CH}_2 \mathrm{CH}(\mathrm{Br}) \mathrm{CH}_3$ | 2-بروموپینٹین $\left(2^{\circ}\right)$ |
| $\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{CH}(\mathrm{Br}) \mathrm{CH}_2 \mathrm{CH}_3$ | 3-بروموپینٹین (2 $\left.{ }^{\circ}\right)$ |
| $\left(\mathrm{CH}_3\right)_2 \mathrm{CHCH}_2 \mathrm{CH}_2 \mathrm{Br}$ | 1-برومو-3-میتھائل بیوٹین (1 $\left.{ }^{\circ}\right)$ |
| $\left(\mathrm{CH}_3\right)_2 \mathrm{CHCHBrCH}_3$ | 2-برومو-3-میتھائل بیوٹین(2 $\left.{ }^{\circ}\right)$ |
| $\left(\mathrm{CH}_3\right)_2 \mathrm{CBrCH}_2 \mathrm{CH}_3$ | 2-برومو-2-میتھائل بیوٹین $\left(3^{\circ}\right)$ |
| $\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{CH}\left(\mathrm{CH}_3\right) \mathrm{CH}_2 \mathrm{Br}$ | 1-برومو-2-میتھائل بیوٹین(1 $\left.{ }^{\circ}\right)$ |
| $\left(\mathrm{CH}_3\right)_3 \mathrm{CCH}_2 \mathrm{Br}$ | 1-برومو-2,2-ڈایمیتھائل پروپین (1 $\left.{ }^{\circ}\right)$ |
مثال 10.2 درج ذیل کے آئی یو پی اے سی نام لکھیں:

حل
(i) 4-بروموپینٹ-2-این
(ii) 3-برومو-2-میتھائل بیوٹ-1-این
(iii) 4-برومو-3-میتھائل پینٹ-2-این
(iv) 1-برومو-2-میتھائل بیوٹ-2-این
(v) 1-بروموبیوٹ-2-این
(vi) 3-برومو-2-میتھائل پروپین
10.3 C-X بانڈ کی نوعیت
ہیلوجن ایٹم کاربن سے زیادہ برقی منفی ہوتے ہیں، اس لیے الکیل ہیلائیڈ کا کاربن-ہیلوجن بانڈ قطبی ہوتا ہے؛ کاربن ایٹم پر جزوی مثبت چارج ہوتا ہے جبکہ ہیلوجن ایٹم پر جزوی منفی چارج ہوتا ہے۔
جیسے جیسے ہم دوری جدول میں گروپ میں نیچے جاتے ہیں، ہیلوجن ایٹم کا سائز بڑھتا جاتا ہے۔ فلورین ایٹم سب سے چھوٹا اور آیوڈین ایٹم سب سے بڑا ہوتا ہے۔ نتیجتاً کاربن-ہیلوجن بانڈ کی لمبائی بھی $\mathrm{C}-\mathrm{F}$ سے $\mathrm{C}-\mathrm{I}$ تک بڑھ جاتی ہے۔ کچھ مخصوص بانڈ لمبائیاں، بانڈ اینتھالپیز اور دو قطبی لمحات جدول 10.2 میں دیے گئے ہیں۔
الکیل ہیلائیڈز الکحل سے بہترین طور پر تیار کیے جاتے ہیں، جو آسانی سے دستیاب ہوتے ہیں۔
جدول 10.2: کاربن-ہیلوجن (C—X) بانڈ لمبائیاں، بانڈ اینتھالپیز اور دو قطبی لمحات
| بانڈ | بانڈ لمبائی/pm | C-X بانڈ اینتھالپیز/ kJmol ${ }^{-1}$ | دو قطبی لمحہ/Debye |
|---|---|---|---|
| $\mathrm{CH}_3-\mathrm{F}$ | 139 | 452 | 1.847 |
| $\mathrm{CH}_3-\mathrm{Cl}$ | 178 | 351 | 1.860 |
| $\mathrm{CH}_3-\mathrm{Br}$ | 193 | 293 | 1.830 |
| $\mathrm{CH}_3-\mathrm{I}$ | 214 | 234 | 1.636 |
10.4 ہیلو الکینز کی تیاری کے طریقے
10.4.1 الکحل سے
الکحل کے ہائیڈروآکسل گروپ کو مرتکز ہیلوجن ایسڈز، فاسفورس ہیلائیڈز یا تھائیونائل کلورائیڈ کے ساتھ رد عمل میں ہیلوجن سے بدل دیا جاتا ہے۔ تھائیونائل کلورائیڈ ترجیحی ہے کیونکہ اس رد عمل میں الکیل ہیلائیڈ گیسیں $\mathrm{SO_2}$ اور $\mathrm{HCl}$ کے ساتھ بنتا ہے۔ دو گیس پیداواریں فرار ہو سکتی ہیں، اس لیے رد عمل خالص الکیل ہیلائیڈز دیتا ہے۔ پرائمری اور سیکنڈری الکحلز کے ساتھ $\mathrm{HCl}$ کے رد عمل کے لیے ایک کیٹالسٹ، $\mathrm{ZnCl_2}$ کی موجودگی درکار ہوتی ہے۔ ٹرشری الکحلز کے ساتھ، رد عمل صرف الکحل کو مرتکز $\mathrm{HCl}$ کے ساتھ کمرے کے درجہ حرارت پر ہلا کر کیا جاتا ہے۔ $\mathrm{HBr}(48 %)$ کے ساتھ مسلسل ابلنے کا استعمال الکیل برومائیڈ تیار کرنے کے لیے کیا جاتا ہے۔ R-I کی اچھی پیداوار الکحلز کو سوڈیم یا پوٹاشیم آیوڈائیڈ کے ساتھ 95% اورتھو فاسفورک ایسڈ میں گرم کرکے حاصل کی جا سکتی ہے۔ دیے گئے ہیلوایسڈ کے ساتھ الکحلز کی رد عمل کی صلاحیت کا ترتیب $3^{\circ}>2^{\circ}>1^{\circ}$ ہے۔ فاسفورس ٹرائی برومائیڈ اور ٹرائی آیوڈائیڈ عام طور پر سرخ فاسفورس کے برومین اور آیوڈین کے ساتھ رد عمل سے بالترتیب رد عمل مرکب میں ہی پیدا کیے جاتے ہیں۔
$$ \begin{aligned} & \mathrm{R}-\mathrm{OH}+\mathrm{HCl} \xrightarrow{\mathrm{ZnCl_2}} \mathrm{R}-\mathrm{Cl}+\mathrm{H_2} \mathrm{O} \\ & \mathrm{R}-\mathrm{OH}+\mathrm{NaBr}+\mathrm{H_2} \mathrm{SO_4} \longrightarrow \mathrm{R}-\mathrm{Br}+\mathrm{NaHSO_4}+\mathrm{H_2} \mathrm{O} \\ & 3 \mathrm{R}-\mathrm{OH}+\mathrm{PX_3} \longrightarrow 3 \mathrm{R}-\mathrm{X}+\mathrm{H_3} \mathrm{PO_3} \quad(\mathrm{X}=\mathrm{Cl}, \mathrm{Br}) \\ & \mathrm{R}-\mathrm{OH}+\mathrm{PCl_5} \longrightarrow \mathrm{R}-\mathrm{Cl}+\mathrm{POCl_3}+\mathrm{HCl} \\ & \mathrm{R}-\mathrm{OH}+\frac{\mathrm{red} \mathrm{P} / \mathrm{X_2}}{\mathrm{X_2}=\mathrm{Br_2}, \mathrm{I_2}} \mathrm{R}-\mathrm{X} \\ & \mathrm{R}-\mathrm{OH}+\mathrm{SOCl_2} \longrightarrow \mathrm{R}-\mathrm{Cl}+\mathrm{SO_2}+\mathrm{HCl} \end{aligned} $$
الکیل کلورائیڈ کی تیاری یا تو الکحل کے محلول میں خشک ہائیڈروجن کلورائیڈ گیس گزار کر کی جاتی ہے یا الکحل اور مرتکز آبی ہیلوجن ایسڈ کے مرکب کو گرم کرکے۔
اوپر دیے گئے طریقے ایرائل ہیلائیڈز کی تیاری کے لیے قابل اطلاق نہیں ہیں کیونکہ فی نولز میں کاربن-آکسیجن بانڈ میں جزوی ڈبل بانڈ کا کردار ہوتا ہے اور یہ ایک سنگل بانڈ سے مضبوط ہونے کی وجہ سے ٹوٹنا مشکل ہوتا ہے۔
10.4.2 ہائیڈروکاربنز سے
(I) الکینز سے فری ریڈیکل ہیلوجنیشن کے ذریعے
الکینز کی فری ریڈیکل کلورینیشن یا برومینیشن سے آئسومرک مونو- اور پولی ہیلو الکینز کا ایک پیچیدہ مرکب ملتا ہے، جسے خالص مرکبات کے طور پر الگ کرنا مشکل ہوتا ہے۔ نتیجتاً، کسی ایک مرکب کی پیداوار کم ہوتی ہے۔
$\mathrm{CH_3}\mathrm{CH_2}\mathrm{CH_2}\mathrm{CH_3} \xrightarrow[ \text {or heat}]{\mathrm{Cl_2} \text {/UV} \quad \text {light}} \mathrm{CH_3}\mathrm{CH_2}\mathrm{CH_2}\mathrm{CH_2}\mathrm{Cl_2} + \mathrm{CH_3}\mathrm{CH_2}\mathrm{CHCl}\mathrm{CH_3} $
(II) الکینز سے
(i) ہائیڈروجن ہیلائیڈز کا اضافہ: ایک الکین ہائیڈروجن کلورائیڈ، ہائیڈروجن برومائیڈ یا ہائیڈروجن آیوڈائیڈ کے ساتھ رد عمل میں تبدیل ہو کر متعلقہ الکیل ہیلائیڈ دیتا ہے۔
پروپین دو مصنوعات دیتا ہے، تاہم مارکوونیکوف کے قاعدے کے مطابق صرف ایک غالب ہوتا ہے۔ (یونٹ 13، کلاس XI)
$$ \mathrm{CH_3} \mathrm{CH}=\mathrm{CH_2}+\mathrm{H}-\mathrm{I} \longrightarrow \underset {\text{minor}}{\mathrm{CH_3} \mathrm{CH_2} \mathrm{CH_2} \mathrm{I}} + \underset{ \text{major }}{\mathrm{CH_3} \mathrm{CHICH_3}} $$
(ii) ہیلوجنز کا اضافہ: لیبارٹری میں، $\mathrm{CCl}_{4}$ میں برومین کا الکین میں اضافہ، جس کے نتیجے میں برومین کا سرخ بھورا رنگ ختم ہو جاتا ہے، ایک سالمہ میں ڈبل بانڈ کی شناخت کا ایک اہم طریقہ ہے۔ اضافہ سے وِک-ڈائی برومائیڈز کی ترکیب ہوتی ہے، جو بے رنگ ہوتے ہیں (یونٹ 9، کلاس XI)۔

مثال 10.3
$\left(\mathrm{CH_3}\right)_{2} \mathrm{CHCH_2} \mathrm{CH_3}$ کے فری ریڈیکل مونو کلورینیشن پر بننے والے تمام ممکنہ مونو کلورو ساختی آئسومرز کی شناخت کریں۔
حل
دیے گئے سالمہ میں، چار مختلف قسم کے ہائیڈروجن ایٹم ہیں۔ ان ہائیڈروجن ایٹموں کی جگہ لینے سے درج ذیل ملے گا:
| $\left(\mathrm{CH_3}\right)_{2} \mathrm{CHCH_2} \mathrm{CH_2} \mathrm{Cl}$ | $\left(\mathrm{CH_3}\right)_{2} \mathrm{CHCH}(\mathrm{Cl}) \mathrm{CH_3}$ |
|---|---|
| $\left(\mathrm{CH_3}\right)_{2} \mathrm{C}(\mathrm{Cl}) \mathrm{CH_2} \mathrm{CH_3}$ | $\mathrm{CH_3} \mathrm{CH}\left(\mathrm{CH_2} \mathrm{Cl_2} \mathrm{CH_2} \mathrm{CH_3}\right).$ |
10.4.3 ہیلوجن تبادلہ
الکیل آیوڈائیڈز اکثر الکیل کلورائیڈز/برومائیڈز کا خشک ایسیٹون میں NaI کے ساتھ رد عمل سے تیار کیے جاتے ہیں۔ اس رد عمل کو فِنکل اسٹائن رد عمل کہا جاتا ہے۔
$$ \begin{aligned} & \mathrm{R}-\mathrm{X}+\mathrm{NaI} \longrightarrow \mathrm{R}-\mathrm{I}+\mathrm{NaX} \\ & \mathrm{X}=\mathrm{Cl}, \mathrm{Br} \end{aligned} $$
اس طرح بننے والا NaCl یا NaBr خشک ایسیٹون میں تہ نشین ہو جاتا ہے۔ یہ لی شاٹیلیئر کے اصول کے مطابق آگے کے رد عمل کو آسان بناتا ہے۔ الکیل فلورائیڈز کی ترکیب الکیل کلورائیڈ/برومائیڈ کو دھاتی فلورائیڈ جیسے $\mathrm{AgF}, \mathrm{Hg}_2 \mathrm{~F}_2, \mathrm{CoF}_2$ یا $\mathrm{SbF}_3$ کی موجودگی میں گرم کرکے بہترین طور پر حاصل کی جاتی ہے۔ اس رد عمل کو $\mathrm{Swarts}$ رد عمل کہا جاتا ہے۔
$$ \mathrm{H}_3 \mathrm{C}-\mathrm{Br}+\mathrm{AgF} \longrightarrow \mathrm{H}_3 \mathrm{C}-\mathrm{F}+\mathrm{AgBr} $$
مثال 6.3 $\left(\mathrm{CH}_3\right)_2 \mathrm{CHCH}_2 \mathrm{CH}_3$ کے فری ریڈیکل مونو کلورینیشن پر بننے والے تمام ممکنہ مونو کلورو ساختی آئسومرز کی شناخت کریں۔
حل
دیے گئے سالمہ میں، چار مختلف قسم کے ہائیڈروجن ایٹم ہیں۔ ان ہائیڈروجن ایٹموں کی جگہ لینے سے درج ذیل ملے گا:
$\left(\mathrm{CH} _{3}\right) _{2} \mathrm{CHCH} _{2} \mathrm{CH} _{2} \mathrm{Cl}$,
$\left(\mathrm{CH} _{3}\right) _{2} \mathrm{CHCH}(\mathrm{Cl}) \mathrm{CH} _{3}$,
$\left(\mathrm{CH} _{3}\right) _{2} \mathrm{C}(\mathrm{Cl}) \mathrm{CH} _{2} \mathrm{CH} _{3}$,
$\mathrm{CH} _{3} \mathrm{CH}\left(\mathrm{CH} _{2} \mathrm{Cl}\right) \mathrm{CH} _{2} \mathrm{CH} _{3}$
10.5 ہیلو ایرینز کی تیاری
(i) ہائیڈروکاربنز سے الیکٹروفائل متبادل کے ذریعے: ایرائل کلورائیڈز اور برومائیڈز آسانی سے ایرینز کی کلورین اور برومین کے ساتھ بالترتیب لوئس ایسڈ کیٹالسٹس جیسے آئرن یا آئرن(III) کلورائیڈ کی موجودگی میں الیکٹروفائل متبادل سے تیار کیے جا سکتے ہیں۔

اورتھو اور پیرا آئسومرز ان کے پگھلنے کے درجہ حرارت میں بڑے فرق کی وجہ سے آسانی سے الگ کیے جا سکتے ہیں۔ آیوڈین کے ساتھ رد عمل فطرت میں الٹ جانے والے ہوتے ہیں اور آیوڈینیشن کے دوران بننے والے $\mathrm{HI}$ کو آکسیدائز کرنے کے لیے ایک آکسیدائز ایجنٹ $\left(\mathrm{HNO_3}\right).$, $\mathrm{HIO_4}$ ) کی موجودگی درکار ہوتی ہے۔ فلورو مرکبات فلورین کی زیادہ رد عمل کی صلاحیت کی وجہ سے اس طریقے سے تیار نہیں کیے جاتے۔
(ii) امینز سے سینڈمائیر کے رد عمل کے ذریعے
جب ایک پرائمری ایرومیٹک امین، جو ٹھنڈے آبی معدنی تیزاب میں حل یا معطل ہے، سوڈیم نائٹریٹ کے ساتھ علاج کیا جاتا ہے، تو ایک ڈائی آزونیم نمک بنتا ہے۔ تازہ تیار شدہ ڈائی آزونیم نمک کے محلول کو کیپرس کلورائیڈ یا کیپرس برومائیڈ کے ساتھ ملانے سے ڈائی آزونیم گروپ کی جگہ $-\mathrm{Cl}$ یا $-\mathrm{Br}$ لے لیتا ہے۔

ڈائی آزونیم گروپ کی جگہ آیوڈین لگانے کے لیے کیپرس ہیلائیڈ کی موجودگی درکار نہیں ہوتی اور یہ صرف ڈائی آزونیم نمک کو پوٹاشیم آیوڈائیڈ کے ساتھ ہلا کر کیا جاتا ہے۔

مثال 10.4 درج ذیل رد عملوں کی مصنوعات لکھیں:

حل

10.6 طبیعی خواص
الکیل ہیلائیڈز خالص ہونے پر بے رنگ ہوتے ہیں۔ تاہم، برومائیڈز اور آیوڈائیڈز روشنی میں آنے پر رنگت پیدا کرتے ہیں۔ بہت سے متغیر ہیلوجن مرکبات میں میٹھی بو ہوتی ہے۔
پگھلنے اور ابلنے کے درجہ حرارت
میتھائل کلورائیڈ، میتھائل برومائیڈ، ایتھائل کلورائیڈ اور کچھ کلورو فلورو میتھینز کمرے کے درجہ حرارت پر گیسیں ہیں۔ اعلیٰ اراکین مائعات یا ٹھوس ہوتے ہیں۔ جیسا کہ ہم پہلے ہی سیکھ چکے ہیں، نامیاتی ہیلوجن مرکبات کے سالمات عام طور پر قطبی ہوتے ہیں۔ والد ہائیڈروکاربن کے مقابلے میں زیادہ قطبیت کے ساتھ ساتھ زیادہ سالماتی کمیت کی وجہ سے، ہیلوجن مشتقات میں انٹر مالیکیولر قوتیں کشش (دو قطبی-دو قطبی اور وان ڈیر والز) زیادہ مضبوط ہوتی ہیں۔ اسی لیے کلورائیڈز، برومائیڈز اور آیوڈائیڈز کے ابلنے کے درجہ حرارت قابل موازنہ سالماتی کمیت والے ہائیڈروکاربنز کے مقابلے میں کافی زیادہ ہوتے ہیں۔
کششیں مضبوط ہوتی جاتی ہیں جیسے جیسے سالمات سائز میں بڑے ہوتے جاتے ہیں اور ان میں زیادہ الیکٹران ہوتے ہیں۔ مختلف ہیلائیڈز کے ابلنے کے درجہ حرارت میں تغیر کا نمونہ شکل 10.1 میں دکھایا گیا ہے۔ ایک ہی الکیل گروپ کے لیے، الکیل ہیلائیڈز کے ابلنے کے درجہ حرارت اس ترتیب میں کم ہوتے ہیں: $\mathrm{RI}>\mathrm{RBr}>\mathrm{RCl}>\mathrm{RF}$۔ اس کی وجہ یہ ہے کہ ہیلوجن ایٹم کے سائز اور کمیت میں اضافے کے ساتھ، وان ڈیر والز قوتوں کی شدت بڑھ جاتی ہے۔
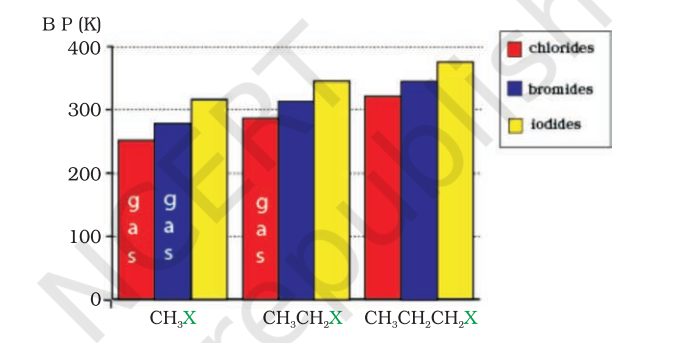
شکل 10.1: کچھ الکیل ہیلائیڈز کے ابلنے کے درجہ حرارت کا موازنہ
آئسومرک ہیلو الکینز کے ابلنے کے درجہ حرارت شاخوں میں اضافے کے ساتھ کم ہوتے ہیں (یونٹ 12، کلاس XI)۔ مثال کے طور پر، 2-برومو-2- میتھائل پروپین کے تینوں آئسومرز میں سب سے کم ابلنے کا درجہ حرارت ہوتا ہے۔
$\mathrm{CH_3} \mathrm{CH_2} \mathrm{CH_2} \mathrm{CH_2} \mathrm{Br}$
آئسومرک ڈائی ہیلو بنزینز کے ابلنے کے درجہ حرارت تقریباً ایک جیسے ہوتے ہیں۔ تاہم، پیرا-آئسومرز ان کے اورتھو- اور میٹا-آئسومرز کے مقابلے میں زیادہ پگھلنے والے ہوتے ہیں۔ یہ پیرا-آئسومرز کی ہم آہنگی کی وجہ سے ہے جو اورتھو- اور میٹا-آئسومرز کے مقابلے میں کرسٹل جالی میں بہتر فٹ بیٹھتے ہیں۔

کثافت
ہائیڈروکاربنز کے برومو، آیوڈو اور پولی کلورو مشتقات پانی سے بھاری ہوتے ہیں۔ کثافت کاربن ایٹموں کی تعداد، ہیلوجن ایٹموں کی تعداد اور ہیلوجن ایٹموں کی جوہری کمیت میں اضافے کے ساتھ بڑھتی ہے (جدول 10.3)۔
جدول 10.3: کچھ ہیلو الکینز کی کثافت
| مرکب | کثافت (g/mL) | مرکب | کثافت (g/mL) |
|---|---|---|---|
| $\mathrm{n}-\mathrm{C}_3 \mathrm{H}_7 \mathrm{Cl}$ | 0.89 | $\mathrm{CH}_2 \mathrm{Cl}_2$ | 1.336 |
| $\mathrm{n}-\mathrm{C}_3 \mathrm{H}_7 \mathrm{Br}$ | 1.335 | $\mathrm{CHCl}_3$ | 1.489 |
| $\mathrm{n}-\mathrm{C}_3 \mathrm{H}_7 \mathrm{I}$ | 1.747 | $\mathrm{CCl}_4$ | 1.595 |
حل پذیری
ہیلو الکینز پانی میں بہت تھوڑے حل پذیر ہوتے ہیں۔ ہیلو الکین کو پانی میں حل کرنے کے لیے، ہیلو الکین سالمات کے درمیان کششوں پر قابو پانے اور پانی کے سالمات کے درمیان ہائیڈروجن بانڈ توڑنے کے لیے توانائی درکار ہوتی ہے۔ جب ہیلو الکین اور پانی کے سالمات کے درمیان نئی کششیں قائم ہوتی ہیں تو کم توانائی خارج ہوتی ہے کیونکہ یہ پانی میں اصل ہائیڈروجن بانڈز جتنی مضبوط نہیں ہوتیں۔ نتیجتاً، ہیلو الکینز کی پانی میں حل پذیری کم ہوتی ہے۔ تاہم، ہیلو الکینز نامیاتی سالوینٹس میں حل ہونے کا رجحان رکھتے ہیں کیونکہ ہیلو الکینز اور سالوینٹ سالمات کے درمیان نئی انٹر مالیکیولر کششیں الگ ہیلو الکین اور سالوینٹ سالمات میں ٹوٹنے والی کششوں کی تقریباً ایک جیسی طاقت رکھتی ہیں۔
10.7 کیمیائی رد عمل
10.7.1 ہیلو الکینز کے رد عمل
ہیلو الکینز کے رد عمل کو درج ذیل زمروں میں تقسیم کیا جا سکتا ہے: 1. نیوکلیوفائل متبادل 2. اخراجی رد عمل 3. دھاتوں کے ساتھ رد عمل۔
(1) نیوکلیوفائل متبادل رد عمل آپ نے کلاس XI میں سیکھا تھا کہ نیوکلیوفائلز الیکٹران سے بھرپور انواع ہیں۔ لہٰذا، وہ سبسٹریٹ سالمہ کے اس حصے پر حملہ کرتے ہیں جو الیکٹران کی کمی کا شکار ہوتا ہے۔ وہ رد عمل جس میں ایک نیوکلیوفائل سالمہ میں پہلے سے موجود نیوکلیوفائل کی جگہ لے لیتا ہے، نیوکلیوفائل متبادل رد عمل کہلاتا ہے۔ ہیلو الکینز ان رد عملوں میں سبسٹریٹ ہوتے ہیں۔ اس قسم کے رد عمل میں، ایک نیوکلیوفائل ہیلو الکین (سبسٹریٹ) کے ساتھ رد عمل کرتا ہے جس کے ہیلوجن سے جڑے کاربن ایٹم پر جزوی مثبت چارج ہوتا ہے۔ ایک متبادل رد عمل ہوتا ہے اور ہیلوجن ایٹم، جسے چھوڑنے والا گروپ کہتے ہیں، ہیلائیڈ آئن کے طور پر نکل جاتا ہے۔ چونکہ متبادل رد عمل کا آغاز نیوکلیوفائل کرتا ہے، اس لیے اسے نیوکلیوفائل متبادل رد عمل کہتے ہیں۔

یہ الکیل ہیلائیڈز کے نامیاتی رد عمل کی سب سے مفید اقسام میں سے ایک ہے جس میں ہیلوجن sp3 ہائبرڈائزڈ کاربن سے جڑا ہوتا ہے۔ ہیلو الکینز کے کچھ عام نیوکلیوفائلز کے ساتھ رد عمل سے بننے والی مصنوعات جدول 10.4 میں دی گئی ہیں۔
جدول 10.4: الکیل ہیلائیڈز کا نیوکلیوفائل متبادل (R–X) $$ \mathrm{R}-\mathrm{X}+\mathrm{Nu}^{-} \rightarrow \mathrm{R}-\mathrm{Nu}+\mathrm{X}^{-} $$
| ری ایجنٹ | نیوکلیوفائل $\left(\mathbf{N u}^{-}\right)$ | متبادل مصنوعات R-Nu | اہم مصنوعات کی کلاس |
|---|---|---|---|
| $\mathrm{NaOH}(\mathrm{KOH})$ | $\mathrm{HO}^{-}$ | $\mathrm{ROH}$ | الکحل |
| $\mathrm{H}_2 \mathrm{O}$ | $\mathrm{H}_2 \mathrm{O}$ | $\mathrm{ROH}$ | الکحل |
| $\mathrm{NaOR}^{\prime}$ | $\mathrm{R}^{\prime} \mathrm{O}^{-}$ | $\mathrm{ROR}^{\prime}$ | ایتھر |
| $\mathrm{NaI}$ | $\mathrm{I}^{-}$ | $\mathrm{R}-\mathrm{I}$ | الکیل آیوڈائیڈ |
| $\mathrm{NH}_3$ | $\mathrm{NH}_3$ | $\mathrm{RNH}_2$ | پرائمری امین |
| $\mathrm{R}^{\prime} \mathrm{NH}_2$ | $\mathrm{R}^{\prime} \mathrm{NH}_2$ | $\mathrm{RNHR}^{\prime}$ | سیکنڈری امین |
| $\mathrm{R}^{\prime} \mathrm{R}^{\prime \prime N H}$ | $\mathrm{R}^{\prime} \mathrm{R}^{\prime \prime} \mathrm{NH}$ | $\mathrm{RNR}^{\prime} \mathrm{R}^{\prime \prime}$ | ٹرشری امین |
| $\mathrm{KCN}$ | $\overline{\mathrm{C}} \equiv \mathrm{N}:$ | $\mathrm{RCN}$ | نائٹرائل (سایانائیڈ) |
| $\mathrm{AgCN}$ | $\mathrm{Ag}-\mathrm{CN}$ : | $\mathrm{RNC}$ (آئسوسایانائیڈ) | آئسونائٹرائل |
| $\mathrm{KNO}_2$ | $\mathrm{O}=\mathrm{N}-\mathrm{O}$ | $\mathrm{R}-\mathrm{O}-\mathrm{N}=\mathrm{O}$ | الکیل نائٹرائٹ |
| $\mathrm{AgNO}_2$ | $\mathrm{Ag}-\ddot{\mathrm{O}}-\mathrm{N}=\mathrm{O}$ | $\mathrm{R}-\mathrm{NO}_2$ | نائٹرو الکین |
| $\mathrm{R}^{\prime} \mathrm{COOAg}$ | $\mathrm{R}^{\prime} \mathrm{COO}^{-}$ | $\mathrm{R}^{\prime} \mathrm{COOR}$ | ایسٹر |
| $\mathrm{LiAlH}_4$ | $\mathrm{H}$ | $\mathrm{RH}$ | ہائیڈروکاربن |
| $\mathrm{R}^{\prime-} \mathrm{M}^{+}$ | $\mathrm{R}^{\prime-}$ | $\mathrm{RR}^{\prime}$ | الکین |
سایانائیڈز اور نائٹرائٹس جیسے گروپوں میں دو نیوکلیوفائل مراکز ہوتے ہیں اور انہیں امبیڈینٹ نیوکلیوفائلز کہا جاتا ہے۔ درحقیقت سای








